Анаболическое действие на белковый и жировой обмен что это такое
2.Тироксин. Влияние на обмен веществ. Изменения обмена при гипо- и гипертиреозе.
Тироксин - гормон щитовидной железы. После частичного превращения в трийодтиронин (в печени и почках) и перехода в клетки организма, оказывает влияние на развитие и рост тканей, на обмен веществ. В малых дозах оказывает анаболическое действие на белковый и жировой обмен. В средних дозах стимулирует рост и развитие, повышает потребность тканей в кислороде, стимулирует метаболизм белков, жиров и углеводов, повышает функциональную активность сердечно-сосудистой системы и центральной нервной системы. В больших дозах угнетает выработку тиротропин-рилизинг гормона гипоталамуса и тиреотропного гормона гипофиза. Тироксин влияет на обмен веществ, развитие тканей, в небольших дозах проявляет себя как анаболик (помогает увеличивать мышечный объем), в средних дозах активизирует жировой, белковый, углеводный обмен, положительно сказывается на состоянии нервной системы, сосудов, сердца.
Гипотиреоз развивается вследствие недостаточности йодтиронинов. Обычно гипотиреоз связан с недостаточностью функции щитовидной железы, но может возникать и при заболеваниях гипофиза и гипоталамуса. Гипотиреоз у новорождённых приводит к развитию кретинизма, который проявляется множественными врождёнными нарушениями и тяжёлой необратимой задержкой умственного развития. Наиболее тяжёлые формы гипотиреоза, сопровождающиеся слизистым отёком кожи и подкожной клетчатки, обозначают термином "микседема". Отёчность обусловлена избыточным накоплением гликозаминогликанов и воды. В подкожной клетчатке накапливается глюкуроновая и в меньшей степени хондроитинсерная кислоты. Характерные проявления заболевания: снижение частоты сердечных сокращений, вялость, сонливость, непереносимость холода, сухость кожи. Эти симптомы развиваются вследствие снижения основного обмена, скорости гликолиза, мобилизации гликогена и жиров, потребления глюкозы мышцами, уменьшения мышечной массы и снижения теплопродукции. В настоящее время у взрослых людей частой причиной гипотиреоза является хронический аутоиммунный тиреоидит, приводящий к нарушению синтеза йодтиронинов (зоб Хашимото).
Гипертиреоз возникает вследствие повышенной продукции йодтиронинов. Диффузный токсический зоб (базедова болезнь, болезнь Грейвса) - наиболее распространённое заболевание щитовидной железы. При этом заболевании отмечают увеличение размеров щитовидной железы (зоб), повышение концентрации йодтиронинов в 2-5 раз и развитие тиреотоксикоза. Характерные признаки тиреотоксикоза: увеличение основного обмена, учащение сердцебиений, мышечная слабость, снижение массы тела (несмотря на повышенный аппетит) , потливость, повышение температуры тела, тремор и экзофтальм (пучеглазие). Гипертиреоз может возникать в результате различных причин: развитие опухоли, тиреоидит, избыточное поступление йода и йодсодер-жащих препаратов, аутоиммунные реакции. В большей мере усиливаются процессы катаболизма, о чём свидетельствует отрицательный азотистый баланс.
3.Почему, если в крови повышены таг хиломикронов, рекомендуют сократить количество пищевых жиров, а если таг повышены за счет лпонп, то рекомендуют сократить потребление углеводов?
В составе хиломикронов экзогенные жиры доставляются в органы и ткани. Липопротеинлипаза (ЛП—липаза) — фермент, обеспечивающий потребление экзогенных жиров тканями. ЛП—липаза, располагающаяся в эндотелии сосудов, взаимодействует с хиломикронами кровотока и гидролизует триацилглирины на глицерин и жирные кислоты, которые поступают в клетку. По мере извлечения ТАГ из хиломикронов последние превращаются в остаточные хиломикроны и затем поступают в печень.
Жиры, как и гликоген, являются формами депонирования энергетического материала. Причем жиры — наиболее долговременные и более эффективные источники энергии. При голодании запасы жира у человека истощаются за 5—7 недель, тогда как гликоген полностью расходуется примерно за сутки. Если поступление жира превышает потребности организма в энергии , то жир депонируется в адипоцитах — специализированных клетках жировой ткани. Кроме того, если количество поступающих углеводов больше, чем надо для депонирования в виде гликогена, то часть глюкозы также превращается в жиры . Таким образом, жиры в жировой ткани накапливаются в результате трех процессов:
поступают из хиломикронов, которые приносят экзогенные жиры из кишечника
поступают из ЛОНП, которые транспортируют эндогенные жиры, синтезированные в печени из глюкозы
образуются из глюкозы в самих клетках жировой ткани.
В первом и во втором случае жиры в составе липопротеинов гидролизуются ЛП—липазой и в клетку поступают жирные кислоты, которые затем используются для синтеза ТАГ. Перед включением в ТАГ жирные кислоты сначала активируются путем образования тиоэфиров кофермента А, а затем взаимодействуют с глицеролфосфатом. Следовательно, синтез ТАГ может протекать только в присутствии глюкозы, из которой в процессе гликолиза образуется диаксиацетонфосфат. Инсулин стимулирует синтез ТАГ, потому что в его присутствии повышается проницаемость мембран клеток жировой ткани для глюкозы.
Билет 19
Биосинтез проколлагена и его превращение в коллаген. Фибриллогенез. Возможные нарушения.
Проколлаген - внутриклеточный предшественник коллагена, синтезируемый на полирибосомах, связанных с мембранами эндоплазматической сети.
Синтез и созревание коллагена – многоэтапный процесс, начинающийся в клетке и завершающийся в межклеточном матриксе. Включает в себя целый ряд посттрансляционных изменений: гидроксилирование пролина и лизина с образованием гидроксипролина и гидроксилизина; гликозилирование гидроксилизина; частичный протеолиз – отщепление «сигнального» пептида, а также N- и С – концевых пропептидов; образование тройной спирали.
Синтез полипептидный цепей коллагена.
Синтезируются на полирибосомах, связанных с мембранами ЭР, в виде более длинных, чем зрелые цепи, предшественников – препро – α – цепей.
Эти предшественники имеют гидрофобный «сигнальный» пептид на N – конце, содержащий около 100 аминокислот.
Функция сигнального пептида – ориентация синтеза пептидных цепей в полости ЭР. После выполнения функции – отщепляется.
Синтезированная молекула проколлагена содержит дополнительные участки – N- и С - концевые пропептиды, в составе которых остатки цистеина, образующие внутри- и межцепочечные S-S связи.
Посттрансляционные модификации коллагена.
Начинается в период трансляции коллагеновой мРНК на рибосомах
Продолжается на растущей полипептидной цепи вплоть до отделения от рибосом.
После образования тройной спирали дальнейшее гидроксилирование пролиновых и лизиловых остатков прекращается.
Реакции гидроксилирования катализируют оксигеназы, связанные с мембранами микросом.
Пролиловые и лизиловые остатки в Y – положении пептида подвергаются действию пролил-4-гидроксилазы и лизил-5-гидроксилазы.
Необходимые компоненты – α – кетоглутарат, кислород и витамин С.
Донор атома кислорода, присоединяющегося к С – 4 пролина, - молекула кислорода.
Гидроксилазы пролина и лизина содержат в активном центре атом железа II. Для сохранения атома железа в ферроформе необходим восстанавливающий агент, роль которого выполняет аскорбиновая кислота, легко окисляющаяся в дегидроаскорбиновую кислоту.
После завершения гидроксилирования при участии гидроксилтрансфераз в состав молекулы проколлагена вводятся углеводные группы – галактоза, дисахарид галактозилглюкоза.
Образуют ковалентную О – гликозидную связь с 5-ОН-группой гидроксилизина.
Гликозилирование происходит в коллагене, езё не претерпевшем спирализации
Завершается после образования тройной спирали
Каждая про – α – цепь соединяется водородными связями с двумя другими про – α – цепями, образуя тройную спираль проколлагена.
Происходит ещё в просвете ЭР и начинаются после образования межцепочечных дисульфидных мостиков в области С – концевых пропептидов.
Из ЭР молекулы проколлагена перемещаются в аппарат Гольджи, включаются в секреторные пузырьки и секретируются в межклеточное пространство.
В межклеточной матриксе концевые пропептиды коллагенов I, II, III типов отщепляются специфическими проколлагенпептидазами
Образуются молекулы тропоколлагена – структурные единицы коллагеновых фибрилл.
Снижение активности ферментов (синдром Элерса – Данло – Русакова, тип VII) концевые пропептиды проколлагена не отщепляются и нарушается образование тропоколлагена и образование нормальный коллагеновых фибрилл.
Клинически – малый рост, искривление позвоночника, привычные вывихи суставов, высокая растяжимость кожи.
Переваривание белков и всасывание аминокислот. Биологическая ценность белков. Механизм транспорта аминокислот через клеточную мембрану. Роль ГГТП.
Химус поступает в 12пк. Низкое значение рН химуса вызывает в кишечнике выделение секретина, поступающего в кровь. Он стимулирует выделение из поджелудочной железы в тонкий кишечник панкреатического сока, содержащего НСО3-, что приводит к нейтрализации HCl желудочного сока и ингибированию пепсина, вследствие чего возрастает рН резко от 1,5 – 2,0 до 7,0. Поступление пептидов в тонкий кишечник вызывает секрецию другого гормона – холецистокинина, который стимулирует выделение панкреатических ферментов с оптимумом 7,5 – 8,0. Под действием ферментов поджелудочной железы и клеток кишечника завершается переваривание белков.
Активация трипсиногена: под действием энтеропептидазы. Она отщепляет с N – конца молекулы трипсиногена гексапептид Вал – (Асп)4 – Лиз. Изменение конформации оставшейся части полипептидной цепи приводит к формированию активного центра, образуется активный трипсин.
Образовавшийся трипсин активирует химотрипсиноген, из которого образуется несколько активных ферментов.
Под действием трипсина расщепляется пептидная связь между 15 и 16 аминокислотами, в результате чего образуется активный π – химотрипсин. Затем под действием π – химотрипсина отщепляется депиптид сер(14)-арг(15), что приводит к образованию δ – химотрипсина. Отщепление дипептида тре(147) – арг(148) завершает образование стабильной формы активного фермента – α – химотрипсина, который состоит из трёх полипептидных цепей, соединённых дисульфидными мостиками.
Остальные проферменты панкреатических протеаз (проэластаза и прокарбоксипептидазы А и В) также активируются трипсином путём частичного пртеолиза. В результате образуются ферменты – эластаза и карбоксипептидаза А и В.
Трипсин гидролизует пептидные связи, образованные карбоксильными группами аргинина и лизина.
Химотрипсины активны в отношении пептидных связей, образованных карбоксильными группами ароматических аминокислот (фен, тир, три).
Карбоксипептидазы А и В – цинкосодержащие ферменты, отщепляют С – концевые остатки аминокислот. КП А отщепляет аминокислоты с ароматическими или гидрофобными радикалами, а КП В – остатки аргинина и лизина.
Последний этап переваривания – гидролиз небольших пептидов, происходит под действием ферментов аминопептидаз и дипептидаз, которые синтезируются клетками тонкого кишечника в активной форме.
Транспорт двумя путями: через воротную систему печени, ведущую прямо в печень, и по лимфатическим сосудам, сообщающимся с кровью через грудной проток.
Всасывание L – аминокислот (не D – изомеров) – активный транспорт, с затратами энергии. Аминокислоты переносятся через кишечную стенку от слизистой её поверхности в кровь.
Перенос через щёточную каёмку переносчиками, многие из которых работают при участии Na – зависимых механизмав симпорта, подобно переносу глюкозы.
Механизм всасывания аминокислот в кишечнике: L – аминокислота поступает в энтероцит симпортом с ионом Na. Далее специфическая транслоказа переносит аминокислоту через мембрану в кровь. Обмен ионов натрия между клетками осуществляется путём первично – активного транспорта с помощью Na/K – АТФ-азы.
Одна из специфических транспортных систем для некоторых нейтральных аминокислот функционирует в кишечнике, полчках и, по-видимому, мозге. Эта система – γ – глутамильный цикл.
В ней участвует 6 ферментов, один из которых находится в клеточной мембране, остальные – в цитозоле.
Ключевая роль в транспорте аминокислот принадлежит ферменту γ – глутамилтрансферазе – гликопротеин, катализирует перенос γ – глутамильной группы от глутатиона на транспортируемую аминокислоту и последующий перенос комплекса в клетку.
Аминокислота, связанная с γ – глутамильным остатком, оказывается внутри клетки. Происходит отщепление γ – глутамильного остатка под действием фермента γ – глутамилциклотрансферазы.
Дипептид цистеинглицин расщепляется под действием пептидазы на 2 аминокислоты – цистеин и глицин.
В результате - перенос одной молекулы аминокислоты в клетку (внутриклеточную структуру).
Следующие три реакции обеспечивают регенерацию глутатиона, благодаря чему цикл повторяется многократно.
Для транспорта в клетку одной аминокислоты с участием γ – глутамильного цикла затрачивается 3 молекулы АТФ.
Азотистый баланс – разница между количеством азота, поступающего с пищей, и количеством выделяемого азота (в виде мочевины и аммонийных солей). Азотистое равновесие – поступающий азот равен выделяемому. Положительный баланс - поступает больше, чем выводится. Отрицательный – выделяется больше, чем поступает. Минимальное количество белков, необходимое для поддержания азотистого равновесия = 30 – 50 г/сут, оптимальное количество при средней физической нагрузке = 100-120 г/сут.
Полноценность в питании: Незаменимые аминокислоты – те, синтез которых сложен и неэкономичен для организма. Их выгоднее получать с пищей. Это - фенилаланин, метионин, треонин, триптофан, валин, лизин, лейцин, изолейцин. Аргинин и гистидин – заменимые – необходимо дополнительное их поступление в организм с пищей, особенно детям. К ним также относят глицин, аспарагиновую кислоту, аспарагин, глутаминовую кислоту, глутамин, серин, пролин, аланин. Питательная ценность белка зависит от его аминокислотного состава и способности усваиваться организмам.
Норма белка в питании: принятые нормы белкового питания для взрослых и детей учитывают климатические условия, профессию, условия труда и др. Взрослый человек при средней физической нагрузке должен получать 100-120 г белка в сутки. При тяжёлой нагрузке – 130-150г. Детям до 12 лет достаточно 50-70 г белка в сутки. При этом подразумевается, что в пищу входят разнообразные белки животного и растительного происхождения.
Перед вами двое больных с анемией. У одного - дефицит витамина В6, у другого – В12. Какие исследования следует провести, чтобы отдифференцировать эти состояния? Как изменятся их результаты?
При дефиците В12 из-за разрушения в красном костном мозге мегалобластов будет повышен уровень билирубина. При дефиците В6, т.к. он является коферментом синтеза гема, будет снижено количество гемоглобина.
Билет 20.
Посттранскрипционный процессинг. Основные этапы. Значение. Регуляция биосинтеза белка на уровне транскрипции.
Первичные транскрипты мРНК, прежде чем будут использованы в ходе синтеза белка, подвергаются ряду вокалентной модификации. Эти модификации необходимы для функционирования мРНК в качестве матрицы.
Модификация 5’ – конца.
Начинается на стадии элонгации.
Когда длина первичного транскрипта достигает примерно 30 нуклеотидных остатков, происходит кэпирование его 5’ – конца гуанилилтрансферазой, которая гидролизует макроэргическую связь в молекуле ГТФ и присоединяет нуклеотиддифосфатный остаток 5’ – фосфатной группой к 5’ – концу синтезированного фрагмента РНК с образованием 5’, 5’ – фосфодиэфирной связи.
Последующее метилирование остатка гуанина в составе ГТФ с образование N7-метилгуанозина завершает формирование кэпа.
Модифицированные 5’ – конец обеспечивает инициацию трансляции, удлиняет время жизни мРНК, защищая её от действия 5’ – экзонуклеаз в цитоплазме.
Кэпирование необходимо для инициации синтеза белка, так как инициирующие триплеты AUG, GUG распознаются рибосомой только если присутствует кэп. Наличие кэпа также нужно для работы сложной ферментной системы, обеспечивающей удаление интронов.
3’ – конец транскриптов, синтезированных РНК – полимеразой II, также подвергаются модификациям, при которых специальным ферментом полиА – полимеразой формируется полиА – последовательность (полиА – «хвост»), состоящая из 100-200 остатков адениловой кислоты.
Сигнал к началу полиаденилирования – последовательность –AAUAAA- на растущей цепи РНК
К 3’ – концу в точке разрыва полиА – полимераза наращивает полиА – «хвост». Наличие полиА – последовательности на 3’ – конце облегчает выход мРНК из ядра и замедляет её годролиз в цитоплазме.
Последовательности нуклеотидов, присутствующие в ДНК, но не входящие в состав зрелой мРНК – интроны, а последовательности, присутствующие в мРНК, - кодирующие, или экзоны.
Первичный транскрипт – строго комплементарная матрице нуклеиновая кислота (пре – мРНК), содержащая как экзоны, так и интроны. Длина – от 80 до 1000 нуклеотидов.
Последовательности интронов «вырезаются» из первичного транскрипта, концы экзонов соединяются друг с другом. Такая модификация РНК – сплайсинг. Происходит в ядре, в цитоплазму поступает уже «зрелая» мРРНРНК.
Процесс «вырезания» интронов протекает при участии малых ядерных рибонуклеопротеинов (мяРНП), в состав которых входит малая ядерная РНК, нуклеотидная цепь которой связана с белковым остовом, состоящим из нескольких протомеров.
первичный транскрипт тРНК содержит около 100 нуклеотидов, а после процессинга – 70-90 нуклеотидных остатков.
Происходят при участии РНК-аз (рибонуклеаз).
Формирование 3’ – конца тРНК катализирует РНК-аза, представляющая собой 3’ – экзонуклеазу, «отрезающую» по одному нуклеотиду, пока не достигает последовательности
-ССА, одинаковой для всех тРНК.
Пре – тРНК содержит всего один интрон, состоящий из 14-16 нуклеотидов. Удаление интрона и сплайсинг приводят к формированию структуры, называемой «антикодон» - триплета нуклеотидов, обеспечивающего взаимодействие тРНК с комплементарным кодоном мРНК в ходе синтеза белков.
Гены рРНК транскрибируются РНК – полимеразой I с образованием идентичных транскриптов. Первичные транскрипты имеют длину около 13000 нуклеотидных остатков (45S рРНК).
Прежде чем покинуть ядро в составе рибосомной частицы, молекула 45S рРНК подвергается процессингу, в результате образуется 28S рРНК (около 2000 нуклеотидов) и 5,8S рРНК (около 160 нуклеотидов), которые являются компонентами рибосом. Остальная часть транскрипта разрушается в ядре.
Рибосома – органелла клетки, участвующая в биосинтезе белка. Рибосома эукариотов состоят из двух, большой и малой, субъединиц: 60S и 40S. Белки рибосом выполняют структурную, регуляторную и каталитическую функции.
Транскрипция – первая стадия реализации генетической информации в клетке. В ходе процессинга образуются молекулы мРНК, служащие матрицей для синтеза белков, а также транспортные, рибосомальные и другие виды молекул РНК, выполняющие структурные, адапторные и каталитические функции.
Происходит в ядре. ДНК служит только матрицей и в ходе транскрипции не изменяется.
Рибонуклеозидтрифосфаты (ЦТФ, ГТФ, АТФ, УТФ) – субстраты и источники энергии, необходимые для протекания полимеразной реакции, образования 3’, 5’ – фосфодиэфирной связи между рибонуклеозидмонофосфатами.
Синтез РНК начинается в определённых последовательностях (сайтах) ДНК – промоторах, и завершается в терминирующих участках (сайты терминации).
Участок ДНК, ограниченный прогмотором и сайтом терминации – единица транскрипции – транскрипт.
Транскрипционные факторы – белки, взаимодействующие с определёнными регуляторными сайтами и ускоряющие или замедляющие процесс транскрипции. Соотношение информативной и неинформативной частей в транскриптонах = 1:9(эукариоты).
Биосинтез РНК осуществляется ДНК – зависимыми РНК – полимеразами. В ядрах эукариотов обнаружены 3 специализированные РНК – полимеразы: РНК – полимераза I, синтезирующая пре – рРНК, РНк – полимераза II, синтезирующая пре – мРНК, РНК – полимераза III – синтезирующая пре – тРНК.
РНК – полимеразы – олигомерные ферменты, состоящие из нескольких субъединиц - 2α, β, β’, σ. Субъединица σ выполняет регуляторну. Функцию, это один из факторов инициации транскрипции.
РНК – полимеразы I, II, III, узнающие разные промоторв, содержат разные по стороению субъединицы σ.
Инициации. Характеризуется активацией промотора с помощью белка – ТАТА – фактора. Его присоединение облегчает взаимодействие промотора с РНК – полимеразой. Образуется транскрипционная вилка.
Элонгация. Её факторы повышают активность РНК – полимеразы и облегчают расхождение цепей ДНК. Синтез РНК идёт от 5’- к 3’ – концу комплементарно матричной цепи ДНК.
Терминация. Раскручивание двойной спирали ДНК в области терминации делает его доступным для фактора терминации. Завершается синтез РНК в строго определённых участках матрицы – терминаторах (сайты терминации). Фактор терминации облегчает отделение первичного транскрипта (пре – мРНК), комплементарного матрице, и РНК – полимеразы от матрицы. РНК – полимераза может вступить в следующийц цикл транскрипции после присоединения субъединицы σ.
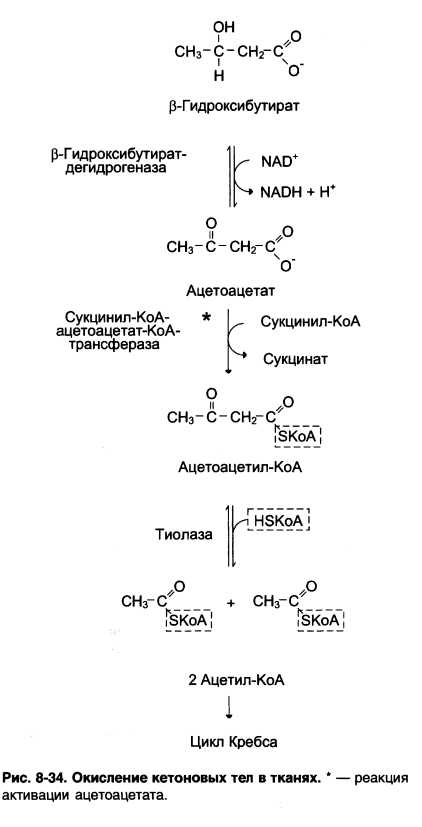
Образование кетоновых тел. Биологическая роль процесса. Причины и последствия кетоза.
В печени часть жирных кислот превращается в кетоновые тела, которые окисляются мозгом, нервной тканью, мышцами, обеспечивая достаточное количество энергии для синтеза АТФ и уменьшая потребление глюкозы. К кетоновым телам относят β – гидроксибутират, ацетоацетат и ацетон. Первые две молекулы могут окисляться в тканях, обеспечивая синтез АТФ. Ацетон образуется только при высоких концентрациях кетоновых тел в крови и, выделяясь с мочой, выдыхаемым воздухом и потом, позволяет организму избавляться от избытка кетоновых тел.
При низком соотношении инсулин – глюкагон в крови в жировой ткани активируется распад жиров. Жирные кислоты поступают в печень в большом количестве, чем в норме. Скорость реакций ЦТК в этих условиях снижена, так как оксалоацетат используется для ГНГ. В результате скорость образования ацетил – КоА превышает способность ЦТК окислять его. Ацетил – КоА накапливается в митохондриях печени и используется для синтеза кетоновых тел. Синтез кетоновых тел происходит только в митохондриях печени.
Синтез начинается с взаимодействия двух молекул ацетил – КоА, которые под действием фермента тиолазы образуют ацетоацетил – КоА. С ним взаимодействует третья молекула ацетил – КоА, образуя 3-гидрокси – 3 – метилглутарил – КоА (ГМГ – КоА). Эту реакцию катализирует расщепление ГМГ – КоА на свободный ацетоацетат и ацетил – КоА.
Ацетоацетат может выделяться в кровь или превращаться в печени в β – гидроксибутират восстановлением.
При активном β – окислении создается высокая концентрация НАДН, что способствует превращению большей части ацетоацетата в β – гидроксибутират. Именно он свляется основным кетоновым телом. При голодании для многих тканей жирные кислоты и кетоновые тела становятся основными топливными молекулами. Глюкоза используется в первую очередь нервной тканью.
При высокой концентрации ацетоацетата часть его неферментативно декарбоксилируется, превращаясь в ацетон. Ацетон не утилизируется тканями, но выделяется с выдыхаемым воздухом и мочой. Таким путём организм удаляет избыточное количество кетоновых тел, которые не успевают окисляться, но, являясь водорастворимыми кислотами, вызывают ацидоз.
Регуляция синтеза: ГМГ – КоА – синтаза. 1) индуцируемый фермент, его синтез увеличивается при повышении концентрации жирных кислот в крови. Это происходит при мобилизации жиров из жировой ткани под действием глюкагона, адреналина, т.е. при голодании или нагрузке. 2) ингибируется высокими концентрациями свободного кофермента А. 3) когда поступление жирных кислот в клетки увеличивается, КоА связывается с ними, концентрация свободного КоА снижается, и фермент становится активным. 4) если поступление жирных кислот в клетки печени уменьшается, то увеличивается концентрация свободного КоА, ингибирующего фермент. Следовательно, скорость синтеза кетоновых тел в печени зависит от поступления жирных кислот.
Синтез кетоновых тел в периферических тканях. Рисунок 8-34.
Кетоацидоз. В норме концентрация кетоновых тел в крови = 1-3мг/мл. Увеличение кетоновых тел в крови - кетонемия, выделение с мочой – кетонурия. Накопление кетоновых тел в организме приводит к кетоацидозу: уменьшению щелочного резерва (компенсаторному ацидозу), а в тяжёлых случаях – к сдвигу рН (некомпенсированному ацидозу), так как кетоновые тела (кроме ацетона) – водорастворимые органические кислоты, способные к диссоциации: СН3-СО-СН2-СООН <-> СН3-СО-СН2-СОО+Н.
Назначьте биохимическое обследование больному с подозрением на поражение поджелудочной железы.
Проверить активность пищеварительных ферментов поджелудочной железы – амилазы, панкреатической липазы, химотрипсина и трипсина.
Билет 21
2.Тироксин. Влияние на обмен веществ. Изменения обмена при гипо- и гипертиреозе.
Тироксин - гормон щитовидной железы. После частичного превращения в трийодтиронин (в печени и почках) и перехода в клетки организма, оказывает влияние на развитие и рост тканей, на обмен веществ. В малых дозах оказывает анаболическое действие на белковый и жировой обмен. В средних дозах стимулирует рост и развитие, повышает потребность тканей в кислороде, стимулирует метаболизм белков, жиров и углеводов, повышает функциональную активность сердечно-сосудистой системы и центральной нервной системы. В больших дозах угнетает выработку тиротропин-рилизинг гормона гипоталамуса и тиреотропного гормона гипофиза. Тироксин влияет на обмен веществ, развитие тканей, в небольших дозах проявляет себя как анаболик (помогает увеличивать мышечный объем), в средних дозах активизирует жировой, белковый, углеводный обмен, положительно сказывается на состоянии нервной системы, сосудов, сердца.
Гипотиреоз развивается вследствие недостаточности йодтиронинов. Обычно гипотиреоз связан с недостаточностью функции щитовидной железы, но может возникать и при заболеваниях гипофиза и гипоталамуса. Гипотиреоз у новорождённых приводит к развитию кретинизма, который проявляется множественными врождёнными нарушениями и тяжёлой необратимой задержкой умственного развития. Наиболее тяжёлые формы гипотиреоза, сопровождающиеся слизистым отёком кожи и подкожной клетчатки, обозначают термином "микседема". Отёчность обусловлена избыточным накоплением гликозаминогликанов и воды. В подкожной клетчатке накапливается глюкуроновая и в меньшей степени хондроитинсерная кислоты. Характерные проявления заболевания: снижение частоты сердечных сокращений, вялость, сонливость, непереносимость холода, сухость кожи. Эти симптомы развиваются вследствие снижения основного обмена, скорости гликолиза, мобилизации гликогена и жиров, потребления глюкозы мышцами, уменьшения мышечной массы и снижения теплопродукции. В настоящее время у взрослых людей частой причиной гипотиреоза является хронический аутоиммунный тиреоидит, приводящий к нарушению синтеза йодтиронинов (зоб Хашимото).
Гипертиреоз возникает вследствие повышенной продукции йодтиронинов. Диффузный токсический зоб (базедова болезнь, болезнь Грейвса) - наиболее распространённое заболевание щитовидной железы. При этом заболевании отмечают увеличение размеров щитовидной железы (зоб), повышение концентрации йодтиронинов в 2-5 раз и развитие тиреотоксикоза. Характерные признаки тиреотоксикоза: увеличение основного обмена, учащение сердцебиений, мышечная слабость, снижение массы тела (несмотря на повышенный аппетит) , потливость, повышение температуры тела, тремор и экзофтальм (пучеглазие). Гипертиреоз может возникать в результате различных причин: развитие опухоли, тиреоидит, избыточное поступление йода и йодсодер-жащих препаратов, аутоиммунные реакции. В большей мере усиливаются процессы катаболизма, о чём свидетельствует отрицательный азотистый баланс.
3.Почему, если в крови повышены таг хиломикронов, рекомендуют сократить количество пищевых жиров, а если таг повышены за счет лпонп, то рекомендуют сократить потребление углеводов?
В составе хиломикронов экзогенные жиры доставляются в органы и ткани. Липопротеинлипаза (ЛП—липаза) — фермент, обеспечивающий потребление экзогенных жиров тканями. ЛП—липаза, располагающаяся в эндотелии сосудов, взаимодействует с хиломикронами кровотока и гидролизует триацилглирины на глицерин и жирные кислоты, которые поступают в клетку. По мере извлечения ТАГ из хиломикронов последние превращаются в остаточные хиломикроны и затем поступают в печень.
Жиры, как и гликоген, являются формами депонирования энергетического материала. Причем жиры — наиболее долговременные и более эффективные источники энергии. При голодании запасы жира у человека истощаются за 5—7 недель, тогда как гликоген полностью расходуется примерно за сутки. Если поступление жира превышает потребности организма в энергии , то жир депонируется в адипоцитах — специализированных клетках жировой ткани. Кроме того, если количество поступающих углеводов больше, чем надо для депонирования в виде гликогена, то часть глюкозы также превращается в жиры . Таким образом, жиры в жировой ткани накапливаются в результате трех процессов:
поступают из хиломикронов, которые приносят экзогенные жиры из кишечника
поступают из ЛОНП, которые транспортируют эндогенные жиры, синтезированные в печени из глюкозы
образуются из глюкозы в самих клетках жировой ткани.
В первом и во втором случае жиры в составе липопротеинов гидролизуются ЛП—липазой и в клетку поступают жирные кислоты, которые затем используются для синтеза ТАГ. Перед включением в ТАГ жирные кислоты сначала активируются путем образования тиоэфиров кофермента А, а затем взаимодействуют с глицеролфосфатом. Следовательно, синтез ТАГ может протекать только в присутствии глюкозы, из которой в процессе гликолиза образуется диаксиацетонфосфат. Инсулин стимулирует синтез ТАГ, потому что в его присутствии повышается проницаемость мембран клеток жировой ткани для глюкозы.
Билет 19
Биосинтез проколлагена и его превращение в коллаген. Фибриллогенез. Возможные нарушения.
Проколлаген - внутриклеточный предшественник коллагена, синтезируемый на полирибосомах, связанных с мембранами эндоплазматической сети.
Синтез и созревание коллагена – многоэтапный процесс, начинающийся в клетке и завершающийся в межклеточном матриксе. Включает в себя целый ряд посттрансляционных изменений: гидроксилирование пролина и лизина с образованием гидроксипролина и гидроксилизина; гликозилирование гидроксилизина; частичный протеолиз – отщепление «сигнального» пептида, а также N- и С – концевых пропептидов; образование тройной спирали.
Синтез полипептидный цепей коллагена.
Синтезируются на полирибосомах, связанных с мембранами ЭР, в виде более длинных, чем зрелые цепи, предшественников – препро – α – цепей.
Эти предшественники имеют гидрофобный «сигнальный» пептид на N – конце, содержащий около 100 аминокислот.
Функция сигнального пептида – ориентация синтеза пептидных цепей в полости ЭР. После выполнения функции – отщепляется.
Синтезированная молекула проколлагена содержит дополнительные участки – N- и С - концевые пропептиды, в составе которых остатки цистеина, образующие внутри- и межцепочечные S-S связи.
Посттрансляционные модификации коллагена.
Начинается в период трансляции коллагеновой мРНК на рибосомах
Продолжается на растущей полипептидной цепи вплоть до отделения от рибосом.
После образования тройной спирали дальнейшее гидроксилирование пролиновых и лизиловых остатков прекращается.
Реакции гидроксилирования катализируют оксигеназы, связанные с мембранами микросом.
Пролиловые и лизиловые остатки в Y – положении пептида подвергаются действию пролил-4-гидроксилазы и лизил-5-гидроксилазы.
Необходимые компоненты – α – кетоглутарат, кислород и витамин С.
Донор атома кислорода, присоединяющегося к С – 4 пролина, - молекула кислорода.
Гидроксилазы пролина и лизина содержат в активном центре атом железа II. Для сохранения атома железа в ферроформе необходим восстанавливающий агент, роль которого выполняет аскорбиновая кислота, легко окисляющаяся в дегидроаскорбиновую кислоту.
После завершения гидроксилирования при участии гидроксилтрансфераз в состав молекулы проколлагена вводятся углеводные группы – галактоза, дисахарид галактозилглюкоза.
Образуют ковалентную О – гликозидную связь с 5-ОН-группой гидроксилизина.
Гликозилирование происходит в коллагене, езё не претерпевшем спирализации
Завершается после образования тройной спирали
Каждая про – α – цепь соединяется водородными связями с двумя другими про – α – цепями, образуя тройную спираль проколлагена.
Происходит ещё в просвете ЭР и начинаются после образования межцепочечных дисульфидных мостиков в области С – концевых пропептидов.
Из ЭР молекулы проколлагена перемещаются в аппарат Гольджи, включаются в секреторные пузырьки и секретируются в межклеточное пространство.
В межклеточной матриксе концевые пропептиды коллагенов I, II, III типов отщепляются специфическими проколлагенпептидазами
Образуются молекулы тропоколлагена – структурные единицы коллагеновых фибрилл.
Снижение активности ферментов (синдром Элерса – Данло – Русакова, тип VII) концевые пропептиды проколлагена не отщепляются и нарушается образование тропоколлагена и образование нормальный коллагеновых фибрилл.
Клинически – малый рост, искривление позвоночника, привычные вывихи суставов, высокая растяжимость кожи.
Переваривание белков и всасывание аминокислот. Биологическая ценность белков. Механизм транспорта аминокислот через клеточную мембрану. Роль ГГТП.
Химус поступает в 12пк. Низкое значение рН химуса вызывает в кишечнике выделение секретина, поступающего в кровь. Он стимулирует выделение из поджелудочной железы в тонкий кишечник панкреатического сока, содержащего НСО3-, что приводит к нейтрализации HCl желудочного сока и ингибированию пепсина, вследствие чего возрастает рН резко от 1,5 – 2,0 до 7,0. Поступление пептидов в тонкий кишечник вызывает секрецию другого гормона – холецистокинина, который стимулирует выделение панкреатических ферментов с оптимумом 7,5 – 8,0. Под действием ферментов поджелудочной железы и клеток кишечника завершается переваривание белков.
Активация трипсиногена: под действием энтеропептидазы. Она отщепляет с N – конца молекулы трипсиногена гексапептид Вал – (Асп)4 – Лиз. Изменение конформации оставшейся части полипептидной цепи приводит к формированию активного центра, образуется активный трипсин.
Образовавшийся трипсин активирует химотрипсиноген, из которого образуется несколько активных ферментов.
Под действием трипсина расщепляется пептидная связь между 15 и 16 аминокислотами, в результате чего образуется активный π – химотрипсин. Затем под действием π – химотрипсина отщепляется депиптид сер(14)-арг(15), что приводит к образованию δ – химотрипсина. Отщепление дипептида тре(147) – арг(148) завершает образование стабильной формы активного фермента – α – химотрипсина, который состоит из трёх полипептидных цепей, соединённых дисульфидными мостиками.
Остальные проферменты панкреатических протеаз (проэластаза и прокарбоксипептидазы А и В) также активируются трипсином путём частичного пртеолиза. В результате образуются ферменты – эластаза и карбоксипептидаза А и В.
Трипсин гидролизует пептидные связи, образованные карбоксильными группами аргинина и лизина.
Химотрипсины активны в отношении пептидных связей, образованных карбоксильными группами ароматических аминокислот (фен, тир, три).
Карбоксипептидазы А и В – цинкосодержащие ферменты, отщепляют С – концевые остатки аминокислот. КП А отщепляет аминокислоты с ароматическими или гидрофобными радикалами, а КП В – остатки аргинина и лизина.
Последний этап переваривания – гидролиз небольших пептидов, происходит под действием ферментов аминопептидаз и дипептидаз, которые синтезируются клетками тонкого кишечника в активной форме.
Транспорт двумя путями: через воротную систему печени, ведущую прямо в печень, и по лимфатическим сосудам, сообщающимся с кровью через грудной проток.
Всасывание L – аминокислот (не D – изомеров) – активный транспорт, с затратами энергии. Аминокислоты переносятся через кишечную стенку от слизистой её поверхности в кровь.
Перенос через щёточную каёмку переносчиками, многие из которых работают при участии Na – зависимых механизмав симпорта, подобно переносу глюкозы.
Механизм всасывания аминокислот в кишечнике: L – аминокислота поступает в энтероцит симпортом с ионом Na. Далее специфическая транслоказа переносит аминокислоту через мембрану в кровь. Обмен ионов натрия между клетками осуществляется путём первично – активного транспорта с помощью Na/K – АТФ-азы.
Одна из специфических транспортных систем для некоторых нейтральных аминокислот функционирует в кишечнике, полчках и, по-видимому, мозге. Эта система – γ – глутамильный цикл.
В ней участвует 6 ферментов, один из которых находится в клеточной мембране, остальные – в цитозоле.
Ключевая роль в транспорте аминокислот принадлежит ферменту γ – глутамилтрансферазе – гликопротеин, катализирует перенос γ – глутамильной группы от глутатиона на транспортируемую аминокислоту и последующий перенос комплекса в клетку.
Аминокислота, связанная с γ – глутамильным остатком, оказывается внутри клетки. Происходит отщепление γ – глутамильного остатка под действием фермента γ – глутамилциклотрансферазы.
Дипептид цистеинглицин расщепляется под действием пептидазы на 2 аминокислоты – цистеин и глицин.
В результате - перенос одной молекулы аминокислоты в клетку (внутриклеточную структуру).
Следующие три реакции обеспечивают регенерацию глутатиона, благодаря чему цикл повторяется многократно.
Для транспорта в клетку одной аминокислоты с участием γ – глутамильного цикла затрачивается 3 молекулы АТФ.
Азотистый баланс – разница между количеством азота, поступающего с пищей, и количеством выделяемого азота (в виде мочевины и аммонийных солей). Азотистое равновесие – поступающий азот равен выделяемому. Положительный баланс - поступает больше, чем выводится. Отрицательный – выделяется больше, чем поступает. Минимальное количество белков, необходимое для поддержания азотистого равновесия = 30 – 50 г/сут, оптимальное количество при средней физической нагрузке = 100-120 г/сут.
Полноценность в питании: Незаменимые аминокислоты – те, синтез которых сложен и неэкономичен для организма. Их выгоднее получать с пищей. Это - фенилаланин, метионин, треонин, триптофан, валин, лизин, лейцин, изолейцин. Аргинин и гистидин – заменимые – необходимо дополнительное их поступление в организм с пищей, особенно детям. К ним также относят глицин, аспарагиновую кислоту, аспарагин, глутаминовую кислоту, глутамин, серин, пролин, аланин. Питательная ценность белка зависит от его аминокислотного состава и способности усваиваться организмам.
Норма белка в питании: принятые нормы белкового питания для взрослых и детей учитывают климатические условия, профессию, условия труда и др. Взрослый человек при средней физической нагрузке должен получать 100-120 г белка в сутки. При тяжёлой нагрузке – 130-150г. Детям до 12 лет достаточно 50-70 г белка в сутки. При этом подразумевается, что в пищу входят разнообразные белки животного и растительного происхождения.
Перед вами двое больных с анемией. У одного - дефицит витамина В6, у другого – В12. Какие исследования следует провести, чтобы отдифференцировать эти состояния? Как изменятся их результаты?
При дефиците В12 из-за разрушения в красном костном мозге мегалобластов будет повышен уровень билирубина. При дефиците В6, т.к. он является коферментом синтеза гема, будет снижено количество гемоглобина.
Билет 20.
Посттранскрипционный процессинг. Основные этапы. Значение. Регуляция биосинтеза белка на уровне транскрипции.
Первичные транскрипты мРНК, прежде чем будут использованы в ходе синтеза белка, подвергаются ряду вокалентной модификации. Эти модификации необходимы для функционирования мРНК в качестве матрицы.
Модификация 5’ – конца.
Начинается на стадии элонгации.
Когда длина первичного транскрипта достигает примерно 30 нуклеотидных остатков, происходит кэпирование его 5’ – конца гуанилилтрансферазой, которая гидролизует макроэргическую связь в молекуле ГТФ и присоединяет нуклеотиддифосфатный остаток 5’ – фосфатной группой к 5’ – концу синтезированного фрагмента РНК с образованием 5’, 5’ – фосфодиэфирной связи.
Последующее метилирование остатка гуанина в составе ГТФ с образование N7-метилгуанозина завершает формирование кэпа.
Модифицированные 5’ – конец обеспечивает инициацию трансляции, удлиняет время жизни мРНК, защищая её от действия 5’ – экзонуклеаз в цитоплазме.
Кэпирование необходимо для инициации синтеза белка, так как инициирующие триплеты AUG, GUG распознаются рибосомой только если присутствует кэп. Наличие кэпа также нужно для работы сложной ферментной системы, обеспечивающей удаление интронов.
3’ – конец транскриптов, синтезированных РНК – полимеразой II, также подвергаются модификациям, при которых специальным ферментом полиА – полимеразой формируется полиА – последовательность (полиА – «хвост»), состоящая из 100-200 остатков адениловой кислоты.
Сигнал к началу полиаденилирования – последовательность –AAUAAA- на растущей цепи РНК
К 3’ – концу в точке разрыва полиА – полимераза наращивает полиА – «хвост». Наличие полиА – последовательности на 3’ – конце облегчает выход мРНК из ядра и замедляет её годролиз в цитоплазме.
Последовательности нуклеотидов, присутствующие в ДНК, но не входящие в состав зрелой мРНК – интроны, а последовательности, присутствующие в мРНК, - кодирующие, или экзоны.
Первичный транскрипт – строго комплементарная матрице нуклеиновая кислота (пре – мРНК), содержащая как экзоны, так и интроны. Длина – от 80 до 1000 нуклеотидов.
Последовательности интронов «вырезаются» из первичного транскрипта, концы экзонов соединяются друг с другом. Такая модификация РНК – сплайсинг. Происходит в ядре, в цитоплазму поступает уже «зрелая» мРРНРНК.
Процесс «вырезания» интронов протекает при участии малых ядерных рибонуклеопротеинов (мяРНП), в состав которых входит малая ядерная РНК, нуклеотидная цепь которой связана с белковым остовом, состоящим из нескольких протомеров.
первичный транскрипт тРНК содержит около 100 нуклеотидов, а после процессинга – 70-90 нуклеотидных остатков.
Происходят при участии РНК-аз (рибонуклеаз).
Формирование 3’ – конца тРНК катализирует РНК-аза, представляющая собой 3’ – экзонуклеазу, «отрезающую» по одному нуклеотиду, пока не достигает последовательности
-ССА, одинаковой для всех тРНК.
Пре – тРНК содержит всего один интрон, состоящий из 14-16 нуклеотидов. Удаление интрона и сплайсинг приводят к формированию структуры, называемой «антикодон» - триплета нуклеотидов, обеспечивающего взаимодействие тРНК с комплементарным кодоном мРНК в ходе синтеза белков.
Гены рРНК транскрибируются РНК – полимеразой I с образованием идентичных транскриптов. Первичные транскрипты имеют длину около 13000 нуклеотидных остатков (45S рРНК).
Прежде чем покинуть ядро в составе рибосомной частицы, молекула 45S рРНК подвергается процессингу, в результате образуется 28S рРНК (около 2000 нуклеотидов) и 5,8S рРНК (около 160 нуклеотидов), которые являются компонентами рибосом. Остальная часть транскрипта разрушается в ядре.
Рибосома – органелла клетки, участвующая в биосинтезе белка. Рибосома эукариотов состоят из двух, большой и малой, субъединиц: 60S и 40S. Белки рибосом выполняют структурную, регуляторную и каталитическую функции.
Транскрипция – первая стадия реализации генетической информации в клетке. В ходе процессинга образуются молекулы мРНК, служащие матрицей для синтеза белков, а также транспортные, рибосомальные и другие виды молекул РНК, выполняющие структурные, адапторные и каталитические функции.
Происходит в ядре. ДНК служит только матрицей и в ходе транскрипции не изменяется.
Рибонуклеозидтрифосфаты (ЦТФ, ГТФ, АТФ, УТФ) – субстраты и источники энергии, необходимые для протекания полимеразной реакции, образования 3’, 5’ – фосфодиэфирной связи между рибонуклеозидмонофосфатами.
Синтез РНК начинается в определённых последовательностях (сайтах) ДНК – промоторах, и завершается в терминирующих участках (сайты терминации).
Участок ДНК, ограниченный прогмотором и сайтом терминации – единица транскрипции – транскрипт.
Транскрипционные факторы – белки, взаимодействующие с определёнными регуляторными сайтами и ускоряющие или замедляющие процесс транскрипции. Соотношение информативной и неинформативной частей в транскриптонах = 1:9(эукариоты).
Биосинтез РНК осуществляется ДНК – зависимыми РНК – полимеразами. В ядрах эукариотов обнаружены 3 специализированные РНК – полимеразы: РНК – полимераза I, синтезирующая пре – рРНК, РНк – полимераза II, синтезирующая пре – мРНК, РНК – полимераза III – синтезирующая пре – тРНК.
РНК – полимеразы – олигомерные ферменты, состоящие из нескольких субъединиц - 2α, β, β’, σ. Субъединица σ выполняет регуляторну. Функцию, это один из факторов инициации транскрипции.
РНК – полимеразы I, II, III, узнающие разные промоторв, содержат разные по стороению субъединицы σ.
Инициации. Характеризуется активацией промотора с помощью белка – ТАТА – фактора. Его присоединение облегчает взаимодействие промотора с РНК – полимеразой. Образуется транскрипционная вилка.
Элонгация. Её факторы повышают активность РНК – полимеразы и облегчают расхождение цепей ДНК. Синтез РНК идёт от 5’- к 3’ – концу комплементарно матричной цепи ДНК.
Терминация. Раскручивание двойной спирали ДНК в области терминации делает его доступным для фактора терминации. Завершается синтез РНК в строго определённых участках матрицы – терминаторах (сайты терминации). Фактор терминации облегчает отделение первичного транскрипта (пре – мРНК), комплементарного матрице, и РНК – полимеразы от матрицы. РНК – полимераза может вступить в следующийц цикл транскрипции после присоединения субъединицы σ.
Образование кетоновых тел. Биологическая роль процесса. Причины и последствия кетоза.
В печени часть жирных кислот превращается в кетоновые тела, которые окисляются мозгом, нервной тканью, мышцами, обеспечивая достаточное количество энергии для синтеза АТФ и уменьшая потребление глюкозы. К кетоновым телам относят β – гидроксибутират, ацетоацетат и ацетон. Первые две молекулы могут окисляться в тканях, обеспечивая синтез АТФ. Ацетон образуется только при высоких концентрациях кетоновых тел в крови и, выделяясь с мочой, выдыхаемым воздухом и потом, позволяет организму избавляться от избытка кетоновых тел.
При низком соотношении инсулин – глюкагон в крови в жировой ткани активируется распад жиров. Жирные кислоты поступают в печень в большом количестве, чем в норме. Скорость реакций ЦТК в этих условиях снижена, так как оксалоацетат используется для ГНГ. В результате скорость образования ацетил – КоА превышает способность ЦТК окислять его. Ацетил – КоА накапливается в митохондриях печени и используется для синтеза кетоновых тел. Синтез кетоновых тел происходит только в митохондриях печени.
Синтез начинается с взаимодействия двух молекул ацетил – КоА, которые под действием фермента тиолазы образуют ацетоацетил – КоА. С ним взаимодействует третья молекула ацетил – КоА, образуя 3-гидрокси – 3 – метилглутарил – КоА (ГМГ – КоА). Эту реакцию катализирует расщепление ГМГ – КоА на свободный ацетоацетат и ацетил – КоА.
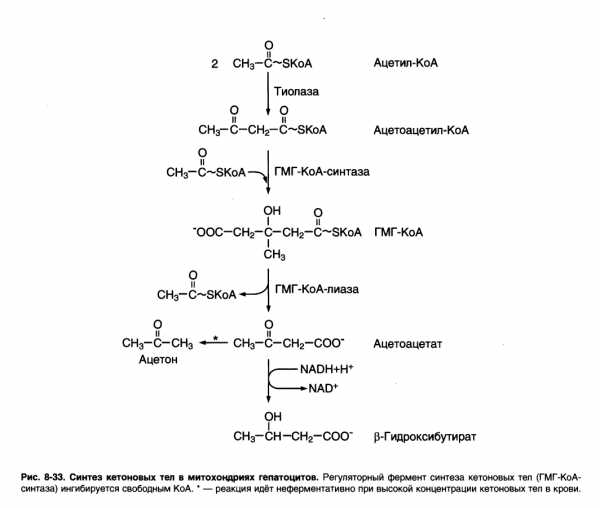
Ацетоацетат может выделяться в кровь или превращаться в печени в β – гидроксибутират восстановлением.
При активном β – окислении создается высокая концентрация НАДН, что способствует превращению большей части ацетоацетата в β – гидроксибутират. Именно он свляется основным кетоновым телом. При голодании для многих тканей жирные кислоты и кетоновые тела становятся основными топливными молекулами. Глюкоза используется в первую очередь нервной тканью.
При высокой концентрации ацетоацетата часть его неферментативно декарбоксилируется, превращаясь в ацетон. Ацетон не утилизируется тканями, но выделяется с выдыхаемым воздухом и мочой. Таким путём организм удаляет избыточное количество кетоновых тел, которые не успевают окисляться, но, являясь водорастворимыми кислотами, вызывают ацидоз.
Регуляция синтеза: ГМГ – КоА – синтаза. 1) индуцируемый фермент, его синтез увеличивается при повышении концентрации жирных кислот в крови. Это происходит при мобилизации жиров из жировой ткани под действием глюкагона, адреналина, т.е. при голодании или нагрузке. 2) ингибируется высокими концентрациями свободного кофермента А. 3) когда поступление жирных кислот в клетки увеличивается, КоА связывается с ними, концентрация свободного КоА снижается, и фермент становится активным. 4) если поступление жирных кислот в клетки печени уменьшается, то увеличивается концентрация свободного КоА, ингибирующего фермент. Следовательно, скорость синтеза кетоновых тел в печени зависит от поступления жирных кислот.
Синтез кетоновых тел в периферических тканях. Рисунок 8-34.
Кетоацидоз. В норме концентрация кетоновых тел в крови = 1-3мг/мл. Увеличение кетоновых тел в крови - кетонемия, выделение с мочой – кетонурия. Накопление кетоновых тел в организме приводит к кетоацидозу: уменьшению щелочного резерва (компенсаторному ацидозу), а в тяжёлых случаях – к сдвигу рН (некомпенсированному ацидозу), так как кетоновые тела (кроме ацетона) – водорастворимые органические кислоты, способные к диссоциации: СН3-СО-СН2-СООН <-> СН3-СО-СН2-СОО+Н.
Назначьте биохимическое обследование больному с подозрением на поражение поджелудочной железы.
Проверить активность пищеварительных ферментов поджелудочной железы – амилазы, панкреатической липазы, химотрипсина и трипсина.
Жировой обмен - Справочник химика 21
Нарушения жирового обмена. В жировом обмене велика роль печени. В печени вырабатывается желчь, а, как указывалось выше, желчные кислоты активируют липазу, способствуют эмульгированию жиров, всасыванию жирных кислот и холестерина. Следовательно, заболевания печени, связанные с нарушением секреции желчи, закупорка желчного протока и воспаление желчного пузыря приводят к нарушению обмена липидов. [c.165]Особую роль в регуляции метаболизма липидов играют гормоны. Следует обратить внимание на то, что жировой обмен регулируется практически теми же гормонами, что и обмен углеводов — адреналин и норадреналин, глюкагон, глюкокортикоиды, гормоны передней доли гипофиза (соматотропный гормон и АКТГ), а также тироксин и половые гормоны. Адреналин и норадреналин активируют липолиз в жировой ткани, в результате усиливается мобилизация жирных кислот из жировых депо и содержание неэстерифицированных жирных кислот в плазме повышается. Клк уже отмечалось (гл. 23.3), эти гормоны через цАМФ активируют соответствующую протеинкиназу, которая способствует фосфорилированию липазы, т. е. образованию ее активной формы. [c.356]
Незаменимые жирные- кислоты — линолевая, линоленовая и. арахидоновая, по-видимому, осуществляют в животном организме функции окисления насыщенных жирных кислот, участвуя тем самым в процессе усвоения жиров [13] и в жировом обмене кожных покровов [14]. [c.621]
Последний фрагмент является активной частью кофермента, так как его тиольная группа легко образует тиоэфирные связи с карбоксильными остатками кислот и переносит их на другие субстраты (например, ацетильную группу передает в цикл три-карбоновых кислот - цикл Кребса). КоА участвует в углеводном и жировом обмене и в синтезе важных биомолекул. [c.168]
Биотин (витамин Н) — органическое вещество, входит в состав ферментов, регулирующих белковый и жировой обмен, обладает высокой активностью. При недостатке Б. наблюдаются поражения кожи, мышечная слабость, замедляется рост. Наиболее богаты Б. дрожжи, помидоры, шпинат, соя, яичный желток. Б. в живом организме концентрируется в печени, почках. [c.26]
Кортизон относится к группе кортикостероидов. Он обладает жаропонижающим действием, особенно при лечении ревматоидного артрита. Холевая кислота входит в группу холевых (желчных) кислот, обладает свойствами поверхностно-активного вещества (ПАВ см. разд. 21.6) и регулирует жировой обмен в организме. [c.236]
Он встречается в некоторых растениях и мыщечной ткани животных. Витамин Вт является активным метаболитом, стимулирует биосинтез белка, проявляет анаболическое действие, нормализуя белковый и жировой обмен, улучшая аппетит, ускоряя рост и увеличивая массу тела. Показан в педиатрии, а также взрослым при хронической ишемической болезни сердца, нервном и физическом истощении, после операций и в спортивной медицине. [c.46]
Витамин Ва связан, кроме того, с углеводным и жировым обменом, метаболизмом аминокислот он необходим для нормального зрения. Эйлер (1938) объясняет влияние витамина В. его светочувствительностью, благодаря которой он превращает действующие на него фиолетовые и синие лучи в длинноволновые (светло-зеленой флуоресценции), к. которым глаз обладает большей чувствительностью таким образом, витамин Bj выполняет как бы роль сенсибилизатора. [c.675]
П. к. в виде КоА участвует в углеводном и жировом обмене, в синтезе ацетилхолина, в коре надпочечников стимулирует образование кортикостероидов. [c.443]
Жировой обмен в организме может быть нарушен в результате нарушения углеводного обмена. Например, при тяжелых формах диабета (сахарная болезнь) происходит нарушение процессов окисления жиров в крови накапливаются промежуточные продукты окисления жиров — ацетоновые тела (ацетон, ацетоуксусная и р-окси-масляная кислоты), вследствие чего ацетоновые тела появляются и в моче. Это явление называется ацетонурией. [c.165]
Участвует в жировом обмене в частности в ути лизации непредельных жирных кислот [c.10]
Предполагается участие в жировом обмене организма [c.10]
В конце 60-х годов в состав косметических изделий начали все более широко вводить полезные добавки и в первую очередь витамины, а также соки и настои некоторых овощей, целебных трав и растений. За счет использования биологически активных добавок удалось создавать эффективные средства целенаправленного действия, влияющие на биологические функции кожи, оказывающие тонизирующее действие, усиливающие белковый, жировой обмен, улучшающие состояние кожи, волос. [c.8]
Отечественная промышленность выпускает для ухода за сухой и нормальной кожей лица кремы, содержащие различные добавки витамины, растительные экстракты, аминокислоты, а также вещества, усиливающие жировой обмен. [c.14]
КРЕМ ЛЕСНАЯ НИМФА изготовлен на основе водно-спиртового настоя биомассы женьшеня, который является активным препаратом, стимулирующим физиологическую активность клеток эпидермиса, белковый и жировой обмен. Крем оказывает эффективное тонизирующее действие на кожу. Жировые компоненты крема — оливковое масло, ланолин, пчелиный воск и другие — хорошо смягчают кожу. Особенно полезен при вялой, анемичной коже, а также тем, кому за тридцать. [c.21]
К высокоэффективным косметическим средствам для ухода за сухой и увядающей кожей лица можно отнести также кремы со специально подобранными добавками, усиливающими жировой обмен в коже. [c.23]
КРЕМ БЕРЕЗКА особенно рекомендуется для ухода за сверхчувствительной и легкораздражимой кожей лица и шеи. Изготавливается из высококачественного сырья. Жировые компоненты крема — спермацет, ацетилированный ланолин, косточковое и кукурузное масло, а также пчелиный воск — оказывают благотворное действие на кожу. Крем хорошо смягчает кожу, устраняет сухость, предупреждает преждевременное появление морщин. Имеет приятную консистенцию, легко впитывается. Кремом можно пользоваться в любое время дня. Небольшое количество крема легкими движениями кончиков пальцев наносят на чистую кожу лица и шеи.
Обмен белков (метаболизм белков) в организме человека
Мы подошли к наиважнейшему аспекту в планировании питания спортсмена. Тема нашей статьи – белковые обменные процессы. В новом материале вы найдёте ответы на вопросы: что такое обмен белков, какую роль протеины и аминокислоты играют в организме и что бывает, если нарушается белковый метаболизм.
Общая суть
Из белка (протеина) состоит большая часть наших клеток. Это основа жизнедеятельности организма и его строительный материал.
Белки регулируют следующие процессы:
- мозговую деятельность;
- переваривание тригидроглицеридов;
- синтез гормонов;
- передачу и хранение информации;
- движение;
- защиту от агрессивных факторов;
Примечание: наличие белка напрямую связано с синтезом инсулина. Без достаточного количества аминокислот, из которых синтезируется этот элемент, повышение сахара в крови становится лишь вопросом времени.
- создание новых клеток – в частности, за счет белковых структур регенерируют клетки печени;
- транспортировку липидов и других важных соединений;
- преобразование липидных связей в смазочные материалы для суставов;
- контроль метаболизма.
И еще десятки различных функций. Фактически белок – это мы. Поэтому люди, которые отказываются от употребления мяса и других животных продуктов, все равно вынуждены искать альтернативные источники белка. В противном случае, их вегетарианская жизнь будет сопровождаться дисфункциями и патологическими необратимыми изменениями.
Как бы это странно не звучало, но небольшой процент белка есть во многих продуктах. Например, крупы (все, за исключением манной) имеют в своем составе до 8% белка, пусть и с неполным аминокислотным составом. Это частично компенсирует дефицит белка, если вы хотите сэкономить на мясе и спортивном питании. Но помните, что организму нужны разные белки – одной гречкой не удовлетворить потребности в аминокислотах. Не все белки расщепляются одинаково и все по разному влияют на деятельность организма.

В пищеварительном тракте белок расщепляется под воздействием специальных ферментов, которые тоже состоят из белковых структур. Фактически, это замкнутый круг: если в организме есть длительный дефицит белковых тканей, то и новые белки не смогут денатурировать до простых аминокислот, что вызовет еще больший дефицит.
Важный факт: белки могут участвовать в энергетическом обмене наравне с липидами и углеводами. Дело в том, что глюкоза – необратимая и самая простейшая структура, которая превращается в энергию. В свою очередь белок, пускай и со значительными энергетическими потерями в процессе окончательной денатурации, может быть превращен в гликоген. Другими словами, организм в критической ситуации способен использовать белок в качестве топлива.
В отличие от углеводов и жиров, белки усваиваются ровно в том количестве, которое необходимо для функционирования организма (включая поддержание постоянного анаболического фона). Никаких протеиновых излишков организм не откладывает. Единственное, что может изменить этот баланс – это прием тестостероновых стимуляторов и аналогов гормона тестостерона (анаболических стероидов). Первичная задача таких препаратов – вовсе не повышение силовых показателей, а увеличение синтеза АТФ и белковых структур, за счет чего и растут мышцы.
Этапы белкового обмена
Белковые обменные процессы гораздо сложнее углеводных и липидных. Ведь если углеводы – это всего лишь энергия, а жирные кислоты поступают в клетки практически в неизменном виде, то главный строитель мышечной ткани претерпевает в организме целый ряд изменений. На некоторых этапах по белок и вовсе может метаболизироваться в углеводы и, соответственно, в энергию.
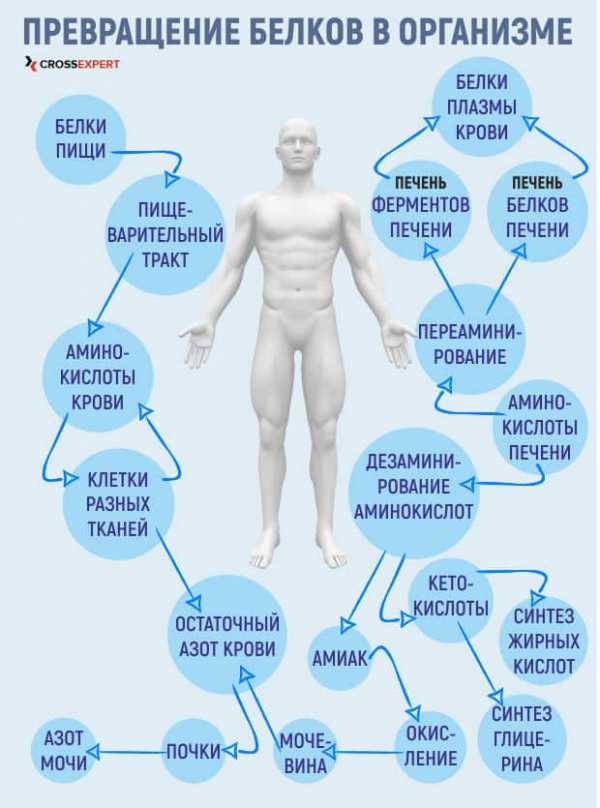
Рассмотрим основные этапы обмена белков в организме человека, начиная с их поступления и запечатывания слюной денатурата будущих аминокислот и заканчивая конечными продуктами жизнедеятельности.
Примечание: мы поверхностно рассмотрим биохимические процессы, которые позволят понять сам принцип переваривания белков. Для достижения спортивных результатов этого будет достаточно. Однако при нарушениях белкового обмена лучше обратится к врачу, который определит причину патологии и поможет устранить её на уровне гормонов или синтеза самих клеток.
| Этап | Что происходит | Суть |
| Первичное попадание белков | Под воздействием слюны расщепляются основные гликогеновые связи, превращаясь в простейшую глюкозу, остальные фрагменты запечатываются для последующей транспортировки. | На этом этапе основные белковые ткани в составе продуктов питания выделяются в отдельные структуры, которые затем будут перевариваться. |
| Переваривание белков | Под воздействием панкреатина и других ферментов происходит дальнейшая денатурация до белков первого порядка. | Организм настроен таким образом, что может получать аминокислоты только из простейших цепочек белков, для чего он воздействует кислотой, чтобы сделать белок более расщепляемым. |
| Расщепление на аминокислоты | Под воздействием клеток внутренней слизистой оболочки кишечника, денатурированные белки всасываются в кровь. | Уже упрощенный белок организм расщепляет на аминокислоты. |
| Расщепление до энергии | Под воздействием огромного количества инсулиновых заменителей и ферментов для переваривания углеводов белок распадается до простейшей глюкозы | В условиях, когда организму не хватает энергии, он не денатурирует белок, а при помощи специальных веществ расщепляет его сразу до уровня чистой энерги. |
| Перераспределение аминокислотных тканей | Циркулируя в общем кровотоке, белковые ткани под воздействием инсулина транспортируются по всем клеткам, отстраивая необходимые аминокислотные связи. | Белки, путешествуя по организму, восстанавливают недостающие части, как в мышечных структурах, так и в структурах связанных с гормоностимуляцией, мозговой активностью или последующей ферментацией. |
| Составление новых белковых тканей | В мышечных тканях аминокислотные структуры, связываясь с микроразрывами, составляют новые ткани, вызывая гипертрофию мышечных волокон. | Аминокислоты в нужном составе превращаются в мышечную-белковую ткань. |
| Вторичный белковый обмен | При наличии переизбытка белковых тканей в организме, они под вторичным воздействием инсулина снова попадают в кровоток для превращения их в другие структуры. | При сильном мышечном напряжении, долгом голоде или во время болезни организм использует мышечные белки для компенсации аминокислотного недостатка в других тканях. |
| Транспортировка липидных тканей | Свободно циркулирующие белки, соединенные в фермент липазу, помогают транспортировать и переваривать вместе с желчью полинасыщенные жирные кислоты. | Белок участвует в транспортировке жиров и синтезе холестерина из них. В зависимости от аминокислотного состава белка синтезируются как полезный, так и вредный холестерин. |
| Выведение окисленных элементов (конечных продуктов) | Отработанные аминокислоты в процессе катаболизма выводятся с продуктами жизнедеятельности организма. | Мышечные ткани, поврежденные в результате нагрузок, транспортируются из организма. |
Нарушения белкового обмена опасны для организма не менее, чем патологии метаболизма жиров и углеводов. Белки участвуют не только в формировании мышц, но практически во всех физиологических процессах.
Что может пойти не так? Как мы все знаем, важнейший энергетический элемент в организме – это молекулы АТФ, которые, путешествуя по крови, раздают клеткам необходимые нутриенты. При нарушении обмена белков “ломается” синтез АТФ и нарушаются процессы, которые косвенно или напрямую влияют на синтезирование из аминокислот новых белковых структур.
В числе наиболее вероятных последствий метаболических нарушений:
- острый панкреатит;
- некроз тканей желудка;
- раковые новообразования;
- общее отекание организма;
- нарушение водно-солевого баланса;
- потеря веса;
- замедление умственного развития и роста у детей;
- невозможность переваривания жирных кислот;
- невозможность транспортировки продуктов жизнедеятельности по кишечнику без раздражения сосудистых стенок;
- резкие катаболические реакции;
- разрушение костной и мышечной ткани;
- разрушение нейрон-мышечной связи;
- ожирение;
- нарушение скорости обмена веществ;
- нарушение всасывания микроэлементов в крови;
- нарушение гормонального фона;
- деградация интеллекта.

Это далеко не полный список того, что может произойти с организмом в случае, если будет нарушен белковый обмен. Однако не все так страшно. Чтобы вывести из строя механизм белкового обмена, нужно, чтобы одновременно совпало хотя бы несколько факторов из перечисленных:
- Под воздействием белковых коктейлей (без натуральной пищи) организм перестаёт вырабатывать пищеварительные ферменты, направленные на регуляцию и последующее расщепление белковых тканей.
- Под воздействием изменений в гормональном балансе катаболические реакции превалируют над анаболическими.
- Без поступления белка из пищи возникает недостаток основных синтезируемых аминокислот.
- В отсутствии достаточного поступления углеводов остаточные белки катаболизируются в метаболиты сахара.
- Полное отсутствие жировой прослойки.
- Есть патологии почек и печени.
Итог
Метаболизм белков в организме человека – сложнейший процесс, требующий изучения и внимания. Однако для поддержания уверенного анаболического фона при правильном перераспределении белковых структур в последующие аминокислоты достаточно придерживаться простых рекомендаций:
- Потребление белка на килограмм тела отличается для тренированного и нетренированного человека (спортсмена и не-спортсмена).
- Для полноценного метаболизма нужны не только углеводы и белки, но и жиры.
- Голодание всегда приводит к разрушению белковых тканей для восполнения энергетических запасов.
- Белки – это в основном потребители, а не носители энергии.
- Оптимизационные процессы в организме направлены на уменьшение энергопотребления с целью сохранения ресурсов на длительное время.
- Белки – это не только мышечные ткани, но и ферменты, мозговая активность и многие другие процессы в организме.
И главный совет для спортсменов: не увлекайтесь соевым протеином, так как из всех белковых коктейлей он обладает самым слабым аминокислотным составом. Более того, продукт плохой очистки может привести к катастрофическим последствиям – изменениям гормонального фона и нарушению обменных процессов. Длительное потребление сои чревато дефицитом невосполнимых в организме аминокислот, что станет первопричиной нарушения белкового синтеза.
Оцените материалЭксперт проекта. диагностика, лечение, первичная, вторичная профилактика заболеваний почек, суставов, сердечно-сосудистой системы; дифференциальная диагностика заболеваний различных органов и систем; рекомендации по диетическому питанию, физическим нагрузкам, лечебной физкультуре, подбор индивидуальной схемы питания.
Редакция cross.expert
2.Тироксин. Влияние на обмен веществ. Изменения обмена при гипо- и гипертиреозе.
Тироксин - гормон щитовидной железы. После частичного превращения в трийодтиронин (в печени и почках) и перехода в клетки организма, оказывает влияние на развитие и рост тканей, на обмен веществ. В малых дозах оказывает анаболическое действие на белковый и жировой обмен. В средних дозах стимулирует рост и развитие, повышает потребность тканей в кислороде, стимулирует метаболизм белков, жиров и углеводов, повышает функциональную активность сердечно-сосудистой системы и центральной нервной системы. В больших дозах угнетает выработку тиротропин-рилизинг гормона гипоталамуса и тиреотропного гормона гипофиза. Тироксин влияет на обмен веществ, развитие тканей, в небольших дозах проявляет себя как анаболик (помогает увеличивать мышечный объем), в средних дозах активизирует жировой, белковый, углеводный обмен, положительно сказывается на состоянии нервной системы, сосудов, сердца.
Гипотиреоз развивается вследствие недостаточности йодтиронинов. Обычно гипотиреоз связан с недостаточностью функции щитовидной железы, но может возникать и при заболеваниях гипофиза и гипоталамуса. Гипотиреоз у новорождённых приводит к развитию кретинизма, который проявляется множественными врождёнными нарушениями и тяжёлой необратимой задержкой умственного развития. Наиболее тяжёлые формы гипотиреоза, сопровождающиеся слизистым отёком кожи и подкожной клетчатки, обозначают термином "микседема". Отёчность обусловлена избыточным накоплением гликозаминогликанов и воды. В подкожной клетчатке накапливается глюкуроновая и в меньшей степени хондроитинсерная кислоты. Характерные проявления заболевания: снижение частоты сердечных сокращений, вялость, сонливость, непереносимость холода, сухость кожи. Эти симптомы развиваются вследствие снижения основного обмена, скорости гликолиза, мобилизации гликогена и жиров, потребления глюкозы мышцами, уменьшения мышечной массы и снижения теплопродукции. В настоящее время у взрослых людей частой причиной гипотиреоза является хронический аутоиммунный тиреоидит, приводящий к нарушению синтеза йодтиронинов (зоб Хашимото).
Гипертиреоз возникает вследствие повышенной продукции йодтиронинов. Диффузный токсический зоб (базедова болезнь, болезнь Грейвса) - наиболее распространённое заболевание щитовидной железы. При этом заболевании отмечают увеличение размеров щитовидной железы (зоб), повышение концентрации йодтиронинов в 2-5 раз и развитие тиреотоксикоза. Характерные признаки тиреотоксикоза: увеличение основного обмена, учащение сердцебиений, мышечная слабость, снижение массы тела (несмотря на повышенный аппетит) , потливость, повышение температуры тела, тремор и экзофтальм (пучеглазие). Гипертиреоз может возникать в результате различных причин: развитие опухоли, тиреоидит, избыточное поступление йода и йодсодер-жащих препаратов, аутоиммунные реакции. В большей мере усиливаются процессы катаболизма, о чём свидетельствует отрицательный азотистый баланс.
3.Почему, если в крови повышены таг хиломикронов, рекомендуют сократить количество пищевых жиров, а если таг повышены за счет лпонп, то рекомендуют сократить потребление углеводов?
В составе хиломикронов экзогенные жиры доставляются в органы и ткани. Липопротеинлипаза (ЛП—липаза) — фермент, обеспечивающий потребление экзогенных жиров тканями. ЛП—липаза, располагающаяся в эндотелии сосудов, взаимодействует с хиломикронами кровотока и гидролизует триацилглирины на глицерин и жирные кислоты, которые поступают в клетку. По мере извлечения ТАГ из хиломикронов последние превращаются в остаточные хиломикроны и затем поступают в печень.
Жиры, как и гликоген, являются формами депонирования энергетического материала. Причем жиры — наиболее долговременные и более эффективные источники энергии. При голодании запасы жира у человека истощаются за 5—7 недель, тогда как гликоген полностью расходуется примерно за сутки. Если поступление жира превышает потребности организма в энергии , то жир депонируется в адипоцитах — специализированных клетках жировой ткани. Кроме того, если количество поступающих углеводов больше, чем надо для депонирования в виде гликогена, то часть глюкозы также превращается в жиры . Таким образом, жиры в жировой ткани накапливаются в результате трех процессов:
поступают из хиломикронов, которые приносят экзогенные жиры из кишечника
поступают из ЛОНП, которые транспортируют эндогенные жиры, синтезированные в печени из глюкозы
образуются из глюкозы в самих клетках жировой ткани.
В первом и во втором случае жиры в составе липопротеинов гидролизуются ЛП—липазой и в клетку поступают жирные кислоты, которые затем используются для синтеза ТАГ. Перед включением в ТАГ жирные кислоты сначала активируются путем образования тиоэфиров кофермента А, а затем взаимодействуют с глицеролфосфатом. Следовательно, синтез ТАГ может протекать только в присутствии глюкозы, из которой в процессе гликолиза образуется диаксиацетонфосфат. Инсулин стимулирует синтез ТАГ, потому что в его присутствии повышается проницаемость мембран клеток жировой ткани для глюкозы.
Билет 19
Биосинтез проколлагена и его превращение в коллаген. Фибриллогенез. Возможные нарушения.
Проколлаген - внутриклеточный предшественник коллагена, синтезируемый на полирибосомах, связанных с мембранами эндоплазматической сети.
Синтез и созревание коллагена – многоэтапный процесс, начинающийся в клетке и завершающийся в межклеточном матриксе. Включает в себя целый ряд посттрансляционных изменений: гидроксилирование пролина и лизина с образованием гидроксипролина и гидроксилизина; гликозилирование гидроксилизина; частичный протеолиз – отщепление «сигнального» пептида, а также N- и С – концевых пропептидов; образование тройной спирали.
Синтез полипептидный цепей коллагена.
Синтезируются на полирибосомах, связанных с мембранами ЭР, в виде более длинных, чем зрелые цепи, предшественников – препро – α – цепей.
Эти предшественники имеют гидрофобный «сигнальный» пептид на N – конце, содержащий около 100 аминокислот.
Функция сигнального пептида – ориентация синтеза пептидных цепей в полости ЭР. После выполнения функции – отщепляется.
Синтезированная молекула проколлагена содержит дополнительные участки – N- и С - концевые пропептиды, в составе которых остатки цистеина, образующие внутри- и межцепочечные S-S связи.
Посттрансляционные модификации коллагена.
Начинается в период трансляции коллагеновой мРНК на рибосомах
Продолжается на растущей полипептидной цепи вплоть до отделения от рибосом.
После образования тройной спирали дальнейшее гидроксилирование пролиновых и лизиловых остатков прекращается.
Реакции гидроксилирования катализируют оксигеназы, связанные с мембранами микросом.
Пролиловые и лизиловые остатки в Y – положении пептида подвергаются действию пролил-4-гидроксилазы и лизил-5-гидроксилазы.
Необходимые компоненты – α – кетоглутарат, кислород и витамин С.
Донор атома кислорода, присоединяющегося к С – 4 пролина, - молекула кислорода.
Гидроксилазы пролина и лизина содержат в активном центре атом железа II. Для сохранения атома железа в ферроформе необходим восстанавливающий агент, роль которого выполняет аскорбиновая кислота, легко окисляющаяся в дегидроаскорбиновую кислоту.
После завершения гидроксилирования при участии гидроксилтрансфераз в состав молекулы проколлагена вводятся углеводные группы – галактоза, дисахарид галактозилглюкоза.
Образуют ковалентную О – гликозидную связь с 5-ОН-группой гидроксилизина.
Гликозилирование происходит в коллагене, езё не претерпевшем спирализации
Завершается после образования тройной спирали
Каждая про – α – цепь соединяется водородными связями с двумя другими про – α – цепями, образуя тройную спираль проколлагена.
Происходит ещё в просвете ЭР и начинаются после образования межцепочечных дисульфидных мостиков в области С – концевых пропептидов.
Из ЭР молекулы проколлагена перемещаются в аппарат Гольджи, включаются в секреторные пузырьки и секретируются в межклеточное пространство.
В межклеточной матриксе концевые пропептиды коллагенов I, II, III типов отщепляются специфическими проколлагенпептидазами
Образуются молекулы тропоколлагена – структурные единицы коллагеновых фибрилл.
Снижение активности ферментов (синдром Элерса – Данло – Русакова, тип VII) концевые пропептиды проколлагена не отщепляются и нарушается образование тропоколлагена и образование нормальный коллагеновых фибрилл.
Клинически – малый рост, искривление позвоночника, привычные вывихи суставов, высокая растяжимость кожи.
Переваривание белков и всасывание аминокислот. Биологическая ценность белков. Механизм транспорта аминокислот через клеточную мембрану. Роль ГГТП.
Химус поступает в 12пк. Низкое значение рН химуса вызывает в кишечнике выделение секретина, поступающего в кровь. Он стимулирует выделение из поджелудочной железы в тонкий кишечник панкреатического сока, содержащего НСО3-, что приводит к нейтрализации HCl желудочного сока и ингибированию пепсина, вследствие чего возрастает рН резко от 1,5 – 2,0 до 7,0. Поступление пептидов в тонкий кишечник вызывает секрецию другого гормона – холецистокинина, который стимулирует выделение панкреатических ферментов с оптимумом 7,5 – 8,0. Под действием ферментов поджелудочной железы и клеток кишечника завершается переваривание белков.
Активация трипсиногена: под действием энтеропептидазы. Она отщепляет с N – конца молекулы трипсиногена гексапептид Вал – (Асп)4 – Лиз. Изменение конформации оставшейся части полипептидной цепи приводит к формированию активного центра, образуется активный трипсин.
Образовавшийся трипсин активирует химотрипсиноген, из которого образуется несколько активных ферментов.
Под действием трипсина расщепляется пептидная связь между 15 и 16 аминокислотами, в результате чего образуется активный π – химотрипсин. Затем под действием π – химотрипсина отщепляется депиптид сер(14)-арг(15), что приводит к образованию δ – химотрипсина. Отщепление дипептида тре(147) – арг(148) завершает образование стабильной формы активного фермента – α – химотрипсина, который состоит из трёх полипептидных цепей, соединённых дисульфидными мостиками.
Остальные проферменты панкреатических протеаз (проэластаза и прокарбоксипептидазы А и В) также активируются трипсином путём частичного пртеолиза. В результате образуются ферменты – эластаза и карбоксипептидаза А и В.
Трипсин гидролизует пептидные связи, образованные карбоксильными группами аргинина и лизина.
Химотрипсины активны в отношении пептидных связей, образованных карбоксильными группами ароматических аминокислот (фен, тир, три).
Карбоксипептидазы А и В – цинкосодержащие ферменты, отщепляют С – концевые остатки аминокислот. КП А отщепляет аминокислоты с ароматическими или гидрофобными радикалами, а КП В – остатки аргинина и лизина.
Последний этап переваривания – гидролиз небольших пептидов, происходит под действием ферментов аминопептидаз и дипептидаз, которые синтезируются клетками тонкого кишечника в активной форме.
Транспорт двумя путями: через воротную систему печени, ведущую прямо в печень, и по лимфатическим сосудам, сообщающимся с кровью через грудной проток.
Всасывание L – аминокислот (не D – изомеров) – активный транспорт, с затратами энергии. Аминокислоты переносятся через кишечную стенку от слизистой её поверхности в кровь.
Перенос через щёточную каёмку переносчиками, многие из которых работают при участии Na – зависимых механизмав симпорта, подобно переносу глюкозы.
Механизм всасывания аминокислот в кишечнике: L – аминокислота поступает в энтероцит симпортом с ионом Na. Далее специфическая транслоказа переносит аминокислоту через мембрану в кровь. Обмен ионов натрия между клетками осуществляется путём первично – активного транспорта с помощью Na/K – АТФ-азы.
Одна из специфических транспортных систем для некоторых нейтральных аминокислот функционирует в кишечнике, полчках и, по-видимому, мозге. Эта система – γ – глутамильный цикл.
В ней участвует 6 ферментов, один из которых находится в клеточной мембране, остальные – в цитозоле.
Ключевая роль в транспорте аминокислот принадлежит ферменту γ – глутамилтрансферазе – гликопротеин, катализирует перенос γ – глутамильной группы от глутатиона на транспортируемую аминокислоту и последующий перенос комплекса в клетку.
Аминокислота, связанная с γ – глутамильным остатком, оказывается внутри клетки. Происходит отщепление γ – глутамильного остатка под действием фермента γ – глутамилциклотрансферазы.
Дипептид цистеинглицин расщепляется под действием пептидазы на 2 аминокислоты – цистеин и глицин.
В результате - перенос одной молекулы аминокислоты в клетку (внутриклеточную структуру).
Следующие три реакции обеспечивают регенерацию глутатиона, благодаря чему цикл повторяется многократно.
Для транспорта в клетку одной аминокислоты с участием γ – глутамильного цикла затрачивается 3 молекулы АТФ.
Азотистый баланс – разница между количеством азота, поступающего с пищей, и количеством выделяемого азота (в виде мочевины и аммонийных солей). Азотистое равновесие – поступающий азот равен выделяемому. Положительный баланс - поступает больше, чем выводится. Отрицательный – выделяется больше, чем поступает. Минимальное количество белков, необходимое для поддержания азотистого равновесия = 30 – 50 г/сут, оптимальное количество при средней физической нагрузке = 100-120 г/сут.
Полноценность в питании: Незаменимые аминокислоты – те, синтез которых сложен и неэкономичен для организма. Их выгоднее получать с пищей. Это - фенилаланин, метионин, треонин, триптофан, валин, лизин, лейцин, изолейцин. Аргинин и гистидин – заменимые – необходимо дополнительное их поступление в организм с пищей, особенно детям. К ним также относят глицин, аспарагиновую кислоту, аспарагин, глутаминовую кислоту, глутамин, серин, пролин, аланин. Питательная ценность белка зависит от его аминокислотного состава и способности усваиваться организмам.
Норма белка в питании: принятые нормы белкового питания для взрослых и детей учитывают климатические условия, профессию, условия труда и др. Взрослый человек при средней физической нагрузке должен получать 100-120 г белка в сутки. При тяжёлой нагрузке – 130-150г. Детям до 12 лет достаточно 50-70 г белка в сутки. При этом подразумевается, что в пищу входят разнообразные белки животного и растительного происхождения.
Перед вами двое больных с анемией. У одного - дефицит витамина В6, у другого – В12. Какие исследования следует провести, чтобы отдифференцировать эти состояния? Как изменятся их результаты?
При дефиците В12 из-за разрушения в красном костном мозге мегалобластов будет повышен уровень билирубина. При дефиците В6, т.к. он является коферментом синтеза гема, будет снижено количество гемоглобина.
Билет 20.
Посттранскрипционный процессинг. Основные этапы. Значение. Регуляция биосинтеза белка на уровне транскрипции.
Первичные транскрипты мРНК, прежде чем будут использованы в ходе синтеза белка, подвергаются ряду вокалентной модификации. Эти модификации необходимы для функционирования мРНК в качестве матрицы.
Модификация 5’ – конца.
Начинается на стадии элонгации.
Когда длина первичного транскрипта достигает примерно 30 нуклеотидных остатков, происходит кэпирование его 5’ – конца гуанилилтрансферазой, которая гидролизует макроэргическую связь в молекуле ГТФ и присоединяет нуклеотиддифосфатный остаток 5’ – фосфатной группой к 5’ – концу синтезированного фрагмента РНК с образованием 5’, 5’ – фосфодиэфирной связи.
Последующее метилирование остатка гуанина в составе ГТФ с образование N7-метилгуанозина завершает формирование кэпа.
Модифицированные 5’ – конец обеспечивает инициацию трансляции, удлиняет время жизни мРНК, защищая её от действия 5’ – экзонуклеаз в цитоплазме.
Кэпирование необходимо для инициации синтеза белка, так как инициирующие триплеты AUG, GUG распознаются рибосомой только если присутствует кэп. Наличие кэпа также нужно для работы сложной ферментной системы, обеспечивающей удаление интронов.
3’ – конец транскриптов, синтезированных РНК – полимеразой II, также подвергаются модификациям, при которых специальным ферментом полиА – полимеразой формируется полиА – последовательность (полиА – «хвост»), состоящая из 100-200 остатков адениловой кислоты.
Сигнал к началу полиаденилирования – последовательность –AAUAAA- на растущей цепи РНК
К 3’ – концу в точке разрыва полиА – полимераза наращивает полиА – «хвост». Наличие полиА – последовательности на 3’ – конце облегчает выход мРНК из ядра и замедляет её годролиз в цитоплазме.
Последовательности нуклеотидов, присутствующие в ДНК, но не входящие в состав зрелой мРНК – интроны, а последовательности, присутствующие в мРНК, - кодирующие, или экзоны.
Первичный транскрипт – строго комплементарная матрице нуклеиновая кислота (пре – мРНК), содержащая как экзоны, так и интроны. Длина – от 80 до 1000 нуклеотидов.
Последовательности интронов «вырезаются» из первичного транскрипта, концы экзонов соединяются друг с другом. Такая модификация РНК – сплайсинг. Происходит в ядре, в цитоплазму поступает уже «зрелая» мРРНРНК.
Процесс «вырезания» интронов протекает при участии малых ядерных рибонуклеопротеинов (мяРНП), в состав которых входит малая ядерная РНК, нуклеотидная цепь которой связана с белковым остовом, состоящим из нескольких протомеров.
первичный транскрипт тРНК содержит около 100 нуклеотидов, а после процессинга – 70-90 нуклеотидных остатков.
Происходят при участии РНК-аз (рибонуклеаз).
Формирование 3’ – конца тРНК катализирует РНК-аза, представляющая собой 3’ – экзонуклеазу, «отрезающую» по одному нуклеотиду, пока не достигает последовательности
-ССА, одинаковой для всех тРНК.
Пре – тРНК содержит всего один интрон, состоящий из 14-16 нуклеотидов. Удаление интрона и сплайсинг приводят к формированию структуры, называемой «антикодон» - триплета нуклеотидов, обеспечивающего взаимодействие тРНК с комплементарным кодоном мРНК в ходе синтеза белков.
Гены рРНК транскрибируются РНК – полимеразой I с образованием идентичных транскриптов. Первичные транскрипты имеют длину около 13000 нуклеотидных остатков (45S рРНК).
Прежде чем покинуть ядро в составе рибосомной частицы, молекула 45S рРНК подвергается процессингу, в результате образуется 28S рРНК (около 2000 нуклеотидов) и 5,8S рРНК (около 160 нуклеотидов), которые являются компонентами рибосом. Остальная часть транскрипта разрушается в ядре.
Рибосома – органелла клетки, участвующая в биосинтезе белка. Рибосома эукариотов состоят из двух, большой и малой, субъединиц: 60S и 40S. Белки рибосом выполняют структурную, регуляторную и каталитическую функции.
Транскрипция – первая стадия реализации генетической информации в клетке. В ходе процессинга образуются молекулы мРНК, служащие матрицей для синтеза белков, а также транспортные, рибосомальные и другие виды молекул РНК, выполняющие структурные, адапторные и каталитические функции.
Происходит в ядре. ДНК служит только матрицей и в ходе транскрипции не изменяется.
Рибонуклеозидтрифосфаты (ЦТФ, ГТФ, АТФ, УТФ) – субстраты и источники энергии, необходимые для протекания полимеразной реакции, образования 3’, 5’ – фосфодиэфирной связи между рибонуклеозидмонофосфатами.
Синтез РНК начинается в определённых последовательностях (сайтах) ДНК – промоторах, и завершается в терминирующих участках (сайты терминации).
Участок ДНК, ограниченный прогмотором и сайтом терминации – единица транскрипции – транскрипт.
Транскрипционные факторы – белки, взаимодействующие с определёнными регуляторными сайтами и ускоряющие или замедляющие процесс транскрипции. Соотношение информативной и неинформативной частей в транскриптонах = 1:9(эукариоты).
Биосинтез РНК осуществляется ДНК – зависимыми РНК – полимеразами. В ядрах эукариотов обнаружены 3 специализированные РНК – полимеразы: РНК – полимераза I, синтезирующая пре – рРНК, РНк – полимераза II, синтезирующая пре – мРНК, РНК – полимераза III – синтезирующая пре – тРНК.
РНК – полимеразы – олигомерные ферменты, состоящие из нескольких субъединиц - 2α, β, β’, σ. Субъединица σ выполняет регуляторну. Функцию, это один из факторов инициации транскрипции.
РНК – полимеразы I, II, III, узнающие разные промоторв, содержат разные по стороению субъединицы σ.
Инициации. Характеризуется активацией промотора с помощью белка – ТАТА – фактора. Его присоединение облегчает взаимодействие промотора с РНК – полимеразой. Образуется транскрипционная вилка.
Элонгация. Её факторы повышают активность РНК – полимеразы и облегчают расхождение цепей ДНК. Синтез РНК идёт от 5’- к 3’ – концу комплементарно матричной цепи ДНК.
Терминация. Раскручивание двойной спирали ДНК в области терминации делает его доступным для фактора терминации. Завершается синтез РНК в строго определённых участках матрицы – терминаторах (сайты терминации). Фактор терминации облегчает отделение первичного транскрипта (пре – мРНК), комплементарного матрице, и РНК – полимеразы от матрицы. РНК – полимераза может вступить в следующийц цикл транскрипции после присоединения субъединицы σ.
Образование кетоновых тел. Биологическая роль процесса. Причины и последствия кетоза.
В печени часть жирных кислот превращается в кетоновые тела, которые окисляются мозгом, нервной тканью, мышцами, обеспечивая достаточное количество энергии для синтеза АТФ и уменьшая потребление глюкозы. К кетоновым телам относят β – гидроксибутират, ацетоацетат и ацетон. Первые две молекулы могут окисляться в тканях, обеспечивая синтез АТФ. Ацетон образуется только при высоких концентрациях кетоновых тел в крови и, выделяясь с мочой, выдыхаемым воздухом и потом, позволяет организму избавляться от избытка кетоновых тел.
При низком соотношении инсулин – глюкагон в крови в жировой ткани активируется распад жиров. Жирные кислоты поступают в печень в большом количестве, чем в норме. Скорость реакций ЦТК в этих условиях снижена, так как оксалоацетат используется для ГНГ. В результате скорость образования ацетил – КоА превышает способность ЦТК окислять его. Ацетил – КоА накапливается в митохондриях печени и используется для синтеза кетоновых тел. Синтез кетоновых тел происходит только в митохондриях печени.
Синтез начинается с взаимодействия двух молекул ацетил – КоА, которые под действием фермента тиолазы образуют ацетоацетил – КоА. С ним взаимодействует третья молекула ацетил – КоА, образуя 3-гидрокси – 3 – метилглутарил – КоА (ГМГ – КоА). Эту реакцию катализирует расщепление ГМГ – КоА на свободный ацетоацетат и ацетил – КоА.
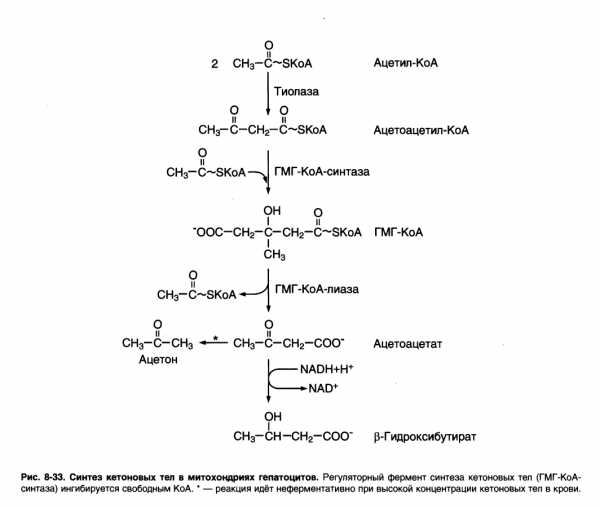
Ацетоацетат может выделяться в кровь или превращаться в печени в β – гидроксибутират восстановлением.
При активном β – окислении создается высокая концентрация НАДН, что способствует превращению большей части ацетоацетата в β – гидроксибутират. Именно он свляется основным кетоновым телом. При голодании для многих тканей жирные кислоты и кетоновые тела становятся основными топливными молекулами. Глюкоза используется в первую очередь нервной тканью.
При высокой концентрации ацетоацетата часть его неферментативно декарбоксилируется, превращаясь в ацетон. Ацетон не утилизируется тканями, но выделяется с выдыхаемым воздухом и мочой. Таким путём организм удаляет избыточное количество кетоновых тел, которые не успевают окисляться, но, являясь водорастворимыми кислотами, вызывают ацидоз.
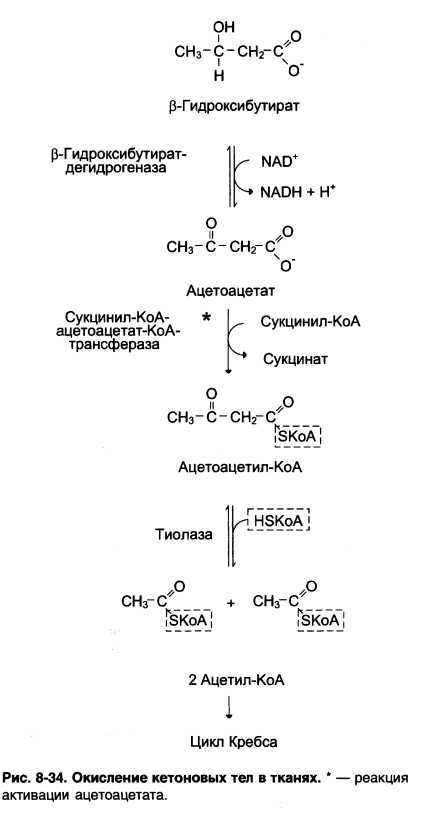
Регуляция синтеза: ГМГ – КоА – синтаза. 1) индуцируемый фермент, его синтез увеличивается при повышении концентрации жирных кислот в крови. Это происходит при мобилизации жиров из жировой ткани под действием глюкагона, адреналина, т.е. при голодании или нагрузке. 2) ингибируется высокими концентрациями свободного кофермента А. 3) когда поступление жирных кислот в клетки увеличивается, КоА связывается с ними, концентрация свободного КоА снижается, и фермент становится активным. 4) если поступление жирных кислот в клетки печени уменьшается, то увеличивается концентрация свободного КоА, ингибирующего фермент. Следовательно, скорость синтеза кетоновых тел в печени зависит от поступления жирных кислот.
Синтез кетоновых тел в периферических тканях. Рисунок 8-34.
Кетоацидоз. В норме концентрация кетоновых тел в крови = 1-3мг/мл. Увеличение кетоновых тел в крови - кетонемия, выделение с мочой – кетонурия. Накопление кетоновых тел в организме приводит к кетоацидозу: уменьшению щелочного резерва (компенсаторному ацидозу), а в тяжёлых случаях – к сдвигу рН (некомпенсированному ацидозу), так как кетоновые тела (кроме ацетона) – водорастворимые органические кислоты, способные к диссоциации: СН3-СО-СН2-СООН <-> СН3-СО-СН2-СОО+Н.
Назначьте биохимическое обследование больному с подозрением на поражение поджелудочной железы.
Проверить активность пищеварительных ферментов поджелудочной железы – амилазы, панкреатической липазы, химотрипсина и трипсина.
2.Тироксин. Влияние на обмен веществ. Изменения обмена при гипо- и гипертиреозе.
Тироксин - гормон щитовидной железы. После частичного превращения в трийодтиронин (в печени и почках) и перехода в клетки организма, оказывает влияние на развитие и рост тканей, на обмен веществ. В малых дозах оказывает анаболическое действие на белковый и жировой обмен. В средних дозах стимулирует рост и развитие, повышает потребность тканей в кислороде, стимулирует метаболизм белков, жиров и углеводов, повышает функциональную активность сердечно-сосудистой системы и центральной нервной системы. В больших дозах угнетает выработку тиротропин-рилизинг гормона гипоталамуса и тиреотропного гормона гипофиза. Тироксин влияет на обмен веществ, развитие тканей, в небольших дозах проявляет себя как анаболик (помогает увеличивать мышечный объем), в средних дозах активизирует жировой, белковый, углеводный обмен, положительно сказывается на состоянии нервной системы, сосудов, сердца.
Гипотиреоз развивается вследствие недостаточности йодтиронинов. Обычно гипотиреоз связан с недостаточностью функции щитовидной железы, но может возникать и при заболеваниях гипофиза и гипоталамуса. Гипотиреоз у новорождённых приводит к развитию кретинизма, который проявляется множественными врождёнными нарушениями и тяжёлой необратимой задержкой умственного развития. Наиболее тяжёлые формы гипотиреоза, сопровождающиеся слизистым отёком кожи и подкожной клетчатки, обозначают термином "микседема". Отёчность обусловлена избыточным накоплением гликозаминогликанов и воды. В подкожной клетчатке накапливается глюкуроновая и в меньшей степени хондроитинсерная кислоты. Характерные проявления заболевания: снижение частоты сердечных сокращений, вялость, сонливость, непереносимость холода, сухость кожи. Эти симптомы развиваются вследствие снижения основного обмена, скорости гликолиза, мобилизации гликогена и жиров, потребления глюкозы мышцами, уменьшения мышечной массы и снижения теплопродукции. В настоящее время у взрослых людей частой причиной гипотиреоза является хронический аутоиммунный тиреоидит, приводящий к нарушению синтеза йодтиронинов (зоб Хашимото).
Гипертиреоз возникает вследствие повышенной продукции йодтиронинов. Диффузный токсический зоб (базедова болезнь, болезнь Грейвса) - наиболее распространённое заболевание щитовидной железы. При этом заболевании отмечают увеличение размеров щитовидной железы (зоб), повышение концентрации йодтиронинов в 2-5 раз и развитие тиреотоксикоза. Характерные признаки тиреотоксикоза: увеличение основного обмена, учащение сердцебиений, мышечная слабость, снижение массы тела (несмотря на повышенный аппетит) , потливость, повышение температуры тела, тремор и экзофтальм (пучеглазие). Гипертиреоз может возникать в результате различных причин: развитие опухоли, тиреоидит, избыточное поступление йода и йодсодер-жащих препаратов, аутоиммунные реакции. В большей мере усиливаются процессы катаболизма, о чём свидетельствует отрицательный азотистый баланс.
3.Почему, если в крови повышены таг хиломикронов, рекомендуют сократить количество пищевых жиров, а если таг повышены за счет лпонп, то рекомендуют сократить потребление углеводов?
В составе хиломикронов экзогенные жиры доставляются в органы и ткани. Липопротеинлипаза (ЛП—липаза) — фермент, обеспечивающий потребление экзогенных жиров тканями. ЛП—липаза, располагающаяся в эндотелии сосудов, взаимодействует с хиломикронами кровотока и гидролизует триацилглирины на глицерин и жирные кислоты, которые поступают в клетку. По мере извлечения ТАГ из хиломикронов последние превращаются в остаточные хиломикроны и затем поступают в печень.
Жиры, как и гликоген, являются формами депонирования энергетического материала. Причем жиры — наиболее долговременные и более эффективные источники энергии. При голодании запасы жира у человека истощаются за 5—7 недель, тогда как гликоген полностью расходуется примерно за сутки. Если поступление жира превышает потребности организма в энергии , то жир депонируется в адипоцитах — специализированных клетках жировой ткани. Кроме того, если количество поступающих углеводов больше, чем надо для депонирования в виде гликогена, то часть глюкозы также превращается в жиры . Таким образом, жиры в жировой ткани накапливаются в результате трех процессов:
поступают из хиломикронов, которые приносят экзогенные жиры из кишечника
поступают из ЛОНП, которые транспортируют эндогенные жиры, синтезированные в печени из глюкозы
образуются из глюкозы в самих клетках жировой ткани.
В первом и во втором случае жиры в составе липопротеинов гидролизуются ЛП—липазой и в клетку поступают жирные кислоты, которые затем используются для синтеза ТАГ. Перед включением в ТАГ жирные кислоты сначала активируются путем образования тиоэфиров кофермента А, а затем взаимодействуют с глицеролфосфатом. Следовательно, синтез ТАГ может протекать только в присутствии глюкозы, из которой в процессе гликолиза образуется диаксиацетонфосфат. Инсулин стимулирует синтез ТАГ, потому что в его присутствии повышается проницаемость мембран клеток жировой ткани для глюкозы.
Билет 19
Биосинтез проколлагена и его превращение в коллаген. Фибриллогенез. Возможные нарушения.
Проколлаген - внутриклеточный предшественник коллагена, синтезируемый на полирибосомах, связанных с мембранами эндоплазматической сети.
Синтез и созревание коллагена – многоэтапный процесс, начинающийся в клетке и завершающийся в межклеточном матриксе. Включает в себя целый ряд посттрансляционных изменений: гидроксилирование пролина и лизина с образованием гидроксипролина и гидроксилизина; гликозилирование гидроксилизина; частичный протеолиз – отщепление «сигнального» пептида, а также N- и С – концевых пропептидов; образование тройной спирали.
Синтез полипептидный цепей коллагена.
Синтезируются на полирибосомах, связанных с мембранами ЭР, в виде более длинных, чем зрелые цепи, предшественников – препро – α – цепей.
Эти предшественники имеют гидрофобный «сигнальный» пептид на N – конце, содержащий около 100 аминокислот.
Функция сигнального пептида – ориентация синтеза пептидных цепей в полости ЭР. После выполнения функции – отщепляется.
Синтезированная молекула проколлагена содержит дополнительные участки – N- и С - концевые пропептиды, в составе которых остатки цистеина, образующие внутри- и межцепочечные S-S связи.
Посттрансляционные модификации коллагена.
Начинается в период трансляции коллагеновой мРНК на рибосомах
Продолжается на растущей полипептидной цепи вплоть до отделения от рибосом.
После образования тройной спирали дальнейшее гидроксилирование пролиновых и лизиловых остатков прекращается.
Реакции гидроксилирования катализируют оксигеназы, связанные с мембранами микросом.
Пролиловые и лизиловые остатки в Y – положении пептида подвергаются действию пролил-4-гидроксилазы и лизил-5-гидроксилазы.
Необходимые компоненты – α – кетоглутарат, кислород и витамин С.
Донор атома кислорода, присоединяющегося к С – 4 пролина, - молекула кислорода.
Гидроксилазы пролина и лизина содержат в активном центре атом железа II. Для сохранения атома железа в ферроформе необходим восстанавливающий агент, роль которого выполняет аскорбиновая кислота, легко окисляющаяся в дегидроаскорбиновую кислоту.
После завершения гидроксилирования при участии гидроксилтрансфераз в состав молекулы проколлагена вводятся углеводные группы – галактоза, дисахарид галактозилглюкоза.
Образуют ковалентную О – гликозидную связь с 5-ОН-группой гидроксилизина.
Гликозилирование происходит в коллагене, езё не претерпевшем спирализации
Завершается после образования тройной спирали
Каждая про – α – цепь соединяется водородными связями с двумя другими про – α – цепями, образуя тройную спираль проколлагена.
Происходит ещё в просвете ЭР и начинаются после образования межцепочечных дисульфидных мостиков в области С – концевых пропептидов.
Из ЭР молекулы проколлагена перемещаются в аппарат Гольджи, включаются в секреторные пузырьки и секретируются в межклеточное пространство.
В межклеточной матриксе концевые пропептиды коллагенов I, II, III типов отщепляются специфическими проколлагенпептидазами
Образуются молекулы тропоколлагена – структурные единицы коллагеновых фибрилл.
Снижение активности ферментов (синдром Элерса – Данло – Русакова, тип VII) концевые пропептиды проколлагена не отщепляются и нарушается образование тропоколлагена и образование нормальный коллагеновых фибрилл.
Клинически – малый рост, искривление позвоночника, привычные вывихи суставов, высокая растяжимость кожи.
Переваривание белков и всасывание аминокислот. Биологическая ценность белков. Механизм транспорта аминокислот через клеточную мембрану. Роль ГГТП.
Химус поступает в 12пк. Низкое значение рН химуса вызывает в кишечнике выделение секретина, поступающего в кровь. Он стимулирует выделение из поджелудочной железы в тонкий кишечник панкреатического сока, содержащего НСО3-, что приводит к нейтрализации HCl желудочного сока и ингибированию пепсина, вследствие чего возрастает рН резко от 1,5 – 2,0 до 7,0. Поступление пептидов в тонкий кишечник вызывает секрецию другого гормона – холецистокинина, который стимулирует выделение панкреатических ферментов с оптимумом 7,5 – 8,0. Под действием ферментов поджелудочной железы и клеток кишечника завершается переваривание белков.
Активация трипсиногена: под действием энтеропептидазы. Она отщепляет с N – конца молекулы трипсиногена гексапептид Вал – (Асп)4 – Лиз. Изменение конформации оставшейся части полипептидной цепи приводит к формированию активного центра, образуется активный трипсин.
Образовавшийся трипсин активирует химотрипсиноген, из которого образуется несколько активных ферментов.
Под действием трипсина расщепляется пептидная связь между 15 и 16 аминокислотами, в результате чего образуется активный π – химотрипсин. Затем под действием π – химотрипсина отщепляется депиптид сер(14)-арг(15), что приводит к образованию δ – химотрипсина. Отщепление дипептида тре(147) – арг(148) завершает образование стабильной формы активного фермента – α – химотрипсина, который состоит из трёх полипептидных цепей, соединённых дисульфидными мостиками.
Остальные проферменты панкреатических протеаз (проэластаза и прокарбоксипептидазы А и В) также активируются трипсином путём частичного пртеолиза. В результате образуются ферменты – эластаза и карбоксипептидаза А и В.
Трипсин гидролизует пептидные связи, образованные карбоксильными группами аргинина и лизина.
Химотрипсины активны в отношении пептидных связей, образованных карбоксильными группами ароматических аминокислот (фен, тир, три).
Карбоксипептидазы А и В – цинкосодержащие ферменты, отщепляют С – концевые остатки аминокислот. КП А отщепляет аминокислоты с ароматическими или гидрофобными радикалами, а КП В – остатки аргинина и лизина.
Последний этап переваривания – гидролиз небольших пептидов, происходит под действием ферментов аминопептидаз и дипептидаз, которые синтезируются клетками тонкого кишечника в активной форме.
Транспорт двумя путями: через воротную систему печени, ведущую прямо в печень, и по лимфатическим сосудам, сообщающимся с кровью через грудной проток.
Всасывание L – аминокислот (не D – изомеров) – активный транспорт, с затратами энергии. Аминокислоты переносятся через кишечную стенку от слизистой её поверхности в кровь.
Перенос через щёточную каёмку переносчиками, многие из которых работают при участии Na – зависимых механизмав симпорта, подобно переносу глюкозы.
Механизм всасывания аминокислот в кишечнике: L – аминокислота поступает в энтероцит симпортом с ионом Na. Далее специфическая транслоказа переносит аминокислоту через мембрану в кровь. Обмен ионов натрия между клетками осуществляется путём первично – активного транспорта с помощью Na/K – АТФ-азы.
Одна из специфических транспортных систем для некоторых нейтральных аминокислот функционирует в кишечнике, полчках и, по-видимому, мозге. Эта система – γ – глутамильный цикл.
В ней участвует 6 ферментов, один из которых находится в клеточной мембране, остальные – в цитозоле.
Ключевая роль в транспорте аминокислот принадлежит ферменту γ – глутамилтрансферазе – гликопротеин, катализирует перенос γ – глутамильной группы от глутатиона на транспортируемую аминокислоту и последующий перенос комплекса в клетку.
Аминокислота, связанная с γ – глутамильным остатком, оказывается внутри клетки. Происходит отщепление γ – глутамильного остатка под действием фермента γ – глутамилциклотрансферазы.
Дипептид цистеинглицин расщепляется под действием пептидазы на 2 аминокислоты – цистеин и глицин.
В результате - перенос одной молекулы аминокислоты в клетку (внутриклеточную структуру).
Следующие три реакции обеспечивают регенерацию глутатиона, благодаря чему цикл повторяется многократно.
Для транспорта в клетку одной аминокислоты с участием γ – глутамильного цикла затрачивается 3 молекулы АТФ.
Азотистый баланс – разница между количеством азота, поступающего с пищей, и количеством выделяемого азота (в виде мочевины и аммонийных солей). Азотистое равновесие – поступающий азот равен выделяемому. Положительный баланс - поступает больше, чем выводится. Отрицательный – выделяется больше, чем поступает. Минимальное количество белков, необходимое для поддержания азотистого равновесия = 30 – 50 г/сут, оптимальное количество при средней физической нагрузке = 100-120 г/сут.
Полноценность в питании: Незаменимые аминокислоты – те, синтез которых сложен и неэкономичен для организма. Их выгоднее получать с пищей. Это - фенилаланин, метионин, треонин, триптофан, валин, лизин, лейцин, изолейцин. Аргинин и гистидин – заменимые – необходимо дополнительное их поступление в организм с пищей, особенно детям. К ним также относят глицин, аспарагиновую кислоту, аспарагин, глутаминовую кислоту, глутамин, серин, пролин, аланин. Питательная ценность белка зависит от его аминокислотного состава и способности усваиваться организмам.
Норма белка в питании: принятые нормы белкового питания для взрослых и детей учитывают климатические условия, профессию, условия труда и др. Взрослый человек при средней физической нагрузке должен получать 100-120 г белка в сутки. При тяжёлой нагрузке – 130-150г. Детям до 12 лет достаточно 50-70 г белка в сутки. При этом подразумевается, что в пищу входят разнообразные белки животного и растительного происхождения.
Перед вами двое больных с анемией. У одного - дефицит витамина В6, у другого – В12. Какие исследования следует провести, чтобы отдифференцировать эти состояния? Как изменятся их результаты?
При дефиците В12 из-за разрушения в красном костном мозге мегалобластов будет повышен уровень билирубина. При дефиците В6, т.к. он является коферментом синтеза гема, будет снижено количество гемоглобина.
Билет 20.
Посттранскрипционный процессинг. Основные этапы. Значение. Регуляция биосинтеза белка на уровне транскрипции.
Первичные транскрипты мРНК, прежде чем будут использованы в ходе синтеза белка, подвергаются ряду вокалентной модификации. Эти модификации необходимы для функционирования мРНК в качестве матрицы.
Модификация 5’ – конца.
Начинается на стадии элонгации.
Когда длина первичного транскрипта достигает примерно 30 нуклеотидных остатков, происходит кэпирование его 5’ – конца гуанилилтрансферазой, которая гидролизует макроэргическую связь в молекуле ГТФ и присоединяет нуклеотиддифосфатный остаток 5’ – фосфатной группой к 5’ – концу синтезированного фрагмента РНК с образованием 5’, 5’ – фосфодиэфирной связи.
Последующее метилирование остатка гуанина в составе ГТФ с образование N7-метилгуанозина завершает формирование кэпа.
Модифицированные 5’ – конец обеспечивает инициацию трансляции, удлиняет время жизни мРНК, защищая её от действия 5’ – экзонуклеаз в цитоплазме.
Кэпирование необходимо для инициации синтеза белка, так как инициирующие триплеты AUG, GUG распознаются рибосомой только если присутствует кэп. Наличие кэпа также нужно для работы сложной ферментной системы, обеспечивающей удаление интронов.
3’ – конец транскриптов, синтезированных РНК – полимеразой II, также подвергаются модификациям, при которых специальным ферментом полиА – полимеразой формируется полиА – последовательность (полиА – «хвост»), состоящая из 100-200 остатков адениловой кислоты.
Сигнал к началу полиаденилирования – последовательность –AAUAAA- на растущей цепи РНК
К 3’ – концу в точке разрыва полиА – полимераза наращивает полиА – «хвост». Наличие полиА – последовательности на 3’ – конце облегчает выход мРНК из ядра и замедляет её годролиз в цитоплазме.
Последовательности нуклеотидов, присутствующие в ДНК, но не входящие в состав зрелой мРНК – интроны, а последовательности, присутствующие в мРНК, - кодирующие, или экзоны.
Первичный транскрипт – строго комплементарная матрице нуклеиновая кислота (пре – мРНК), содержащая как экзоны, так и интроны. Длина – от 80 до 1000 нуклеотидов.
Последовательности интронов «вырезаются» из первичного транскрипта, концы экзонов соединяются друг с другом. Такая модификация РНК – сплайсинг. Происходит в ядре, в цитоплазму поступает уже «зрелая» мРРНРНК.
Процесс «вырезания» интронов протекает при участии малых ядерных рибонуклеопротеинов (мяРНП), в состав которых входит малая ядерная РНК, нуклеотидная цепь которой связана с белковым остовом, состоящим из нескольких протомеров.
первичный транскрипт тРНК содержит около 100 нуклеотидов, а после процессинга – 70-90 нуклеотидных остатков.
Происходят при участии РНК-аз (рибонуклеаз).
Формирование 3’ – конца тРНК катализирует РНК-аза, представляющая собой 3’ – экзонуклеазу, «отрезающую» по одному нуклеотиду, пока не достигает последовательности
-ССА, одинаковой для всех тРНК.
Пре – тРНК содержит всего один интрон, состоящий из 14-16 нуклеотидов. Удаление интрона и сплайсинг приводят к формированию структуры, называемой «антикодон» - триплета нуклеотидов, обеспечивающего взаимодействие тРНК с комплементарным кодоном мРНК в ходе синтеза белков.
Гены рРНК транскрибируются РНК – полимеразой I с образованием идентичных транскриптов. Первичные транскрипты имеют длину около 13000 нуклеотидных остатков (45S рРНК).
Прежде чем покинуть ядро в составе рибосомной частицы, молекула 45S рРНК подвергается процессингу, в результате образуется 28S рРНК (около 2000 нуклеотидов) и 5,8S рРНК (около 160 нуклеотидов), которые являются компонентами рибосом. Остальная часть транскрипта разрушается в ядре.
Рибосома – органелла клетки, участвующая в биосинтезе белка. Рибосома эукариотов состоят из двух, большой и малой, субъединиц: 60S и 40S. Белки рибосом выполняют структурную, регуляторную и каталитическую функции.
Транскрипция – первая стадия реализации генетической информации в клетке. В ходе процессинга образуются молекулы мРНК, служащие матрицей для синтеза белков, а также транспортные, рибосомальные и другие виды молекул РНК, выполняющие структурные, адапторные и каталитические функции.
Происходит в ядре. ДНК служит только матрицей и в ходе транскрипции не изменяется.
Рибонуклеозидтрифосфаты (ЦТФ, ГТФ, АТФ, УТФ) – субстраты и источники энергии, необходимые для протекания полимеразной реакции, образования 3’, 5’ – фосфодиэфирной связи между рибонуклеозидмонофосфатами.
Синтез РНК начинается в определённых последовательностях (сайтах) ДНК – промоторах, и завершается в терминирующих участках (сайты терминации).
Участок ДНК, ограниченный прогмотором и сайтом терминации – единица транскрипции – транскрипт.
Транскрипционные факторы – белки, взаимодействующие с определёнными регуляторными сайтами и ускоряющие или замедляющие процесс транскрипции. Соотношение информативной и неинформативной частей в транскриптонах = 1:9(эукариоты).
Биосинтез РНК осуществляется ДНК – зависимыми РНК – полимеразами. В ядрах эукариотов обнаружены 3 специализированные РНК – полимеразы: РНК – полимераза I, синтезирующая пре – рРНК, РНк – полимераза II, синтезирующая пре – мРНК, РНК – полимераза III – синтезирующая пре – тРНК.
РНК – полимеразы – олигомерные ферменты, состоящие из нескольких субъединиц - 2α, β, β’, σ. Субъединица σ выполняет регуляторну. Функцию, это один из факторов инициации транскрипции.
РНК – полимеразы I, II, III, узнающие разные промоторв, содержат разные по стороению субъединицы σ.
Инициации. Характеризуется активацией промотора с помощью белка – ТАТА – фактора. Его присоединение облегчает взаимодействие промотора с РНК – полимеразой. Образуется транскрипционная вилка.
Элонгация. Её факторы повышают активность РНК – полимеразы и облегчают расхождение цепей ДНК. Синтез РНК идёт от 5’- к 3’ – концу комплементарно матричной цепи ДНК.
Терминация. Раскручивание двойной спирали ДНК в области терминации делает его доступным для фактора терминации. Завершается синтез РНК в строго определённых участках матрицы – терминаторах (сайты терминации). Фактор терминации облегчает отделение первичного транскрипта (пре – мРНК), комплементарного матрице, и РНК – полимеразы от матрицы. РНК – полимераза может вступить в следующийц цикл транскрипции после присоединения субъединицы σ.
Образование кетоновых тел. Биологическая роль процесса. Причины и последствия кетоза.
В печени часть жирных кислот превращается в кетоновые тела, которые окисляются мозгом, нервной тканью, мышцами, обеспечивая достаточное количество энергии для синтеза АТФ и уменьшая потребление глюкозы. К кетоновым телам относят β – гидроксибутират, ацетоацетат и ацетон. Первые две молекулы могут окисляться в тканях, обеспечивая синтез АТФ. Ацетон образуется только при высоких концентрациях кетоновых тел в крови и, выделяясь с мочой, выдыхаемым воздухом и потом, позволяет организму избавляться от избытка кетоновых тел.
При низком соотношении инсулин – глюкагон в крови в жировой ткани активируется распад жиров. Жирные кислоты поступают в печень в большом количестве, чем в норме. Скорость реакций ЦТК в этих условиях снижена, так как оксалоацетат используется для ГНГ. В результате скорость образования ацетил – КоА превышает способность ЦТК окислять его. Ацетил – КоА накапливается в митохондриях печени и используется для синтеза кетоновых тел. Синтез кетоновых тел происходит только в митохондриях печени.
Синтез начинается с взаимодействия двух молекул ацетил – КоА, которые под действием фермента тиолазы образуют ацетоацетил – КоА. С ним взаимодействует третья молекула ацетил – КоА, образуя 3-гидрокси – 3 – метилглутарил – КоА (ГМГ – КоА). Эту реакцию катализирует расщепление ГМГ – КоА на свободный ацетоацетат и ацетил – КоА.
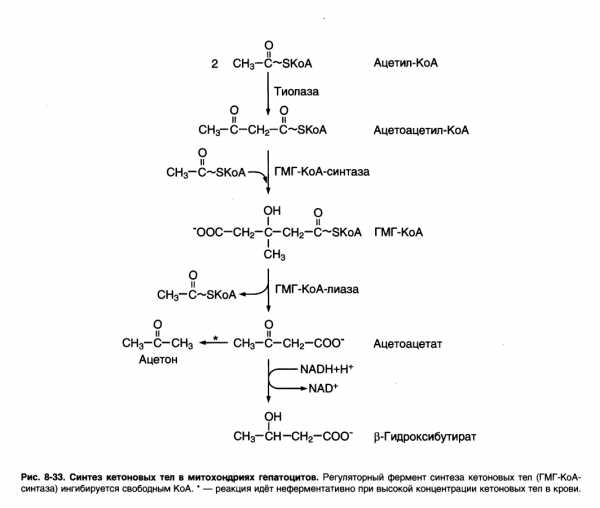
Ацетоацетат может выделяться в кровь или превращаться в печени в β – гидроксибутират восстановлением.
При активном β – окислении создается высокая концентрация НАДН, что способствует превращению большей части ацетоацетата в β – гидроксибутират. Именно он свляется основным кетоновым телом. При голодании для многих тканей жирные кислоты и кетоновые тела становятся основными топливными молекулами. Глюкоза используется в первую очередь нервной тканью.
При высокой концентрации ацетоацетата часть его неферментативно декарбоксилируется, превращаясь в ацетон. Ацетон не утилизируется тканями, но выделяется с выдыхаемым воздухом и мочой. Таким путём организм удаляет избыточное количество кетоновых тел, которые не успевают окисляться, но, являясь водорастворимыми кислотами, вызывают ацидоз.
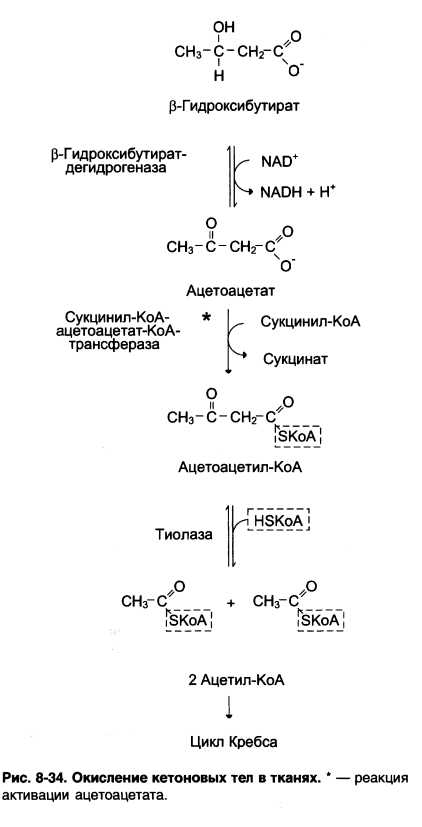
Регуляция синтеза: ГМГ – КоА – синтаза. 1) индуцируемый фермент, его синтез увеличивается при повышении концентрации жирных кислот в крови. Это происходит при мобилизации жиров из жировой ткани под действием глюкагона, адреналина, т.е. при голодании или нагрузке. 2) ингибируется высокими концентрациями свободного кофермента А. 3) когда поступление жирных кислот в клетки увеличивается, КоА связывается с ними, концентрация свободного КоА снижается, и фермент становится активным. 4) если поступление жирных кислот в клетки печени уменьшается, то увеличивается концентрация свободного КоА, ингибирующего фермент. Следовательно, скорость синтеза кетоновых тел в печени зависит от поступления жирных кислот.
Синтез кетоновых тел в периферических тканях. Рисунок 8-34.
Кетоацидоз. В норме концентрация кетоновых тел в крови = 1-3мг/мл. Увеличение кетоновых тел в крови - кетонемия, выделение с мочой – кетонурия. Накопление кетоновых тел в организме приводит к кетоацидозу: уменьшению щелочного резерва (компенсаторному ацидозу), а в тяжёлых случаях – к сдвигу рН (некомпенсированному ацидозу), так как кетоновые тела (кроме ацетона) – водорастворимые органические кислоты, способные к диссоциации: СН3-СО-СН2-СООН <-> СН3-СО-СН2-СОО+Н.
Назначьте биохимическое обследование больному с подозрением на поражение поджелудочной железы.
Проверить активность пищеварительных ферментов поджелудочной железы – амилазы, панкреатической липазы, химотрипсина и трипсина.
Билет 21
Какой у вас ОБМЕН ВЕЩЕСТВ: белковый, углеводный или смешанный?
Если вы употребляете продукты в соответствии с вашим обменом веществ, питание будет обеспечивать вам огромный прилив энергии, заметное улучшение умственных способностей и эмоционального благополучия, а также чувство насыщения на несколько часов.
Дэвид Кирхофф, президент Weight Watchers («Следящие за весом»), крупнейшей в мире диетической компании, недавно заявил на сайте компании:
«Подсчитывать калории бесполезно.
Если у нас в одной руке – яблоко пищевой ценностью 100 калорий, а в другой руке - пачка печенья пищевой ценностью 100 калорий, и мы считаем их «одинаковыми», поскольку в них содержится одинаковое количество калорий, это значит, что при выборе продуктов питания мы ограничиваемся только калориями».
Кирхофф и Weight Watchers отказались от популярной в компании системы «подсчета» благодаря которой, те, кто сидели на диете, чтобы похудеть, могли есть любые продукты, но маленькими порциями. Новая система призывает сидящих на диете употреблять больше натуральных и меньше обработанных продуктов.
По данным Time Magazine:
«Радикальный пересмотр, который является первым крупным изменением в программе баллов, происходит одновременно с тем, как Weight Watchers пытается возродить свой пострадавший от кризиса бизнес».
Это весьма примечательная новость. Более десяти лет Weight Watchers были лидерами по подсчету калорий, для стремящихся похудеть, поэтому признание «бесполезности» подсчета калорий – это, конечно же, радикальный шаг.
Возвращение к натуральным, необработанным продуктам – путь к здоровью и избавлению от лишнего веса
Посмотрим, поможет это и навредит их бизнесу, но в целом программа изменилась в лучшую сторону. Я говорю «в целом», потому что есть одно правило, которое может стать причиной заблуждения некоторых людей в рамках этой новой программы, и далее я расскажу вам об этом.
Почему империя по разработке методов похудения отказалась от своей всемирно известной системы?
Если вы не слышали о Weight Watchers, вы, должно быть, последние десять лет жили в глухом лесу. Их бизнес стал целой империей похудения, стоимость которой перевалила за $2,7 млрд после того, как в 1997 году они ввели свою популярную «систему подсчета».
Придерживаясь этой системы, люди, сидящие на диете, могли есть все, что хотели, но каждому продукту присваивалось определенное количество баллов, что упрощало процесс подсчета калорий, благодаря чему эту систему использовали миллионы людей.
Самое важный фактор в их пересмотренной программе - то, что теперь они стремятся к более натуральным, необработанным продуктам и «наказывают» сидящих на диете, если они позволяют себе продукты, богатые пустыми калориями, т.е. продукты с низкой питательной ценностью.
Подписывайтесь на наш аккаунт в INSTAGRAM!
Как по мне, так лучше поздно, чем никогда. Я долго выступал против подсчета калорий именно по этой причине. Вы не станете здоровее, если будете есть меньше печенья, чем раньше, даже если вам удастся сбросить килограммы. Если вы действительно хотите похудеть и улучшить свое здоровье, то замените пустые калории и денатурированные продукты питательными веществами!
По этому, я аплодирую WeightWatchers – они, наконец, увидели свет. Возвращение к натуральным, цельным (желательно, органическим, местного производства), необработанным продуктам – это самый правильный путь к улучшению здоровья.
Возвращение к натуральным, необработанным продуктам – ключ к похудению и здоровью
Журнал Time объясняет основные изменения в программе подсчета:
«Как и в старой программе, в новой практически любому существующему продукту присваивается некое количество баллов, и рассчитывается ежедневный рацион в баллах, с учетом роста, веса и возраста участника. Но теперь изменилось большинство значений баллов.
Теперь в системе отдается предпочтение продуктам с высоким содержанием белка или клетчатки, который требуют от организма больше усилий по превращению их в энергию, а также обеспечивают более продолжительное чувство сытости. В то же время, увеличились баллы за продукты, нагруженные углеводами, которые легко усваиваются организмом и превращаются в жир».
На первый взгляд все выглядит вполне логично. Белок – является богатым источником, насыщающим человеческий организм, даже больше, чем углеводы и жиры. Проще говоря, употребления белка помогает вам дольше чувствовать сытость.
Тем не менее, несмотря на то, что употребление большего количества белка является полезным для большинства людей, также важно понимать, что количество и тип необходимого вам белка существенно зависит от вашего пола, роста, веса, уровня нагрузки, и, что самое главное, вашего обмена веществ.
Для определения индивидуальных особенностей организма, вам следует установить какой у вас обмен веществ - белковый, углеводный или смешанный.
Для людей с белковым обменом веществ более эффективны диеты с низким содержанием углеводов, высоким содержанием белков и жиров. Типичное соотношение – это 40% белка и по 30% жиров и углеводов, но эти количества можно легко изменять на 50% жиров и всего лишь 10% углеводов - в зависимости от индивидуальных генетических требований.
Люди, у которых обнаружен углеводный обмен веществ, как правило, лучше всего себя чувствуют, если большая часть их пищи является растительными углеводами. Но они также нуждаются в определенном количестве белка и жиров в своем рационе. (Люди смешанного типа находятся где-то посередине.)]
Богатые на белок продукты
Помимо определения идеального для себя количества или соотношения белка, необходимо обратить внимание и на тип белка, потому что правила по его употреблению тоже зависит от вашего обмена веществ.
Людям с белковым обменом веществ, например, прекрасно подходит мясо с высоким содержанием пурина, такое как красное мясо курицы или высокого качества стейки, а люди углеводного типа в качестве источника белка предпочитают белое мясо или даже бобы.
Тем не менее, по моему опыту, большинство людей едят недостаточно белка, поэтому, перемещение внимание от белков в сторону углеводов, скорее всего, направит большинство людей в правильном направлении.
К традиционно хорошим источникам белка (хотя нужно определить свой обмен веществ, чтобы ваше питание стало по-настоящему полезным для оптимального здоровья) относятся:
-
Яйца (в идеале, сырые органические, от птицы, выращенной на вольном выпасе)
-
Мясо выпасных коров и зубров
-
Органическое мясо выпасных кур и страусов
-
Молочные продукты от выпасных животных (сырое молоко, сыр из сырого молока, и т.д.)
-
Пойманная в природе, не содержащая ртути рыба (можно есть только в том случае, если лабораторно подтверждено, что она не загрязненная)
При выборе источников белка крайне важно найти высококачественную продукцию.
Это может быть мясо выпасных (а не вскормленных зерном) животных, сырые (не пастеризованные) молочные продукты и пойманная (а не выращенная на ферме) рыба, которая точно не загрязнена ртутью и другими загрязняющими веществами.
Белок, действительно, очень полезен. Но, все же, ваше здоровье не станет лучше, если вы будете есть говядину от вскормленных на зерне коров (а именно такая продается в супермаркетах), курятину, напичканную пестицидами или богатую ртутью рыбу. Ваша задача обращать внимание на источники белка и то, как эта продукция была выращена.
Основной недостаток новой программы Weight Watchers
Теперь давайте рассмотрим главный недостаток новой программы Weight Watchers: они разрешают есть фрукты в неограниченном количестве. Если вы читаете эту информацию не в первый раз, то вы сразу же поймете, почему это может быть опасно для здоровья многих людей.
Дэвид Кирхофф все-таки предупреждает своих клиентов о переедании, говоря:
«Радуйтесь тому, что «стоимость» фруктов – 0 баллов, но не теряйте голову.
Лишь 10% американцев едят рекомендуемое количество фруктов, поэтому большинство из нас не рискуют переесть фруктов по новой программе. Тем не менее, если вы уже едите много фруктов ежедневно, не нужно удваивать или утраивать их количество - это приведет к замедлению потери веса.
В случае сомнений, используйте здравый смысл, слушайте сигналы своего тела (съешьте немного фруктов, потому что вы действительно голодны, а не потому, что можно) и старайтесь избегать бездумных перекусов (я, правда, тоже этим злоупотребляю)».
Однако, без учета остается тот факт, что фруктоза, в том числе, и полученная из фруктов, тоже очень вредна, с точки зрения здоровья, для тех, кто борется с резистентностью к инсулину, метаболическим синдромом, диабетом, высоким артериальным давлением или высоким уровнем холестерина. Все они, как правило, идут рука об руку с ожирением и избыточным весом...
Но даже с учетом этого, цельные плоды и содержащаяся в них фруктоза не так опасны, как фруктоза из добавленных сахаров. Считается, что одной из причин этого является наличие в цельных фруктах большого количества природных антиоксидантов, а также других синергетических веществ, которые могут помочь противостоять вреду от фруктозы.
Почему подсчет калорий неэффективен?
Итак, возвращаясь к основной проблематике, гораздо более важно учитывать источник калорий, чем вести их подсчет. Если бы было иначе, то можно было заменить один прием пищи шоколадкой и все равно худеть...
Еще в 2004 году в докладе Центра по контролю и профилактике заболеваний (ЦКЗ) сделаны точные выводы о том, что углеводы (читай: сахар и зерновые) являются причиной того, что за последние 30 с лишним лет американцы потребляют все большее количество калорий.
В то же время, показатели ожирения подскочили с 14,5% у взрослого населения США в 1971 году до почти 28% в 2010 г. Предыдущие исследования связывали этот рост с увеличением потребления соленых закусок, пиццы и другого фаст-фуда - другими словами, большим потреблением углеводов в виде зерновых.
Каков же ответ?
По большому счету, именно потребление углеводов, будь то в виде зерновых (включая цельное зерно) и сахаров (особенно фруктозы), определит, можете ли вы контролировать свой вес и поддерживать оптимальное состояние здоровья.
Если вы страдаете избыточного веса и/или других проблем со здоровьем, отказ или серьезное ограничение употребления зерновых углеводов и сахара может помочь вам избавится от этой проблемы.
Настоящим лекарством для вас станет возвращение на кухню и приготовление еды по добрым старым рецептам. Если вы не хотите тратить на это время, вы можете попросить об этом ваших родных, которые с радостью потратят время, что бы приготовить для вас свежие, полезные блюда.
Как и у многих людей, в моей жизни очень мало «свободного времени», но, ради своего здоровья, 95% своей еды я готовлю сам. Это по-настоящему важный процесс, который МОЖНО выполнять самостоятельно.
Голод – показатель оптимального уровня сытости для вашего организма
Многие этого не понимают, но частый голод может быть основным признаком того, что вы питаетесь не правильно. Это не только признак того, что вы едите неправильную еду, но это также говорит о том, что у вас, вероятно, имеется нарушение вашего индивидуального рациона питания.
Прелесть питания в соответствии с вашим обменом веществ заключается в отказе от пищевых пристрастий, благодаря чему намного легче уменьшить порции – безо всякого подсчета калорий или баллов.
Приемы пищи можно разделить на пять-шесть порций меньшего объема, при этом гораздо меньше ощущать чувство голода, чем раньше, потому что организм, наконец, получает топливо, необходимое ему для жизни.
Как правило, подбор оптимального рациона питания включает в себя пересмотр соотношения белков, жиров и углеводов, после того, как вы определите, для каких видов пищи предназначено ваше тело. Оптимальное здоровье, возможно, связано даже не с типом употребляемой пищи, а с относительным процентным содержанием каждого потребляемого продукта.
Если вы употребляете продукты в соответствии с вашим обменом веществ, питание будет обеспечивать вам огромный прилив энергии, заметное улучшение умственных способностей и эмоционального благополучия, а также чувство насыщения на несколько часов.
Но если после еды (через час или около того) вы чувствуете себя хуже, например:
-
Все еще чувствуете голод, даже если физически вы наелись
-
Возникает тяга к сладкому
-
Падает уровень энергии
-
Ощущаете возбудимость, нервозность, гнев или раздражительность
-
Чувствуете себя подавленным
... то вы, вероятно, употребляете неправильное для вашего обмена веществ сочетание белков, жиров и углеводов. В этом случае, я настоятельно рекомендую вам прочитать мою книгу Возьмите здоровье под свой контроль, в которой эти вопросы обсуждаются более подробно.опубликовано econet.ru.
© Джозеф Меркола
Остались вопросы — задайте их здесь
P.S. И помните, всего лишь изменяя свое сознание - мы вместе изменяем мир! © econet
Как организм превращает жир в энергию, и с какой эффективностью это происходит?
Жиры – это наиболее насыщенные энергией питательные вещества. При расщеплении одного грамма жира вырабатывается больше молекул АТФ, чем при расщеплении грамма белка или углеводов. АТФ служит универсальной энергетической валютой клетки: любой энергозатратный процесс в живом организме можно выразить в количестве молекул АТФ, необходимых для его протекания.
Поэтому жиры используются как энергетический резерв для организма: избыток питательных веществ, полученных с пищей в течении дня, откладывается в виде жировых капель в адипоцитах – клетках жировой ткани. Между приемами пищи жирные кислоты, из которых состоят жиры, могут поступать в кровь и использоваться в качестве источника энергии. Это происходит в процессе липолиза – отщепления жирной кислоты от молекулы триглицерида (жира). Липазы, отщепляющие жирные кислоты, активируются под действием адреналина или глюкагона – двух гормонов, разгоняющих обмен веществ, когда возникает дефицит питательных веществ, например, при голодании или большой физической нагрузке. Жирные кислоты связываются с альбумином и переносятся кровью к клеткам, которым необходима энергия.
Внутрь клеток жирные кислоты переносятся специальным транспортером. В цитоплазме клетки к жирной кислоте присоединяется кофермент А: затем в виде ацил-КоА жирная кислота переносится внутрь митохондрии – энергетической станции клетки. Там происходит процесс бета-окисления – от длинной углеродной цепочки жирной кислоты отсоединяется по 2 углеродных атома, до тех пор пока вся цепочка не расщепится полностью на двухуглеродные фрагменты в виде ацетил-КоА. Образованные в ходе бета-окисления молекулы ацетил-КоА поступают в цикл лимонной кислоты, где в процессе получения АТФ полностью расщепляются на воду и углекислый газ; за каждый оборот цикла в клетке образуется около 10 молекул АТФ. Общая энергоэффективность процесса будет зависеть от длины углеродной цепочки в составе жирных кислот.
Если исключить из диеты углеводы, жирные кислоты могут использоваться по-другому. В этому случае в клетках печени из них образуются кетоновые тела, которые поступают в кровь и могут использоваться как альтернативный глюкозе источник энергии.
Расщепление жиров – более трудоемкий и долгий процесс, чем использование углеводов. При физической нагрузке в первые несколько секунд для получения энергии используется накопленный АТФ, затем начинает расходоваться глюкоза, циркулирующая в крови, после этого начинает расщепляться гликоген, запасенный в мышцах. Примерно через 10-20 мин активных физических нагрузок все большую роль в обеспечении организма энергией начинает играть расщпление жиров.
12.5. Нарушения белкового обмена
Белок занимает центральное место в обмене веществ, обеспечивая жизнедеятельность организма, его связь с окружающей средой, адекватность реакций на внешние раздражители. Белки формируют структурную организацию всех клеточных элементов, пластическая роль неизмеримо выше энергетической, она незаменима. Без белков, их составных частей — аминокислот — невозможен синтез ферментов и гормонов, обеспечивающих анаболические и катаболические процессы в организме, их регуляцию. С белками связаны иммунная защита, функция опорных тканей, накопление и расходование энергии, сокращение мышц. Белки хранят генетическую информацию, формируемую в ходе эволюционного развития, являются материальными носителями жизни.
К основным причинам, вызывающим нарушения белкового обмена у домашних животных, следует отнести неполноценное, несбалансированное питание, заболевания органов пищеварения, почек, легких, нейроэндокринные расстройства, злокачественные новообразования, инвазионные и инфекционные болезни, сопутствующие им лихорадочные состояния.
Нарушение переваривания и всасывания белков. В желудочно-кишечном тракте белки подвергаются ферментативному расщеплению до аминокислот, которые подлежат всасыванию. Полноценный гидролиз возможен при нормальном функционировании желудка, кишечника, пищеварительных желез, симбионтной микрофлоры. Уменьшение поступления белков с кормом, нарушение его переваривания приводят к алиментарной белковой недостаточности.
Начинается процесс гидролиза крупных белковых молекул в желудке под влиянием пепсина. Снижение содержания хлористоводородной кислоты (гипо-, анацидные гастриты) тормозит превращение пепсиногена в пепсин; переваривающая сила желудочного сока падает. Гидролиз белков еще в большей степени может быть ослаблен при ограниченном поступлении в кишечник панкреатического сока, содержащего трипсин, хемотрипсин, карбок-сипептидазы, пептидазы. Внешнесекреторная недостаточность поджелудочной железы может усугубляться слабой активацией ферментов из-за дефицита энтерокиназы и желчи, разрушением, инактивацией ферментов вследствие роста микрофлоры в проксимальной части тонкой кишки.
Заключительный этап переваривания и интегрированное с ним всасывание аминокислот нарушаются при энтеритах, энтероколитах, гиповитаминозе А, лучевой патологии, нарушениях микроциркуляции, отеке слизистой оболочки кишечника.
Неутилизированные белки корма поступают в толстый кишечник. Пептиды и аминокислоты подвергаются там бактериальному расщеплению. Результатом гнилостного разложения будут образование, накопление и всасывание токсигенных аминов, таких, как кадаверин, гистамин, путресцин, тирамин; ядовитых ароматических соединений — фенол, крезол, индол; газов — метан, сероводород. Печень не в состоянии обезвредить избыточно образующиеся продукты гниения белка, возникает токсикоз.
Нарушение межуточного обмена белка. Аминокислоты, транспортированные через мембрану щеточной каймы энтероцитов, поступают в сосуды кишечной ворсинки, направляются к печени и включаются в обменные процессы. Метаболизм белков складывается из синтеза белковых молекул, их расщепления, превращения аминокислот, образования и выведения из организма конечных продуктов.
С момента зарождения в организме происходят синтез белка и распад его составляющих. Интенсивность этих процессов определяется физиологическим состоянием организма и регулируется нейроэндокринным механизмом. После денервации развивается атрофия тканей, их клетки становятся объектом аутоагрессии.
Многообразно влияние гормонов на синтез белков. Оно может распространяться на генетический аппарат клетки, стимулируя ее к размножению, на функции органоидов. Одним из важнейших гормонов, участвующих в регуляции метаболизма вообще и белкового обмена в частности, является соматотропин. Усиление белкового синтеза под его влиянием объясняют стимуляцией образования информационной РНК в ядре клетки, формирования рибосом, где синтезируется белок, подавлением внутриклеточных катаболических процессов, повышением проницаемости клеточной мембраны для аминокислот. Необычное повышение содержания гормона в раннем постнатальном периоде ведет к гигантизму, снижение — к противоположному эффекту. Избыток тироксина способствует катаболическим процессам, так же действуют глюкокортикоиды с преимущественным влиянием на лимфоидную, мышечную, соединительную ткани. Анаболическим эффектом, усиленным синтезом мышечного белка, обладают андрогены, тогда к эстрогены стимулируют развитие молочных желез, матки, эпителия влагалища. К анаболическим гормонам следует отнести инсулин, повышающий проницаемость клеточных мембран для аминокислот.
Повышенный распад белковых структур клеток (катаболизм) возникает при воспалительных процессах (альтерация, раневое истощение), гипоксии, аутоиммунных реакциях, ожоговой болезни язвенной болезни, злокачественных опухолях (раковая кахексия).
Нарушение соотношений между анаболическими и катаболи-жими процессами может сопровождаться изменениями содержания в крови белков и белковых фракций. Количество общего 1ка плазмы крови у здоровых животных колеблется в пределах -8,6 г/100 мл.
Гиперпротеинемия — повышение содержания общего белка в плазме крови. Бывает относительной (за счет обезвоживания) и абсолютной. Абсолютная часто сочетается с гиперглобулинемией — повышением глобулиновой фракции белков и соответствующим снижением альбуминов. Такую гиперпротеинемию блюдают у животных, страдающих многими инфекционными заболеваниями, пневмонией, нефрозом, злокачественными но-вообразованиями. Гиперпротеинемию выявляют в поствакцинальном периоде, при многих инфекционных заболеваниях в период нарастания антителогенеза за счет гамма-глобулинов, держание бета-глобулиновой фракции отмечают в случаях заболевания животных нефрозом, миеломой, гепатитом.
Гипопротеинемия — уменьшение содержания общего белка в плазме крови. Может быть результатом алиментарной недостаточности, нарушения переваривания и всасывания белка, усиленного деления его почками (нефрит, нефроз). Через почки обычно теряется мелкодисперсный белок — альбумин (альбуминурия). Гипопротеинемию наблюдают у животных с заболеваниями пета, когда снижена ее белковообразовательная функция после кровопотерь. Обильная экссудация, особенно у лошадей, приведет к падению уровня белка в крови, то же у животных, пострадавших от массивного ожога, гнойного распада тканей.
Диспротеинемия — многообразные нарушения соотношений жду отдельными фракциями белков крови. Рассматривают дишуноглобулинемию — нарушение нормального соотношения 1ельных иммуноглобулинов (IgG, IgM, IgE, IgA, IgD), дисглобулинемию — нарушение соотношений между отдельными фракции глобулинов (альфа-, бета-, гамма-глобулина), дисгамма-гло-шнемию — они могут быть количественными и качественными. Особую значимость имеет изменение содержания фибрина, зличение его концентрации в крови наблюдают у больных крупозной пневмонией, при острых и хронических воспалительных процессах, опухолях. Этот белок крови синтезируется в печени, поэтому гепатопатии могут вызвать снижение его уровня в крови, что приводит к замедлению свертываемости крови, ангиопатиям.
Нарушение конечных этапов белкового обмена. Метаболизм белков сопровождается синтезом и распадом белковых структур. В результате распада часть аминокислот вновь используется для процессов синтеза, а часть превращается в конечные продукты. Такими конечными азотистыми продуктами являются аммиак, мочевина, мочевая кислота, ее соли. Самыми токсичными свойствами обладает аммиак. В обычных условиях он нейтрализуется в печени угольной, фосфорной, другими кислотами с образованием аммонийных солей. Посредством сложных превращений аммиак преобразуется в мочевину.
Аммиак, мочевина, мочевая кислота, другие азотистые продукты обмена белка входят в состав остаточного, небелкового азота крови. У домашних животных уровень остаточного азота сыворотки крови колеблется от 26 мг/100 мл (собака) до 34 мг/100 мл (лошадь). Основная его часть представлена мочевиной, немочевинная названа резидуальным азотом.
Многие заболевания животных сопровождаются увеличением содержания остаточного азота в крови — гиперазотемией. Различают продукционную гиперазотемию и ретенционную.
Продукционная гиперазотемия наблюдается при усиленном патологическом распаде белка тканей (ожог, лучевая патология, травмы) с образованием большого количества безбелковых азотистых продуктов. Сюда же следует отнести последствия эксикоза — высыхания тканей из-за обезвоживания и утери электролитов. Мочевинообразовательная функция печени подавлена. В крови повышается содержание резидуального азота, главным образом за счет аммиака, не преобразованного в мочевину. Аммиак легко преодолевает гематоэнцефалический барьер и способен вызвать уремическую кому.
Ретенционная гиперазотемия развивается при заболеваниях почек, нарушениях выделительной функции обеих почек, обусловленных острым диффузным нефритом, механическим препятствием оттоку мочи (уролитиаз, аденома). Количество остаточного азота пропорционально степени тяжести патологического процесса. Возникающая уремия сопровождается токсикозом.
Конечный продукт обмена нуклеиновых кислот — мочевая кислота. Избыточное образование и снижение выведения мочевой кислоты возможны при заболеваниях животных лейкозом, поражениях почек. Давно описано заболевание, вызываемое увеличением содержания мочевой кислоты в крови, — подагра. Причины и механизм гиперурикемии изучены недостаточно. К факторам риска относят избыточное поступление пуринов (мясо) в организм, молибденоз. У животных классифицируется как суставная форма мочекислого диатеза. Описана у кур и собак. Образующиеся соли мочевой кислоты начинают усиленно откладываться на суставных поверхностях, в хрящах, связках. Возникает острое воспаление суставов (подагрический артрит), сопровождающийся отечностью, сильной болью, лихорадочной реакцией, хромотой, деформацией суставов.
66. Депонирование и мобилизация жиров в жировой ткани. Регуляция синтеза и мобилизации жиров. Роль инсулина, глюкагона и адреналина.
Какой процесс будет преобладать в организме - синтез жиров (липогенез) или их распад (липолиз), зависит от поступления пищи и физической активности. В абсорбтивном состоянии под действием инсулина происходит липогенез, в постабсорбтивном состоянии - липолиз, активируемый глюкагоном. Адреналин, секреция которого увеличивается при физической активности, также стимулирует липолиз.
Регуляция синтеза жиров. В абсорбтивный период при увеличении соотношения инсулинглюкагон в печени активируется синтез жиров. В жировой ткани индуцируется синтез ЛП-липазы в адипоцитах и осуществляется её экспонирование на поверхность эндотелия; следовательно, в этот период увеличивается поступление жирных кислот в адипоциты. Одновременно инсулин активирует белки-переносчики глюкозы - ГЛЮТ-4. Поступление глюкозы в адипоциты и гликолиз также активируются. В результате образуются все необходимые компоненты для синтеза жиров: глицерол-3-фосфат и активные формы жирных кислот. В печени инсулин, действуя через различные механизмы, активирует ферменты путём дефосфорилирования и индуцирует их синтез. В результате увеличиваются активность и синтез ферментов, участвующих в превращении части глюкозы, поступающей с пищей, в жиры. Это - регуляторные ферменты гликолиза, пируватдегидрогеназный комплекс и ферменты, участвующие в синтезе жирных кислот из ацетил-КоА. Результат действия инсулина на обмен углеводов и жиров в печени - увеличение синтеза жиров и секреция их в кровь в составе ЛПОНП. ЛПОНП доставляют жиры в капилляры жировой ткани, где действие ЛП-липазы обеспечивает быстрое поступление жирных кислот в адипоциты, где они депонируются в составе триацилглицеринов. Запасание жиров в жировой ткани - основная форма депонирования источников энергии в организме человека. Запасы жиров в организме человека массой 70 кг составляют 10 кг, но у многих людей количество жиров может быть значительно больше. Жиры образуют в адипоцитах жировые вакуоли. Жировые вакуоли иногда заполняют значительную часть цитоплазмы. Скорость синтеза и мобилизации подкожного жира происходит неравномерно в разных частях организма, что связано с неодинаковым распределением рецепторов гормонов на адипоцитах.
Регуляция мобилизации жиров. Мобилизация депонированных жиров стимулируется глюкагоном и адреналином и, в меньшей степени, некоторыми другими гормонами (соматотроп-ным, кортизолом). В постабсорбтивный период и при голодании глюкагон, действуя на адипоциты через аденилатциклазную систему, активирует протеинкиназу А, которая фосфо-рилирует и, таким образом, активирует гормончувствительную липазу, что инициирует липо-лиз и выделение жирных кислот и глицерина в кровь. При физической активности увеличивается секреция адреналина, который действует через β-адренергические рецепторы адипоцитов, активирующие аденилатциклазную систему. В настоящее время обнаружено 3 типа β-рецепторов: β1, β2, β3, активация которых приводит к липолитическому действию. К наибольшему липолитическому действию приводит активация β3-рецепторов. Адреналин одновременно действует и на α2-рецепторы адипоцитов, связанные с ингибирующим G-белком, что инактивирует аденилатциклазную систему. Вероятно, действие адреналина двояко: при низких концентрациях в крови преобладает его антилиполитическое действие через α2-рецепторы, а при высокой - преобладает липолитическое действие через β-рецепторы.Для мышц, сердца, почек, печени при голодании или физической работе жирные кислоты становятся важным источником энергии. Печень перерабатывает часть жирных кислот в кетоновые тела, используемые мозгом, нервной тканью и некоторыми другими тканями как источники энергии. В результате мобилизации жиров концентрация жирных кислот в крови увеличивается приблизительно в 2 раза, однако абсолютная концентрация жирных кислот в крови невелика даже в этот период. Т1/2 жирных кислот в крови тоже очень мал (менее 5 мин), что означает существование быстрого потока жирных кислот из жировой ткани к другим органам. Когда постабсорбтивный период сменяется аборбтивным, инсулин активирует специфическую фосфатазу, которая дефосфорилирует гормончувствительную липазу, и распад жиров останавливается.

2.5 Взаимосвязь белкового и углеводного обменов
|
|
|
|
| O |
|
|
| диацилглицерол- |
|
|
|
|
|
|
| O | |
O |
| Ch3 | O C R1 |
|
|
| O |
| Ch3 | O | C R1 | |||||||
|
|
| O ацилтрансфераза |
| ||||||||||||||
R2 | С O | HC | + | R3 |
| С |
| R2 | С O | HC |
|
|
| O | ||||
|
|
|
|
|
|
|
|
| ||||||||||
| Ch3 |
| OH |
|
| SКоА |
|
| Ch3 |
| O | C |
| R3 | ||||
|
|
|
|
|
|
|
|
|
| |||||||||
1,2-диацилглицерол |
|
| НS-КоА |
| триацилглицерол | |||||||||||||
ацил-КоА |
|
| ||||||||||||||||
|
|
|
|
|
|
|
|
|
| |||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||
Связующим звеном белкового и углеводного объемов является цикл трикарбоновых кислот. Продукты гликолиза и окислительного расщепление углеводов в ЦТК – пировиноградная, α-кетаглутаровая, щавелевоуксусная кислота в результате аминирования и переаминирования образуют многие аминокислоты, используемые для синтеза белка. Из фосфоенолпирувата (гликолиз) через ряд превращений синтезируется предшественник фенилаланина, тирозина, триптофана – шикимовая кислота. Гистидин образуется из рибозо-5-фосфата (участника пентозофосфатного цикла). Таким образом, продукты расщепления углеводов при аминировании дают аминокислоты, из которых синтезируются белки.
Переход от белков к углеводам начинается с гидролиза белков до аминокислот, которые затем дезаминируются, а выделившиеся кетокислоты (ПВК, α-ке- тоглутарат, оксалоацетат) вступают в ЦТК и через пируват включаются в реакции глюконеогенеза с образованием углеводов. Однако белки по сравнению с углеводами являются для живого организма более ценными соединениями, образующими основу всех клеточных структур, поэтому их превращение в углеводы происходит в природе в небольших масштабах.
Использование белков в процессе дыхания также наблюдается крайне редко, при длительном углеводном дефиците. Активно образуются углеводы из белков и аминокислот у больных сахарным диабетом.
2.6 Взаимосвязь белкового и липидного обменов
Рассмотренные взаимосвязи «белки углеводы» и «углеводы липиды»
дают основание для объединения их в единую цепь «белки углеводы липиды», в которой углеводы являются связующим звеном между белками и липидами.
Один из основных продуктов расщепления липидов – ацетил-КоА, включаясь в ЦТК, образует кетокислоты, аминирование которых дает аминокислоты.
Из другого продукта гидролиза липидов глицерина – в результате цепи превращений синтезируются циклические аминокислоты.
В известной мере возможен и обратный процесс синтеза липидов за счет распадающихся белков. Продукты дезаминирования аминокислот через ЦТК и другие метаболические процессы образуют ПВК, при окислительном декарбоксилировании которого возникает ацетил-КоА – исходное соединение для синтеза жирных кислот и других компонентов липидов.
Из всего вышесказанного видно, что превращения веществ в организме тесно связаны друг с другом. В Приложении А приведена обобщенная схема взаимо-