Гипербилирубинемия у новорожденных что это такое
Гипербилирубинемия новорожденных
У новорожденных, в отличие от детей других возрастных групп, гипербилирубинемия чаще всего является проявлением функциональной незрелости печени. Эта так называемая физиологическая желтуха является обычным состоянием, однако часто на ее фоне возникают многочисленные патологические состояния, которые сопровождаются высоким содержанием несвязанного билирубина в крови.
Поскольку билирубин обладает токсическим действием необходимо проводить мониторинг его в крови и назначать своевременное лечение, направленное на снижение уровня несвязанного билирубина в крови.
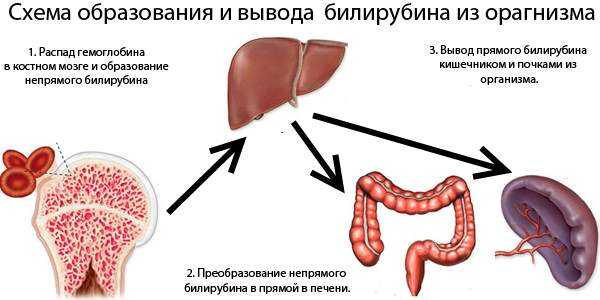
Образование и экскреция билирубина
Билирубин является продуктом распада гема и производится ретикулоэндотелиальной системой печени, селезенки и костного мозга. Основным источником билирубина является гемоглобин. Небольшое количество его синтезируется из гемовых белков.
Несвязанный билирубин плохо растворяется в воде, но хорошо проникает в жировые клетки. В плазме крови транспортируется с помощью альбумина (связывается с альбумином).
У здорового человека в плазме крови определяется только небольшое количество несвязанного билирубина, но его уровень может повышаться при гипоальбуминемии и при наличии в крови таких конкурентов за связь с альбумином, как свободные жирные кислоты и некоторые лекарственные средства.
Билирубин поступает в печень с помощью переносчиков-лигандов, связывается с глюкуроновой кислотой в присутствии глюкуронилтрансферазы и превращается в моно -, а затем в диглюкуронид билирубина, который является нетоксичным водорастворимым соединением. В дальнейшем диглюкуронид билирубина экскретируется в желчь.
У новорожденных, особенно недоношенных, отмечается незрелость некоторых печеночных функций, таких как потребление, связывание и экскреция билирубина. У доношенных новорожденных эти функции развиваются в течение первых 2 недель постнатальной жизни.
Кишечник новорожденного ребенка содержит глюкуронидазу, под влиянием которой происходит деконъюгация связанного билирубина, поступающего в кишечный просвет с желчью. При этом в кишечнике отсутствуют бактерии, способные его редуцировать в уробилиноген.
Часть связанного билирубина реабсорбируется в кишечнике – таким образом, возникает кишечно-печеночная циркуляция желчи. У новорожденных билирубин, секвестрированный в меконий, является важным компонентом общего билирубинового пула. Чем больше время транзиторного прохождения билирубина через кишечник, тем больше он реабсорбируется.
Причины развития желтухи у новорожденных.
Сразу после рождения относительно незрелая печень новорожденного ребенка обеспечивает единственный путь экскреции билирубина, который может легко подавляться на фоне перенесенной гипоксии, инфекционного заболевания и по другим причинам.
Итак, у новорожденных, в отличие от детей других возрастных групп, гипербилирубинемия может быть не патологической, а проявлением функциональной незрелости печени.
Под физиологической желтухой часто скрыты многочисленные патологические варианты желтухи, которые имеются у новорожденных.
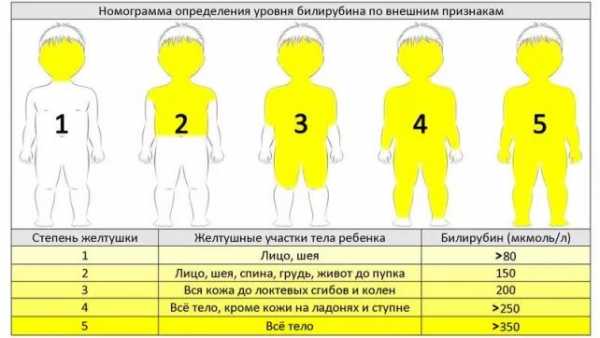
Желтушность кожи становится видимой, если уровень билирубина в крови достигает 85 мкмоль/л. Если желтушность кожи возникает в первые 24 часа жизни, это свидетельствует о ее патологическом характере и необходимости исключения гемолиза. У здоровых доношенных новорожденных пиковая концентрация билирубина в сыворотке крови наблюдается на 3 — 4-е сутки жизни, однако она исчезает до 2-х недель. При этом физиологический уровень прироста билирубина в сыворотке крови не должен превышать 80 — 100 мкмоль/л.
Патологические факторы, вызывающие желтуху у новорожденных.
Гемолиз:
- Резус конфликт;
- Несовместимость по ABO системе;
- Другие виды красноклеточной антигенной несовместимости,
например Kell, Kid, Duffi; - Нарушение структуры мембраны эритроцитов, например сфероцитоз;
- Нарушение ферментов эритроцитов, например недостаточность глюкозо-6-фосфатдегидрогеназы, пируваткиназы;
- Альфа-талассемия;
- Бета-, гамма-талассемия;
- Инфекционные процессы.
Недостаточность глюкуронилтрансферазы:
- Синдром Клиглера-Найара;
- Синдром Жильбера.
Нарушение экскреции билирубина:
Сочетание связанного и несвязанного билирубина метаболического и инфекционного происхождения:
- Метаболического происхождения: муковисцидоз, галактоземия, недостаточность α-антитрипсина, фуктоземия, тирозинемия.
- Инфекционного происхождения: гепатит, вызванный цитомегаловирусом, возбудителями токсоплазмоза, ветряной оспы, герпеса, сифилиса, гепатита В, листериоза, вирусом Коксаки;
Кишечно-печеночная циркуляция билирубина:
- Акинезия кишечника;
- Высокая кишечная непроходимость;
- Мекониальный илеус.
Внутри и внепеченочные причины:
- Холестаз;
- Синдром сгущения желчи;
- Атрезия желчевыводящих протоков.
Лечение гипербилирубинемии новорожденных
Объем терапевтических мероприятий и их неотложность определяются по следующим показателям:
- Время возникновения гипербилирубинемии;
- Уровень билирубина в крови;
- Почасовая скорость прироста билирубина;
- Величина гемоглобина в пуповинной крови новорожденного ребенка;
- Возраст ребенка (гестационный и неонатальный).
В первые 12 часов жизни при исходном уровне билирубина 100 мкмоль /л за 1 час и содержании гемоглобина в пуповинной крови менее чем 120 г/л на фоне показателя гематокрита 35% показано немедленное заменное переливание крови.
В более поздний срок (после 12 — 24 часов жизни) объем и скорость терапевтических мероприятий зависит от уровня несвязанного билирубина в крови.
Фототерапию начинают, если уровень билирубина в крови превышает 100 мкмоль/л.
Во время проведения фототерапии имеют значение три физические характеристики:
- Длина световой волны. Нет сомнения в том, что волны синего света (425 — 427 нм) эффективны в разрушении билирубина. Однако синий свет содержит некоторые волны, которые являются потенциально токсичными. Волны длиной 350 — 450 нм является мутагенным, а значит потенциально канцерогенными. Кроме того, у медицинского персонала, работающего с источниками синего света, часто отмечается головная боль. Иногда во время проведения фототерапии трудно оценить цвет кожи новорожденного ребенка. Во время проведения фототерапии обязательно следует использовать подгузники, а глаза надежно закрывать повязкой.
- Световой поток — это мера потока излучения, попадающего на определенный участок кожи новорожденного ребенка и выражается в милливаттах на 1 см2. Клинические данные предполагают повышение клиренса билирубина в зависимости от увеличения светового потока до момента достижения точки насыщения. Для синего спектра с длиной волны 425 — 475 нм эта точка находится между 1 и 3 мВт/см2.
- Продолжительность экспозиции. Фототерапию необходимо проводить постоянно, в зависимости от уровня билирубина в крови. Его контроль проводят через 4 часа после начала фототерапии. При критических значениях непрямого билирубина его уровень определяют и во время проведения светотерапии.
Побочные эффекты фототерапии:
- Термическое воздействие. Хотя инфракрасные лучи рассеиваются, но дети, которые находятся в инкубаторах, во время проведения фототерапии получают достаточное количество тепла, чтобы перегреться.
- Потеря жидкости. За время проведения фототерапии объем жидкости, который вводится ребенку, увеличивается на 1 мл/кг в час.
- Изменения перистальтики кишечника. В некоторых новорожденных отмечается учащение стула, сопровождающееся потерей жидкости. Однако дополнительно введение электролитов при этом не требуется.
- Синдром «бронзового ребенка». Этим термином обозначают развитие у новорожденного ребенка ярко желтушного окрашивания кожи при обструктивной желтухе во время проведения фототерапии. Вероятно, это связано с накоплением и распадом фотоизомера билирубина, вследствие нарушенной билиарной экскреции.
- Сыпь. Возникает нечасто и быстро исчезает. Считается, что ее проявление свидетельствует о местном высвобождение гистамина из тучных клеток кожи.
Показания к заменому переливанию крови в случае неэффективности фототерапии.
- У недоношенных детей заменное переливание крови показано, если уровень билирубина (мкмоль/л), несмотря на проведение фототерапии, достигает 10% от массы тела + 100 мкмоль/л.
- У доношенного ребенка заменное переливание крови показано, если на протяжении 4 – 6 часов облучения синим светом концентрация общего билирубина превышает 430 мкмоль/л. Его осуществляют при любых обстоятельствах, если уровень общего билирубина превышает 510 мкмоль/л.
Другие методы терапии
- Раннее начало кормления грудью улучшает отхождение мекония и стимулирует желчеотделение.
- Парантеральное введение жидкости и электролитов уменьшает степень выраженности дегидратации, ацидоза, предотвращает накопление свободных жирных кислот, которые конкурируют с билирубином за связывание с альбумином.
- Фенобарбитал — назначают при длительной гипербилирубинемии, в дозе 5 — 10 мг/кг в сутки. Начало его действия отмечается не ранее чем через 3 суток от назначения.
Литература: Интенсивная терапия в педиатрии Г. И. Белебезев, Киев, 2008 год.
Похожие статьи:
О причинах длительной гипербилирубинемии у новорожденных детей
За последние годы отмечена тенденция к более длительному (затяжному) течению так называемой физиологической (конъюгационной) желтухи у практически здоровых детей, получающих не только грудное, но и смешанное или искусственное вскармливание. Продолжительность желтухи нередко переходит границы первого месяца жизни (Г.В. Яцык, И.А. Беляева, Е.П. Бомбардирова 2007). Неонатальная желтуха в педиатрии всегда требует дифференциальной диагностики. Необходимо исключать гемолитический, паренхиматозный и механический патогенез желтухи. Желтуха у любого ребенка старше 3 недель должна вызывать подозрение на заболевание и побуждать к соответствующей оценке. Умение распознать желтуху, отнести ее в ту или иную группу, выбрать тактику лечения – все это определяет не только ближайший, но и отдаленный прогноз развития ребенка. Как правило, наиболее частые установленные причины длительной гипербилирубинемии выявляются в следующих случаях: использование фармакологических препаратов, желтуха у детей с эндокринной патологией, желтуха при избыточном гемолизе эритроцитов. Желтуха при нарушении пассажа кишечного содержимого, наследственные заболевания с непрямой гипербилирубинемией, желтуха при инфекционных заболеваниях и при сепсисе, желтуха от недокорма желтухой от материнского молока. Однако в ряде случаев установить причину затяжной желтухи не представляется возможным. Анализируя другие причины длительной гипербилирубинемии, следует учесть ухудшающуюся экологическую ситуацию на планете. Современный уровень развития науки не позволяет предусмотреть и охватить все агрессивные факторы, воздействующие на плод. Известно, что соли тяжелых металлов, диоксины провоцируют длительное течение гипербилирубинемии (Хлебович И.А, 2001,Юфит С.С.2001). Хазанов А.А. (2009) не исключает, что ранняя вакцинация детей способствует более длительной и более продолжительной гипербилирубинемии. При введении в 2001году в график вакцинации детей прививки против гепатита В, вводимой в первые сутки жизни количество случаев госпитализации детей с длительной неонатальной желтухой увеличилось, по собственным данным, с 5,7 на 100, до 10 случаев на 100 госпитализаций с последующей стабилизацией в последующие годы. Приобретает огромное значение изменение качества пищевых ингредиентов. Исследования Генри Ландана (1948), Пола Бергмана (1998) показали, что практически во всех основных «пунктах» биологической цепи «почва – растения – животные – человек» отмечено в 8 раз снижение эссенциальных нутриентов – минеральных веществ и витаминов. Не только традиционные технологии выращивания питательных культур, но и современные технологии переработки приводят к потере важных нутриентов. Например, рафинирование растительных масел приводит к потере лецитина, витаминов А и Е, минеральных веществ. Отрицательная динамика экономического статуса основной части населения России, сложившиеся стереотипы питания, в том числе основанные на fast-food и полуфабрикатах, изменили структуру питания в сторону значительного уменьшения потребления наиболее ценных пищевых продуктов. Повседневный рацион большинства россиян на сегодняшний день – это углеводно-жировая, с недостаточным количеством животного белка, дефицитом витаминов, микроэлементов и балластных веществ. Дефицит любой из незаменимых аминокислот в рационе ведет к нарушению синтеза белковых веществ. Не всякий белок имеет полный набор всех аминокислот, и не все аминокислоты одинаково важны для организма. Существенной особенностью аминокислот и белкового обмена у новорожденных детей является неспособность к эндогенному образованию ряда аминокислот, из-за чего перечень незаменимых аминокислот для них оказывается дополненным еще тремя - гистидином, тирозином и цистином. Под нашим наблюдением находился на лечении 99 пациент с длительной неонатальной желтухой с неуточненной этиологией. Дети поступали в стационар в возрасте от 6 суток до 3 месяцев жизни. Во всех случаях желтуха имела признаки патологической, то есть длилась более 3 недель. В тоже время гемолитический, механический и паренхиматозный характер желтух был исключен в ходе наблюдения за детьми. Все дети родились после 37 недель гестации. В первые сутки жизни всем детям введена вакцина против гепатита В. Проведен анализ историй болезни этих детей, с выявлением наиболее часто встречающихся клинических проявлений, регистрацией предполагаемых причин возникновения пролонгированной желтухи, динамики изменения клинико-лабораторных показателей. У всех пациентов определялся ряд лабораторных, клинических и инструментальных тестов на момент поступления и в динамике наблюдения (исследование билирубина, общего белка, щелочной фосфатазы, гемоглобина, ультразвуковое исследование печени и желчевыводящих путей). С помощью прибора флуориметра «АКЛ-1» и набора реактивов «Зонд-Альбумин» определялась общая и эффективная концентрация альбумина. По интенсивности флуоресценции определяют два показателя: общую концентрацию альбумина (ОКА) и так называемую эффективную концентрацию альбумина (ЭКА), являющуюся “эквивалентом полноценного альбумина”. Рассчитаны показатели связывающей способности (РСА - резерв связывания альбумина) и "индекс токсичности" (Т=ОКА/ЭКА - 1).Индекс токсичности более 0,1 -признак интоксикации организма. Все больные с высоким показателем индекса токсичности (более 0,1) включены в основную группу(49детей) и распределены на подгруппы с учетом степени гипербилирубинемии. В контрольную группу(50детей) вошли дети с нормальными показателями индекса токсичности ( до 0,1). При хорошей альбуминсвязывающей функции альбумина уровень венозного и периферического билирубина отличается в среднем на 22,06 мкмоль\л при низкой гипербилирубинемии, и на 70,25 мкмоль\л при высокой гипербилирубинемии. При сниженной связывающей способности альбумина разница венозного и периферического билирубина выражена меньше- 7,44 мкмоль\л при низкой гипербилирубинемии и 59,4 мкмоль\л,т.е .разница составляет 15- 20 мкмоль\л.Общая концентрация альбумина практически одинакова у детей в основной-36,43+_4,86г\л и контрольной группах-38,6+_5,95г\л. Достоверные различия(р<0,05) выявлены при определении эффективной концентрации альбумина. В основной группе-29,55+_5,5г\л, в контрольной группе-36,3+_5,97. Волнообразное течение неонатальной желтухи, то есть повторное повышение уровня билирубина после эпизода его снижения, является важным признаком патологического течения желтухи. Снижение билирубинсвязывающей способности альбумина сопровождаются более низкими показателями гемоглобина, что является косвенным признаком дефицитного состояния. У детей с достаточной билирубинсвязывающей способности альбумина желтуха разрешается быстрее на 5,67+_2,76 дня(p<0,05).У матерей детей со сниженными показателями альбуминсвязывающей функции плазмы группы чаще выявлены гестозы беременных, артериальная гипертензия. Обращает внимание большое количество женщин с угрозой невынашивания беременности и в основной, и в контрольной группах (р>0,001). В основной группе -13 (26,5+_6,3%) детей родилось с помощью оперативных родов, в контрольной группе -7 (14%+_4,91%). Применение дополнительных медикаментов, а также причины, повлекшие оперативное родоразрешение оказывают влияние на состояние связывающей функции альбумина, поэтому у детей основной группы в 1,8 раза чаще зарегистрированы оперативные роды. На основании полученных данных выяснено, что причина пролонгированной желтухи у детей контрольной группы более очевидна, чем в основной. Чаще выявлены транзиторная гипофункция щитовидной железы, желтуха, как следствие рассасывания кровоизлияний, желтуха грудного молока, прием препаратов, конкурирующих за альбумин, холестаз в желчных путях, встречается наследственная патология по нарушениям обмена веществ. В основной группе происходит нарушение билирубинового обмена на уровне нарушения связывания билирубина с альбумином, в результате желтушный синдром протекает торпидно и волнообразно. Предложено классифицировать данный тип желтухи, как «Неонатальная желтуха вследствие снижения альбуминсвязывающей функции плазмы».
Проведенное исследование позволило сформировать клинические критерии для определения этого типа желтух:
· Анамнез – тяжелые гестозы, низкие весовые прибавки, анемия, гиповитаминозы, декомпенсация соматической патологии
· Стериотип питания – вегетарианство матери и необычные пищевые пристрастия.
· Сопутствующие состояния – выявленные дефицитные состояния у ребенка (анемия, дефицит витаминов и минералов)
· Особенности течения желтухи – длительное, торпидное, волнообразное
· Особенности распределения билирубина – билирубин периферической крови больше или равен билирубину венозной крови.
Качество грудного молока определяет качество образовавшегося альбумина в организме ребенка. Аминокислотный состав материнского молока отражает состав белков пищи матери. При нормально протекающей беременности и хорошем питании матери женское молоко содержит все необходимые вещества в оптимальных соотношениях. Однако при наличии осложнений (гестозы, анемии) или несбалансированном, неполноценном питании матери грудное молоко не содержит в достаточном количестве многих незаменимых веществ, в частности, отмечается дефицит ряда аминокислот (лейцина, изолейцина, метионина, валина) и микроэлементов (цинка, меди, кобальта). В настоящее время проблематично обеспечить полноценный рацион питания беременных, содержащий все необходимые вещества. Это связано с истощением почв, загрязнением внешней среды ксенобиотиками, использованием различных химических добавок (красителей, консервантов, улучшителей вкуса и др.) при производстве продуктов питания, сложным экономическим положением неработающих женщин, находящихся в декретном отпуске по беременности и уходу за ребенком. Более значительные отклонения по содержанию витаминов и микроэлементов имеет грудное молоко при изменении диеты кормящей женщины и явно нарушается при их низком содержании в продуктах питания (долго хранящиеся продукты питания). Отсутствие необходимых микронутриентов в питании лактирующей женщины отражается на удовлетворении потребностей ребенка, а, следовательно, и на формировании его физического и интеллектуального здоровья в раннем возрасте и последующей жизни. Чтобы грудное молоко было наиболее полноценным по всему набору микронутриентов (минеральные вещества, микроэлементы, витамины), необходимо в рацион питания лактирующей женщины включать разнообразные продукты. Однако, даже в относительно свежих продуктах, в их необходимом ежедневном количестве содержание витаминов и микроэлементов в большинстве случаев будет недостаточным. Так у женщин, проживающих в сельской местности, уровень основных ингредиентов выше, чем в городе. (Л.А.Каминская, И.Г.Данилова, И.Ф.Гетте, Н.Е.Санникова, И.В.Вахлова.2006)Поскольку, затяжная желтуха у грудных детей чаще всего связана с грудным вскармливанием, следует обеспечить достаточную секрецию молока, создать его качественную адекватность. Дефицит калорий ухудшает коньюгацию билирубина, дефицит углеводов уменьшает количество глюкуроновой кислоты, снижает энергетическое обеспечение на всех этапах билирубинового обмена, дефицит белка снижает альбуминсвязывающую функцию плазмы, также необходимо достаточное обеспечение витаминами и микроэлементами.
Защита от ксенобиотиков в каждом индивидуальном случае должна включать: ограничение животных жиров, употребление очищенной воды, ограничение в питании пищевых консервантов и красителей, использование овощей и фруктов, выращенных естественным путем.
Литература:
1. Грызунов Ю.А., Добрецов Г.Е. «Проведение измерений параметров ЭКА И ОКА на анализаторе АКЛ-01.», «"Альбумин сыворотки крови в клинической медицине" Под ред. Ю.А.Грызунова, Г.Е.Добрецова. Кн. 1, Москва., «ГЭОТАР», 1998. -с.104-107
2. Грызунов Ю.А., Миллер Ю.И.,Добрецов Г.Е., Пестова А.Б. «Флюоресцентный способ определения массовой концентрации альбумина сыворотки крови человека», «Клинико-лабораторная диагностика»,1994,5,27-31
3. Грызунов Ю.А.,Иванов А.И., Белова Е.С. «Влияние некоторых метаболитов на связывание флуоресцентного зонда К-35 с альбумином», «Альбумин сыворотки крови в клинической медицине» Под ред. Ю.А.Грызунова, Г.Е.Добрецова, Москва, «Ириус»,1994,93-103.
4. Л.А.Каминская, И.Г.Данилова, И.Ф.Гетте, Н.Е.Санникова, И.В.Вахлова. «Лабораторный мониторинг состава грудного молока для оценки развития ребенка»,2006, Уральский государственный медицинский институт, Екатеринбург. http://blago.toms
5. Нисевич Л.Л., Язык Г.В., Аширова А.А., Дворяковский И.В. «Затяжные желтухи у недоношенных новорожденных», журнал «Педиатрия», № 6, 1998,с.59-63.
6. Омаров, Н.С-М. Абдуллаев Р.А. ,« Аминокислотный состав белков женского молока при позднем гестозе на фоне железодефицитной анемии», «Южно-Российский медицинский журнал » № 4-5 '99 , стр. 32-37
7. Сафонов А.Б., Сергеев В.Н. «Лечебно-профилактические аспекты метаболической терапии хронических неинфекционных заболеваний» журнал «Педиатрия имени Г.Н. Сперанского»№1, 2004,с.92-99
8. Хазанов А.И. «Клиническая неонатология», «Гиппократ», 424
9. Хлебович Игорь Александрович. « Системный анализ географических предпосылок болезней человека»: диссертация ... доктора географических наук в форме науч. докл. : 25.00.36.- Барнаул, 2001.- 61 с.: ил. РГБ ОД, 71 02-11/25-4
10. Хорошилов И.Е « Правильное питание беременных и кормящих женщин», «Гинекология» том 08/N 5/2006,стр. 32-37
11. Юфит С.С. «Диоксины в грудном молоке» Материалы семинара "Стойкие органические загрязнители и здоровье человека" Москва, 15-16 мая, 2001г
12. Яцык Г.В., Беляева, Е И. Бомбардирова А..П. «Эффективность препарата Хофитол в терапии желтух новорожденных» «Российский вестник перинатологии и педиатрии», том 52, №2, 2007, стр.20-22, Москва
Желтуха (гипербилирубинемия) у новорожденных – симптомы
Типы желтухи у новорожденных
Желтуха у новорожденных, которая вызывает пожелтение кожи и глаз, вызвана накоплением билирубина в крови (гипербилирубинемия). В утробе плод получает питательные вещества и избавляется от продуктов побочной деятельности, например от билирубина, через пуповину. После рождения органы ребенка должны исполнять эту функцию.
У новорожденных может развиться желтуха от накопления билирубина по слегка различным причинам.
Физиологическая желтуха
Физиологическая желтуха развивается в течение 1-5 дней после рождения из-за того, что органы ребенка не в состоянии эффективно избавляться от излишнего билирубина. Факт того, будет этот тип желтухи заметен или нет зависит от того, насколько высокий уровень билирубина в крови.
Если желтуха протекает в заметной форме, пожелтение кожи и глаз проявляется примерно в первые 24 часа после рождения и может усиливаться до трех-четырех дней. Чаще всего, уровень билирубина в крови постепенно понижается, а желтизна пропадает или проходит сама по себе в течение недели и при этом не возникает осложнений.
Недоношенные дети, чьи органы не полностью развиты, не могут эффективно избавляться от билирубина, как это делают дети, которых выносили полный срок, в результате чего появляется заметное пожелтение, которое соотносят с развитием желтухи.
Желтуха при кормлении грудью
Желтуха при кормлении грудью может быть вызвана легким обезвоживанием, в результате которого продляется и усиливается физиологическая желтуха. Обезвоживание способствует развитию желтухи, потому что из-за обезвоживания организму ребенка труднее выводить билирубин из организма. Желтуха при кормлении грудью может развиться, когда ребенок не получает достаточного количества жидкости, чаще всего это происходит из-за большого промежутка между кормлениями. При каждом приеме пищи у матери обычно вырабатывается от 14.17 г до 21.26 г молозива перед тем, как пойдет молоко. Большинству детей каждые 4 часа необходимо от 28.35 г до 42.52 г жидкости. Если кормить детей грудью каждые 4 часа или реже (как это обычно происходит с детьми, которых выращивают на искусственном питании) постепенно столкнуться с обезвоживанием, а уровень билирубина в крови увеличится или останется на том достаточно высоком уровне.
Если ребенка кормить грудью регулярно, то вероятность развития желтухи намного ниже. Американская академия педиатров рекомендует, чтоб матери кормили ребенка грудью 8-12 раз в день. Если признаки желтухи проявляются очень сильно, то можете кормить ребенка каждые 2 часа.
Частые кормления повышают выработку молозива (а также молока, в состав которого входит молозиво), в результате чего ребенок получает достаточное количество питательных веществ и жидкости, позволяющей ему избавиться от излишнего билирубина. Если Вы будете добавлять в молоко воду или сахар, то не снизите уровень билирубина в крови ребенка.
Желтуха от грудного молока
После физиологической желтухи или желтухи при кормлении грудью, или после выздоровления после обоих видов желтухи (обычно к 5-7 дню от рождения), у детей, которых кормят грудью, уровень билирубина может снова увеличиться в течении второй недели (10-14 дней), Этот тип желтухи скорее всего связан с тем, каким образом определенные компоненты в грудном молоке влияют на уменьшение билирубина в крови ребенка.
Обычно, желтуха от грудного молока постепенно проходит, хотя у большинства детей сохраняются легкие симптомы желтухи на протяжении всего периода кормления грудью. Уровень билирубина редко поднимается до опасного уровня, а чаще всего профессионалы рекомендуют продолжать практику частого кормления грудью. Иногда проводят анализ уровня билирубина в крови, чтобы убедится, что уровень билирубина находится на приемлемом уровне.
Чаще всего билирубин не вызывает проблем, но время от времени уровень билирубина в крови новорожденных поднимается до уровня, который может составлять опасность. Когда это происходит, пожелтение на коже и глазах ребенка (желтуха) становятся более заметными, и ребенок может стать раздражительным и пассивным, при этом ребенок будет громко кричать. Родители должны немедленно сообщить об этих симптомах своему доктору.
В редких случаях чрезмерное накопление билирубина в крови ребенка может привести к повреждению мозга (билирубиновая энцефалопатия), что в свою очередь может привести к потере слуха, развитию умственной отсталости и проблемам с поведением.
Гипербилирубинемия - причины, диагностика и лечение
Гипербилирубинемия (ГБН) – это не самостоятельное заболевание, а лабораторный синдром, возникающий при многих нозологических формах. Билирубин – это пигмент желтого цвета, который образуется из гемоглобина эритроцитов, подвергшихся разрушению ретикуло-эндотелиальной системой (синусоиды селезенки). Затем он метаболизируется печенью и экскретируется с желчью. Его повышение подтверждает наличие у пациента истинной желтухи. Определение концентрации фракций билирубина (неконъюгированного, конъюгированного) оказывает помощь в установлении происхождения желтухи (надпеченочной, печеночной, подпеченочной).
Причины гипербилирубинемии
Гипербилирубинемия практически всегда свидетельствует о патологии. Однако есть исключения. Например, причиной гипербилирубинемии может быть длительное голодание (дефицит альбумина, клеточных белков-переносчиков), применение лекарственных препаратов, вызывающих конкурентное торможение захвата гепатоцитами билирубина (рентгеноконтрастные вещества, средства для лечения гельминтозов).
У новорожденных причиной гипербилирубинемии является физиологическая желтуха, развивающаяся вследствие незрелости ферментных систем метаболизма билирубина. Причины патологической гипербилирубинемии следующие (перечислены в порядке частоты развития):
- Болезни печени. Наиболее частая причина гипербилирубинемии. Разрушение мембран гепатоцитов приводит к высвобождению билирубина и его попаданию в кровоток. Это происходит при любых инфекционных поражениях печени (вирусных, бактериальных, протозойных гепатитах), алкогольном, аутоиммунном гепатите, циррозе.
- Заболевания желчевыводящих путей. Вторая по частоте причина гипербилирубинемии. В результате внутрипеченочного и внепеченочного холестаза, который наблюдается при холецистите, желчнокаменной болезни, холангите, повышается проницаемость желчных капилляров. Под действием высокого гидростатического давления билирубин диффундирует в кровеносные сосуды.
- Гемолитические анемии (ГА). При усиленном разрушении эритроцитов (гемолизе) в крови нарастает количество свободного билирубина. Это характерно как для врожденных (наследственный микросфероцитоз, серповидно-клеточная анемия, талассемии), так и для приобретенных гемолитических анемий (пароксизмальная ночная гемоглобинурия, аутоиммунные, лекарственные ГА).
- Наследственные энзимопатии. Генетически обусловленные дефекты ферментов печеночного метаболизма билирубина приводят к нарушению его захвата гепатоцитами, конъюгации с глюкуроновой кислотой или секреции в желчь. Данная группа болезней носит название доброкачественные гипербилирубинемии (синдром Жильбера, Криглера-Найара, Дабина-Джонса).
- Метаболические расстройства. Это редкие наследственные заболевания, поражающие паренхиму печени, при которых в кровь попадает связанный билирубин. К ним относятся гемохроматоз, болезнь Вильсона-Коновалова, лизосомные болезни накопления (болезнь Гоше, Ниманна-Пика).
- Патология верхних отделов ЖКТ. Некоторые болезни органов пищеварения (псевдотуморозный панкреатит, опухоль поджелудочной железы, стеноз большого дуоденального сосочка) могут создавать механическое препятствие оттоку желчи за счет сдавления желчных протоков, тем самым приводя к их переполнению, диффузии желчного пигмента в капилляры.
Патогенез
Особенности патогенеза (механизмов возникновения) гипербилирубинемии определяются причиной. Свободный (непрямой, неконъюгированный) билирубин плохо растворяется в воде, но зато обладает высокой липофильностью, т.е. хорошо растворяется в жирах. Поэтому он может взаимодействовать с фосфолипидами клеточных мембран, особенно клеток головного мозга, благодаря чему проникает через гематоэнцефалический барьер, где разобщает процессы окислительного фосфорилирования и снижает синтез АТФ.
Этим объясняется токсичность свободного билирубина для клеток нервной системы. Наиболее ярко это проявляется у новорожденных детей. Билирубин способен окрашивать кожные покровы, видимые слизистые, мочу, а также кал в характерный желтый или темно-коричневый цвет. При длительном холестазе, вызывающем увеличение концентрации связанного билирубина, может нарушаться катаболизм, экскреция холестерина, что ведет к его накоплению в крови, прогрессированию атеросклероза.
Классификация
В зависимости от того, какая фракция желчного пигмента увеличена, различают:
- Непрямую гипербилирубинемию. Повышен неконъюгированный (не связанный) билирубин. Причиной являются патологии, вызывающие надпеченочную желтуху ‒ гемолитические анемии, доброкачественные гипербилирубинемии.
- Прямую гипербилирубинемию. Сопровождается увеличением уровня конъюгированного (связанного) билирубина. Причиной выступают болезни, приводящие к печеночно-клеточной и подпеченочной желтухе. Наиболее частые из них ‒ это вирусный, алкогольный гепатит, холецистит.
Отдельно выделяется билирубиновая энцефалопатия (ядерная желтуха). Она встречается при гемолитической болезни новорожденных, причиной которой является несовместимость эритроцитарных антигенов (резус-конфликт) матери и плода. Данное заболевание очень тяжелое, оно характеризуется поражением подкорковых ядер, коры головного мозга и требует немедленного лечения.
Симптомы гипербилирубинемии
Накопление желтого пигмента в коже, слизистых оболочках, биологических жидкостях приводит к изменению их окраски, что является основным симптомом гипербилирубинемии. Желтушность склер – наиболее ранний признак, он возникает, когда концентрация билирубина превышает нормальные показатели в 2 раза. Также рано начинают окрашиваться нёбо, задняя часть языка. Кожа приобретает желтый цвет при уровне выше 80-85 мкмоль/л.
При разных заболеваниях наблюдается неодинаковая интенсивность окрашивания кожи, различные ее оттенки. Так, например, при гемолитических анемиях кожа и слизистые имеют слабый лимонно-желтый цвет, кал становится темным. При заболеваниях печени кожа приобретает оранжево-желтую, а моча - темную окраску. При патологии желчевыводящих путей накапливающийся в коже билирубин окисляется до биливердина, что придает ей яркий зелено-желтый цвет, а кал, напротив, из-за нарушения оттока желчи становится светлым («ахоличный кал»). В случае длительного холестаза билирубин в коже начинает усиливать ее пигментацию, из-за чего она становится темной.
Остальные симптомы зависят от причины, вызвавшей гипербилирубинемию. У пациентов с гемолитическими анемиями наблюдается лихорадка (вследствие пирогенной активности свободного билирубина), увеличение селезенки, анемичный синдром – бледность кожи, учащение сердцебиения, снижение артериального давления. При болезнях печени и ЖП пациентов часто беспокоит тяжесть или тупая боль в правом подреберье, приступы желчной колики, нестерпимый кожный зуд.
У больных доброкачественными гипербилирубинемиями в клинической картине преобладает астеновегетативный синдром (общая слабость, сонливость, ухудшение концентрации внимания). У взрослых, в отличие от новорожденных, несмотря на высокую концентрацию желчного пигмента, энцефалопатия не развивается.
Осложнения
Наиболее частые и опасные осложнения связаны не с самой гипербилирубинемией, а с причиной, ее вызвавшей. Тяжелые неблагоприятные последствия гипербилирубинемии возникают у новорожденных при ядерной желтухе. Глубокое повреждение подкорковых ядер и коры больших полушарий головного мозга без своевременного лечения могут привести к нейросенсорной тугоухости, судорогам, а в некоторых случаях, к летальному исходу. Из-за ухудшения экскреции холестерина в желчь возрастает его плазменная концентрация, в результате чего ускоряется процесс формирования атеросклеротической бляшки. Это повышает риск инфаркта миокарда, ишемического инсульта.
Диагностика
Профиль специалиста, который курирует пациента с гипербилирубинемией, определяется вызвавшей ее причиной. Чаще всего такими больными занимаются гастроэнтерологи, гематологи. При обследовании больного внимательно осматриваются кожные покровы, слизистые оболочки глаз, рта, проводится пальпация живота на предмет гепатоспленомегалии, симптомов поражения желчных путей (Мерфи, Ортнера, Кера). Для выяснения причины гипербилирубинемии назначается дополнительное обследование, включающее:
- Лабораторные исследования. В общем анализе крови оценивается уровень эритроцитов, гемоглобина, в мазке крови изучается морфология эритроцитов. В биохимии крови определяются значения фракций билирубина, печеночных трансаминаз, щелочной фосфатазы, гамма-глутамилтранспептидазы. Проверяются показатели обмена железа (ферритин, трансферрин). В анализе мочи измеряется концентрация уробилина, билирубина. С помощью ИФА выявляются антитела к антигенам вирусов гепатита A, B, C, аутоиммунные антитела (ANCA, AMA).
- Инструментальные исследования. На УЗИ органов брюшной полости обнаруживается увеличение, диффузные изменения паренхимы печени, наличие камней, утолщение стенок желчного пузыря. При гемолитической анемии значительно выражена спленомегалия. При некоторых патологиях желчных протоков, поджелудочной железы на ретроградной панкреатохолангиографии отмечаются участки стеноза, расширения протоков.
- Провокационные пробы. Для диагностики доброкачественных гипербилирубинемий, вызванных генетическими дефектами энзимов метаболизма билирубина, проводятся специальные пробы (проба с 48 часовым голоданием, внутривенным введением раствора никотиновой кислоты, бромсульфалеина). При повышении уровня билирубина более, чем на 50%, проба считается положительной.
Дифференциальный диагноз гипербилирубинемии можно проводить по ее основному клиническому проявлению – желтухе. Желтушное окрашивание кожи возможно при употреблении в пищу большого количества продуктов, богатых каротином (моркови, тыквы, авокадо), приеме некоторых лекарственных препаратов (акрихина). Основной отличительный признак «псевдожелтухи» от истинной состоит в том, что склеры остаются неокрашенными.
Лечение гипербилирубинемии
Консервативная терапия
Для нормализации показателей желчного пигмента необходимо бороться с причиной гипербилирубинемии. В зависимости от состояния пациента, он может проходить лечение как амбулаторно, так и в стационаре. Чаще всего таких больных госпитализируют в гастроэнтерологическое отделение. Применяются следующие методы лечения:
- Диета. При заболевании печени и желчного пузыря любой этиологии назначается стол №5 по Певзнеру, при котором питание должно быть частым, малыми порциями. Обязательно исключается алкоголь, жирные, жареные блюда, копчености. Следует избегать употребления продуктов, вызывающих спазм желчного пузыря (помидоры, орехи).
- Непосредственное снижение билирубина в крови. Для лечения ГБН очень эффективная фототерапия ультрафиолетовыми лампами. Под действием УФ-лучей свободный билирубин, накапливаемый в коже, становится водорастворимым, благодаря чему быстро выводится из организма через почки. При неэффективности данного лечения прибегают к переливанию плазмы или крови. Для снижения концентрации непрямого билирубина при доброкачественной ГБН применяется фенобарбитал.
- Противовирусное лечение. Для лечения вирусных гепатитов применяются лекарственные препараты, подавляющие жизнедеятельность вируса гепатита – пелигированный интерферон-альфа, ламивудин, рибавирин. Для лечения гепатита С эффективна трехкомпонентная терапия с энтекавиром.
- Лечение холестаза. При многих заболеваниях, сопровождающихся застоем желчи, необходимо использование медикаментов, стимулирующих желчную экскрецию. Это ЛС, содержащие желчные кислоты (урсодезоксихолевая кислота, аллохол, холензим), растительные желчегонные препараты (кориандр, календула, тысячелистник), секвестранты ЖК (холестирамин).
- Предотвращение гемолиза. Для лечения гемолитических анемий применяются глюкокортикостероиды, внутривенное введение иммуноглобулина, гидроксимочевина. Для лучшей стабилизации мембран эритроцитов назначается постоянный прием фолиевой кислоты.
Хирургическое лечение
Основной метод лечения желчнокаменной болезни и калькулезного холецистита – это оперативное удаление желчного пузыря (лапароскопическая холецистэктомия). В случае безуспешности консервативных методов лечения гемолитической анемии прибегают к удалению селезенки (спленэктомии). Опухоли поджелудочной железы или 12-перстной кишки, вызывающие сдавление протоков, также подлежат оперативному удалению.
Прогноз и профилактика
Прогноз и продолжительность жизни при гипербилирубинемии определяется причиной, т.е. основным заболеванием. Например, гемолитическая болезнь новорожденных, вирусные гепатиты B, C, некоторые формы гемолитических анемий (гемоглобинопатии) характеризуются высокой частотой летального исхода. Доброкачественные гипербилирубинемии, хронический холецистит, напротив, имеют благоприятный прогноз, никак не влияют на продолжительность жизни.
Для профилактики гипербилирубинемии следует ограничить употребление алкоголя, жирной пищи. Резус-отрицательным беременным женщинам для предотвращения развития ГБН вводится антирезусный иммуноглобулин (анти-D-иммуноглобулин).
Гипербилирубинемия у новорожденных и взрослых: что это такое
Гипербилирубинемия – это патологическое изменение сыворотки крови, проявляющееся в повышении концентрации билирубина, возникающее как следствие усиленного распада гемоглобина.

Причины гипербилирубинемии
Синдром гипербилирубинемии развивается чаще всего по одному из двух главных патогенетических механизмов. Первый механизм запускается процессом избыточного синтеза билирубина, который наблюдается при остром одномоментном массивном разрушении эритроцитарных клеток крови.
Согласно второй этиопатогенетической теории развития гипербилирубинемии, существует ряд патологических состояний организма, сопровождающихся нарушением метаболических превращений билирубина в печени и элиминации продуктов его распада. Таким образом, повышение той или иной билирубиновой фракции позволяет предположить этиопатогенетические факторы развития гипербилирубинемии.
Причины конъюгационной гипербилирубинемии
В основу этиопатогенетической классификации всех форм гипербилирубинемии положен принцип определения билирубиновой фракции, за счет которой увеличен показатель общего сывороточного билирубина.
Так, конъюгационная гипербилирубинемия проявляется повышенной концентрацией прямой билирубиновой фракции, спровоцированной нарушением элиминации билирубина из организма.
Для развития данного типа патологических изменений необходимо наличие у пациента каких-либо органических изменений структуры гепато-билиарной системы (наличие конкрементов в просвете желчных путей, диффузные и узловые поражения паренхимы печени), продолжительный прием лекарственных средств группы гормонального ряда.
Причины неконъюгированной гипербилирубинемии
В ситуации, когда в организме происходит усиленный гемолиз эритроцитарных кровяных клеток, сопровождающийся повышенным синтезированием непрямой фракции билирубина, устанавливается диагноз «неконъюгированная гипербилирубинемия».
Данные изменения чаще всего наблюдаются в практике неонатологов при гемолитических анемиях периода новорожденности, а у взрослой категории пациентов этот тип гипербилирубинемии провоцируется токсическим влиянием ядовитых веществ.

Симптомы гипербилирубинемии
- Самым распространенными проявлениями повышения показателя билирубина в крови является повреждение кожных покровов в виде изменения окраски кожи на лимонно-желтый оттенок. Однако первично поражаются все слизистые оболочки ротовой полости, конъюнктивы и глазных белков, которые приобретают ярко выраженный желтый цвет. Вышеперечисленные симптомы имеют место только лишь при значительном увеличении билирубина.
- В ситуации, когда гипербилирубинемия у пациента спровоцирована патологией печени и органов билиарной системы, помимо изменения окраски кожных покровов больной отмечает выраженный зуд измененной кожи, особенно в ночное время.
- Повышение концентрации билирубина и продуктов его метаболического превращения оказывает токсическое влияние на структуры центральной нервной системы, в связи с чем, практически в 100% случаев гипербилирубинемия сопровождается симптомами астеновегетативного симптомокомплекса в виде повышенной утомляемости, невозможности выполнения привычной физической активности, сонливости, а в тяжелых случаях даже различных степенях нарушения сознания.
- Больные с печеночным вариантом гипербилирубинемии помимо патогномоничных жалоб, свидетельствующих в пользу повышения концентрации билирубина, отмечают постоянное присутствие симптомов основного фонового заболевания печени – тяжесть и дискомфорт в проекции правого подреберья, ощущение горького привкуса в ротовой полости, постоянная изжога и тошнота, а в период обострения неукротимая рвота.
- Подпеченочный вариант гипербилирубинемии также имеет характерные клинические черты в виде выраженного астено-невротического синдрома, характерного изменения стула, который меняет не только окраску, но и консистенцию в сторону жидкой, с присутствием большого количества жира.
- Все клинические и патоморфологические варианты гипербилирубинемии сопровождаются типичным потемнением мочи и посветлением кала, которые в большей степени наблюдаются при печеночном и подпеченочном типе гипербилирубинемии.
Гипербилирубинемия у новорожденных
Функциональная гипербилирубинемия
Период новорожденности является критическим в отношении развития признаков доброкачественных форм гипербилирубинемии, которые провоцируются генетическими энзимопатиями.
В связи с тем, что повышение концентрации билирубина у новорожденного ребенка не сопровождается структурными изменениями и функциональными нарушениями печени, а также у ребенка полностью отсутствуют клинические проявления холестаза и гемолиза, данные изменения трактуются как «функциональная гипербилирубинемия».
Дебют клинических проявлений функциональной гипербилирубинемии приходится на вторые-третьи сутки после рождения ребенка, и самостоятельно нивелируются не более чем через месяц. Для этой формы гипербилирубинемии характерно постепенное желтушное прокрашивание кожных покровов, начиная от головы и заканчивая нижними конечностями.
Симптомы так называемой ядерной желтухи проявляются только в случае критического повышения концентрации билирубина, результатом чего является развитие признаков поражения структур центральной нервной системы.

Транзиторная гипербилирубинемия
Отдельную категорию гипербилирубинемии составляет так называемый «физиологический вариант» или транзиторная гипербилирубинемия новорожденных, которая наблюдается у всех детей в периоде новорожденности и не вызывает болезненных ощущений и патологических изменений состояния здоровья.
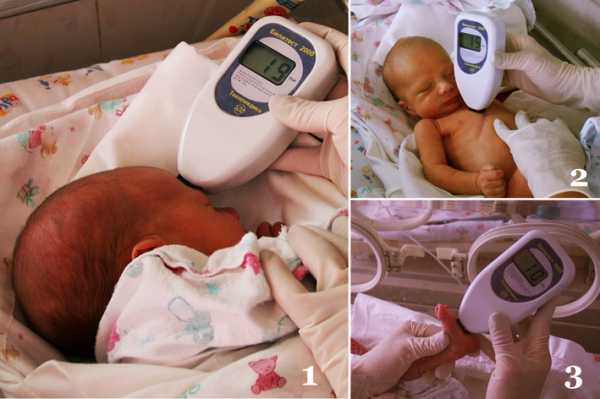
Несмотря на благоприятное транзиторное течение, все дети, находящиеся в периоде новорожденности подлежат контролю показателей билирубина, для чего в настоящее время применяется современный анализатор гипербилирубинемии, позволяющий в кратчайшие сроки определить уровень различных фракций билирубина.
Проведение скринингового обследования детей позволяет исключить возможность развития тяжелой степени гипербилирубинемии, которая в большинстве случаев провоцирует возникновение энцефалопатических проявлений.
Благоприятное течение гипербилирубинемии, наблюдающееся у большинства здоровых доношенных детей, развивается как следствие несовершенства ферментативных систем, не позволяющих быстро осуществлять элиминацию продуктов распада фетального гемоглобина.
В настоящее время практикующие педиатры отмечают еще одну особенность течения гипербилирубинемии у новорожденных детей, заключающуюся в прогрессирующем увеличении показателя билирубина после кормления грудью. Однако, несмотря на данную закономерность, гипербилирубинемия не является показанием для прерывания грудного вскармливания.
Настораживающими симптомами, свидетельствующими о прогрессировании гипербилирубинемии, является немотивируемая вялость и апатия ребенка, снижение интереса к кормлению и вялый акт сосания.
Присоединение ригидности затылочных мышц и опистотонуса свидетельствует в пользу развития тяжелого поражения оболочек головного мозга, которое при отсутствии неотложного медикаментозного вмешательства приводит к летальному исходу.
Симптомами необратимого поражения центральной нервной системы новорожденного ребенка является глубокая степень нарушения сознания в виде отсутствия реакции на световой, болевой и температурный раздражители.

В ситуации, когда высокие показатели билирубина в крови у новорожденного ребенка не сопровождаются тяжелым расстройством здоровья, применение каких-либо лечебных мероприятий считается необоснованным. Значительная концентрация билирубина хорошо поддается лечению методом ультрафиолетовых ванн, способствующих скорейшему выведению билирубина.
Критическое повышение содержания билирубина, превышающее 120 мкмоль/л, является абсолютным показанием для применения заменного переливания крови.
Последние научные наблюдения отмечают значительный рост заболеваемости гипербилирубинемией у детей с родовыми травмами, сопровождающимися развитием кефалогематом. Повышенная концентрация билирубина в этой ситуации развивается в результате массивного разрушения эритроцитов, находящихся в составе гематомы.
Данная форма гипербилирубинемии сопровождается высокой концентрацией непрямой фракции (т. н. непрямая гипербилирубинемия у новорожденных) и подлежит коррекции с помощью заменного переливания эритроцитарной массы.
Лечение гипербилирубинемии
Гипербилирубинемия относится к категории патологических состояний, лечение которых должно быть этиологически обоснованным, то есть залогом выздоровления является устранение фонового заболевания.
В ситуации, когда проявления гипербилирубинемии развиваются у человека впервые, необходимо проводить его полное обследование и лечение в условиях стационара гастроэнтерологического профиля. Лишь доброкачественная гипербилирубинемия не нуждается в медикаментозной коррекции и в большинстве случаев нивелируется при соблюдении пациентом основных рекомендаций по коррекции пищевого поведения.
Помимо коррекции питания пациентам с гипербилирубинемией, обусловленной патологией гепатобилиарной системы необходимо исключить факт влияния физических и психоэмоциональных перегрузок организма.
Медикаментозное лечение гипербилирубинемии любой клинической формы разделяется на следующие категории: этиопатогенетическое, симптоматическое и профилактическое.
В связи с тем, что продукты метаболического превращения билирубина оказывают токсическое влияние на все структуры человеческого организма, особенно центральную нервную систему, первоочередно необходимо проводить адекватную дезинтоксикационную терапию с применением лекарственных средств группы антиоксидантов (Цистамин в суточной дозе 0,2 г, Токоферол по 50 мг в сутки перорально).
В ситуации, когда у пациента наблюдается критическая концентрация билирубина и имеются признаки токсического поражения головного мозга в виде признаков энцефалопатии, необходимо проводить парентеральную дезинтоксикационную терапию в виде сочетания Инсулина дозе 4 ЕД подкожно с 40 мл 40% раствора Глюкозы внутривенно.
Если диагностируется иммунновоспалительный вариант гипербилирубинемии, возникающий в результате массивного диффузного повреждения печеночной паренхимы, целесообразно применение краткого курса глюкокортикостероидной терапии (Преднизолон в суточной дозе 30 мг перорально в течение двух недель).
В связи с тем, что паренхиматозная гипербилирубинемия в большинстве случаев сопровождается тяжелыми геморрагическими осложнениями, всем пациентам этой категории рекомендуется в профилактических целях применять Викасол в суточной дозе 0,015 г перорально или внутримышечно.
Для облегчения кожного зуда, который часто сопровождает холестатический вариант желтухи, используются средства наружного применения – обтирание камфорным спиртом и уксусные ванны. С целью снижения концентрации желчных кислот в сыворотке крови следует применять лекарственные препараты, действие которых направлено на связывание желчных кислот в тонком отделе кишечника (Холестирамин в суточной дозе 2 г).
Кроме того, хорошим эффектом обладает метод дуоденального зондирования и применение желчегонных препаратов (Холосас в суточной дозе 15 мл перорально), при условии отсутствия признаков механического типа желтухи.
В ситуации, когда возникновение повышенной концентрации билирубина наблюдается как результат механической обтурации просвета желчных путей, единственным вариантом лечения является хирургическое устранение дефекта (холецистэктомия лапароскопическим доступом).
Автор статьи врач-инфекционист, гепатолог
© 2019 – 2020. Все права защищены.
Много способов перепробовано, но ничего не помогает? И Вы готовы воспользоваться любой возможностью, которая подарит хорошее самочувствие! Вы даже думали о хирургическом вмешательстве и применении токсичных препаратов, которые рекламируют? Оно и понятно, ведь Вас уже замучили такие симптомы как:
И это совсем не полный перечень возможных симптомов заболевания печени… Тому то, каким бы “ужасающим” для вас не казалось заболевание затягивать его лечение никак нельзя.
Поэтому мы рекомендуем Вам прочитать историю Елены о том, как можно восстановить свою печень без дорогостоящих процедур и в кратчайшие строки... Читать далее>>>
Гипербилирубинемия у новорожденных и взрослых
Гипербилирубинемия – состояние, при котором в крови повышена концентрация билирубина. Данная патология диагностируется в первую неделю жизни ребенка. Что такое гипербилирубинемия и как лечить состояние? Именно об этом идет речь в данной статье.
Что такое гипербилирубинемия
Гипербилирубинемия – это комплекс симптомов, которые обуславливаются превышением допустимой нормы объема билирубина в организме. В некоторых случаях это выступает причиной развития определенных заболеваний внутренних органов, например, недостаточности печени или холецистита.
Но обычно такое явление не связано с нарушением функциональности печени и ее морфологической деформацией. Чаще всего наблюдается доброкачественная гипербилирубинемия, характеризующаяся пожелтением кожи.
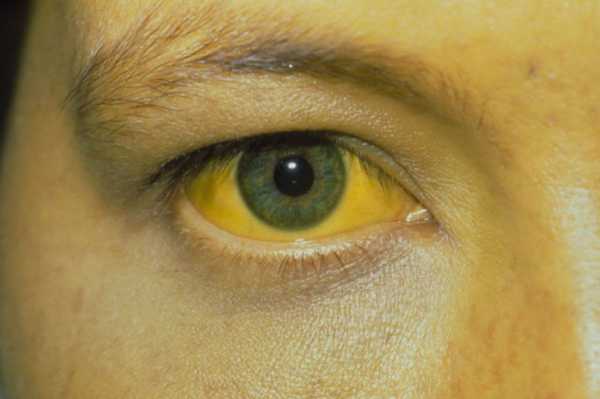
Билирубин – желчный пигмент, что продуцируется из гемоглобина кострового мозга, печени и иных органов. Превышение его нормы в организме может быть спровоцировано многими факторами. Это связано с нарушением процесса связывания пигмента с глюкуроновой кислотой и его выведения вместе с желчью.
Часто обнаруживается гипербилирубинемия у новорожденных. У взрослых симптоматика может усиливаться из-за неправильного питания, злоупотребления алкоголем, некоторых болезней, переутомления и т.д.
Разновидности патологии
Гипербилирубинемия, что за болезнь? В медицине принято выделять несколько видов данной патологии:
- Болезнь Жильбера – наследственное заболевание, свойственное мужчинам. Оно характеризуется расстройством обмена билирубина в результате недостаточного продуцирования одного из ферментов. При патологии развивается желтуха. Обычно патология начинает прогрессировать после переутомления, как физического, так и эмоционального.
- Функциональная гипербилирубинемия– генетически обусловленная патология, что проявляется после перенапряжения. Характеризуется накоплением коньюгированного билирубина, пожелтением кожи. Заболевание не дает осложнений.
- Неконъюгированная гипербилирубинемия (болезнь Криглера-Наджара) – ядерная желтуха, при которой поражается головной мозг. При появлении патологии в раннем возрасте прогноз неутешительный. Если заболевание было диагностировано после пяти лет, оно поддается терапии.
Формы заболевания
Существует несколько форм болезни:
- Печеночная форма. Наблюдается увеличение продуцирования билирубина в результате повреждения печени.
- Подпеченочная форма. Происходит закупорка желчных протоков, что ведет к застою желчи.
- Надпеченочная форма . Большой объем билирубина поступает в кровь из-за разрушения гемоглобина в почках.
Причины возникновения
Гипербилирубинемия – болезнь, которая может иметь несколько форм в зависимости от причин ее появления. К основным факторам, провоцирующим появление патологии, относят:
- Анемия – недостаток в организме гемоглобина. Заболевание может быть врожденным или протекать на фоне иных патологий в организме. Также такое явление может наблюдаться при нехватке витамина В12. В результате всего этого эритроциты погибают;
- Наследственная предрасположенность. Риск появления болезни увеличивается при наличии близких родственников с данной патологией;
- Болезни аутоиммунного характера, например, волчанка, гепатит;
- Лейкоз, при котором кровь меняет свой состав;
- Внутренние кровотечения вследствие травм органов брюшины или осложнений после хирургического вмешательства;
- Осложнение вирусной инфекции, что приводит к сепсису;
- Переливание крови, что приводит к гибели эритроцитов;
- Интоксикация организма суррогатами, ядами, токсинами;
- Длительное употребление медикаментов, например, стероидов и гормонов;
- Жировой гепатоз печени;
- Опухоли доброкачественного или злокачественного характера;
- Болезнь Дабина-Джонсона и Ротора;
- Индивидуальные особенности организма;
- Беременность;
- Камни в желчевыводящих протоках;
- Малярия;
- Инфаркт легкого.

Осложнения и последствия
Что такое гипербилирубинемия, теперь известно. Но к каким последствиям может она привести? Обычно патология не приводит к осложнениям, билирубину не свойственно накапливаться в кожном покрове, поэтому зуда не возникает. Но иногда непрямая гипербилирубинемия у новорожденных может поражать головной мозг, провоцируя развитие энцефалопатии или ядерной желтухи, что приводит к нарушениям со стороны неврологии.
Симптомы
Гипербилирубинемия симптомы проявляет такие, что свойственны поражению ЦНС: утомляемость, слабость, заторможенность. При легком протекании болезни болезненные ощущения не возникают, печень не увеличивается в размерах, трудоспособность человека сохраняется.

Непрямая гипербилирубинемия отказывает токсическое воздействие на головной мозг. Дети с такой патологией умирают.
Доброкачественная гипербилирубинемия не приводит к расстройству функциональности органов и системы организма. В данном случае у человека только желтеет кожа, особенно актуально это при стрессах и переутомлении. Если заболевание обостряется, возможно появление тошноты, болевых ощущений в области ребер, снижение аппетита.
Заболевание может проявлять различную симптоматику в зависимости от его формы:
- При надпочечной форме урина и кал приобретают темный окрас, кожа становится желтого оттенка, слизистые оболочки бледнеют, снижается острота зрения, появляется нервозность. Человек может потерять сознание.
- Подпеченочная форма характеризуется появлением слабой боли в области ребер, кал приобретает белый цвета, становится жирным, в ротовой полости ощущается горечь, развивается гиповитаминоз, кожа желтеет, вес человека снижается.
- Печеночная форма проявляется в покраснении кожи и слизистого эпителия, неприятными ощущениями в области живота, зудом кожи, присутствием горечи в ротовой полости, рвотами, потемнением урины. Через некоторое время кожа может слегка позеленеть.

Патология при беременности
Во время беременности иммунная система работает в замедленном режиме. Поэтому в этот период часто развиваются инфекционные и вирусные болезни. Не исключение и доброкачественная гипербилирубинемия.
Заболевание может быть спровоцировано инфекцией или вирусом или появиться в результате изменений, которые происходят в организме женщины в данный период. В первом случае заболевание сопровождается болью в области живота, увеличением температуры тела, пожелтением кожи. Нередко заболевание может привести к развитию негативных последствий, поэтому требует медикаментозной терапии. Во втором случае недуг не несет опасности и развивается на фоне токсикоза.
Почему болеют новорожденные?
После рождения у ребенка в организме находится большая концентрация билирубина, постепенно она снижается. Обычно в педиатрии такое явление именуют детской желтушкой. При хорошем самочувствии новорожденного терапия не проводится. Если наблюдаются серьезные нарушения здоровья ребенка, врач назначает лечение.

Появление транзиторной гипербилирубинемии у новорожденных обуславливается тем, что кровяные тельца за короткое время распадаются, тем временем происходит замедление процесса ферментации. В результате этого билирубин выходит из ткани печени свободно. Такое происходит обычно из-за несовместимости резус-фактора и группы крови у матери и ребенка.
Лечение
Лечение гипербилирубинемии проводит терапевт или педиатр, если это ребенок. Сначала врач осматривает пациента, изучает анамнез, результаты лабораторных анализов крови и мочи, а также УЗИ органов брюшины. Изучив результаты анализов, доктор устанавливает причину развития заболевания и разрабатывает план терапии.
Если причиной патологии выступает анемия, лечением будет заниматься гематолог. Этого врача рекомендуется посещать женщинам и во время беременности для предупреждения риска развития осложнений.
Гипербилирубинемия лечение предполагает комплексное. В качестве медикаментов назначаются иммуномодуляторы для увеличения защитных сил организма. Если патология спровоцирована вирусом или инфекцией, врач выписывает антибактериальные препараты и противовирусные средства. Также назначаются желчегонные средства, антиоксиданты, витамины. Часто выписываются такие препараты, как «Зиксорин», «Урсофальк», «Гепабене», «Сорбовит-К».

Хорошо себя зарекомендовала фототерапия в лечении болезни у новорожденных. В данном случае проводится облучение кожи синей лампой. Она помогает уничтожить некоторую долю билирубина. При первых симптомах неконъюгированной гипербилирубинемии проводят переливание крови.
Взрослым важно соблюдать диету во время терапии, использовать умеренные физические нагрузки, избегать стрессов. Нельзя кушать вредные продукты, мучные изделия, блюда должны быть приготовлены без соли и иных специй. Также не рекомендуется употреблять в пищу блюда, которые готовились с добавлением соды или разрыхлителя. Кушать нужно часто, но небольшими порциями.
Также в качестве лечебных средств могут применяться рецепты народной медицины. Но лучше, чтобы врач сам одобрил их. Иногда их использование допускается на последнем этапе терапии или в том случае, если у человека проблема является врожденной. В этом случае допустимо использовать травы и сборы, которые имеют желчегонное действие, например, мята, календула. Их используют на протяжении месяца.
Прогноз и профилактика
Прогноз патологии хороший. Но неконъюгированная гипербилирубинемия часто становится причиной смерти ребенка.
В профилактических целях нужно отказаться от алкогольных напитков, острой и жирной пищи. Недопустимы стрессовые ситуации и силовые нагрузки в большой степени. Нужно следить за своим здоровьем и самочувствием детей.

Таким образом, гипербилирубинемия – это болезнь, при которой в организме увеличивается концентрация билирубина. Обычно заболевание не несет угрозы жизни, но иногда может развиться из-за него холецистит, в самом тяжелом случае – поражение мозга. Но при своевременном реагировании на проблему этого удается избежать. Поэтому в родильных домах медики пристально наблюдают за состоянием детей, особенно тех, у кого появилась детская желтушка.
Большую роль в терапии взрослых играет соблюдение диеты. При врожденных пороках ее нужно соблюдать все время. Так удается нормализовать уровень пигмента желчи в организме длительное время.
© 2018 – 2019, MedPechen.ru. Все права защищены.
Гипербилирубинемия и желтуха у новорожденных
Гипербилирубинемия это состояние, при котором в крови слишком много билирубина.
У взрослых причины повышения билирубина в крови могут быть связаны с разрушением эритроцитов, с разрушением печени и с нарушением оттока желчи, содержащей билирубин, по желчным протокам в кишку. У детей причины могут быть такие же, но в большей мере связаны с разрушением эритроцитов и неспособностью младенческой печени связать образующийся билирубин. Образовавшийся билирубин может накапливаться в тканях и жидкостях тела ребенка. Поскольку билирубин является пигментным веществом, он вызывает пожелтение кожи ребенка и тканей. Это называется желтухой. В зависимости от причины гипербилирубинемии, желтуха может появиться сразу после рождения или в любое время после этого. Около 60 процентов доношенных новорожденных и 80 процентов недоношенных детей в той или иной степени выраженности переносят желтуху. Более выражена она у младенцев, матери которых страдают сахарным диабетом и другими хроническими заболеваниями.
Какие причины желтухи?
Во время вынашивания плацента матери отфильтровывает из крови ребенка токсические вещества, которые затем утилизируются печенью матери. Когда же ребенок рождается, печень ребенка принимает на себя эту функцию, но не всегда справляется. Причины гипербилирубинемии и желтухи, включают следующие:
Физиологическая желтуха новорожденных – возникает как "нормальный" ответ в первые дни (3-4 день) сразу после рождения и связана именно с неспособностью печени ребенка утилизировать и выводить билирубин. Механизм желтухи гемолитический, обусловлен разрушением фетального гемоглобина плода и заменой его на обычный гемоглобин А. Проходит физиологическая желтуха к 7-8 дню. Желтуха связанная с началом грудного вскармливания - развивается у 2 процентов детей на грудном вскармливании после первой недели кормления. Достигает пика около двухнедельного возраста и может сохраняться от трех до 12 недель. Этот вид желтухи связывают с усилением обратного всасывания билирубина связанного с грудным молоком. Процесс называется кишечно-печеночная циркуляция.
Желтуха связанная с отказом от грудного вскармливания- накопление билирубина происходит вследствие отсутствия достаточного поступления жидкости с молоком, уменьшения выработки мочи. Особенно этот вид желтухи актуален для недоношенных ( 34 - 36 недель) младенцев поскольку им не хватает сил и активности для полноценного питания.
Гемолитическая желтуха – может быть обусловлена резус конфликтом матери и плода, когда резус-отрицательная мать, вырабатывает антитела к резус-положительной крови ребенка. Антитела проникают через гемато-плацентарный барьер и начинают разрушать эритроциты плода. После рождения детоксицирующая функция плаценты и организма матери прекращается, и в крови ребенка начинает накапливаться билирубин. Возникает в течение первых 24 часов после рождения
Желтуха, связанная с недостаточной функцией печени вследствие инфекции или других факторов.
Симптомы и чем опасна желтуха.
Даже незначительное повышение билирубина крови должно настораживать, поскольку билирубин оказывает токсическое воздействие на головной мозг ребенка, может приводить к тяжелым энцефалопатиям.
Симптомы желтухи включают пожелтение слизистых и кожного покрова, в начале на лице, в дальнейшем по всему телу; нарушения сна- либо капризное поведение, либо наоборот повышенную сонливость; плохой аппетит и отказ от кормления; изменение цвета мочи. В тяжелых случаях возможны судороги и кома.
Диагностика желтухи новорожденных.
Диагностировать наличие желтухи не представляется сложным, поскольку желтушность кожи не оставляет сомнений в диагнозе. Важно установить причину её появления. Сроки возникновения желтухи помогут сориентироваться в этом. Желтуха, возникшая в первые 24 часа от рождения представляет опасность и требует незамедлительного лечения; возникшая на 2-4 день вероятнее физиологическая и если выражена не активно, то лечения не требует; в более поздние сроки либо связана с активным началом грудного кормления, либо имеет инфекционную или какую-либо другую причину.
Диагностические исследования включают: Определение количества билирубина крови – прямого и связанного; Определение количества эритроцитов крови, микроскопия мазка крови с определением формы эритроцитов; резус тестирование плода и матери, определение совместимости их крови (проба Кумбса)
Лечение гипербилирубинемии и желтухи.
Лечение ребенка будет основываться на его возрасте (доношенность, послеродовый), общем состоянии здоровья, наличии дополнительной патологии, степени выраженности желтухи. Задача лечения - остановить дальнейшее повышение билирубина и выведение его из организма. Исключить желтуху новорожденных полностью нельзя, раннее распознавание и лечение имеют значение в предотвращении опасных осложнений.
В легких случаях при физиологической желтухе достаточно увеличить кратность кормления грудью для повышения гидратации организма ребенка. Сонливость ребенка не должна останавливать мать, дитя нужно разбудить и накормить, ведь сонливость может быть обусловлена гипербилирубинемией.
В более тяжелых случаях прибегают к внутривенным вливаниям жидкости и гемофильтрации (плазмоферезу).
Фототерапия один из основных методов лечения желтухи, под действием специальной лампы синего спектра билирубин, содержащийся в крови, метаболизируется и легко выводится из организма ребенка. Разработаны специальные волоконно-оптические пеленки, которые оказывают такой же эффект. Светом воздействуют на кожу ребенка постоянно, поворачивая его. Глаза должны быть защищены, а температура контролироваться в процессе фототерапии. Контролируется уровень билирубина для определения эффективности фототерапии.
Способ лечения конъюгационных гипербилирубинемий у детей первого года жизни
Изобретение относится к области медицины, а именно к педиатрии и неонатологии, и может быть использовано для лечения конъюгационных гипербилирубинемий у детей раннего возраста. Для этого вводят суспензию урсофалька в вечернее время в дозе 20-30 мг/кг в сутки в 1 приём. При этом объём потребляемой жидкости составляет до 10 мл/кг массы тела у недоношенных детей и до 20 мл/кг массы тела у доношенных детей. Кроме того, в динамике один раз в месяц контролируют биохимические показатели сыворотки крови, проводят сонографическое исследование печени, определяют уровень гемоглобина, эритроцитов, ретикулоцитов. Также осуществляют комплексное выявление герпетических инфекций: ЦМВИ, ВЭБ, ВПГ-1,2 типа. При наличии инфекции в комплекс терапии включают препарат интерферона альфа-2b в суппозиториях - генферон-лайт 125000 мг по 1 свече 2 раза в день 10 дней. Далее лечение проводят по схеме: по 1 свече 2 раза в день три раза в неделю, до трех месяцев. Способ обеспечивает повышение эффективности лечения и минимизацию осложнений со стороны печени и селезёнки за счёт учёта этиопатогенетических механизмов развития конъюгационных желтух и анатомо-физиологических особенностей биллиарной системы у детей первого года жизни. 1 табл., 1 пр.
Предлагаемое изобретение относится к медицине и может быть использовано в педиатрии, неонатологии при лечении конъюгационных гипербилирубинемий у детей первого года жизни.
Уровень техники
Согласно имеющимся данным на первой неделе жизни гипербилирубинемия встречается у 25-50% доношенных и у 70-90% недоношенных новорожденных. Чаще всего отмечается физиологическая гипербилирубинемия, на долю которой приходится до 60-70% всех гипербилирубинемий. При грудном вскармливании 10% детей остаются субиктеричными до месячного возраста [Шеплягина Л.А., Дейнеко О.Я., Легонькова Т.Н., Вахлова И.В. Рациональное вскармливание детей первого года жизни // Педиатрия. - 2006. - №6. - С. 46-52.; Gartner L. Hyperbilirubinemia and breastfeeding // Textbook on Lactation / Hale T.W., Hartmann P.E., eds. - Pharmasoft Publishing, Amarillo, TX, 2007].
В большинстве случаев гипербилирубинемия носит физиологический характер, является «пограничным состоянием» и не требует лечения. Тем не менее необходимо помнить, что гипербилирубинемия может быть связана с разными патогенетическими механизмами, в том числе с холестазом на фоне анатомических особенностей желчевыводящих путей или если ее появление определяется после 8 для жизни, то необходимо исключить влияние герпетических инфекций (ЦМВИ, ВЭБ, ВПГ - 1, 2 типа) [Васильченко Н.В., Сафина С.Г., Мажитова С.А. Затянувшаяся конъюгационная желтуха // «Педиатрия», №3, 2011. - 63-65 с.]. Недооценка динамики развития патологического процесса при гипербилирубинемии, несвоевременное вмешательство могут привести к тяжелым осложнениям или летальному исходу.
Известными методами лечения желтухи у новорожденных являются фототерапия с использованием необходимого оборудования и назначение препарата фенобарбитал, а также с целью улучшения метаболических процессов в печени часто используют препараты, улучшающие отток желчи (хофитол, урсосан) [«Основы перинатологии» под ред. Н.П. Шабалова, Ю.В. Цвелева, 2004; «Гипербилирубинемии у новорожденных детей», авторы И.В. Александрович, И.М. Шатилло, 2006; Проект протокола дифференциальной диагностики и лечения синдрома холестаза у новорожденных детей». А.В. Дегтярева, Ю.Г. Мухина, Н.Н. Володин, 2008].
Фототерапию начинают при угрозе роста билирубина до токсического значения. Суть действия фототерапии заключается в фотоизомеризации непрямого билирубина, то есть превращении его в водорастворимую форму. В настоящее время существует несколько разновидностей ламп синего света, с длиной волны 425-475 нм [Волянюк Е.В., Кузнецова А.В. Тактика педиатра при неонатальной желтухе // Практическая медицина. - 2009. - №7 - с. 13-15]. Вышеуказанный способ использования фенобарбитала активирует глюкуронилтрансферазу, увеличивая секрецию желчи, таким образом, вмешиваясь в различные этапы метаболизма билирубина, позволяет активизировать ферментные системы гепатоцитов. Аналогичным действием обладают вышеуказанные желчегонные препараты (хофитол и урсосан).
К недостаткам фототерапии, препарата фенобарбитал и гепатопротекторов относятся следующие особенности: данные методики разработаны и успешно используются в неонатальном периоде, и их эффективность у пациентов старше одного месяца не дает клинико-лабораторного подтверждения, учитывая различные патогенетические механизмы длительных гипербилирубинемий. Использование фототерапии невозможно в домашних условиях, так как необходимо использование ламп фототерапии. Назначение препаратов хофитол и урсосан, обладающих гепатопротекторным и желчегонными свойствами, широко используются при лечении неонатального холестаза, но недостатком препарата хофитол является его растительное происхождение и спиртовой состав раствора, а у препарата урсосан имеется только капсулированная форма препарата, что не рекомендовано к применению у детей до 3 лет. Влияние инфекционного фактора также не учитывается при диагностики и лечении заболевания, что удлиняет период наблюдения, а, следовательно и лечения данного контингента детей.
За ближайший аналог принят способ лечения воспалительных заболеваний печени и холестаза у новорожденных детей с использованием препарата урсодезоксихолевой кислоты (урсофальк - суспензия) в дозе 20-30 мг/кг в сутки в 2 приема [«Неонатология. Национальное руководство», гл. редактор Н.Н.Володин, 2007; Синдром холестаза у новорожденных детей: Пособие для врачей / Дегтярева А.В. и др. - 2010. - С. 34]. Данный препарат используется с момента рождения, отличается высокой эффективностью в отношении лечения холестатических желтух и неонатальных гепатитов у детей. Применение вышеуказанного лекарственного средства не имеет побочных эффектов и сочетается с удобной формой применения в виде суспензии, что исключает передозировку.
Недостатком этого способа лечения является недооценивание влияния герпетических инфекций (ЦМВИ, ВЭБ, ВПГ 1, 2 типа) на развитие затяжных гипербилирубинемий у детей первого года жизни.
Особенностью герпетических инфекций, в особенности ЦМВ-инфекции, является ее способность как бы проявлять другую патологию: гемолитическую болезнь плода и новорожденного, наследственные болезни, ферментопатии и др. Для манифестной формы врожденной ЦМВИ характерно: гепатосленомегалия, стойкая желтуха, геморрагическая или пятнисто-папулезная сыпь, выраженная тромбоцитопения, тогда как в 8-15% случаях нет яркой клинической симптоматики, что впоследствии ведет к формированию поздних осложнений в виде ухудшения слуха [«Цитомегаловирусная инфекция», Кошерова Б.Н., Бейсенова Г.Р., 2010 г.].
У 60-80% случаев первичная ВЭБ-инфекция характеризуется асимптомной сероконверсией [«Герпесвирусные инфекции и инфекционный мононуклеоз (обзор литературы)», Шарипова Е.В., Бабаченко И.В., 2013 г.] У детей первых двух лет жизни доля инаппарантного течения ВЭБ-инфекции достигает до 90% [«Infectious mononucleosis», H. Wakiguchi et al., 2006], что затрудняет дифференциальный диагноз.
В частности, при внутриутробном заражении ВПГ 1, 2 типа у ребенка наблюдаются желтуха, гепатоспленомегалия, нестабильность температуры, повышенная возбудимость, судороги, везикулезная сыпь, что приводит к формированию генерализованных форм, а также латентному персистированию [«Герпетическая инфекция человека, вызываемая ВПГ 1/2 (этиология, патогенез, клиника, диагностика, лечение, профилактика)», Карпов И.А. и др., 2008]. Приведенные выше литературные источники приводят данные, что при герпетических инфекциях у детей первого года жизни первичным органом для поражения являются печень, с клинической картиной гипербилирубинемии, что необходимо учитывать при лечебно-диагностическом процессе.
Задачами изобретения является разработка способа лечения конъюгационных гипербилирубинемий у детей первого года жизни, имеющих клинические, лабораторные, сонографические изменения печени, проявляющиеся длительной желтухой после первого месяца жизни.
Сущностью изобретения является назначение урсодезоксихолевой кислоты в виде суспензии урсофальк в вечернее время в дозе 20-30 мг/кг в сутки в 1 прием и увеличенный объем потребляемой жидкости, до 10 мл/кг массы тела у недоношенных детей и до 20 мл/кг массы тела у доношенных детей, контролируя один раз в месяц биохимические показатели сыворотки крови (АЛТ, ACT, общий билирубин, прямой билирубин, щелочная фосфатаза), проводя сонографическое исследование печени, определяя уровень гемоглобина, эритроцитов, ретикулоцитов в общем анализе крови, выявляя возможные герпетические инфекции (ЦМВИ, ВЭБ, ВПГ - 1, 2 типа), а при наличии положительных результатов, в данную тактику лечения включают препарат интерферона альфа-2b в суппозиториях генферон-лайт 125000 мг по 1 свече 2 раза в день 10 дней, далее по схеме по 1 свече 2 раза в день три раза в неделю до трех месяцев.
Технический результат изобретения связан с комплексным подходом к лечению конъюгационных желтух у детей более одного месяца жизни, с учетом инфекционного анамнеза, патогенетических механизмов пролонгированных желтух, учета анатомических особенностей билиарной системы. Протокол лабораторной диагностики герпетических инфекций (ЦМВИ, ВЭБ, ВПГ - 1, 2 типа), включенный в изобретение, позволяет на ранних этапах диагностировать этиологическую причины гипербилирубинемий, а также назначить базовую противовирусную терапию.
Способ апробирован в течение 4 лет на 678 детях первого года жизни, имеющих длительную конъюгационную желтуху, обратившихся на амбулаторный прием в клинико-диагностическое отделение ГБУЗ «Специализированная детская инфекционная больница» г. Краснодар.
Полученные результаты отражены в таблице, где к первой группе относятся дети, получавшие вышеуказанный протокол лечения: суспензия урсофальк в дозе 20-30 мг/кг в сутки в 1 прием в вечернее время, увеличенный объем потребляемой жидкости, до 10 мл/кг массы тела у недоношенных детей и до 20 мл/кг массы тела у доношенных детей, осуществлялось динамическое наблюдение биохимических показателей сыворотки крови (АЛТ, ACT, общий билирубин, прямой билирубин, щелочная фосфатаза), проводилось сонографическое исследование печени, определялся уровень гемоглобина, эритроцитов, ретикулоцитов в общем анализе крови, проводилось комплексное выявление возможных герпетических инфекций (ЦМВИ, ВЭБ, ВПГ - 1, 2 типа). Выявление положительных результатов привносило в коррекцию терапии назначение препарата интерферона альфа-2b в суппозиториях генферон-лайт 125000 мг по 1 свече 2 раза в день 10 дней, далее по схеме по 1 свече 2 раза в день три раза в неделю до трех месяцев.

Вторая группа детей получала только урсодезоксихолевую кислоту (суспензия урсофальк) в дозе 20-30 мг/кг в сутки в 1 прием в вечернее время, под контролем биохимических показателей сыворотки крови (АЛТ, ACT, общий билирубин, прямой билирубин, щелочная фосфатаза), определение уровня гемоглобина, эритроцитов, ретикулоцитов в общем анализе крови.
Динамика клинико-лабораторных показателей у детей с гипербилирубинемией (в днях)
Примечание: достоверные различия длительности клинико-лабораторных показателей между I и II группами:
*p≤0,05. **p≤0,01.
При контрольных анализах биохимических исследований в двух клинических группах проходило снижение уровня общего билирубина, но клиническое разрешение желтухи наблюдалось на 15-19 дней раньше в первой клинической группе.
Снижение билирубина в группе сравнения шло медленнее, потребовало продолжения комплексной терапии, а нормализация общего билирубина до сходных значений наступила в более поздние сроки на 15-18 дней от начала лечения.
Способ осуществляют следующим образом: в вечернее время в дозе 20-30 мг/кг в сутки в 1 прием назначают урсодезоксихолевую кислоту (суспензия урсофальк) и увеличенный объем потребляемой жидкости, до 10 мл/кг массы тела у недоношенных детей и до 20 мл/кг массы тела у доношенных детей, причем в динамике, один раз в месяц контролируют биохимические показатели сыворотки крови, проводя сонографическое исследование печени, определяют уровень гемоглобина, эритроцитов, ретикулоцитов, проводят выявление возможных герпетических инфекций (ЦМВИ, ВЭБ, ВПГ - 1, 2 типа), а при наличии положительных результатов, в данную тактику лечения включают препарат интерферона альфа-2b в суппозиториях генферон-лайт 125000 мг по 1 свече 2 раза в день 10 дней, далее по схеме по 1 свече 2 раза в день три раза в неделю до трех месяцев.
Пример: на амбулаторный прием обратились родители доношенного мальчика 3,5 месяцев с жалобами на длительную желтуху, причем из анамнеза заболевания стало известно, что по назначению врача педиатра ребенок получал сорбенты (смекта в течение 7-10 дней, хофитол в дозе 5 капель 3 раза в день в течение 21 дня), но клинического эффекта не наблюдалось.
Со слов матери во время беременности выявлялись IgG к ЦМВИ, ВПГ 1, 2 типа, не требующие лечения. В антенатальном периоде наблюдалась угроза прерывания, гестоз легкой степени, маловодие, вероятно, не исключалось внутриутробное влияние инфекционного агента. При рождении масса ребенка 3570 г, рост 57 см, 7-8 баллов по Апгар при рождении. В родильном доме находился на совместном пребывании с матерью, получал грудное вскармливание, медикаментозное лечение не осуществлялось. Прививки в родильном доме: в первые 12 часов - вакцина против гепатита В, на 5 сутки - БЦЖ.
При клиническом обследовании обращало на себя внимание затяжное течение желтухи, наличие низкой прибавки массы тела, появление гепатомегалии до 2-2,5 см ниже реберной дуги, увеличение селезенки до 1 см.
При лабораторном обследовании в OAK определялось снижение эритроцитов до 3,4 Т/л и гемоглобина до 98 г/л, при увеличении в формуле лимфоцитов до 69% и моноцитов до 12%. По данным биохимических исследований крови уровень общего билирубина при первичном обращении составил 172,3 мкмоль/л, прямого билирубина 9,7 мкмоль/л, АЛТ - 49 Ед/л, ACT 78 Ед/л, ЩФ - 875 Ед/л. Выявленные изменения подтверждали клиническую картину заболевания и выявляли у пациента признаки анемии 1 степени, изменения в ОАК, характерные для течения вирусной инфекции. В биохимическом обследовании выявлялись симптом цитолиза, симптом холестаза.
По результатам сонографического обследования печени выявлялись увеличенные размеры правой доли, диффузные изменения паренхимы, что говорит о внутриутробном влиянии инфекционного агента, а также наличие анатомической аномалии формы желчного пузыря в виде перетяжки в верхней трети, что нарушало отток желчи, являясь причиной холестаза.
Учитывая данные клинико-лабораторных обследований: длительную субиктеричность кожи и слизистых, отсутствие эффекта от проведенной стартовой терапии, гепатолиенальный синдром, низкую прибавку массы тела, гипербилирубинемия за счет непрямой фракции, симптома цитолиза, холестаза, анемию, лимфоцитоз, моноцитоз в ОАК, увеличение размеров правой доли печени, диффузные изменения, перетяжку в верхней трети желчного пузыря, сбор анамнеза беременности с наличием выявления IgG к ЦМВИ, ВПГ 1, 2 типа, угрозы прерывания, гестоза легкой степени, маловодия, все выше перечисленное не исключает развитие внутриутробного влияния герпетических инфекций.
При обследовании методом ИФА определялись антитела класса IgM к цитомегаловирусу, ПЦР ДНК ЦМВ положительный анализ из крови, на ВПГ 1, 2 типа выявлялись материнские антитела IgG, данные обследования подтвердили влияние герпетических инфекций и дали возможность поставить диагноз: Врожденная цитомегаловирусная инфекция, висцеральная форма (гепатит - минимальной степени активности), острое течение. Анемия легкой степени, аномалия формы желчного пузыря.
До первичного обращения и неэффективности проведенной терапии в протокол лечения включили урсофальк суспензия 20 мг/кг на 1 прием в вечернее время длительностью до 1 месяца, увеличенный объем потребляемой жидкости, до 20 мл/кг массы тела, препарат интерферона альфа-2b в суппозиториях (генферон-лайт 125000 мг по 1 свече 2 раза в день 10 дней, далее по схеме по 1 свече 2 раза в день три раза в неделю до трех месяцев.
За время терапии цвет кожных покровов и слизистых оболочек восстановился к 21 суткам, отмечалась стабильная прибавка массы тела, гепатоспленомегалия с регрессией показателей отмечена на втором месяце наблюдения.
При динамическом обследовании к месяцу лечении гемоглобин нормализовался и достиг 109 г/л без использования препаратов железа, нормализовались лимфоциты и моноциты в ОАК. Стабилизация показателей биохимии наблюдалась на 34 сутки наблюдения, где уровень общего билирубина снизился до 15,4 мкмоль/л, АЛТ 27,4 ед/л, ACT 39,5 ед/л, в ИФА определялись антитела IgG к ЦМВ, a IgM - отрицательные, ДНК ЦМВ в крови не определялось.
После проведенного лечения на сонографическом исследовании печени паренхима восстановилась, правая доля уменьшилась до нормальных значений. Во время использования указанной схемы лечения, мать ребенка не отмечала побочных эффектов терапии и сама отмечала ее эффективность.
Применение комплексного подхода, анализ возможных причин, ранняя диагностика затяжной гипербилирубинемии, подбор адекватной этиопатогенетической терапии позволил не только определить причину заболевания, но и в максимально короткие сроки привел к клинико-лабораторной нормализации измененных показателей, что показывает высокую эффективность выбранного подхода.
Способ лечения конъюгационных гипербилирубинемий у детей первого года жизни, включающий назначение урсодезоксихолевой кислоты, отличающийся тем, что суспензию урсофальк вводят в вечернее время в дозе 20-30 мг/кг в сутки в 1 прием, вводят увеличенный объем потребляемой жидкости до 10 мл/кг массы тела у недоношенных детей и до 20 мл/кг массы тела у доношенных детей, причем в динамике один раз в месяц контролируют биохимические показатели сыворотки крови, проводят сонографическое исследование печени, определяют уровень гемоглобина, эритроцитов, ретикулоцитов, проводят комплексное выявление герпетических инфекций: ЦМВИ, ВЭБ, ВПГ - 1, 2 типа, а при наличии положительных результатов в данную тактику лечения включают препарат интерферона альфа-2b в суппозиториях генферон-лайт 125000 мг по 1 свече 2 раза в день 10 дней, далее по схеме по 1 свече 2 раза в день три раза в неделю до трех месяцев.