Канальцевая протеинурия что это такое
Протеинурия : причины, симптомы, диагностика, лечение
При наличии выраженной лейкоцитурии и особенно гематурии положительная качественная реакция на белок в моче обусловлена распадом клеточных элементов при длительном стоянии мочи; в этой ситуации патологической считают протеинурию, превышающую 0,3 г/сут.
Осадочные белковые пробы дают ложноположительные результаты при наличии в моче йодсодержащих контрастных веществ, большого количества антибиотиков (пенициллинов или цефалоспоринов), метаболитов сульфаниламидов.
В ранних стадиях развития большинства нефропатий в мочу проникают преимущественно низкомолекулярные плазменные белки (альбумин, церулоплазмин, трансферрин и др.). Однако возможно обнаружение и высокомолекулярных протеинов (альфа2-макроглобулина, у-глобулина), более типичных для выраженного поражения почек с «большой» протеинурией.
К селективной относят протеинурию, представленную белками с низкой молекулярной массой не более 65 000 кДа, главным образом альбумином. Неселективная протеинурия характеризуется повышением клиренса средне- и высокомолекулярных белков: в составе белков мочи преобладают а2-макроглобулин, бета-липопротеиды, у-глобулин. Кроме плазменных белков в моче определяют белки почечного происхождения - уропротеин Тамма-Хорсфолла, секретируемый эпителием извитых канальцев.
Клубочковая (гломерулярная) протеинурия обусловлена увеличением фильтрации плазменных белков через клубочковые капилляры. Это зависит от структурного и функционального состояния стенки клубочковых капилляров, свойств белковых молекул, давления и скорости кровотока, определяющих СКФ. Клубочковая протеинурия - обязательный признак большинства заболеваний почек.
Стенку клубочковых капилляров составляют эндотелиальные клетки (с округлыми отверстиями между ними), трехслойная базальная мембрана - гидратированный гель, а также эпителиальные клетки (подоциты) со сплетением ножковых отростков. Благодаря сложному строению клубочковая капиллярная стенка может «просеивать» плазменные молекулы из капилляров в пространство капсулы клубочка, причём эта функция «молекулярного сита» в значительной степени зависит от давления и скорости кровотока в капиллярах.
В патологических условиях размеры «пор» увеличиваются, отложения иммунных комплексов вызывают локальные изменения капиллярной стенки, повышают её проницаемость для макромолекул. Помимо размеров клубочковых «пор», важны и электростатические факторы. Клубочковая базальная мембрана заряжена отрицательно; отрицательный заряд несут на себе и ножковые отростки подоцитов. В нормальных условиях отрицательный заряд клубочкового фильтра отталкивает анионы - отрицательно заряженные молекулы (в том числе молекулы альбумина). Изменение заряда способствует фильтрации альбумина. Предполагают, что слияние ножковых отростков - морфологический эквивалент изменения заряда.
Канальцевая (тубулярная) протеинурия обусловлена неспособностью проксимальных канальцев реабсорбировать плазменные низкомолекулярные белки, профильтрованные в нормальных клубочках. Протеинурия редко превышает 2 г/сут, экскретируемые белки представлены альбумином, а также фракциями с ещё более низкой молекулярной массой (лизоцим, бета2-микроглобулин, рибонуклеаза, свободные лёгкие цепи иммуноглобулинов), отсутствующими у здоровых лиц и при клубочковой протеинурии в связи со 100% реабсорбцией эпителием извитых канальцев. Характерный признак канальцевой протеинурии - преобладание бета 2-микроглобулина над альбумином, а также отсутствие высокомолекулярных белков. Канальцевую протеинурию наблюдают при поражении почечных канальцев и интерстиция: при тубулоинтерстициальном нефрите, пиелонефрите, калийпенической почке, остром канальцевом некрозе, хроническом отторжении почечного трансплантата. Канальцевая протеинурия характерна также для многих врождённых и приобретённых тубулопатий, в частности синдрома Фанкони.
Протеинурия «переполнения» развивается при повышении концентрации низкомолекулярных белков (лёгких цепей иммуноглобулинов, гемоглобина, миоглобина) в плазме крови. При этом данные белки фильтруются неизменёнными клубочками в количестве, превышающем способность канальцев к реабсорбции. Таков механизм протеинурии при множественной миеломе (протеинурии Бенс-Джонса) и других плазмоклеточных дискразиях, а также миоглобинурии.
Выделяетсят так называемая функциональная протеинурия. Механизмы развития и клиническое значение большинства её вариантов не известны.
- Ортостатическая протеинурия возникает при длительном стоянии или ходьбе («proteinuria en marche») с быстрым исчезновением в горизонтальном положении. При этом величина экскреции белков с мочой не превышает 1 г/сут. Ортостатическая протеинурия является клубочковой и неселективной и, по данным длительных проспективных исследований, всегда доброкачественна. При изолированном её характере отсутствуют другие признаки поражения почек (изменения в мочевом осадке, повышение артериального давления). Чаще наблюдается в юношеском возрасте (13-20 лет), у половины людей исчезает через 5-10 лет от момента возникновения. Характерно отсутствие белка в анализах мочи, взятых сразу после пребывания больного в горизонтальном положении (в том числе утром до подъёма с постели).
- Протеинурия напряжения, обнаруживаемая после интенсивных физических нагрузок не менее чем у 20% здоровых лиц, в том числе у спортсменов, по-видимому, также доброкачественна. По механизму возникновения её считают канальцевой, обусловленной перераспределением внутрипочечного кровотока и относительной ишемией проксимальных канальцев.
- При лихорадке с температурой тела 39-41 °С, особенно у детей и лиц пожилого и старческого возраста, обнаруживают так называемую лихорадочную протеинурию. Она является клубочковой, механизмы её развития не известны. Возникновение протеинурии у больного с лихорадкой иногда указывает на присоединение поражения почек; в пользу этого свидетельствуют одновременно возникающие изменения мочевого осадка (лейкоцитурия, гематурия), большие, особенно нефротические величины экскреции белков с мочой, а также артериальная гипертензия.
Протеинурия, превышающая 3 г/сут, - ключевой признак нефротического синдрома.
Протеинурия и прогрессирование хронических нефропатий
Значение протеинурии как маркёра прогрессирования поражений почек во многом обусловлено механизмами токсического действия отдельных компонентов белкового ультрафильтрата на эпителиоциты проксимальных канальцев и другие структуры почечного тубулоинтерстиция.
Компоненты белкового ультрафильтрата, оказывающие нефротоксическое действие
| Белок | Механизм действия |
| Альбумин | Увеличение экспрессии провоспалительных хемокинов (моноцитарного хемоаттрактантного протеина типа 1, RANTES*) Токсическое действие на эпителиоциты проксимальных канальцев (перегрузка и разрыв лизосом с высвобождением цитотоксических ферментов) Индукция синтеза молекул вазоконстрикции, усугубляющих гипоксию тубулоинтерстициальных структур Активация апоптоза эпителиоцитов проксимальных канальцев |
| Трансферрин | Индукция синтеза компонентов комплемента эпителиоцитами проксимальных канальцев Увеличение экспрессии провоспалительных хемокинов Образование реактивных кислородных радикалов |
| Компоненты комплемента | Формирование цитотоксического МАК** (С5b-С9) |
- * RANTES (Regulated upon activation, normal T-lymphocyte expressed and secreted) - активируемая субстация, экспрессируемая и секретируемая нормальными Т-лимфоцитами.
- ** МАК - мембраноатакующий комплекс.
Многие мезангиоциты и гладкомышечные клетки сосудов претерпевают аналогичные изменения, означающие приобретение основных свойств макрофага. В почечный тубулоинтерстиций активно мигрируют моноциты из крови, также превращающиеся в макрофаги. Белки плазмы индуцируют процессы тубулоинтерстициального воспаления и фиброза, называемые протеинурическим ремоделированием тубулоинтерстиция.
Выраженность протеинурического ремоделирования тубулоинтерстиция - один из основных факторов, определяющих скорость прогрессирования почечной недостаточности при хронических нефропатиях. Зависимость увеличения концентрации сывороточного креатинина от величины протеинурии и распространённости тубулоинтерстициального фиброза неоднократно продемонстрирована для различных форм хронического гломерулонефрита и амилоидоза почек.
[9], [10], [11], [12], [13], [14], [15], [16], [17]
Протеинурия — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 5 июля 2015; проверки требуют 8 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 5 июля 2015; проверки требуют 8 правок.Протеинурия — обнаружение белка в анализе мочи.
Классификация по Бергштейну[править | править код]
Классификация протеинурии по J. Bergstein (1992):
- Непатологическая протеинурия
- Постуральная (ортостатическая)
- Фебрильная
- Физические нагрузки
- Патологическая протеинурия
- Гломерулярные
- Тубулярные наследственные
- Тубулярные приобретённые
Классификация по Робсону[править | править код]
Классификация протеинурии в зависимости от основного патофизиологического механизма по А. Robson (1987)
Персистирующая протеинурия
- Увеличенная клубочковая проницаемость для белков плазмы
- Повреждение базальных мембран: гломерулонефриты.
- Потеря клубочкового полианиона: нефротический синдром с минимальными изменениями.
- Другие возможные механизмы: увеличение фильтрационной фракции, уменьшение массы нефронов с повышением проницаемости оставшихся нефронов.
- Снижение кальциевой реабсорбции профильтровавшихся белков
Синдром Фанкони, Балканская нефропатия, наследственные канальцевые нарушения, действие нефротоксичных лекарственных препаратов.
- Протеинурия по механизму «переполнения»
- Секреторная протеинурия
- Протеинурия Тамма-Хорсфалла: неонатальный период, пиелонефрит.
- Почечно-специфические антигены: анальгетическая нефропатия, отравление тяжелыми металлами, быстропрогрессирующий гломерулонефрит.
- Другие белки: патология предстательной железы, других вторичных половых желез.
Постуральная протеинурия
Периодическая протеинурия
- Случайное обнаружение — причина неизвестна.
- Экстраренальные нарушения — лихорадка, стресс, физическая нагрузка, пребывание на холоде.
- Почечная патология (в редких случаях изолированные нарушения) — инфекция мочевыводящих путей, обструкция.
- Загрязнение мочи — влагалищные секреты.
- Ложноположительный тест — сульфаниламиды, пенициллины, бутамид, хлоргексидин, рентгенконтрастные вещества.
Существует физиологическое выделение белка из мочевого тракта, предстательной железы, но оно не превышает 150 мг/сут. Такая небольшая концентрация не выявляется в разовых порциях.
Методы определения белка в моче можно разделить на:
- Качественные
- Полуколичественные
- Метод Брандберга-Робертса-Стольникова,
- Определение белка в моче с помощью диагностических тест-полосок.
- Количественные
Физиологическая протеинурия:
- в разовых порциях мочи — до 0,033 г\л.
- суточная экскреция белка с мочой 30-50 мг\сут (у детей до 1 мес 240 мг\м2; у детей старше 1 мес — 60 мг\м2\сут).
Увеличивают протеинурию: лихорадка, стресс, физические нагрузки, введение норадреналина.
Белок в моче во время беременности:
- до 30 мг - норма;
- 30 – 300 мг – микроальбуминурия;
- от 300 мг – макроальбуминурия.
В период беременности показатель белка, который превышает 300 мг за сутки, зачастую является показателем преэклампсии. У женщин, которые ждут ребёнка, показатель белка в анализах мочи за 12 часов коррелирует с показаниями за сутки. Учёные доказали, что 300 мг белка в суточном анализе мочи не является показателем осложнений во время беременности (гипертония, преждевременные роды, маленький вес ребёнка). Поэтому исследователями было предложено отодвинуть суточный показатель до 500 мг.[3]
Слабо выраженная протеинурия 150—500 мг\сут. Причины — острый постстрептококковый гломерулонефрит; хронический гломерулонефрит, гематурическая форма; наследственный нефрит; тубулопатии; интерстициальный нефрит; обструктивная уропатия.
Умеренно выраженная протеинурия 500—2000 мг\сут. Причины — острый постстрептококовый гломерулонефрит; наследственный нефрит; хронический гломерулонефрит.
Выраженная протеинурия более 2000 мг\сут. Причины — нефротический синдром, амилоидоз.
Преренальная протеинурия — усиленный распад белка в тканях и гемолиз.
Ренальная протеинурия — клубочковая или канальцевая.
Постренальная протеинурия — связанная с патологией мочевыводящей системы (мочеточник, мочевой пузырь, уретра, половые органы).
Постоянная протеинурия — при заболеваниях почек.
Переходящая протеинурия — при лихорадке, ортостатическая.
- М. В. Эрман — Нефрология детского возраста в схемах и таблицах, СпБ, 1997, стр 14-15.
- А. В. Папаян, Н. Д. Савенкова — Клиническая нефрология детского возраста, СпБ, 1997.
Протеинурия. Клиническое значение выявления общего белка в моче
В последнее время в отечественной литературе достаточно часто обсуждается вопрос: что считать протеинурией? Если раньше протеинурией называли просто обнаружение белка в моче обычными качественными или количественными методами, чувствительность и специфичность которых была не очень высока, то сейчас, учитывая все большее внедрением в практику более чувствительных и специфичных методов, о протеинурии говорят, когда уровень белка в моче превышает норму. Варьирует и понятие нормы белка в моче – что связано с использованием как старых, так и новых методов определения белка в моче, которые отличаются чувствительностью и специфичностью. Некоторые авторы, учитывая наличие белка в моче и у здорового человека, понимают под термином протеинурия вообще выделение белка с мочой и для простоты делят протеинурию на физиологическую и патологическую, что сейчас также дискутируется. Обычно под термином протеинурия понимается увеличение содержания белка в моче.
В большинстве лабораторий при исследовании мочи «на белок» сначала пользуются качественными реакциями, которые не обнаруживают белок в моче здорового человека. Если же белок в моче обнаружен качественными реакциями, проводят количественное (или полуколичественное) его определение. При этом имеют значение особенности используемых методов, охватывающих различный спектр уропротеинов. Так, при определении белка с помощью 3% сульфосалициловой кислоты, нормальным считается количество белка до 0,03 г/л, при использовании же пирогаллолового метода, граница нормальных значений белка повышается до 0,1 г/л. В связи с этим в бланке анализа необходимо указывать нормальное значение белка для того метода, которым пользуется лаборатория.
При определении минимальных количеств белка рекомендуется повторить анализ, в сомнительных случаях следует определять суточную потерю белка с мочой. В норме суточная моча содержит белок в незначительных количествах. В физиологических условиях профильтровавшийся белок практически полностью реабсорбируется эпителием проксимальных канальцев и содержание его в суточном количестве мочи колеблется по разным авторам от следов до 20 – 50, 80 – 100 мг и даже до 150 – 200 мг. Некоторые авторы считают, что суточная экскреция белка в количестве 30 – 50 мг/сут является физиологической нормой для взрослого человека. Другие полагают, что выделение белка с мочой не должно превышать 60 мг/м2 поверхности тела в сутки, исключая первый месяц жизни, когда величина физиологической протеинурии может в четыре раза превышать указанные значения.
Общим условием появления белков в моче здорового человека являются достаточно высокая их концентрация в крови и молекулярная масса не более 100 – 200 кДа.
У практически здоровых людей под воздействием различных факторов может появляться преходящая протеинурия. Такую протеинурию называют также физиологической, функциональной или доброкачественной, так как она, в отличие от патологической, не требует лечения.
Физиологическая протеинурия
Маршевая протеинурия
Преходящее выделение белка с мочой у здоровых людей может появляться после тяжелой физической нагрузки (длительные походы, марафонский бег, игровые виды спорта). Это так называемая рабочая (маршевая) протеинурия или протеинурия напряжения, наблюдавшаяся и описанная многими исследователями. Работы этих авторов, иллюстрирующие возможность развития протеинурии под влиянием физической нагрузки, свидетельствуют о высокой степени ее выраженности, а также ее обратимости. Генез такой протеинурии объясняют гемолизом с гемоглобинурией и стрессовой секрецией катехоламинов с преходящим нарушением гломерулярного кровотока. При этом протеинурия выявляется в первой после физической нагрузки порции мочи.
Значение фактора охлаждения в генезе скоропреходящей протеинурии было отмечено у здоровых людей под влиянием холодных ванн.
Albuminuria solaris
Известна albuminuria solaris, возникающая при выраженной реакции кожи на инсоляцию, а также при раздражении кожи некоторыми веществами, например, при смазывании ее йодом.
Протеинурия при повышении уровня адреналина и норадреналина в крови
Установлена возможность появления протеинурии при повышении уровня адреналина и норадреналина в крови, чем объясняют выделение белка с мочой при феохромоцитоме и гипертонических кризах.
Алиментарная протеинурия
Выделяют алиментарную протеинурию, появляющуюся иногда после употребления обильной белковой пищи.
Центрогенная протеинурия
Доказана возможность появления центрогенной протеинурии – при эпилепсии, сотрясении мозга.
Эмоциональная протеинурия
Описана эмоциональная протеинурия во время экзаменов.
Пальпаторная протеинурия
К протеинурии функционального происхождения относят и описываемое некоторыми авторами выделение белка с мочой при энергичной и продолжительной пальпации живота и области почек (пальпаторная протеинурия).
Лихорадочная протеинурия
Лихорадочная протеинурия наблюдается при острых лихорадочных состояниях, чаще у детей и стариков. Механизм ее малоизучен. Этот вид протеинурии сохраняется в период повышения температуры тела и исчезает при ее снижении и нормализации. Если протеинурия сохраняется в течение многих дней и недель после нормализации температуры тела, то следует исключить возможное органическое заболевание почек - либо вновь возникшее, либо уже существующее.
Застойная (сердечная) протеинурия
При заболеваниях сердца часто выявляют застойную, или сердечную протеинурию. С исчезновением сердечной недостаточности она обычно исчезает.
Протеинурия новорождённых
У новорождённых в первые недели жизни также наблюдается физиологическая протеинурия.
Ортостатическая (постуральная, лордотическая) протеинурия
Ортостатическая (постуральная, лордотическая) протеинурия наблюдается у 12 – 40% детей и подростков, характеризуется выявлением белка в моче при длительном стоянии или ходьбе с быстрым исчезновением (преходящий вариант ортостатической протеинурии) или уменьшением его (персистирующий вариант) в горизонтальном положении. Генез ее связывают с нарушениями почечной гемодинамики, развивающимися за счет лордоза, сдавливающего нижнюю полую вену в положении стоя, или выброса ренина (ангиотензина II) в ответ на изменения объема циркулирующей плазмы при ортостатизме.
Физиологическая протеинурия, как правило, незначительная – не более 1,0 г/сут.
Современные методы исследования позволяют выявить ряд изменений в микроструктуре почек, следствием которых и является так называемая физиологическая протеинурия. Исходя из таких соображений, многие авторы сомневаются в правомочности выделения «функциональной» протеинурии.
Патологическая протеинурия
Патологическая протеинурия бывает почечного и внепочечного происхождения.
Почечная протеинурия
Почечная протеинурия является одним из наиболее важных и постоянных признаков заболеваний почек и может быть гломерулярной, или клубочковой, и тубулярной, или канальцевой. При сочетании этих двух типов развивается смешанный тип протеинурии.
Клубочковая протеинурия
Клубочковая протеинурия обусловлена повреждением гломерулярного фильтра, возникает при гломерулонефритах и при нефропатиях, связанных с обменными или сосудистыми заболеваниями. При этом из крови в мочу в большом количестве фильтруются плазматические белки.
В основе нарушения работы клубочкового фильтра лежат различные патогенетические механизмы:
- токсические или воспалительные изменения гломерулярной базальной мембраны (отложение иммунных комплексов, фибрина, клеточная инфильтрация), вызывающие структурную дезорганизацию фильтра;
- изменения гломерулярного кровотока (вазоактивные агенты – ренин, ангиотензин II, катехоламины), влияющие на гломерулярное транскапиллярное давление, процессы конвекции и диффузии;
- недостаток (дефицит) специфических гломерулярных гликопротеидов и протеогликанов, ведущий к потере фильтром отрицательного заряда.
Клубочковая протеинурия наблюдается при остром и хроническом гломерулонефрите, амилоидозе, диабетическом гломерулосклерозе, тромбозе почечных вен, застойной почке, гипертонической болезни, нефросклерозе.
Клубочковая протеинурия может быть селективной и неселективной в зависимости от тяжести повреждения гломерулярного фильтра.
Селективная протеинурия
Селективная протеинурия встречается при минимальном (нередко обратимом) повреждении гломерулярного фильтра (нефротический синдром с минимальными изменениями), представлена белками с молекулярной массой не выше 68000 – альбумином и трансферрином.
Неселективная протеинурия
Неселективная протеинурия чаще встречается при более тяжелом повреждении фильтра, отличается повышением клиренса средне- и высокомолекулярных плазматических белков (в составе белков мочи присутствуют также альфа2-глобулины и гамма-глобулины). Неселективная протеинурия наблюдается при нефротической и смешанной формах гломерулонефрита, вторичном гломерулонефрите.
Канальцевая протеинурия (тубулярная протеинурия)
Канальцевая протеинурия связана либо с неспособностью канальцев реабсорбировать белки, прошедшие через неизмененный гломерулярный фильтр, либо обусловлена выделением белка эпителием самих канальцев.
Канальцевая протеинурия наблюдается при остром и хроническом пиелонефрите, отравлении тяжелыми металлами, остром канальцевом некрозе, интерстициальном нефрите, хроническом отторжении почечного трансплантата, калийпенической нефропатии, генетических тубулопатиях.
Степень выраженности протеинурии
В зависимости от степени выраженности выделяют легкую, умеренную и тяжелую протеинурию.
Легкая протеинурия
Легкая протеинурия (от 300 мг до 1 г/сут) может наблюдаться при острой инфекции мочевыводящих путей, обструктивной уропатии и пузырно-мочеточниковом рефлюксе, тубулопатиях, мочекаменной болезни, хроническом интерстициальном нефрите, опухоли почки, поликистозе.
Умеренная протеинурия
Умеренная протеинурия (от 1 до 3 г/сут) отмечается при остром канальцевом некрозе, гепаторенальном синдроме, первичном и вторичном гломерулонефрите (без нефротического синдрома), протеинурической стадии амилоидоза.
Тяжёлая (выраженная) протеинурия
Под тяжелой, или выраженной протеинурией понимают потерю белка с мочой, превышающую 3,0 г в сутки или 0,1 г и более на килограмм массы тела за 24 часа. Такая протеинурия почти всегда связана с нарушением функции клубочкового фильтрационного барьера в отношении размера или заряда белков и наблюдается при нефротическом синдроме.
Выявление и количественная оценка протеинурии важны как для диагностики, так и для оценки течения патологического процесса, эффективности проводимого лечения. В заключении необходимо отметить, что диагностическая значимость протеинурии оценивается в совокупности с другими изменениями в моче.
Литература:
- Л. В. Козловская, А. Ю. Николаев. Учебное пособие по клиническим лабораторным методам исследования. Москва, Медицина, 1985 г.
- А. В. Папаян, Н. Д. Савенкова "Клиническая нефрология детского возраста", Санкт-Петербург, СОТИС, 1997 г.
- Куриляк О.А. "Белок в моче – методы определения и границы нормы (современное состояние проблемы)"
- А. В. Козлов, «Протеинурия: методы ее выявления», лекция, Санкт-Петербург, СПбМАПО, 2000 г.
- В. Л. Эмануэль, «Лабораторная диагностика заболеваний почек. Мочевой синдром», - Справочник заведующего КДЛ, № 12, декабрь 2006 г.
- О. В. Новоселова, М. Б. Пятигорская, Ю. Е. Михайлов, «Клинические аспекты выявления и оценки протеинурии», Справочник заведующего КДЛ, № 1, январь 2007 г.
причины, признаки, прогноз — Онлайн-диагностика
Медучреждения, в которые можно обратитьсяОбщее описание
Протеинурия — это выделение с мочой белка в количестве, превышающем нормальные значения. Это самый распространенный признак поражения почек. В норме за сутки в мочу экскретируется не более 50 мг белка, состоящего из профильтровавшихся плазменных низкомолекулярных белков.
Причины:
- Поражение почечных канальцев (интерстициальный нефрит, тубулопатии) приводит к нарушению реабсорбции профильтровавшегося белка и появлению его в моче.
- Гемодинамические факторы — скорость и объем капиллярного кровотока, баланс гидростатического и онкотического давления также имеют значение для появления протеинурии. Проницаемость капиллярной стенки возрастает, способствуя протеинурии, как при снижении скорости тока крови в капиллярах, так и при гиперперфузии клубочков и внутриклубочковой гипертензии. Возможная роль гемодинамических изменений должна учитываться при оценке протеинурии, особенно преходящей, и у больных с недостаточностью кровообращения.
Симптомы и диагностика протеинурии
| Виды протеинурии | |||
| по связи с заболеваниями | по источнику | по составу | по величине или степени выраженности |
| 1. Функциональная. 2. Патологическая. | 1. Преренальная («переполнения»). 2. Ренальная: клубочковая и канальцевая. 3. Постренальная. | 1. Селективная. 2. Неселективная. | 1. Микроальбуминурия. 2. Низкая. 3. Умеренная. 4. Высокая (нефротическая). |
По связи с заболеваниями протеинурия подразделяется на функциональную и патологическую.
Функциональная протеинурия наблюдается у пациентов со здоровыми почками. Функциональная протеинурия невысокая (до 1 г/сутки), обычно преходящая, изолированная (отсутствуют другие признаки поражения почек), редко сочетается с эритроцитурией, лейкоцитурией, цилиндрурией. Существует несколько типов функциональной протеинурии:
- Ортостатическая. Встречается у молодых лиц 13–20 лет, не превышает 1 г/сутки, исчезает в положении лежа. Данный вид протеинурии диагностируется при помощи ортостатической пробы — первую утреннюю порцию мочи пациент собирает, не вставая с постели, затем выполняет небольшую физическую нагрузку (ходьба по лестнице), после чего собирает вторую порцию мочи на анализ. Отсутствие белка в первой и наличие во второй порции мочи свидетельствуют об ортостатической протеинурии.
- Лихорадочная (до 1–2 г/сутки). Наблюдается при лихорадочных состояниях, чаще у детей и стариков, исчезает при нормализации температуры тела, в ее основе лежит повышение клубочковой фильтрации.
- Протеинурия напряжения (маршевая). Возникает после тяжелого физического напряжения, выявляется в первой порции мочи, исчезает при обычных физических нагрузках. В ее основе лежит перераспределение кровотока с относительной ишемией проксимальных канальцев.
- Протеинурия при ожирении. Связана с развитием внутриклубочковой гипертензии и гиперфильтрации на фоне повышенной концентрации ренина и ангиотензина. При потере массы тела и лечении ингибиторами АПФ может уменьшаться и даже исчезать.
- Физиологическая протеинурия. К ее появлению может привести беременность, поскольку она сопровождается возрастанием клубочковой фильтрации без увеличения канальцевой реабсорбции. Уровень не должен превышать 0,3 г/сутки.
- Идиопатическая преходящая. Выявляется у здоровых лиц при медицинском обследовании и отсутствует при последующих исследованиях мочи.
Патологическая протеинурия выявляется при заболеваниях почек, мочевыводящих путей, а также при воздействии внепочечных факторов.
По источнику протеинурия может быть преренальной, ренальной и постренальной.
Преренальная, или протеинурия «переполнения», наблюдается при миеломной болезни (протеинурия Бенс-Джонса), рабдомиолизе, макроглобулинемии Вальденстрема, массивном внутрисосудистом гемолизе. Протеинурия переполнения может колебаться от 0,1 до 20 г/сутки. Высокая протеинурия (более 3,5 г/сутки.) в этом случае не является признаком нефротического синдрома, так как не сопровождается гипоальбуминемией и другими его признаками. Для выявления миеломной нефропатии больному необходимо исследовать мочу на белок Бенс-Джонса.
Ренальная протеинурия по механизму возникновения может быть клубочковой и канальцевой.
Клубочковая протеинурия наблюдается при большинстве заболеваний почек — гломерулонефритах (первичных и при системных заболеваниях), амилоидозе почек, диабетическом гломерулосклерозе, а также при гипертонической болезни, «застойной» почке.
Канальцевая протеинурия наблюдается при интерстициальном нефрите, пиелонефрите, врожденных тубулопатиях (синдром Фанкони) и других заболеваниях почек с преимущественным поражением канальцев.
Клубочковая и канальцевая протеинурия дифференцируются наличием α1-микроглобулина и количественным сравнением уровня альбумина и β2-микроглобулина в моче, которое в норме составляет от 50:1 до 200:1. Соотношение альбумина и β2-микроглобулина — 10:1, и α1-микроглобулин указывают на канальцевую протеинурию. При клубочковой протеинурии такое соотношение будет превышать 1000:1.
Постренальная протеинурия имеет внепочечное происхождение, развивается при наличии бактериального воспалительного процесса в мочевыделительной системе (пиелонефриты) из-за увеличения экссудации протеинов плазмы в мочу.
По составу выделяют селективную и неселективную протеинурии.
Селективная протеинурия отличается выделением белка с низкой молекулярной массой, в основном альбумина. Прогностически она считается более благоприятной, чем неселективная.
При неселективной протеинурии белок выделяется со средней и высокой молекулярной массой (α2-макроглобулины, β-липопротеиды, γ-глобулины). Широкий белковый спектр неселективной протеинурии свидетельствует о тяжелом поражении почек, характерен для постренальной протеинурии.
По степени выраженности (величине) выделяют микроальбуминурию, низкую, умеренную, высокую (нефротическую) протеинурию.
Микроальбуминурия — выделение с мочой минимального, лишь слегка превышающего физиологическую норму, альбумина (от 30 до 300–500 мг/сутки). Микроальбуминурия является первым ранним симптомом диабетической нефропатии, поражения почек при артериальной гипертензии, отторжения почечного трансплантата. Поэтому категориям пациентов с такими показателями необходимо назначать исследование суточной мочи на микроальбуминурию при отсутствии изменений в общем анализе мочи.
Низкая (до 1 г/сутки) и умеренная (от 1 до 3 г/сутки) отмечаются при различных заболеваниях почек и мочевыводящих путей (гломерулонефрит, пиелонефрит, нефролитиаз, опухоли почек, туберкулез и др.). Величина протеинурии зависит от степени повреждения почек и от выраженности воспалительного процесса в мочевыводящих путях.
При высокой (нефротической) протеинурии потеря белка составляет более 3,5 г/сутки. Наличие высокой протеинурии в сочетании гипоальбуминемией и является признаком нефротического синдрома.
Следует помнить, что концентрация белка в разовых порциях мочи в течение суток различается. Для более точного представления о степени выраженности протеинурии исследуют суточную мочу (суточная протеинурия).
Рекомендации при протеинурии
- Консультация нефролога.
- Консультация уролога.
- Суточная протеинурия.
Заболеваемость (на 100 000 человек)
| Мужчины | Женщины | |||||||||||||
| Возраст, лет | 0-1 | 1-3 | 3-14 | 14-25 | 25-40 | 40-60 | 60 + | 0-1 | 1-3 | 3-14 | 14-25 | 25-40 | 40-60 | 60 + |
| Кол-во заболевших | 0 | 0 | 0 | 2.5 | 0 | 0 | 0 | 0 | 0 | 0 | 2.5 | 0 | 0 | 0 |
Что нужно пройти при подозрении на протеинурию
- 1. Анализ мочи общий
Симптомы
| Вcтречаемость (насколько часто симптом проявляется при данном заболевании) | |
|---|---|
| Отек век по утрам | 10% |
Протеинурия у взрослых: диагностический подход
Анализ мочи:
10.04.2009
M. F. Carroll, M.D. and J. L. Temte, M.D., PH.D.
University of Wisconsin-Madison Medical School, Madison, Wisconsin
Am Fam Physician 2000; 62:1333–40
Перевод к.б.н. Куриляк О.А.
По данным популяционных исследований, при анализе мочи диагностическими полосками, у 17% пациентов выявляется протеинурия [1]. Однако тяжелая патология мочевых путей подтверждается лишь не более чем у 2% пациентов, в моче которых диагностическими полосками обнаруживается белок [2]. Причиной развития протеинурии является целый ряд заболеваний, которые могут заканчиваться как благополучным, так и летальным исходом. К диагностике протеинурии надо подходить очень ответственно, так как диагноз влияет на психологическое состояние пациента, его карьеру и условия страхования.
Определение протеинурии
24 столетия тому назад Гиппократ указал на связь между «пузырьками на поверхности мочи» и заболеваниями почек [3,4]. В наше время под протеинурией понимают выделение белка с мочой в количестве более 150 мг/сут. Содержание белка в моче у здоровых лиц значительно варьирует и при определенных обстоятельствах увеличивается до уровня, который соответствует протеинурии. В большинстве случаев, когда при исследовании мочи диагностические полоски (например, Albustix, Multistix) дают положительную реакцию на белок, речь идет о доброкачественной протеинурии, которая не связана с увеличением заболеваемости или смертности (табл. 1).
Таблица 1. Распространенные причины развития доброкачественной протеинурии
| Обезвоживание | Воспалительные процессы |
| Эмоциональный стресс | Физическая нагрузка |
| Лихорадка | Большинство острых заболеваний |
| Перегревание | Ортостатическая (постуральная) протеинурия |
Примерно 20% общего количества белка, который выделяется почками в физиологических условиях, приходится на долю низкомолекулярных белков, таких как иммуноглобулины (молекулярная масса около 20 000 дальтон), 40% представлены высокомолекулярным альбумином (около 65 000 дальтон) и 40% составляют мукопротеины Тамм-Хорсфалла, секретируемые дистальными канальцами.
Механизмы развития протеинурии
В физиологических условиях барьеры для фильтрующихся белков находятся в клубочках, которые состоят из специфических капилляров, проницаемых для жидкости и низкомолекулярных растворенных веществ, но эффективно препятствующих фильтрации плазматических белков. Прилегающая базальная мембрана и эпителиальные клетки (подоциты) покрыты отрицательно заряженными гепарансульфат‑протеогликанами [5].
Количество белков, профильтровавшихся в канальцевую жидкость, обратно пропорционально молекулярной массе и величине отрицательного заряда молекул. Белки с молекулярной массой менее 20 000 дальтон легко проходят через стенку клубочковых капилляров [6]. Напротив, в физиологических условиях ограничена фильтрация альбумина, который имеет молекулярную массу 65 000 дальтон и отрицательный заряд. Белки с меньшей молекулярной массой реабсорбируются главным образом в проксимальных канальцах, и лишь в незначительном количестве выделяются с мочой.
Различают три патофизиологических механизма развития протеинурии: клубочковый, канальцевый и преренальный (протеинурия переполнения, которая возникает при избыточном содержании белка в плазме) (табл. 2) [7].
Таблица 2. Классификация протеинурии
| Тип | Патофизиологические характеристики | Причины |
| Клубочковая | Увеличение проницаемости клубочковых капилляров для белков | Первичная или вторичная гломерулопатия |
| Канальцевая | Уменьшение канальцевой реабсорбции белков из клубочкового фильтрата | Патология канальцев или интерстициальной ткани |
| Преренальная | Увеличенная продукция низкомолекулярных белков | Моноклональные гаммапатии, лейкозы |
| Адаптировано: AbueloJG. Proteinuria: Diagnostic principles and procedures. Ann Intern Med 1983; 98:186–91. | ||
Самая распространенная причина развития патологической протеинурии - поражение клубочков [8]. При патологии клубочкового аппарата увеличивается проницаемость клубочковой базальной мембраны, что приводит к потерям иммуноглобулинов и альбумина с мочой [7]. Нарушение функции клубочков сопровождается выделением большого количества белка. Экскреция белка с мочой в количестве, превышающем 2 г/сут, обычно служит признаком заболевания почек, которое протекает с поражением клубочкового аппарата (табл. 3) [9].
Таблица 3. Классификацияпричин развития протеинурии с учетом количества белка, выделяемого с мочой
| Суточная экскреция белка | Причина |
| 0,15 – 2,0 г | Гломерулопатия легкой степени |
| Канальцевая протеинурия | |
| Преренальная протеинурия | |
| 2,0 – 4,0 г | Как правило, гломерулопатия |
| > 4,0 г | Всегда гломерулопатия |
| Адаптировано: McConnellKR, Bia MJ. Evaluation of proteinuria: an approach for the internist. Resident Staff Phys 1994; 40:41–8. | |
Канальцевая протеинурия встречается при тубуло‑интерстициальной патологии, когда в проксимальных канальцах нарушена реабсорбция низкомолекулярных белков (составляющих часть физиологического клубочкового ультрафильтрата). При заболеваниях канальцев белок с мочой обычно выделяется в количестве менее 2 г/сут. Патология канальцев включает нефросклероз при гипертонической болезни, а также тубуло‑интерстициальную нефропатию, которая опосредована приемом нестероидных противовоспалительных средств.
У пациентов с преренальной протеинурией, сопровождающейся высокой концентрацией низкомолекулярных белков в плазме, подавлена способность проксимальных канальцев реабсорбировать профильтрованные белки. В большинстве случаев причина развития гиперпротеинемии — избыточная продукция моноклонального белка при множественной миеломе. Легкие цепи иммуноглобулинов (белки Бенс‑Джонса) при электрофорезе мочевых белков формируют моноклональный пик [10]. В табл. 4 [11] представлена классификация протеинурии, которая учитывает патофизиологические механизмы развития протеинурии.
Таблица 4. Классификация основныхпричин протеинурии, учитывающая механизмы развития этой патологии
Клубочковая протеинурия
|
Канальцевая протеинурия
Преренальная протеинурия
|
|
*ВИЧ – вирус иммунодецита человека, **НПВС – нестероидные противовопалительные средства Адаптировано:GlassrockRJ. Proteinuria. In: Massry SJ, Glassrock RJ, eds. Textbook of nephrology. 3d ed. Baltimore: William & Wilkins, 1995:602. |
|
Диагностика и количественная оценка протеинурии
В большинстве поликлиник и амбулаторий для полуколичественного определения белка в моче применяют диагностические полоски. Если моча не содержит белка, тестовая зона полоски сохраняет желтую окраску. Растворимые белки мочи взаимодействуют с красителем и буферными веществами, при этом тестовая зона окрашивается в зеленый цвет. При исследовании щелочной мочи (рН >7,5) ложноположительные результаты получают в следующих случаях: при погружении полоски в исследуемую мочу на длительное время; при анализе концентрированной мочи; при макрогематурии; при наличии в моче пенициллина, сульфаниламидов или толбутамида; при контаминации мочи гноем, спермой или влагалищным отделяемым. Ложноотрицательные результаты получают при анализе разбавленной мочи (относительная плотность менее 1,015) и в тех случаях, когда в состав белков мочи не входит альбумин, или когда белки мочи имеют небольшую молекулярную массу.
При уровне белка в моче ниже 100 мг/л реакция считается отрицательной. Если в моче определяются «следы» белка, концентрация белка варьирует от 100 до 200 мг/л. Затем результаты выражают в крестах от 1+ до 4+, в частности 1+ (300 мг/л), 2+ (1 000 мг/л), 3+ (3 000 мг/л), 4+ (10 000 мг/л). Эта реакция в большей мере чувствительна по отношению к альбумину и в меньшей мере — к глобулинам или глобулиновым фрагментам (тяжелым или легким цепям иммуноглобулинов, а также белкам Бенс‑Джонса) [12].
Диагностические полоски и качественные методы с использование сульфосалициловой кислоты позволяют лишь ориентировочно определить концентрацию белка в моче; результаты зависят от количества выделенной мочи. Поэтому между результатами, которые получают указанным методом, и точными количественными методами выявлена слабая корреляция [6].
У большинства пациентов с постоянной протеинурией определяют количество белка в суточной моче. Утром пациент опорожняет мочевой пузырь; эту пробу мочи для анализа не используют. Затем собирают все порции мочи, включая первую порцию мочи, которая выделяется на следующее утро (после сна). В собранной моче определяют содержание белка, а также креатинина, чтобы оценить правильность сбора образца. Количество выделяемого креатинина зависит от мышечной массы, и концентрация этого вещества остается постоянной в течение суток. У молодых мужчин и пациентов среднего возраста креатинин выделяется в количестве от 16 до 26 мг/кг/сут, у женщин эта величина составляет 12–24 мг/кг/сут. У истощенных пациентов и пожилых креатинин выделяется в меньшем количестве.
Наряду с исследованием суточной мочи иногда определяют отношение «белок/креатинин» в произвольно собранном образце мочи; пациент находится на обычном режиме [13,14]. Корреляция между отношением «белок/креатинин» и количеством белка в суточной моче установлена при нескольких заболеваниях, включая сахарный диабет, преэклампсию и ревматические заболевания [15–17]. Отношение «белок/креатинин» — более точный лабораторный показатель, чем количество белка в суточной моче [18]. К счастью, отношение «белок/креатинин» примерно соответствует числу грамм белка, выделяемого с мочой за сутки. Таким образом, отношение менее 0,2 соответствует 0,2 г белка/сут и считается нормальной величиной, отношение 3,5 соответствует 3,5 г белка/сут и рассматривается как признак протеинурии, степень которой соответствует протеинурии у пациентов с нефротическим синдромом (протеинурии тяжелой степени).
Диагностическая оценка протеинурии
Микроскопия мочевого осадка
Если при исследовании мочи диагностическим полосками находят протеинурию, проводят микроскопию мочевого осадка (рис. 1). В табл. 5 перечислены элементы организованного осадка, которые встречаются при тех или иных заболеваниях мочевых органов [6]. Дисморфные эритроциты, которые появляются при осмотических нарушениях в нефроне, — признак поражения клубочков. При макрогематурии, в отличие от микрогематурии, диагностические полоски дают положительную реакцию на белок.
Признаки инфекции, которые находят при микроскопии мочевого осадка, служат основанием для проведения антибиотикотерапии и последующего анализа мочи с помощью диагностических полосок. Если выявлены изменения мочи, характерные для основного заболевания почек, пациента направляют к нефрологу.
Транзиторная протеинурия
Если при микроскопии мочевого осадка получают сомнительные результаты, а содержание белка в моче варьирует от «следов» до 2+, в течение месяца не менее двух раз повторяют анализ утренней мочи. С этой целью используют диагностические полоски. Если степень протеинурии соответствует 3+ или 4+, для определения белка, выделяемого с мочой, используют количественный метод. Если при повторных исследованиях мочи диагностическими полосками белок не найден, не исключено, что протеинурия у пациента имеет преходящий характер. Это состояние не связано с увеличенной заболеваемостью или смертностью, поэтому нет необходимости проводить динамическое наблюдение.
Таблица 5. Интерпретация результатов микроскопии мочевого осадка
| Результаты микроскопии | Патологический процесс |
| Цилиндры из жировых капель, свободно лежащие жировые капли или овальные жировые тельца | Протеинурия, степень которой соответствует таковой при нефротическом синдроме (> 3,5 г/сут) |
| Лейкоциты, лейкоцитарные цилиндры с бактериями | Инфекции мочевых путей |
| Лейкоциты, лейкоцитарные цилиндры без бактерий | Заболевания почек с преимущественным поражением интерстиция |
| Эритроциты обычной формы | Вероятный признак заболевания нижних мочевых путей |
| Дисморфные эритроциты | Вероятный признак заболевания верхних мочевых путей |
| Эритроцитарные цилиндры | Патология клубочкового аппарата почек |
| Восковидные, зернистые или эпителиальные цилиндры | Далеко зашедшие хронические заболевания почек |
| Эозинофилы* | Вероятный признак индуцированного лекарствами острого интерстициального нефрита |
| Гиалиновые цилиндры | Не являются признаком заболевания почек. В моче находят при обезвоживании и терапии мочегонными препаратами |
|
*Выявляются при окраске по Райту Адаптировано: LarsonTS. Evaluationofproteinuria. MayoClinProc 1994; 69:1154–8. |
|
Постоянная протеинурия
Если установлен диагноз постоянной протеинурии, собирают подробный анамнез и проводят физикальное исследование, чтобы исключить системные заболевания, при которых почки вовлекаются в патологический процесс (табл. 4) [11]. Выясняют, принимал ли пациент лекарственные препараты.
В произвольно собранной пробе мочи определяют отношение «белок/креатинин». Если у пациента с установленным диагнозом (например, сахарный диабет или декомпенсированная сердечная недостаточность) клиренс креатинина находится в пределах нормы, лечат основное заболевание и тщательно контролируют протеинурию и функцию почек (клубочковую фильтрацию). Пациенту с умеренной или тяжелой протеинурией и сниженной клубочковой фильтрацией, или неясной причиной развития протеинурии, после консультации нефролога назначают дополнительные исследования. В табл. 6 перечислены основные исследования, которые проводят больному с выраженной протеинурией [19].
Примечание: клиренс креатининарассчитывают по формуле Cockcroft‑Gault:
(140 – возраст) x масса тела (кг)
Клиренс креатинина = –––––––––––––––––––––––––––––––––––––––––
Креатинин сыворотки (мг/дл) x 72
При исследовании клиренса креатинина у женщин полученный результат умножают на 0,85. При выраженном асците или ожирении для расчета используют идеальную массу тела [6].
Нефротический синдром
Нефротический синдром и протеинурия, степень которой соответствует таковой при нефротическом синдроме, — признаки патологии клубочкового аппарата почек. Диагностические критерии нефротического синдрома: тяжелая протеинурия или протеинурия, степень которой соответствует таковой при нефротическом синдроме, гипоальбуминемия, отеки, гиперлипидемия и липидурия. Патологический процесс представлен первичной или вторичной гломерулонефропатией, как указано в табл. 4 [11]. Распространенные вторичные причины — диабетическая нефропатия, амилоидоз и системная красная волчанка.
Таблица 6. Диагностические исследования при протеинурии
| Исследования | Интерпретация полученных результатов |
| Противоядерные антитела | Содержание увеличено при системной красной волчанке |
| Титр антистрептолизина О | Повышен после стрептококкового гломерулонефрита |
| Компоненты комплемента С3 и С4 | Уровень снижен при заболеваниях почек с преимущественным поражением клубочкового аппарата |
| Скорость оседания эритроцитов | Нормальные величины помогают исключить воспалительные и инфекционные заболевания |
| Уровень глюкозы в крови натощак | Повышен при сахарном диабете |
| Гемоглобин, гематокрит, или оба показателя | Уровень снижен у пациентов с хронической почечной недостаточностью, при которой нарушается гемопоэз |
| ВИЧ, реакция Вассермана, и иммунологические исследования при гепатитах | ВИЧ, гепатиты В и С, и сифилис ассоци-ированы с клубочковой протеинурией |
| Содержание альбумина и липидов в сыворотке | При нефротическом синдроме снижена концентрация альбумина и повышен уровень холестерина |
| Содержание электролитов в сыворотке (Na+, K+, Cl–, HCO3–, Ca++, PO4– –) | Определяют при обследовании пациентов с любыми осложнениями, которые являются следствием заболевания почек |
| Электрофорез белков сыворотки и мочи | Патологические результаты при множественной миеломе |
| Содержание мочевой кислоты в сыворотке | Повышенный уровень мочевой кислоты, как и наличие камней в мочевых органах, приводят к тубуло‑интерстициальным поражениям |
| Ультразвуковое исследование почек | Помогает выявить изменения почечной структуры |
| Рентгенография грудной клетки | Способствует диагностике системных заболеваний (например, саркоидоз) |
| Адаптировано: KrauseES. Proteinuria. In: BakerLR, BurtonJR, Zieve PD, eds. Principlesofambulatorymedicine. 5thed. Baltimore: William & Wilkins, 1999:546. | |
Ортостатическая протеинурия
У пациентов моложе 30 лет с протеинурией менее 2 г/сут и нормальным клиренсом креатинина исключают ортостатическую, или постуральную, протеинурию. Это доброкачественное состояние встречается у 3–5% лиц в подростковом и юношеском возрасте. У этих пациентов в положении стоя белок выделяется в увеличенном количестве, но в положении лежа количество белка в моче остается в нормальных пределах. Для того чтобы диагностировать ортостатическую протеинурию, проводят сравнительный анализ обеих проб. Утром пациент опорожняет мочевой пузырь; эту пробу мочи не исследуют. Мочу собирают днем, в течение 16 ч, при этом пациент находится на обычном режиме. Мочу заканчивают собирать вечером, перед сном. Вторую пробу мочи, за 8 ч, собирают утром.
В типичных случаях в первой пробе мочи содержание белка увеличено, тогда как в утренней моче, собранной после сна, концентрация белка не отличается от нормы. У пациентов с патологией клубочкового аппарата почек экскреция белка уменьшена в положении стоя, но не нормализуется (менее 50 мг за 8 ч) в положении лежа, как это отмечается при ортостатической протеинурии.
Ортостатическая протеинурия — доброкачественное состояние. По данным динамических наблюдений, почечная функция остается в нормальных пределах в течение 20–50 лет [20,21]. У этих пациентов ежегодно измеряют артериальное давление и проводят общий клинический анализ мочи.
Изолированная протеинурия
Диагноз изолированной протеинурии устанавливают в том случае, если у пациента с повышенной концентрацией белка в моче артериальное давление находится в пределах нормы, нет признаков системного заболевания, почечная функция не нарушена, и при микроскопическом исследовании мочевого осадка патологии не найдено. Обычно белок выделяется в количестве менее 2 г/сут. Риск развития почечной недостаточности у этих пациентов через 10 лет составляет 20%. Поэтому у этих пациентов каждые 6 мес измеряют артериальное давление, исследуют мочу и определяют клиренс креатинина [7]. Изолированная протеинурия, при которой белок выделяется в количестве более 2 г/сут, встречается редко и обычно является признаком гломерулонефрита [7]. Этим пациентам назначают дополнительные исследования, а также консультацию нефролога.
Заключение
Клиническое значение протеинурии варьирует в широких пределах. Системный подход к пациенту, у которого в моче увеличено содержание белка, позволяет клиницисту дифференцировать доброкачественные и патологические процессы, которые являются причиной развития протеинурии. Диагностический алгоритм, включающий определение отношения «белок/креатинин», способствует установлению точного и объективного диагноза. Пациентов с неустановленной причиной развития протеинурии после диагностического исследования направляют к нефрологу. Кроме того, протеинурия более 2 г/сут служит вероятным признаком патологии клубочков почек; таким пациентам требуется консультация нефролога.
Литература
- Pegg JF, Reinhardt RW, O'Brien JM. Proteinuria in adolescent sports physical examinations. J Fam Pract 1986;22:80-1.
- Woolhandler S, Pels RJ, Bor DH, Himmelstein DU, Lawrence RS. Dipstick urinalysis screening of asymptomatic adults for urinary tract disorders: I. hematuria and proteinuria. JAMA 1989;262:1214-9.
- Beetham R, Cattell WR. Proteinuria: pathophysiology, significance and recommendation for measurement in clinical practice. Ann Clin Biochem 1993;30(pt 5):425-34.
- Adams F. The genuine works of Hippocrates. Vol 2. London: Sydenham Society, 1849:766.
- Kanwar YS. Biophysiology of glomerular filtration and proteinuria. Lab Invest 1984;51:7-21.
- Larson TS. Evaluation of proteinuria. Mayo Clin Proc 1994;69:1154-8.
- Abuelo JG. Proteinuria: diagnostic principles and procedures. Ann Intern Med 1983;98:186-91.
- Stone RA. Office evaluation of the patient with proteinuria. Postgrad Med 1989;86(5):241-4.
- McConnell KR, Bia MJ. The evaluation of proteinuria: an approach for the internist. Res Staff Physician January 1994:41-8.
- Longo DL. Plasma cell disorders. In: Fauci AS, Braunwald E, Isselbacher KJ, et al, eds. Harrison's Principles of internal medicine. 14th ed. New York: McGraw-Hill, 1998:712-8.
- Glassrock RJ. Proteinuria. In: Massry SJ, Glassrock RJ, eds. Textbook of nephrology. 3d ed. Baltimore: Williams & Wilkins, 1995:602.
- Laffeyette RA, Perrone RD, Levey AS. Laboratory evaluation of renal function. In: Schrier RW, Gottschalk CW, eds. Diseases of the kidney. Boston, Mass: Little Brown, 1996:339.
- Ginsberg JM, Chang BS, Matarese RA, Garella S. Use of single voided urine samples to estimate quantitative proteinuria. N Engl J Med 1983;309:1543-6.
- Schwab SJ, Christensen RL, Dougherty K, Klahr S. Quantitation of proteinuria by the use of protein-to-creatinine ratios in single urine samples. Arch Intern Med 1987;147:943-4.
- Rodby RA, Rohde RD, Sharon Z, Pohl MA, Bain RP, Lewis EJ. The urine protein to creatinine ratio as a predictor of 24-hour protein excretion in type 1 diabetic patients with nephropathy: the Collaborative Study Group. Am J Kidney Dis 1995;26:904-9.
- Saudan PJ, Brown MA, Farrell T, Shaw L. Improved methods of assessing proteinuria in hypertensive pregnancy. Br J Obstet Gynaecol 1997;104:1159-64.
- Ralston SH, Caine N, Richards I, O'Reilly D, Sturrock RD, Capell HA. Screening for proteinuria in a rheumatology clinic: comparison of dipstick testing, 24-hour urine quantitative protein, and protein/creatinine ratios in random urine samples. Ann Rheum Dis 1988;47:759-63.
- Ruggenenti P, Gaspari F, Perna A, Remuzzi G. Cross sectional longitudinal study of spot morning urine protein:creatinine ratio, 24-hour urine protein excretion rate, glomerular filtration rate, and end stage renal failure in chronic renal disease in patients without diabetes. BMJ 1998;316:504-9.
- Krause ES. Proteinuria. In: Barker LR, Burton JR, Zieve PD, eds. Principles of ambulatory medicine. 5th ed. Baltimore: Williams & Wilkins, 1999:546.
- Springberg PD, Garrett LE Jr, Thompson AL Jr, Collins NF, Lordon RE, Robinson RR. Fixed and reproducible orthostatic proteinuria: results of a 20-year follow-up study. Ann Intern Med 1982;97:516-9.
- Rytand DA, Spreiter S. Prognosis in postural (orthostatic) proteinuria: forty to fifty-year follow-up of six patients after diagnosis by Thomas Addis. N Engl J Med 1981;305:618-21.
Протеинурия
Под термином протеинурия понимается увеличение содержания белка в моче.
В большинстве лабораторий при исследовании мочи «на белок» сначала пользуются качественными реакциями, которые не обнаруживают белок в моче здорового человека. Если же белок в моче обнаружен качественными реакциями, проводят количественное (или полуколичественное) его определение. При этом имеют значение особенности используемых методов, охватывающих различный спектр уропротеинов. Так, при определении белка с помощью 3% сульфосалициловой кислоты, нормальным считается количество белка до 0,03 г/л.
При определении минимальных количеств белка рекомендуется повторить анализ, в сомнительных случаях следует определять суточную потерю белка с мочой. В норме суточная моча содержит белок в незначительных количествах. В физиологических условиях профильтровавшийся белок практически полностью реабсорбируется эпителием проксимальных канальцев и содержание его в суточном количестве мочи колеблется по разным авторам от следов до 20 – 50, 80 – 100 мг и даже до 150 – 200 мг. Суточная экскреция белка в количестве 30 – 50 мг/сут является физиологической нормой для взрослого человека, выделение белка с мочой не должно превышать 60 мг/м2 поверхности тела в сутки, исключая первый месяц жизни, когда величина физиологической протеинурии может в четыре раза превышать указанные значения.
Общим условием появления белков в моче здорового человека являются достаточно высокая их концентрация в крови и молекулярная масса не более 100 – 200 кДа.
У практически здоровых людей под воздействием различных факторов может появляться преходящая протеинурия. Такую протеинурию называют также физиологической, функциональной или доброкачественной, так как она, в отличие от патологической, не требует лечения.
Физиологическая протеинурия
Преходящее выделение белка с мочой у здоровых людей может появляться после тяжелой физической нагрузки (длительные походы, марафонский бег, игровые виды спорта). Это так называемая рабочая (маршевая) протеинурия или протеинурия напряжения, наблюдавшаяся и описанная многими исследователями. Работы этих авторов, иллюстрирующие возможность развития протеинурии под влиянием физической нагрузки, свидетельствуют о высокой степени ее выраженности, а также ее обратимости. Генез такой протеинурии объясняют гемолизом с гемоглобинурией и стрессовой секрецией катехоламинов с преходящим нарушением гломерулярного кровотока. При этом протеинурия выявляется в первой после физической нагрузки порции мочи.
Значение фактора охлаждения в генезе скоропреходящей протеинурии было отмечено у здоровых людей под влиянием холодных ванн.
Известна albuminuriasolaris, возникающая при выраженной реакции кожи на инсоляцию, а также при раздражении кожи некоторыми веществами, например, при смазывании ее йодом.
Установлена возможность появления протеинурии при повышении уровня адреналина и норадреналина в крови, чем объясняют выделение белка с мочой при феохромоцитоме и гипертонических кризах.
Выделяют алиментарную протеинурию, появляющуюся иногда после употребления обильной белковой пищи.
Доказана возможность появления центрогенной протеинурии – при эпилепсии, сотрясении мозга.
Описана эмоциональная протеинурия во время экзаменов.
К протеинурии функционального происхождения относят и описываемое некоторыми авторами выделение белка с мочой при энергичной и продолжительной пальпации живота и области почек (пальпаторная протеинурия).
Лихорадочная протеинурия наблюдается при острых лихорадочных состояниях, чаще у детей и стариков. Механизм ее малоизучен. Этот вид протеинурии сохраняется в период повышения температуры тела и исчезает при ее снижении и нормализации. Если протеинурия сохраняется в течение многих дней и недель после нормализации температуры тела, то следует исключить возможное органическое заболевание почек - либо вновь возникшее, либо уже существующее.
При заболеваниях сердца часто выявляют застойную, или сердечную протеинурию. С исчезновением сердечной недостаточности она обычно исчезает.
У новорожденных в первые недели жизни также наблюдается физиологическая протеинурия.
Ортостатическая (постуральная, лордотическая) протеинурия наблюдается у 12 – 40% детей и подростков, характеризуется выявлением белка в моче при длительном стоянии или ходьбе с быстрым исчезновением (преходящий вариант ортостатической протеинурии) или уменьшением его (персистирующий вариант) в горизонтальном положении. Генез ее связывают с нарушениями почечной гемодинамики, развивающимися за счет лордоза, сдавливающего нижнюю полую вену в положении стоя, или выброса ренина (ангиотензина II) в ответ на изменения объема циркулирующей плазмы при ортостатизме.
Физиологическая протеинурия, как правило, незначительная – не более 1,0 г/сут.
Современные методы исследования позволяют выявить ряд изменений в микроструктуре почек, следствием которых и является так называемая физиологическая протеинурия. Исходя из таких соображений, многие авторы сомневаются в правомочности выделения «функциональной» протеинурии.
Патологическая протеинурия
Патологическая протеинурия бывает почечного и внепочечного происхождения.
Почечная протеинурия
Почечная протеинурия является одним из наиболее важных и постоянных признаков заболеваний почек и может быть гломерулярной, или клубочковой, и тубулярной, или канальцевой. При сочетании этих двух типов развивается смешанный тип протеинурии.
Клубочковая протеинурия
Клубочковая протеинурия обусловлена повреждением гломерулярного фильтра, возникает при гломерулонефритах и при нефропатиях, связанных с обменными или сосудистыми заболеваниями. При этом из крови в мочу в большом количестве фильтруются плазматические белки.
В основе нарушения работы клубочкового фильтра лежат различные патогенетические механизмы:
- токсические или воспалительные изменения гломерулярной базальной мембраны (отложение иммунных комплексов, фибрина, клеточная инфильтрация), вызывающие структурную дезорганизацию фильтра;
- изменения гломерулярного кровотока (вазоактивные агенты – ренин, ангиотензин II, катехоламины), влияющие на гломерулярноетранскапиллярное давление, процессы конвекции и диффузии;
- недостаток (дефицит) специфических гломерулярных гликопротеидов и протеогликанов, ведущий к потере фильтром отрицательного заряда.
Клубочковая протеинурия наблюдается при остром и хроническом гломерулонефрите, амилоидозе, диабетическом гломерулосклерозе, тромбозе почечных вен, застойной почке, гипертонической болезни, нефросклерозе.
Клубочковая протеинурия может быть селективной и неселективной в зависимости от тяжести повреждения гломерулярного фильтра.
Селективная протеинурия встречается при минимальном (нередко обратимом) повреждении гломерулярного фильтра (нефротический синдром с минимальными изменениями), представлена белками с молекулярной массой не выше 68000 – альбумином и трансферрином.
Неселективная протеинурия чаще встречается при более тяжелом повреждении фильтра, отличается повышением клиренса средне- и высокомолекулярных плазматических белков (в составе белков мочи присутствуют также альфа2-глобулины и гамма-глобулины). Неселективная протеинурия наблюдается при нефротической и смешанной формах гломерулонефрита, вторичном гломерулонефрите.
Канальцевая протеинурия (тубулярная протеинурия)
Канальцевая протеинурия связана либо с неспособностью канальцев реабсорбировать белки, прошедшие через неизмененный гломерулярный фильтр, либо обусловлена выделением белка эпителием самих канальцев.
Канальцевая протеинурия наблюдается при остром и хроническом пиелонефрите, отравлении тяжелыми металлами, остром канальцевом некрозе, интерстициальном нефрите, хроническом отторжении почечного трансплантата, калийпенической нефропатии, генетическихтубулопатиях.
Внепочечная протеинурия
Внепочечная протеинурия возникает при отсутствии патологического процесса в самих почках и делится на преренальную и постренальную.
Преренальная протеинурия развивается при наличии необычно высокой плазматической концентрации низкомолекулярного белка, который фильтруется нормальными клубочками в количестве, превышающем физиологическую способность канальцев к реабсорбции. Подобный тип протеинурии наблюдается при миеломной болезни (в крови появляется низкомолекулярный белок Бенс-Джонса и другие парапротеины), при выраженном гемолизе (за счет гемоглобина), рабдомиолизе, миопатии (за счет миоглобина), моноцитарном лейкозе (за счет лизоцима).
Постренальная протеинурия обусловлена выделением с мочой слизи и белкового экссудата при воспалении мочевых путей или кровотечением. Заболевания, которые могут сопровождаться внепочечной протеинурией - мочекаменная болезнь, туберкулез почки, опухоли почки или мочевых путей, циститы, пиелиты, простатиты, уретриты, вульвовагиниты. Постренальная протеинурия чаще весьма незначительна и практически менее важна.
Степень выраженности протеинурии
В зависимости от степени выраженности выделяют легкую, умеренную и тяжелую протеинурию.
Легкая протеинурия (от 300 мг до 1 г/сут) может наблюдаться при острой инфекции мочевыводящих путей, обструктивнойуропатии и пузырно-мочеточниковом рефлюксе, тубулопатиях, мочекаменной болезни, хроническом интерстициальном нефрите, опухоли почки, поликистозе.
Умеренная протеинурия (от 1 до 3 г/сут) отмечается при остром канальцевом некрозе, гепаторенальном синдроме, первичном и вторичном гломерулонефрите (без нефротического синдрома), протеинурической стадии амилоидоза.
Под тяжелой, или выраженной протеинурией понимают потерю белка с мочой, превышающую 3,0 г в сутки или 0,1 г и более на килограмм массы тела за 24 часа. Такая протеинурия почти всегда связана с нарушением функции клубочкового фильтрационного барьера в отношении размера или заряда белков и наблюдается при нефротическом синдроме.
Выявление и количественная оценка протеинурии важны как для диагностики, так и для оценки течения патологического процесса, эффективности проводимого лечения. Диагностическая значимость протеинурии оценивается в совокупности с другими изменениями в моче.
Врач лабораторной диагностики ЦДЛ
Новополоцкой городской больницы
Костюк К.С.
Протеинурия: причины, симптомы и лечение
Расскажите об этой статье в социальных сетях
Почки поддерживают ваше здоровье, фильтруя кровь. У них есть маленькие кровеносные сосуды. Эти структуры удаляют отходы, которые попадают в мочу, и реабсорбируют белок, который остается в крови.
Но если ваши почки не функционируют должным образом, белок может проникнуть в мочу. Результатом является высокий уровень белка в моче, известный как протеинурия.
Существуют различные виды протеинурии, в том числе:
- клубочковая протеинурия;
- тубулярная протеинурия;
- перегрузочная протеинурия;
- почечная протеинурия.
Кроме того, альбуминурия представляет собой тип протеинурии, где избыток белка альбумин. Это связано с клубочковой протеинурией.
Протеинурия может быть связана с временными условиями, такими как обезвоживание или более серьезное повреждение почек. Давайте рассмотрим возможные причины протеинурии, а также ее симптомы и лечение.
Что вызывает высокое содержание белка в моче?
Если у вас протеинурия, обратите внимание на другие симптомы. Это поможет врачу определить причину.
Дегидратация
Обезвоживание происходит, когда ваше тело теряет слишком много жидкости. Это частая, временная причина протеинурии.
Тело использует воду для доставки питательных веществ, таких как белок, в почки. Но без достаточного количества жидкости это будет трудно сделать.
В свою очередь, почки не могут правильно восстановить белки. Вместо этого белок попадает в мочу.
Другие симптомы зависят от степени дегидратации. Вы можете испытать:
- усталость;
- головные боли;
- головокружение;
- усиление жажды;
- моча темного цвета;
- снижение мочеиспускания;
- сухость во рту или на коже.
Обезвоживание может быть вызвано:
- понос;
- рвота;
- чрезмерное потоотделение;
- лихорадка;
- не пьете достаточно воды.
Высокое кровяное давление
Важно! Гипертония может ослабить кровеносные сосуды в почках. Это уменьшает их способность реабсорбировать белок, который поступает в мочу.
Поскольку высокое кровяное давление развивается медленно, симптомы могут не проявляться годами. Но если это становится серьезным, это может вызвать:
- головные боли;
- сбивчивое дыхание.
У большинства случаев высокого кровяного давления нет основной причины. Но у некоторых людей высокое кровяное давление обусловлено:
- заболевание почек;
- проблемы с щитовидной железой;
- обструктивное апноэ во сне;
- опухоли надпочечников;
- некоторые лекарства, такие как противозачаточные средства или противоотечные.
Сахарный диабет
Сахарный диабет — это нарушение обмена веществ, вызывающее высокий уровень сахара в крови. Существует несколько типов диабета, включая диабет 1 и 2 типа.
При диабете высокий уровень сахара в крови заставляет почки чрезмерно фильтровать кровь. Это может вызвать повреждение почек, позволяя белку проникать в мочу.
Симптомы диабета зависят от тяжести и типа. У вас может быть:
- усиление жажды и голода;
- частое мочеиспускание;
- усталость;
- нечеткое зрение;
- необъяснимая потеря веса.
Гломерулонефрит
Важно! Протеинурия может указывать на гломерулонефрит или воспаление клубочков.
Обычно, когда клубочки фильтруют кровь, они реабсорбируют белок. Но если они травмированы, белок может пройти и проникнуть в мочу.
Гломерулонефрит может вызвать ряд симптомов, называемых нефротическим синдромом. Помимо протеинурии это включает в себя:
- гиперлипидемия или высокий уровень жиров и холестерина в крови;
- опухшие ноги, ступни или лодыжки;
- гипоальбуминемия или низкий уровень белка в крови.
Это может также вызвать высокое кровяное давление и гематурию или эритроциты в моче. Это заставляет мочу выглядеть розовой.
Как правило, гломерулонефрит возникает, когда иммунная система атакует почки. Это может быть связано с:
- бактериальный эндокардит;
- ВИЧ;
- гепатит Б;
- гепатит С;
- волчанка;
- диабетическая нефропатия;
- высокое кровяное давление.

Хроническая болезнь почек
Хроническая болезнь почек (ХБП) — это прогрессирующая потеря функции почек. Это может вызвать протеинурию на ранних стадиях, но обычно она не вызывает каких-либо заметных симптомов.
По мере развития ХБП у вас могут возникнуть:
- сбивчивое дыхание;
- частое мочеиспускание;
- икота;
- усталость;
- тошнота;
- рвота;
- проблемы со сном;
- сухая, зудящая кожа;
- опухшие руки и ноги;
- плохой аппетит.
Следующие заболевания могут повредить почки и привести к ХБП:
- гломерулонефрит;
- диабет;
- высокое кровяное давление;
- болезнь сердца;
- интерстициальный нефрит;
- поликистоз почек;
- рецидивирующая почечная инфекция.
Важно! Если ХБП прогрессирует, это может привести к почечной недостаточности.
Аутоиммунные заболевания
Иммунная система обычно вырабатывает антитела и иммуноглобулины, которые борются с чужеродными организмами. Но если у вас аутоиммунное заболевание, иммунная система вырабатывает антитела и иммуноглобулины, которые атакуют ткани организма. Эти вещества называются аутоантителами.
Если аутоантитела повреждают клубочки, может возникнуть воспаление. Это приводит к повреждению почек и, в конечном итоге, протеинурии.
Следующие аутоиммунные заболевания связаны с протеинурией:
- Системная красная волчанка. Хотя системная красная волчанка (СКВ) в основном затрагивает кожу и суставы, она также может поражать почки.
- Синдром Гудпасчера. При синдроме Гудпасчера аутоантитела специфически атакуют почки и легкие.
- IgA нефропатия. IgA нефропатия возникает, когда отложения иммуноглобулина A накапливаются в клубочках.
Преэклампсия
При преэклампсии у беременной развивается высокое кровяное давление на или после 20 недель беременности. Это временно ухудшает способность почек фильтровать белок, который вызывает протеинурию.
Другие симптомы преэклампсии включают в себя:
- опухшие руки и лицо;
- головные боли;
- нечеткое зрение;
- боль в животе на правой стороне;
- увеличение веса.
Хотя преэклампсия обычно проходит после родов, это серьезное заболевание, которое может привести к преждевременным родам. Беременные люди с преэклампсией должны быть тщательно проверены.
Рак
В тяжелых случаях протеинурия вызвана раком. Несколько типов рака связаны с высоким уровнем белка в моче, в том числе:
- карцинома почек;
- рак легких;
- рак молочной железы;
- колоректальный рак;
- неходжкинские лимфомы;
- лимфома Ходжкина;
- множественная миелома.
Важно! Воспалительный эффект рака изменяет функцию почек.
В некоторых случаях, таких как множественная миелома, повреждение почек происходит, когда аномальные белки в крови связываются с нормальными белками в моче. Когда функция почек снижается, больше белка попадает в мочу.
Хотя симптомы рака сильно различаются, общие симптомы включают в себя:
- необъяснимая потеря веса;
- усталость;
- лихорадка;
- боль;
- изменения кожи.
Факторы риска протеинурии
Некоторые люди более склонны к развитию протеинурии. Общие факторы риска включают в себя:
- Возраст. Взрослые 65 лет и старше более подвержены обезвоживанию и проблемам с почками. Беременные люди старше 40 лет имеют больший риск преэклампсии.
- Высокое кровяное давление. Люди с высоким кровяным давлением имеют более высокий риск развития диабета и заболеваний почек.
- Диабет. Диабет является наиболее распространенной причиной ХБП. Это также связано с преэклампсией и гломерулонефритом.
- История семьи. У вас больше шансов на развитие протеинурии, если у вас в анамнезе есть заболевание почек или преэклампсия.
- Определенные национальности. Люди афроамериканского, латиноамериканского, индейского и азиатского происхождения имеют больший риск возникновения проблем с почками.
- Избыточный вес или ожирение. Высокое кровяное давление, диабет и преэклампсия связаны с избыточным весом или ожирением.

Симптомы
Важно! На ранних стадиях повреждения почек у вас не будет никаких симптомов. Это потому, что в вашей моче только небольшое количество белка.
Но по мере прогрессирования поражения почек в вашу мочу будет поступать больше белка. Это может вызвать такие симптомы, как:
- пенистая моча;
- опухшие руки, ноги, лицо или живот;
- частое мочеиспускание;
- мышечные спазмы ночью;
- тошнота;
- рвота;
- плохой аппетит.

Тестирование на белок в моче
Важно! Единственный способ диагностировать протеинурию — это анализ мочи, который измеряет количество белка в моче.
Во время процедуры вы мочитесь в баночку для образцов. Врач помещает в пробу мочи маленькую пластиковую палочку, покрытую химикатами. Если в нем слишком много белка, палочка изменит цвет.
Остальная часть мочи будет отправлена в лабораторию, где она будет исследована под микроскопом.
Если врач считает, что у вас проблемы с почками, он будет повторять анализ мочи три раза в течение трех месяцев. Это помогает им исключить временные причины протеинурии.
Доктор может также использовать следующие тесты, чтобы определить, что вызывает протеинурию:
- 24-часовой сбор мочи. При 24-часовом анализе мочи ваша моча собирается в течение 24 часов и отправляется в лабораторию.
- Анализ крови на скорость клубочкового фильтрата. Этот тест проверяет функцию почек.
- Визуальные тесты. Вы можете пройти УЗИ или КТ, которые делают подробные фотографии ваших почек и мочевыводящих путей.
- Биопсия почки. Образец вашей почки исследуется на наличие признаков повреждения почек.
Лечение
Если у вас временная или легкая протеинурия, вам скорее всего не понадобится лечение. Но если у вас постоянная протеинурия, вам нужно лечить основное состояние.
Лечение может включать в себя:
- Диетические изменения. Если у вас есть заболевание почек, диабет или высокое кровяное давление, врач порекомендует конкретные изменения в диете.
- Потеря веса. Потеря веса может справиться с ситуацией, которые нарушают функцию почек.
- Лекарство от кровяного давления. Если у вас гипертония или диабет, врач может назначить вам лекарство, чтобы снизить артериальное давление.
- Диабет лекарства. Вам может потребоваться медикаментозное лечение или инсулинотерапия для контроля высокого уровня глюкозы в крови.
- Диализ. При гломерулонефрите и почечной недостаточности диализ используется для контроля высокого кровяного давления и жидкостей.
Важно! Протеинурия часто означает, что ваши почки неправильно фильтруют кровь. Поэтому целью лечения является лечение основного заболевания. Врач может составить план лечения, чтобы защитить ваши почки.
Персональный сайт - Протеинурии
Протеинурия - это появление белка в моче.
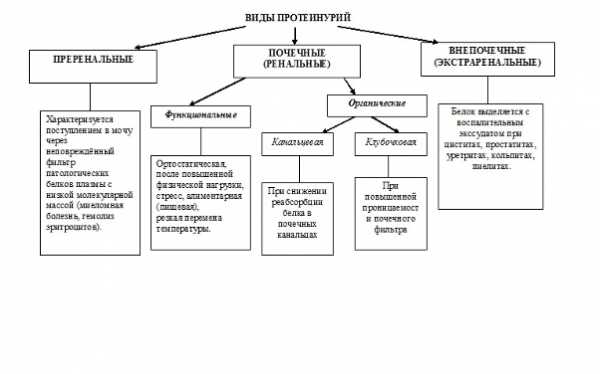
Протеинурии возникают при фильтрации белка из крови в почке или присоединении белка к моче в мочевыводящих путях. В зависимости от причины, вызвавшей протеинурию, различают преренальную, ренальную (почечную) – (функциональная и органическая (клубочковая и канальцевая) и экстраренальную (постренальную/внепоченую) протеинурию.
В физиологических условиях прохождение белков через клубочковый фильтр определяется размером пор базальной мембраны, молекулярной массы белка, формой и электрическим зарядом его молекул, зависимостью между концентрацией белка в плазме и фильтрате.
Фильтрация носит избирательный (селективный) характер. В проксимальном отделе почечного канальца с помощью ферментных систем эпителиальных клеток осуществляется реабсорбция большей части белков. Активность ферментных систем определяет функциональные возможности почечного эпителия (предел реабсорбции эпителием проксимальных канальцев почек). Превышение концентрации белка, которое может быть реабсорбировано, сопровождается появлением его в окончательной моче.
Усиление протеинурии зависит от:
§ Поражения базальной мембраны и подоцитов
§ Недостаточности канальцевой реабсорбции
§ Фильтрации патологических белков (парапротеинов) с низкой молекулярной массой, которые из-за большого количества их или связи с их качественными особенностями полностью не реабсорбируются
§ Повышенной секреции белков (слизь) эпителием почек, мочевыводящих путей, вспомогательных желёз.
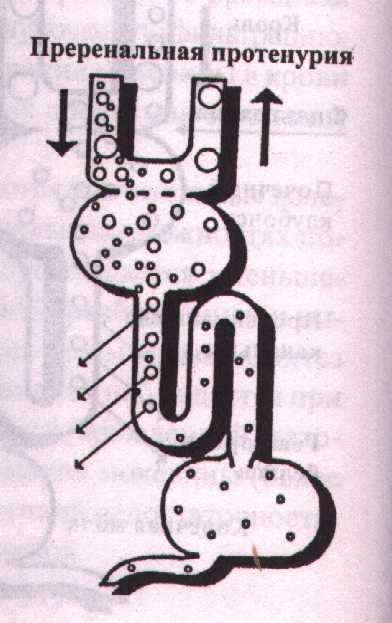
Преренальная протеинурия характеризуется поступлением в мочу через неповреждённый почечный фильтр патологических белков плазмы с низкой молекулярной массой. Наблюдается преренальная протеинурия при гаммапатиях вследствие повышенного синтеза лёгких цепей иммуноглобулинов, гемолитических анемий с внутрисосудистым гемолизом эритроцитов, а также при некротическом, травматическом, токсическом и др. повреждениях мышц, сопровождающихся миоглобинемией и миоглобинурией, при миеломной болезни. Эти состояния лишь при небольших концентрациях вызывают поражение почечного нефрона. Высокие концентрации или/и длительный патологический процесс рано или поздно приводит к нарушению почечного фильтра и развитию острой почечной недостаточности.
Ренальная протеинурия
-
Функциональные (физиологические) (ортостатическая, алиментарная, переохлаждение, после физической нагрузки)
- Органические, обусловленные поражением почечного нефрона (клубочковая и канальцевая)
Клубочковая (гломерулярная) протеинурия развиватеся вследствие повреждения клубочкового фильтра, в результате нарушается фильтрация и диффузия в клубочках. Клубочковая протеинурия наблюдается при всех заболеваниях почек, протекающих с поражение клубочков (острый и хронический гломерулонефрит, сахарный диабет, опухоль почки, токсикоз беременных, нефрозы, подагра, киста почек, хронический дефицит калия, коллагенозы, гипертоническая болезнь и др.).
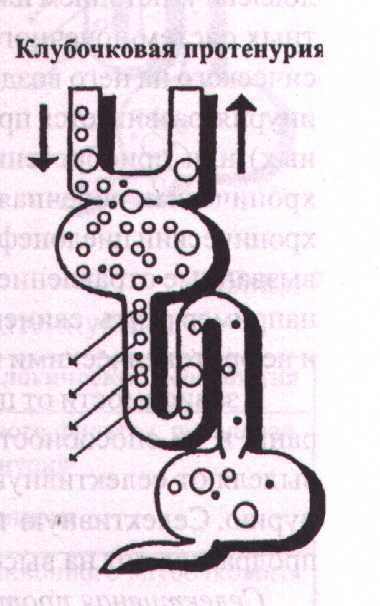
Канальцевая (тубулярная) протеинурия обусловлена угнетением или недостаточностью ферментативных систем почечного эпителия в результате токсического на него воздействия. Канальцевая протеинурия развивается при наследственных (врождённых) или приобретённых тубулопатиях (острая и хроническая почечная недостаточность, острый и хронический пиелонефрит, тубулярные нефропатии, вызванные отравлением тяжёлыми металлами, как например ртуть, свинец, токсические веществами и нефротоксическими препаратами).
В зависимости от целостности базальной мембраны и её способности пропускать в мочу белок выделяют селективную и неселективную протеинурию. Селективная протеинурия в свою очередь продразделяется на высоко-, умеренно и низкоселективную.
Селективная протеинурия характеризуется избирательной способностью базальной мембраны, при которой фильтруется белок низкой молекулярной массой (альбумины, трансферрин).
Низкоселективная протеинурия в мочу переходят не только низкомолекулярные , но и высокомолекулярные белки. Поэтому в моче обнаруживаются все протеины плазмы. Низкоселективная протеинурия наблюдается при выраженных поражениях клубочков (хронические нефриты в стадии обострения).
Микроальбуминурия – выделение с мочой белка. Отмечается при нарушении фильтрации альбумина в клубочках и является критерием ранней нефропатии при диабете.
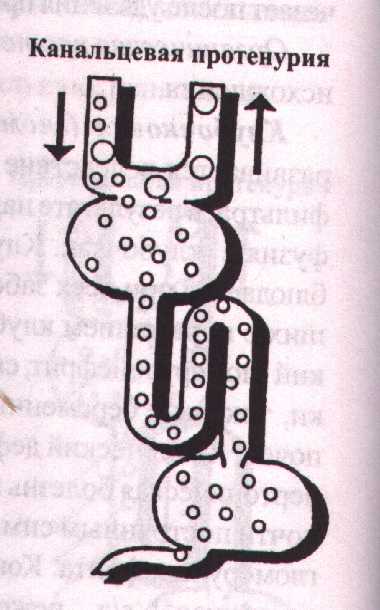
Постренальная (внепочечная) протеинурия возникает при поражении мочевыводящих путей и половых органов.
Белок выделяется с воспалительным экссудатом при циститах, простатитах, простатитах, уретритах, кольпитах, пиелитах.
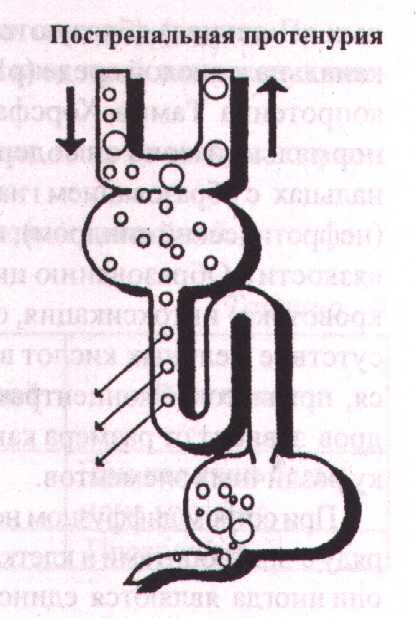
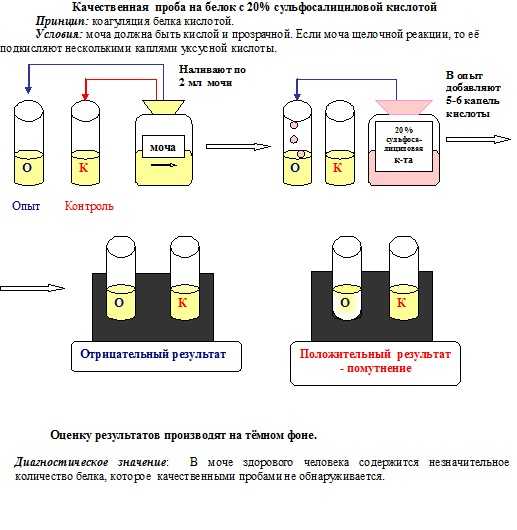
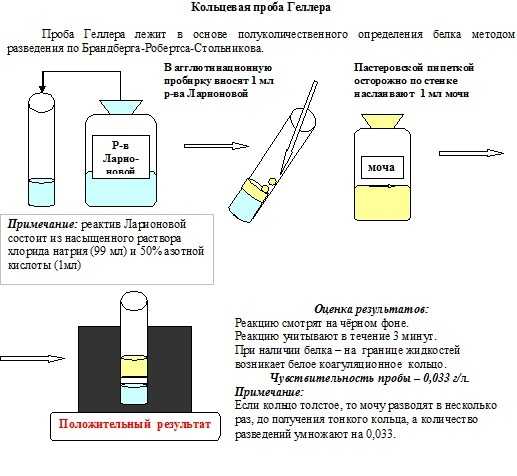
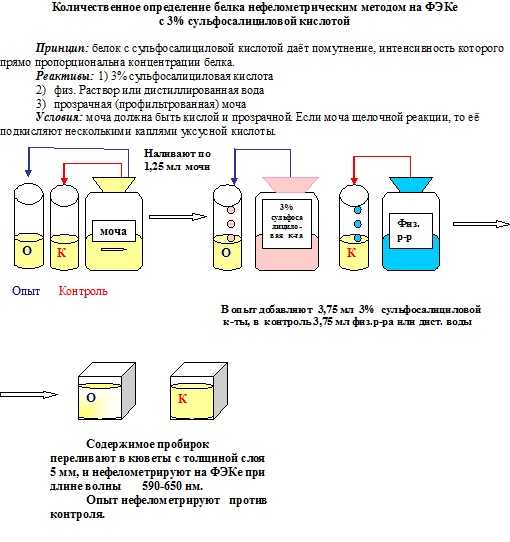
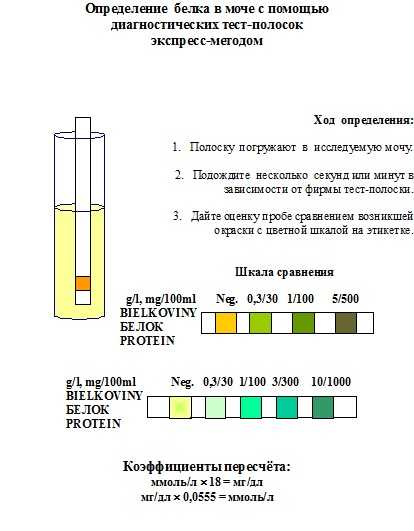
Практическая часть "Качественные и количественные пробы на определение белка в моче"
http://narod.ru/disk/25662185000/%D0%98%D0%A1%D0%A1%D0%9B%D0%95%D0%94%D0%9E%D0%92%D0%90%D0%9D%D0%98%D0%95%20%D0%A5%D0%98%D0%9C%D0%98%D0%A7%D0%95%D0%A1%D0%9A%D0%9E%D0%93%D0%9E%20%D0%A1%D0%9E%D0%A1%D0%A2%D0%90%D0%92%D0%90%20%D0%91%D0%95%D0%9B.doc.html
Определение белка в моче с помощью тест-полосок
http://narod.ru/disk/25662190000/%D0%9E%D0%BF%D1%80%D0%B5%D0%B4%D0%B5%D0%BB%D0%B5%D0%BD%D0%B8%D0%B5%20%20%D0%B1%D0%B5%D0%BB%D0%BA%D0%B0%20%D0%B2%20%D0%BC%D0%BE%D1%87%D0%B5%20%D1%81%20%D0%BF%D0%BE%D0%BC%D0%BE%D1%89%D1%8C%D1%8E.doc.html
Протеинурия и нефротический синдром » Медвестник
Л.Ю. МИЛОВАНОВА, кандидат медицинских наук, старший научный сотрудник отдела нефрологии Научно-исследовательского центра ММА им. И.М. Сеченова
Л.В.ЛЫСЕНКО, доктор медицинских наук, профессор кафедры терапии и профболезней ММА им. И.М. Сеченова
Экскреция белка с мочой, превышающая нормальные значения (30—50 мг/сут), называется протеинурией и, как правило, является признаком поражения почек. Различают несколько видов протеинурии. Клубочковая протеинурия развивается из-за повышения проницаемости клубочкового фильтра для белков. Канальцевая протеинурия — результат поражения проксимальных канальцев, в которых в норме реабсорбируются низкомолекулярные белки, прошедшие через клубочковый фильтр. Характерным признаком тубулярной протеинурии служит преобладание ?2-микроглобулинемии над альбумином и отсутствие высокомолекулярных белков. Гиперпротеинемическая протеинурия есть протеинурия «переполнения», возникает из-за избытка какого-либо белка в крови, свободно проходящего через малоизмененный клубочковый фильтр – легкие цепи иммуноглобулинов, лизоцим, ?2-микроглобулин, ретинолсвязывающий белок, гемоглобин, миоглобин в количестве, превышающем способность канальцев к его реабсорбции.
Канальцевая протеинурия почти никогда не превышает 2 г/сут и не приводит к нефротическому синдрому, также как и гиперпротеинемическая протеинурия.
К функциональным протеинуриям, точные механизмы развития которых недостаточно установлены, относят ортостатическую протеинурию, протеинурию напряжения, лихорадочную протеинурию.
Микроальбуминурия — экскреция с мочой альбумина, не превышающая 300 мг/сут. Микроальбуминурию рассматривают в качестве маркера генерализованной дисфункции эндотелия, что свидетельствует о значительном ухудшении не только почечного прогноза, но и повышении риска сердечно-сосудистых осложнений, в том числе и у лиц, не страдающих нарушениями углеводного обмена. В клинической практике для определения белка в моче применяют пробы с добавлением сульфасалициловой или трихлоруксусной кислоты с последующей нифелометрией или рефрактометрией, а также с помощью более точного биуретового метода. В последние годы широко используется метод исследования белка в моче с помощью тест-полосок. Более тонкими методами белковой химии (иммуноэлектрофорез, лазерная нефелометрия, иммуноблотинг, иммунофиксация и др.) в моче могут быть выявлены различные белковые фракции — низкомолекулярные (?2-микроглобулины, легкие цепи иммуноглобулинов и т. д.) и высокомолекулярные (?2-макроглобулин, ?-глобулин).
Нефротический синдром — одно из наиболее характерных и серьезных проявлений острых и особенно хронических заболеваний почек. Шесть главных причин, на долю которых приходится более 90% всех случаев нефротического синдрома, — это гломерулонефриты (болезнь минимальных изменений, фокально-сегментарный гломерулосклероз, мембранозная нефропатия, мезангиокапиллярный гломерулонефрит), диабетический гломерулосклероз и амилоидоз. В основе большой протеинурии, ведущей к нефротическому синдрому, может быть только клубочковая протеинурия, когда при любом поражении клубочкового фильтра базальная мембрана или фильтрационные щели между ножками подоцитов структурно повреждаются и/или теряют отрицательный заряд.
Компоненты нефротического синдрома:
1. Обязательные
» «большая» протеинурия (более 3 г/сут у взрослых, более 50 мг/кг/сут у детей)гипоальбуминемия (менее 30 г/л)отеки
2. Факультативные
» гиперхолестеринемия, дислипопротеинемияактивация факторов коагуляции (гиперфибриногенемия)нарушение фосфорно-кальциевого обмена, гипокальциурия, остеопороз)иммунодепрессия (в том числе снижение иммуноглобулина IgG, фагоцитарной функции моноцитов и нейтрофилов).
Атериальную гипертензию, гематурию не относят к проявлениям нефротического синдрома.
Гипоальбуминемия — прямое следствие протеинурии; уровень альбумина тем ниже, чем больше его экскреция с мочой. Другие причины гипоальбуминемии — распад реабсорбированного альбумина в проксимальных канальцах и недостаточное повышение синтеза альбумина в печени.
Причины образования отеков при нефротическом синдроме не совсем ясны. Наиболее распространенная гиповолемическая гипотеза. При гипоальбуминемии снижается онкотическое давление плазмы, что приводит к выходу воды из сосудов в интерстиций. В ответ на уменьшение объема циркулирующей крови (ОЦК) активируется ренин-ангиотензиновая система, повышается симпатический тонус, увеличивается секреция антидиуретического гормона гипофиза, в то же время секреция предсердного натрийуретического гормона снижается. Все это приводит к задержке натрия и воды, которая продолжает перемещаться в интерстициальное тканевое пространство. Однако не совсем понятно, почему развиваются отеки и у тех больных, у которых ОЦК не снижен, а даже повышен и ренин-ангиотензиновая система подавлена? По-видимому, в таких случаях образование отеков обусловлено первичнопочечной ретенцией соли и воды.
Гиперлипидемия, как полагают, развивается из-за того, что печень усиливает выработку липопротеидов в ответ на снижение онкотического давления плазмы, а также из-за потери с мочой белков, регулирующих обмен липопротеидов. При этом уровень общего холестерина и липопротеидов низкой плотности (ЛПНП) повышен у большинства больных, а липопротеидов очень низкой плотности и триглицеридов — в наиболее тяжелых случаях. Гиперлипопротеинемия у больных с нефротическим синдромом способствует развитию атеросклероза и прогрессированию хронической почечной недостаточности.
Повышение свертываемости крови при нефротическом синдроме имеет несколько причин: потеря с мочой антитромбина III, протеинов C и S, усиленный синтез фибриногена в печени, ослабление фибринолиза и повышение агрегации тромбоцитов. Клинически эти нарушения проявляются тромбозами периферических сосудов и почечных вен, тромбоэмболией легочной артерии. Симптомы острого тромбоза почечных вен: внезапная боль в пояснице и животе, микрогематурия, у мужчин левостроннее варикоцеле (вена левого яичка впадает в полую вену), резкое нарастание протеинурии и падение скорости клубочковой фильтрации (СКФ). Хронический тромбоз почечных вен обычно протекает бессимптомно. Тромбоз почечных вен особенно часто (до 40% случаев) развивается у больных с нефротическим синдромом при мембранозной нефропатии, мезангиокапиллярном гломерулонефрите и амилоидозе.
Микроцитарная гипохромная анемия развиваются из-за потери трансферрина. Наблюдается белковая недостаточность — потеря сывороточных белков, переносящих витамин D, ведет к авитаминозу D с гипокальциемией и вторичным гиперпаратиреозом, потеря транстиретина — к снижению уровня Т4, Ig — к снижению сопротивляемости инфекциям. Может непредсказуемо меняться и фармакокинетика препаратов, которые связываются с белками плазмы.
Классификация
I. Первичный нефротический синдром
1. Первичный (брайтов) гломерулонефрит (в скобках указана частота среди причин первичного нефротического синдрома у взрослых)
» нефропатия минимальных изменений (до 15%)фокально-сегментарный гломерулосклероз (20—25%)мембранозная нефропатия (25—30%)мезангиокапиллярный гломерулонефрит (5%)другие формы гломерулонефрита (в том числе фибриллярная, коллабирующая и иммунотактоидная гломерулопатии) (15—30%).
II. Вторичный нефротический синдром
1. При системных заболеваниях:
» сахарный диабетамилоидозсистемная красная волчанкагеморрагический васкулитпарапротеинемии (множественная миелома, болезнь легких цепей)смешанная криоглобулинемияподострый инфекционный эндокардит.
2. При инфекционных заболеваниях:
» бактериальные (стрептококковая инфекция, сифилис, туберкулез, сепсис)вирусные (гепатиты B и C, ВИЧ)паразитарные инвазии (малярия, токсоплазмоз, шистосомоз).
3. В результате действия лекарственных средств:
» препараты золота, висмута, ртутипеницилламинпрепараты литиянестероидные противовоспалительные препаратыпротивосудорожные препаратыантибиотики и противотуберкулезные препаратыпротивоподагрические препаратывакцины и сыворотки.
4. При опухолях:
» лимфогранулематоз и неходжкинские лимфомы (ассоциированные с нефропатией минимальных изменений и вторичным амилоидозом)солидные опухоли (ассоциированы с мембранозной нефропатией и вторичным амилоидозом).
III. Наследственные заболевания
» врожденный нефротический синдром финского типасемейный нефротический синдромнаследственный онихоартрозсерповидно-клеточная анемияболезнь Фабрипарциальная липодистрофия.
IV. Другие причины
» тромбоз почечных венморбидное ожирениебеременностьхроническая сердечная недостаточностьхроническая трансплантационная нефропатия.
Клиническая картина
Важно отметить, что первичное нарушение при нефротическом синдроме — это высокая протеинурия, которая возникает из-за повышенной проницаемости клубочкового фильтра, все остальные проявления нефротического синдрома — следствие протеинурии, хотя они могут быть и при умеренной протеинурии и отсутствовать, когда протеинурия очень высока.
Отеки у больных нефротическим синдромом нередко достигают степени анасарки. Наблюдают не только периферические, но и полостные отеки (гидроторакс, асцит, гидроперикард).
Вследствие длительно существующей дислипопротеинемии у больных с нефротическим синдромом возможно ускорение прогрессирования атеросклероза с формированием сердечно-сосудистых осложнений. Кроме того, нарушения липидного обмена непосредственно способствуют прогрессированию поражения почек. Нарушения липидного обмена часто особенно выражены при нефротическом синдроме персистирующего течения и у больных, получающих кортикостероиды. Нарушения фосфорно-кальциевого обмена у детей с нефротическим синдромом нередко приводят к тетании, у взрослых возможна остеомаляция.
Иногда нефротический синдром, особенно при мезангиопролиферативном гломерулонефрите, сопровождается гематурией. При наличии клеточных или зернистых цилиндров в мочевом осадке необходимо исключить волчаночный нефрит и гломерулонефрит, например, при эссенциальной смешанной криоглобулинемии, инфекционном эндокардите и геморрагическом васкулите.
У взрослых для диагностики и выбора лечения необходима биопсия почки. Детям биопсию обычно не делают, т.к. в подавляющем большинстве случаев нефротический синдром у них обусловлен болезнью минимальных изменений.
Осложнения нефротического синдрома
1. Инфекционные осложнения (пневмонии, эмпиема плевры, перитонит, инфекции кожных покровов, инфекции мочевыводящих путей, сепсис) в добактериальную эру являлись одной из основных причин смерти больных с нефротическим синдромом. Входными воротами инфекции нередко служат кожные трещины и язвы в области локализации отеков. К инфекционным осложнениям у больных с нефротическим синдромом предрасполагает также лечение иммунодепрессантами.
2. Тромботические и тромбоэмболические осложнения включают периферические флеботромбозы, тромбоэмболию легочной артерии, тромбозы артерии почки с развитием инфарктов ее паренхимы.
3. Обусловленные прогрессированием атеросклероза осложнения: развитие ишемической болезни сердца, в том числе острого инфаркта миокарда.
4. Отек мозга при нефротическом синдроме наблюдается редко, обычно при наличии анасарки. Характерны вялость, заторможенность пациента, в последующих стадиях — кома. Кроме того, при выраженном отечном синдроме нередко возникает отек сетчатки глаз, обратимый при повышении альбумина в сыворотке крови.
5. Нефротический криз — особый вариант гиповолемического шока, для которого характерна выраженная гиперпродукция кининов, обусловливающая появление анорексии, рвоты, болей в животе, болезненную мигрирующую («рожеподобную») эритему (чаще в области живота и нижних конечностей). Развивается артериальная гипотензия, коллапс. Одна из причин нефротического криза — неадекватное назначение диуретиков. Лечение предусматривает восполнение объема крови. Ориентировочное определение состояния объема циркулирующей крови у больных с нефротическим синдромом возможно на основании анализа клинических данных (табл.)
6. Острая почечная недостаточность — относительно редкое осложнение нефротического синдрома. Обусловлена тромбозом почечных вен, гиповолемией, использованием нестероидных противовоспалительных препаратов и рентгеноконтрастных средств, а также сепсисом.
Лабораторные исследования
Помимо гипоальбуминемии и гипопротеинемии при нефротическом синдроме обнаруживают существенную диспротеинемию: почти всегда увеличено содержание ?2-глобулинов, уменьшено содержание ?-глобулинов (при системной красной волчанке – гипер-?-глобулинемия).
Важный признак нефротического синдрома — дислипопротеинемия, характеризующаяся гипертриглицеридемией, повышением содержания общего холестерина за счет холестерина ЛПНП.
Нефротический синдром рассматривают в ряду приобретенных иммунодефицитов. Нарушения регистрируют главным образом в системе гуморального звена иммунитета: значительно снижена продукция антител, нередко наблюдают значительное уменьшение содержания IgG в сыворотке крови.
Лечение
Безусловно, наиболее прогрессивным является этиологический принцип лечения нефротического синдрома, поэтому уточнение его этиологии имеет важное практическое значение. Устранение причинного фактора (элиминация антигена) — борьба с инфекцией, радикальное удаление опухоли — может уже само по себе вызвать обратное развитие нефротического синдрома. В тех случаях, когда этиологический принцип лечения нефротического синдрома невозможен, используют меры общего характера, позволяющие в ряде случаев купировать большинство его симптомов (рис.)
Выраженность нефропротективного действия большинства препаратов (ингибиторы ангиотензинпревращающего фермента (АПФ), блокаторы рецепторов ангиотензина II, статины, блокаторы кальциевых каналов) обусловлена именно их антипротеинурическим действием. Воздействие на протеинурическое ремоделирование интерстиция — один из наиболее эффективных способов, тормозящих прогрессирование хронической болезни почек.
Выделение гиповолемического варианта нефротического синдрома важно с точки зрения показаний и противопоказаний к назначению диуретиков. При гиповолемическом варианте нефротического синдрома эти препараты значительно усугубляют гиповолемию и провоцируют нефротический криз. Гипоальбуминемия обусловливает уменьшение интенсивности транспорта многих веществ, в том числе лекарственных препаратов, например фуросемида.
Продолжаются поиски салуретиков, не транспортируемых белками плазмы, более эффективных при гипопротеинемических состояниях, в том числе при нефротическом синдроме. С целью усиления действия диуретиков при рефрактерных к мочегонным препаратам отеках может использоваться парентеральное введение различных белковых растворов (альбумин, свежезамороженная плазма и др.).
Прогноз
Прогноз больных с нефротическим синдромом обусловлен риском развития разнообразных осложнений. Некоторые из них, в частности нефротический криз, могут быть ятрогенными. При оценке прогноза нефротического синдрома следует учитывать также другие клинические критерии — маркеры неблагоприятного прогноза при нефротическом синдроме:
» Персистирующее течение, особенно при массивной протеинурииСочетание с артериальной гипертензиейБыстрое присоединение признаков почечной недостаточности.
Важна динамика экскреции белка с мочой при назначении патогенетической терапии. Относительно быстрое уменьшение протеинурии рассматривают как благоприятный прогностический признак.
Своевременная диагностика и воздействие на протеинурию позволяют в большинстве случаев предупредить или, по крайней мере, уменьшить темп прогрессирования большинства хронических нефропатий.
Протеинурия. Причины, симптомы и лечение протеинурии.!
1.Общие сведения
Знакомая многим фразам «Нашли белок в анализе мочи» на медицинском языке звучит кратко: протеинурия. Именно так называют повышенную концентрацию полипептидных аминокислотных соединений, – белков, – в составе выводимой из организма мочи.
Чаще всего пациент, у которого лабораторно диагностирована протеинурия, первым делом думает о чем-то вроде урогенитальной инфекции или почечного воспаления – и действительно, во многих случаях причина кроется именно в этом. Однако наиболее известные из существующих классификаций протеинурии (по Бергштейну, по Робсону и т.д.) насчитывают свыше двадцати различных ее видов и типов, разбиваемых на несколько крупных групп. Есть также отдельный нозологический код в Международной классификации болезней: N06, «Изолированная протеинурия с уточненным морфологическим поражением», который, в свою очередь, предполагает ряд подвидов.
Повышенное содержание белка в моче может быть физиологической, естественной реакцией организма на определенные условия – реакцией преходящей, не связанной с какой-либо патологией мочевыводящей системе и не оставляющей последствий. Однако в большинстве случаев это все-таки симптом, признак нефрологического неблагополучия, который (даже при отсутствии других симптомов или, вернее сказать, особенно в этом случае) нуждается в обязательном дальнейшем исследовании и уточнении.
Обязательно для ознакомления!
Помощь в лечении и госпитализации!
2.Причины
Концентрация и состав белков, выводимых мочевыми путями, зависит от ряда факторов. Так, транзиторным и относительно нормальным является протеинурия как реакция на повышенную температуру или физическую активность, а также ортостатическая протеинурия, обусловленная продолжительным пребываниям в положении стоя (как правило, встречается в подростковом и молодом возрасте). Повышается уровень белка и при гематурии, т.е. в случае присутствия в моче примеси крови, – что уже никак не может считаться нормальным явлением. Кроме того, т.н. ложноположительные лабораторные результаты протеинурии могут быть следствием приема антибиотиков, сульфаниламидов, йодсодержащих препаратов (например, рентген-контрастных веществ). В отдельных случаях причину повышенной концентрации белка установить вообще не удается, и остается предполагать, что представленный на анализ материал был чем-либо загрязнен. Наиболее частой из сугубо патологических причин протеинурии являются нарушения сложнейших процессов фильтрации крови в почках, – в частности, в клубочковых образованиях, или гломерулах. При гломерулонефрите и других заболеваниях почек проницаемость клубочковых капиллярных стенок-мембран может значительно увеличиваться, и, соответственно, в мочу проникает гораздо больше белков (альбумина, трансферрина и др.), чем это предусмотрено природой. Однако не только гломерулярные структуры отвечают за фильтрацию полипептидов, и при канальцевой патологии (пиелонефрит, острый некроз и пр.) также может наблюдаться протеинурия.
Значительно и стойко повышается концентрация белка в моче при развивающихся онкопроцессах и некоторых наследственных метаболических заболеваниях, а также при наркоманиях, интоксикациях соединениями тяжелых металлов, дефиците калия в моче, избытке витамина D в организме.
Посетите нашу страницу
Нефрология
3.Симптомы и диагностика
Протеинурия ситуационная, транзиторная, – самостоятельной клинической картины не имеет. В тех случаях, когда белок в моче повышается вследствие патологического процесса, доминирует симптоматика основного заболевания, и, опять же, не приходится говорить о клинике протеинурии как таковой.
Нормальным считается вывод белка в суточной массе около 0,03 грамма. Если этот уровень в клиническом анализе мочи существенно превышен (и очевидных причин тому найти не удается), будет обязательно назначен повторный анализ. Если же и он выявит протеинурию, то даже при отсутствии каких-либо субъективных жалоб понадобится тщательное обследование у нефролога и, возможно, у смежных специалистов, поскольку пренебрегать такого рода явлениями неразумно и, более того, опасно.
В медицине употребляется специальный термин «нефротический синдром», подразумевающий сочетание протеинурии с пониженным содержанием белка в крови и одновременным повышением концентрации липидов (жиров) в крови и моче.
О нашей клинике
м. Чистые пруды
Страница Мединтерком!
4.Лечение
Нетрудно видеть, что и диагностика, и последующая терапия (если она понадобится) будут нацелены не на протеинурию как таковую, а на причины, обусловившие сверхнормативное присутствие белка в моче. Практически всегда при заболеваниях почек назначается особая диета (подбирается индивидуально) и препараты из группы нефропротекторов, – дословно «защитников почек», – а именно ингибиторы ангиотензинпревращающего фермента (сокр. иАПФ), блокаторы кальциевых каналов, статины и др. Такого рода лечение нормализует функцию почек и, в частности, снижает уровень белка в моче до приемлемой или нормальной концентрации.
причины, признаки, симптомы и лечение
Протеинурия – состояние, при котором с уриной выводится количество белка, значительно превышающее норму. Это не самостоятельная нозологическая единица – это своеобразный симптом, который в большинстве клинических ситуаций указывает на прогрессирование патологий почек. В норме за одни сутки с уриной выводится до 50 мг белка.
Онлайн консультация по заболеванию «Протеинурия».
Задайте бесплатно вопрос специалистам: Уролог.Выявить протеинурию самостоятельно невозможно. Повышенную концентрацию данного вещества в урине можно выявить только посредством проведения лабораторных анализов. Стоит отметить, что данное состояние в одинаковой мере может возникать как у взрослых, так и у детей. Не исключена также протеинурия при беременности.
Этиология
Причины прогрессирования протеинурии у пациентов довольно разнообразные. Но стоит отметить тот факт, что они одинаковы как у взрослых, так и у детей. Как правило, основной причиной возникновения протеинурии являются патологии почек и мочевыделительной системы в целом.
Протеинурия прогрессирует на фоне таких недугов:
Причиной возникновения протеинурии также может стать гипертоническая болезнь. Часто она проявляется на фоне гипертонического криза. К причинам повышения концентрации белка в урине у детей и взрослых относят уретрит, сахарный диабет, наличие злокачественного поражения жизненно важных органов (сердца, мозга, лёгких и прочее).
Протеинурия у детей
Разновидности
В зависимости от связи с патологиями:
- функциональная протеинурия;
- патологическая.
В зависимости от источника:
- постренальная;
- ренальная. Подразделяется на канальцевую и клубочковую;
- преренальная или переполненная.
В зависимости от состава:
- селективная протеинурия;
- неселективная.
В зависимости от степени выраженности:
- микроальбуминурия;
- низкая;
- умеренная;
- высокая.
Функциональная протеинурия может возникнуть у пациентов с абсолютно здоровыми почками. В случае её развития концентрация белка в урине повышается выше нормы на 50 мг (в целом за сутки с мочой выделяется 1 грамм белка). В этом случае повышение белка имеет изолированный или переходящий характер и редко когда сочетается с цилиндрурией, эритроцитурией, лейкоцитурией.
Типы функциональной протеинурии:
- ортостатическая протеинурия. Чаще выявляется у людей в возрасте от 13 и до 20 лет. У детей диагностируется редко. При ортостатической протеинурии наблюдается повышение концентрации белка в урине до 1 грамма за сутки. Что примечательно, данный симптом пропадает в положении лёжа;
- лихорадочная. Повышение белка выше нормы наблюдается при лихорадочных состояниях. Обычно такое наблюдается у детей и людей преклонного возраста. Как только температура тела снижается до нормальных показателей, уровень белка в моче также возвращается к норме;
- напряжённая. У детей возникает редко. Обычно она проявляется при повышенных физических нагрузках и исчезает сразу же, как нагрузки будут возвращены к норме;
- повышение белка при ожирении;
- физиологическая. Обычно наблюдается у женщин во время вынашивания ребёнка;
- идиопатическая преходящая.
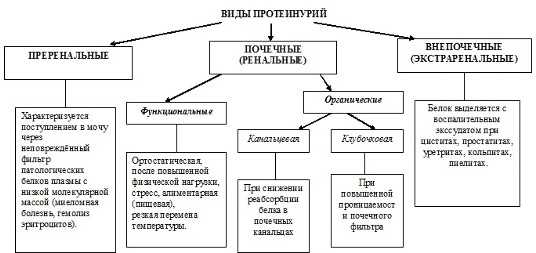
Виды протеинурий
Симптоматика
Протеинурия уже сама по себе является симптомом некоторых патологических состояний у детей и взрослых. Выявить её наличие можно посредством проведения лабораторной диагностики. Самостоятельно определить наличие у себя такого состояния довольно сложно, так как симптомы скудны.
Указывать на развитие протеинурии могут такие симптомы:
- отёк век (особенно в утреннее время). Данный признак чаще наблюдается у детей;
- на урине появляется специфическая «пенка» беловатого цвета;
- в урине можно заметить осадок или «хлопья», имеющие белый или сероватый окрас.
При обнаружении у себя таких признаков следует незамедлительно отправиться в медицинское учреждение на приём к нефрологу или урологу для проведения комплексной диагностики. Важно помнить, что протеинурия - не болезнь, а признак, указывающий на то, что в теле человека развивается какая-либо патология.
Диагностика
Во время проведения диагностики важно не только выявить повышенную концентрацию белка в урине, но и выявить истинную причину этого. Врачу нужно будет уточнить, какой именно Стандартный план диагностики:
- осмотр;
- сбор анамнеза и оценка симптомов;
- анализ мочи;
- проба Реберга;
- анализ мочи по Нечипоренко;
- бакпосев мочи;
- анализ крови;
- УЗИ почек и мочевыводящих путей;
- суточная протеинурия.
Лечебные мероприятия
Лечение будет назначено только после того, как врач выявит истинную причину повышения концентрации белка в урине. Ведь лечить нужно не протеинурию, а недуг, её спровоцировавший. Поэтому в план лечения пациенту включают такие фармацевтические препараты:
- антикоагулянты;
- антибиотики. В план лечения их добавляют в случае обнаружения инфекционного очага;
- гипотензивные лекарства используют для коррекции АД;
- препараты, содержащие активные вещества, снижающие отёчность;
- антивоспалительные средства;
- противоопухолевые средства используют для лечения опухолевых процессов доброкачественного и злокачественного характера.
В план лечения также обязательно входит диетотерапия. Основывается она на таких принципах:
- в рацион питания обязательно включают тыкву, пареные овощи, свеклу, фрукты;
- следует исключить из дневного рациона продукты, содержащие белок;
- уменьшить количество потребляемой соли;
- больше потреблять молока и молочную продукцию.
Лечение патологии проводится в стационарных условиях, чтобы медицинские специалисты могли контролировать состояние пациента. При необходимости план лечения может корректироваться. Многие пациенты отдают предпочтение средствам народной медицины, так как считают их более натуральными и безопасными. Но стоит помнить, что для лечения любого недуга принимать их можно только после согласования со своим лечащим врачом. Самолечение недопустимо.