Клостридии что это такое
что это, чем опасны, симптомы, лечение
Клостридии – это бактерии, которые в нормальном состоянии флоры ЖКТ, а также половых путей женщины всегда присутствуют в анализах. В некоторых случаях они могут быть обнаружены в полости рта, а также на кожном покрове.
Наличие клостридий в нормофлоре не означает, что все плохо. На самом деле род клостридий состоит из свободно живущих видов и патогенных представителей. Первые не представляют угрозы для организма. Их можно вовсе не заметить.
А вот вторые могут производить сильнейшие яды – тетаноспазмин (C. tetani), ботулотоксин (C. botulinum), ε-токсин (C. perf.). Эти яды представляют сильнейшую опасность для организма.
Содержание статьи
Клостридиии – что это
В организме человека живут различные микроорганизмы. Каждая группа способна отвечать за определённое состояние человека. К примеру – Клостридии, это обширный вид микроорганизмов. Они могут быть как полезны, так и причинить вред человеку.
При многочисленных размножениях, эти микроорганизмы способны поразить человека различными инфекциями. Живут они, как правило, в кишечнике, в толстой кишке, но могут находиться и в других местах человеческого организма – в пищеводе, в половой сфере, на коже.
Врачи указывают какое количество этих микроорганизмов должно быть в человеке, например, у грудничка их количество составляет – 100 000. С возрастом количество клостридий меняется. Если же у взрослого человека в организме произошло резкое их увеличение, то вероятность инфицирования следующих заболеваний очень высока:
- Инфекция столбняка.
- Заболевание ботулизмом.
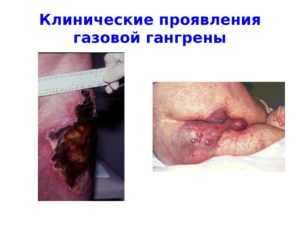
- Поражение участков кожи газовой гангреной.
Если подробно рассматривать клостридии в организме человека, то можно сказать следующее – они сине-фиолетового цвета, относятся к грамположительным микробам. Эти палочки очень подвижные, и способны вырабатывать ферменты.
Они способные образовывать так называемые – эндоспоры, которые практически недоступны для антибиотика и могут выдерживать высокие температуры. Кроме этого они прекрасно размножаются без кислорода. К роду «Clostridium» можно отнести более ста видов бактерий. Самыми распространенными являются такие микроорганизмы, который вызывают ряд тяжелых заболеваний –
- Ботулиум – способствует развитию ботулизма.
- Тетани – являются возбудителем столбняка.
- Клостридии перфрингенс – возбудитель газовой гангрены и токсичных инфекций.
Многие микроорганизмы, например, диффициле – это нормальные представители кишечной флоры. Чаще всего диффициле живут на коже человека, в кишечнике, во рту, в женской половой сфере.
Еще один вид – Клостридии перфрингенс, прекрасно переносят высокие и низкие температуры, ультрафиолетовые лучи. Количество клостридий в организме человека зависит от возраста.
Микроорганизмы клостридии, в природе встречаются повсеместно. Их можно увидеть под микроскопом в водоемах, в почве, ну а основное место обитания, остается кишечник, где для них благоприятная атмосфера жизни.
Опасность размножения клостридий
Если число клостридий в норме, то опасности для человека они не представляют. Но когда рост их увеличивается, то возникают в организме различные патологические состояния. При размножении они выделяют токсины и белок, который угнетает перистальтику кишечника. Кроме этого, активное развитие и увеличение микроорганизмов может вызвать состояние – клостридиоз. Проверяют рост и активность клостридий в фекалиях. Если их рост повышен, врачи назначают дополнительную диагностику.
Очень часто рост микроорганизмов провоцирует курс лечения антибиотиками. Такое медикаментозное лечение, является риском для организма, так как антибиотики способны уничтожить не только вредные микроорганизмы, но и необходимые для нормальной работы микробы.
В условиях стационара может произойти, так называемое инфицирование. С применением в стационарах различных антибактериальных и дезинфицирующих препаратов, провоцируется рост и размножение микроорганизмов, стойких к таким профилактическим мерам.
Размножение бактерий – клостридий, опасно для человека, так как они провоцируют развитие страшных для организма человека, возбудителей.
- Острое инфекционное заболевание ботулизм – способно поражать нервную систему человека. Приводит к параличу различных участков тела.
- Инфекция – столбняк, также поражает нервную систему человека. Эта инфекция имеет отличительную черту, она вырабатывает сильный токсин. В результате само заболевание протекает в тяжелой форме.
- Инфекция, поражающая участки кожи – газовая гангрена. Очень часто она развивается после травм, ранений, ампутаций. Гангрена представляет собой пораженный и мёртвый участок кожи, который постепенно переносится на здоровые участки.
Как уже писалось, рост и развитие клостридий проверяют по фекалиям человека. Если они были там обнаружены, это не значит, что требуется срочное лечение. Они стимулируют перистальтику, и в то же время расщепляют белки, главное, чтобы их количество не превышало. Поэтому нужно постоянно следить за их количеством, периодически сдавая кал.
Симптомы заболевания и лечение
Первые признаки заболевания и роста количества клостридий, проявляются в нарушении стула взрослого и ребенка. При более тяжелых формах инфицирования может возникнуть – псевдомембранозный колит. Он возникает на 10-е сутки после интенсивного применения антибиотиков. Основные симптомы заболевания клостридиозом проявляются в следующих признаках:
- Повышение температуры тела до 39,5.
- Вздутие живота.
- Снижение или потеря аппетита.
- Резкая потеря веса.
- Беспричинная рвота.
- Колики в области живота.
- Водянистый кал, с зеленоватым оттенком и гнилым запахом.
При первых таких проявлениях, необходимо срочное лечение. Сначала доктора определяют инфицирование и выявляют болезнь, если это острая форма и развитие ботулизма, столбняка, газовой гангрены, то, как правило, лечение проходит в стационаре. Это тяжелые формы поражения, и они напрямую влияют на жизнь человека.
Кроме этого некоторые виды диареи, также требуют стационарного лечения. Как уже писалось в организме человека могут жить более 30 видов клостридий, в зависимости от вида и роста, той или иной бактерии и назначается лечение.
- Вводятся специальные препараты, которые нейтрализуют токсины в организме. Токсины требуют строго расчета и наблюдения врача, чтобы не было передозировки препаратом.
- Терапия, направленная на антибактериальное снижение, к котором клостридии имеют чувствительность.
- Хирургическое вмешательство (газовая гангрена) – в этом случает поврежденные участки тела ампутируются.
- Пациенту даются противовоспалительные, жаропонижающие препараты – это зависит от синдрома.
Каждый человек может снизить риск заболевания клостридиозом. Для этого достаточно придерживаться элементарных правил личной гигиены. Необходимо постоянно мыть руки перед едой, после прогулок с посещением общественных мест. Свежие плоды и овощи желательно обдавать кипятком. Принимать антибиотики строго по назначению доктора, следить за своим кишечником.
Клостридия, Clostridium, клостридиоз: характеристика, анализы, лечение
Клостридии (clostridium) — нормальные обитатели микрофлоры человека, способные при определенных условиях интенсивно размножаться, приобретать патогенные свойства и вызывать развитие заболеваний. Они относятся к облигатным анаэробам, живущим в отсутствии кислорода или при крайне низком его содержании. Клостридии выполняют ряд важнейших функций в организме: расщепляют белки, тонизируют кишечную стенку и стимулируют перистальтику.
Термин «клостридии» в переводе с древнегреческого языка означает «веретено». Это связано со способностью микробов раздуваться в центральной части при спорообразовании и приобретать соответствующую форму.
Клостридии являются обитателями микрофлоры кишечника, женской половой сферы, кожного покрова, респираторного тракта и полости рта. Количество клостридий в кале здоровых людей может колебаться, что необходимо учитывать в процесса диагностики. У лиц старше 60 лет количество клостридий в фекалиях составляет 106 КОЕ/г, у детей старше года и у взрослых – до 105 КОЕ/г. Клостридии в кале у ребенка первого года жизни не должны превышать 103 – 104 КОЕ/г.
По механизму возникновения все клостридиозы классифицируют на:
- Травматические, вызванные Сlostridium tetani и Clostridium perfringens. При этом входными воротами инфекции становятся раневые поверхности.
- Энтеральные, вызванные Clostridium difficile или Clostridium botulinum. Возбудители проникают в организм с контаминированной пищей.
Характеристика возбудителя
Clostridia под микроскопом
Клостридии окрашиваются по Грамму в синий цвет и имеют палочковидную форму, в мазке располагаются попарно или короткими цепочками. Они подвижны и размножаются при полном отсутствии кислорода.
Благодаря способности образовывать споры микробы устойчивы к нагреванию, воздействию антибиотиков и современных дезинфектантов. Центрально расположенная спора придает бактериям форму веретена, а терминально расположенная — форму барабанных палочек.
Клостридии вырабатывают токсины и вызывают развитие клостридиозов, к которым относятся: ботулизм, столбняк, газовая гангрена, клостридиальная пищевая инфекция.
Факторы патогенности:
- Токсигенность. Клостридии вырабатывают мощные микробиологические токсины – ботулотоксин, тетаноспазмин, токсин, разрушающий эритроциты. Благодаря способности к токсинообразованию бактерии оказывают нейротоксическое, гемотоксическое, лейкотоксическое, некротоксическое и летальное воздействие на организм. Для патогенных клостридий характерен летальный и нелетальный паразитизм.
- Инвазивность, обусловленная ферментативной активностью бактерии.
- Выработка гидролитических ферментов — протеиназы, коллагеназы, лецитиназы и гиалуронидазы, желатиназы, ДНК-азы, нейраминидазы.
- Перитрихиально расположенные жгутики, обеспечивающие подвижность и адгезию.
- Штаммы некоторых клостридий синтезируют энтеротоксин, действие которого аналогично токсинам энтеротоксигенных эшерихий, оказывающим повреждение кишечной стенки.
Клостридии растут в глубине среды Вильсон-Блер. Колонии имеют шаровидную или чечевидную форму черного цвета. Бактерии обладают слабой биологической активностью: не восстанавливают сульфаты в сульфиды, не синтезируют каталазу и цитохромы, не содержат флавиновых ферментов.
Клостридиоз — заболевание, характеризующееся выраженными некротическими и общетоксическими изменениями, которые являются основными и преобладают над воспалительными процессами. Это основной отличительный признак анаэробной инфекции от аэробной. Некроз, отек и газообразование в тканях — патоморфологические признаки любых клостридиозов.
Эпидемиология
Сульфитредуцирующие клостридии с фекалиями больного человека или бактерионосителя попадают во внешнюю среду и довольно долго сохраняют свою биологическую активность в почве. Для клостридиозов характерна осенне-летняя сезонность, спорадическая и вспышечная заболеваемость. Восприимчивы к клостридиозам представители различных возрастных группах, но в наибольшей степени — дети.
Механизмы распространения инфекции – фекально-оральный и контактно-бытовой, которые реализуются пищевым и контактным путями.
- Инфекция передается алиментарным путем через пищевые продукты – мясо, фрукты и овощи, молоко. Для ботулизма это продукты с малым содержанием кислорода – консервы, соленья, копченая, вяленая рыба и колбаса, приготовленные дома.
- Контактный путь — передача возбудителя через инфицированные предметы окружающей среды и грязные руки.
Под воздействием токсинов в тонком кишечнике нарушается транспорт глюкозы, поражается эпителий, слизистая становится гиперемированной, отечной, на ней появляются геморрагии, язвы и очаги некроза. Токсины оказывают капилляротоксическое действие, что приводит к дистрофическим и некробиотическим процессам во внутренних органах.
Активация собственной микрофлоры человека может стать причиной клостридиоза. После лечения антибиотиками или цитостатиками размножение клостридий усиливается.
Факторы, способствующие развитию клостридиозной инфекции:
- Напряженная экологическая обстановка,
- Стрессы,
- Длительная гормональная и антибактериальная терапия,
- Иммунодефицит,
- Недоношенность,
- Дисфункции ЦНС,
- Хроническая бессонница,
- Внутрибольничные инфекции,
- Респираторные инфекции,
- Операции.
Формы и симптоматика
Ботулизм — опасная инфекция, развивающееся в результате воздействия на человеческий организм ботулотоксина – продукта жизнедеятельности бактерии Clostridium botulinum. Первыми клиническими признаками патологии являются: сильные боли в эпигастрии, приступообразная головная боль, жидкий стул, многократная рвота, общее недомогание, лихорадка. Внезапно нарушается зрение, появляется двоение в глазах, теряется четкость предметов, перед глазами плавают мушки. Ботулизм проявляется афонией, дисфагией, офтальмоплегией, параличами и парезами глоточных и гортанных мышц. Больные поперхиваются жидкой пищей, у них нарушается фонация и артикуляция, голос становится «носовым», гнусавым, осиплым. Разгар болезни проявляется шаткостью походки, мышечной гипотонией, дизурией, бледностью кожи, тахикардией. В заключительной стадии заболевания преобладают симптомы нарушения дыхательной функции: одышка, чувство сжатия или стеснения в груди, удушье.
 Столбняк – острое инфекционное заболевание, развивающееся при контактном инфицировании столбнячной палочкой Clostridium tetani, распространенной повсеместно. Возбудитель C.tetani вырабатывает мощнейший яд – столбнячный нейротоксин, который поражает двигательные клетки спинного и головного мозга. Паралич сердечной мышцы и дыхательного центра — причины смерти больных при столбняке. Заболевание развивается преимущественно у лиц в возрасте 3-7 лет. Это связано с высокой подвижностью детей и их частой травматизацией. Заболеваемость столбняком максимальна в южных районах с развитой сельскохозяйственной сферой, особенно в теплое время года.
Столбняк – острое инфекционное заболевание, развивающееся при контактном инфицировании столбнячной палочкой Clostridium tetani, распространенной повсеместно. Возбудитель C.tetani вырабатывает мощнейший яд – столбнячный нейротоксин, который поражает двигательные клетки спинного и головного мозга. Паралич сердечной мышцы и дыхательного центра — причины смерти больных при столбняке. Заболевание развивается преимущественно у лиц в возрасте 3-7 лет. Это связано с высокой подвижностью детей и их частой травматизацией. Заболеваемость столбняком максимальна в южных районах с развитой сельскохозяйственной сферой, особенно в теплое время года.
Газовая гангрена – специфическое поражение глубоко расположенных раневых поверхностей, вызываемое Clostridium perfringens (клостридия перфрингенс). Через пару дней после получения тяжелой травмы появляются симптомы патологии. В ране создаются необходимые условия для роста и развития клостридий: отсутствует кислород, имеются омертвевшие клетки. Бактерии в очаге продуцируют токсины, что приводит к тяжелой интоксикации организма. Пораженные ткани отекают и отмирают. Симптомами патологии являются: крепитация, возникающая при пальпации пораженной ткани; зловонное отделяемое из раны; лихорадочное состояние.
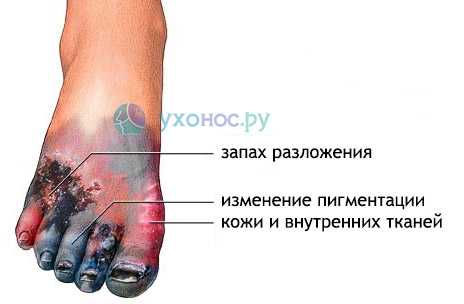
Газовая гангрена
Псевдомембранозный колит является следствием антибиотикотерапии. У больного развивается дисбактериоз кишечника с преобладающей активностью Clostridium difficile (клостридия диффициле). Микроб колонизирует слизистую кишечника и выделяет энтеротоксин и цитотоксин. Воспаление слизистой сопровождается образованием «псевдомембран», которые представляют собой фибринозные налеты. При отсутствии активной терапии колита развиваются тяжелые осложнения – прободение кишечной стенки, перитонит и летальный исход. Обычно данное заболевание возникает у лиц преклонного возраста, онкологических больных, пациентов после операций. Патология имеет острое начало. У больных появляется лихорадка, метеоризм, схваткообразные болезненные ощущения в животе, упорная рвота, отрыжка, головная боль и прочие симптомы интоксикации. У них развивается анорексия, кахексия, неухоженность, потеря телесного веса, тенезмы, потуги, моральная подавленность, депрессия. Резко снижается иммунитет, возникает диарея. Жидкий стул содержит наложения фибрина и издает гнилостный запах.
Антибиотикоассоциированные диареи развиваются у пациентов ЛПУ, прошедших длительную антибиотикотерапию. Клостридии, обитающие в кишечнике, становятся устойчивыми к лекарствам. Болезненность в околопупочной области быстро распространяется по всему животу. Стул учащается, но общее состояние больных остается удовлетворительным. Новорожденный дети и малыши первого года жизни не болеют данной патологией, поскольку они получают с материнским молоком антитела против антигенов-клостридий.
Некротический энтерит — воспаление стенки кишечника с образованием очагов некроза, эррозий и язв. У больных поднимается температура, озноб, диспепсия, жидкий стул с кровавой пеной. Специалисты обнаруживают гепатоспленомегалию, резкое вздутие живота, указывающее на парез кишечника. Возможно развитие кровотечений, тромбоза артериол и венул, прободения язв. Некротический энтерит обычно развивается у ослабленных лиц, детей и пожилых людей.
Пищевая токсикоинфекция, вызванная клостридиями, проявляется классическими симптомами пищевого отравления: лихорадкой, диареей, диспепсией, отсутствием аппетита, болью в животе. Диспепсический и интоксикационный синдромы — основа данной формы патологии. Больные становятся вялыми и беспокойными. Симптомы сохраняют 3-4 дня, а потом утихают.
Диагностика
Диагностика клостридиозов начинается с изучения симптомов заболевания, выяснения его взаимосвязи с травмой, антибактериальной терапией, употреблением определенных продуктов. Диагноз ставится с учетом анамнеза, эпидемиологических факторов, клинических проявлений. Лабораторные и инструментальные методики позволяют поставить окончательный диагноз.
- Микроскопическое исследование биоматериала позволяет обнаружить грамположительные палочки со слегка закругленными концами и спорами.
- Бактериологическое исследование. Материал для исследования — раневое отделяемое, испражнения, рвотные массы, моча, кровь, трупный материал. Подготовка для сдачи анализа не требуется. В микробиологической лаборатории биоматериал засевают на специальные питательные среды — Кита-Тароцци или Вильсон-Блер. Посевы инкубируют в анаэростате 3 суток. На Вильсон-Блер появляются черные колонии, растущие в глубине среды и имеющие шаровидную и чечевицеобразную форму. Подсчитывают их общее количество, подтверждают принадлежность к клостридиям изучением мазка по Грамму. Затем проводят полную идентификацию выделенного возбудителя до вида. Посев кала для определения рода и вида возбудителя проводят в бактериологической лаборатории.
- Биологическая проба на белых мышах проводится с целью выявления токсинов клостридий и их нейтрализации.
- Антигенный тест выполняют в иммунологических лабораториях ЛПУ и диагностических центров.
- Экспресс-диагностика – исследование кала методом иммуноферментного анализа, позволяющее обнаружить в фекалиях больного энтеротоксин.
- Биопсия слизистой оболочки кишечника выявляет характерные воспалительные изменения.
- Серодиагностика – определение токсина в РНГА с антительным диагностикумом и постановка реакции встречного иммуноэлектрофореза.
- Инструментальная диагностика – рентгенография кишечника, в ходе которой специалисты-рентгенологи обнаруживают скопление газа в тканях организма.
- Эндоскопическое и томографическое исследование дает картину локального или разлитого воспаления кишечника с наличием псевдомембран.
Если в бактериологическом анализе кала у грудного ребенка повышены клостридии, это указывает на имеющий дисбактериоз кишечника. При этом у грудничка появляется вздутие живота, частые срыгивания, снижение аппетита, нерегулярный стул, нарушение сна. Количество бактерий в кале у грудных детей, превышающее 10 4 — признак патологии, которую необходимо лечить.
Нормальное содержание клостридий в анализе на дисбактериоз обеспечивает оптимальную работу желудочно-кишечного тракта. Если их количество резко увеличивается, появляется диарея, вздутие и прочие признаки диспепсии.
Лечение
Клостридиозы — заболевания, требующие лечения в условиях стационара и оказания квалифицированной медицинской помощи. Если у больного имеются диспепсические симптомы и интоксикация, ему промывают желудок и ставят очистительную клизму. В течение первых суток специалисты рекомендуют соблюдать водно-голодную диету.
Медикаментозная терапия:
 Антитоксические сыворотки и иммуноглобулины нейтрализуют токсины при ботулизме и столбняке.
Антитоксические сыворотки и иммуноглобулины нейтрализуют токсины при ботулизме и столбняке.- Антибиотики, к которым чувствительны клостридии — макролиды «Азитромицин», «Кларитромицин», цефалоспорины «Цефтриаксон», «Цефазолин», защищенные пенициллины «Амоксиклав», «Метронидазол», «Ванкомицин».
- Пробиотики и пребиотики для нормализации биоценоза кишечника – «Аципол», «Бифиформ», «Лактофильтрум», «Хилак-форте», «Линекс», «Энтерол».
- Инфузионная терапия для нормализации баланса жидкости в организме. Для борьбы с интоксикацией внутривенно вливают «Реополиглюкин».
- В тяжелых случаях применяют антигистаминные препараты и кортикостероиды.
- Симптоматическая терапия — гепатопротекторы, ферменты, энтеросорбенты, витамины, жаропонижающие средства, ноотропы, сердечные гликозиды.
Профилактика
Профилактические мероприятия, позволяющие предупредить развитие клостридиозов:
- Cоблюдение санитарных правил и норм,
- Тщательное мытье и термическая обработка продуктов питания,
- Поддержание здоровой микрофлоры кишечника и работы иммунитета,
- Своевременное выявление и изоляция инфицированных лиц,
- Определение бактерионосителей клостридии,
- Прием антибактериальных средств только по назначению врача,
- Обеспечение санитарно-гигиенического режима в ЛПУ.
В настоящее время разработана и активно применяется специфическая профилактика столбняка, которая заключается в создания активного иммунитета всем детям, начиная с 3-месячного возраста. Для иммунизации используют вакцину АКДС, АДС или АС. Проводят вакцинацию в соответствии с Национальным календарем прививок.
Мнения, советы и обсуждение:
Клостридии в кале у ребенка и взрослого, лечение клостридиоза
Закрыть- Болезни
- Инфекционные и паразитарные болезни
- Новообразования
- Болезни крови и кроветворных органов
- Болезни эндокринной системы
- Психические расстройства
- Болезни нервной системы
- Болезни глаза
- Болезни уха
- Болезни системы кровообращения
- Болезни органов дыхания
- Болезни органов пищеварения
- Болезни кожи
- Болезни костно-мышечной системы
- Болезни мочеполовой системы
- Беременность и роды
- Болезни плода и новорожденного
- Врожденные аномалии (пороки развития)
- Травмы и отравления
- Симптомы
- Системы кровообращения и дыхания
- Система пищеварения и брюшная полость
- Кожа и подкожная клетчатка
- Нервная и костно-мышечная системы
- Мочевая система
- Восприятие и поведение
- Речь и голос
- Общие симптомы и признаки
- Отклонения от нормы
- Диеты
- Снижение веса
- Лечебные
- Быстрые
- Для красоты и здоровья
- Разгрузочные дни
- От профессионалов
- Монодиеты
- Звездные
- На кашах
- Овощные
- Детокс-диеты
- Фруктовые
- Модные
- Для мужчин
- Набор веса
- Вегетарианство
- Национальные
- Лекарства
- Антибиотики
- Антисептики
- Биологически активные добавки
- Витамины
- Гинекологические
- Гормональные
- Дерматологические
- Диабетические
- Для глаз
- Для крови
- Для нервной системы
- Для печени
- Для повышения потенции
- Для полости рта
- Для похудения
- Для суставов
- Для ушей
- Желудочно-кишечные
- Кардиологические
- Контрацептивы
- Мочегонные
- Обезболивающие
- От аллергии
- От кашля
- От насморка
- Повышение иммунитета
- Противовирусные
- Противогрибковые
- Противомикробные
- Противоопухолевые
- Противопаразитарные
- Противопростудные
- Сердечно-сосудистые
- Урологические
- Другие лекарства
- Врачи
- Клиники
- Справочник
- Аллергология
- Анализы и диагностика
- Беременность
- Витамины
- Вредные привычки
- Геронтология (Старение)
- Дерматология
- Дети
- Женское здоровье
- Инфекция
- Контрацепция
- Косметология
- Народная медицина
- Обзоры заболеваний
- Обзоры лекарств
- Ортопедия и травматология
- Питание
- Пластическая хирургия
- Процедуры и операции
- Психология
- Роды и послеродовый период
- Сексология
- Стоматология
- Травы и продукты
- Трихология
- Другие статьи
- Словарь терминов
- [А] Абазия .. Ацидоз
- [Б] Базофилы .. Богатая тромбоцитами плазма
- [В] Вазопрессин .. Выкидыш
- [Г] Галлюциногены .. Грязи лечебные
- [Д] Деацетилазы гистонов .. Дофамин
- [Ж] Железы .. Жиры
- [И] Иммунитет .. Искусственная кома
- [К] Каверна .. Кумарин
- [Л]
Клостридиоз. Симптомы, формы и лечение клостридиоза.
Клостридиоз – это острая, антропонозная, анаэробная инфекция с энтеральным путем заражения, характеризующаяся различной степенью выраженности клинических проявлений.
Основной причиной развития тяжелых форм заболевания при Clostridium difficile является антибиотикотерапия. Является причиной так называемой Антибиотик-ассоциированной диареи.
При этом исследования доказывают, что даже однократный прием антибиотика широкого спектра действия, независимо от дозы и способа введения, может привести к развитию Диареи и Псевдомембранозного колита, обусловленных Clostridium difficile.
20% осложнений клостридиоза составляют антибиотик-ассоциированные диареи, а 90-100% - псевдомембранозные колиты.
Отравление токсином при Clostridium perfringens возникает также после употребления продуктов, обсемененных клостридиями. Характеризуется тяжелым течением, высокой летальностью.
Этиология.
Возбудитель Clostridium difficile – строго анаэробная, спорообразующая, грамположительная бацилла.
Споры Clostridium difficile высокоустойчивы к факторам внешней среды и к стандартным дезинфицирующим средствам, а вегетативные формы резистентны к большинству антибиотиков.
Микробы Clostridium perfringens – это крупные грамположительные палочки. Растут в анаэробных условиях, способны образовывать споры.
Эпидемиология.
Clostridium difficile часто обнаруживаются в окружающей среде и могут быть изолированы из почвы.
Основной механизм передачи инфекции – фекально-оральный.
Источником инфекции является человек (чаще – пациенты, получающие антибиотики широкого спектра действия, а также дети).
К здоровым лицам инфекция может передаться через руки и предметы ухода, а также через постельные принадлежности, мебель, душевые, туалеты и др.
В группу риска также входят дети раннего возраста (ослабленные), а также пациенты, длительно находящиеся в стационаре и, тем более, получающие антибиотики.
Clostridium perfringens широко распространены в почве, в испражнениях людей и животных. Все это создает возможности для обсеменения продуктов. Отравления чаще бывают при употреблении мясных продуктов домашнего приготовления, мясными и рыбными консервами. В некоторых странах отравления токсином CL perfringens регистрируются довольно часто, занимая 3-е место после сальмонеллезных гастроэнтеритов и стафилококковых пищевых отравлений.
Патогенез и патоморфология.
Под действием антибиотиков и других повреждающих факторов нарушается нормальная микрофлора кишечника, снижается анаэробная микрофлора кишечника. Это создает благоприятные условия для размножения Clostridium difficile и перехода её в токсинобразующую форму.
Вегетативные формы Clostridium difficile продуцируют экзотоксины, из которых энтеротоксин (токсин А) и цитотоксин (токсин В) повреждают кишечную стенку.
Токсин А, стимулируя гуанилатциклазу, повышает секрецию жидкости в просвет кишечника и способствует развитию диареи.
Токсин В обладает выраженным цитопатогенным действием, действуя на клеточные мембраны кишечника.
Это приводит к потере калия и развитию электролитных нарушений.
А сам возбудитель не обладает инвазивными свойствами и не оказывает цитотоксического воздействия на слизистые кишечника.
При отравлении токсинами, вырабатываемыми CLostridium perfringens, в патогенезе заболевания людей наибольшее значение имеет альфа-токсин и бета-токсин.
В кишечнике токсины повреждают слизистую оболочку, попадая в кровь, проникают в различные органы, связываясь с митохондриями клеток печени, почек, селезенки, легких. Повреждают также сосудистую стенку, что сопровождается геморрагическими явлениями. Иногда в кровь проникает и сам возбудитель, а не только токсины; в этих случаях может развиться тяжелый Анаэробный сепсис.
Клинические симптомы и течение при Clostridium difficile.
Клостридиоз при Clostridium difficile может протекать в виде:
- Бессимптомного бактерионосительства,
- Легкой диареи,
- Тяжелых форм заболевания в виде Псевдомембранозного колита.
Антибиотик-ассоциированная диарея у детей по причине Clostridium difficile часто характеризуется клиническими симптомами нетяжелого колита или энтероколита.
Обычно протекает без лихорадки и интоксикации.
При этом возможно появление болей в животе, но чаще болезненность выявляется лишь при пальпации кишечника. Отмечается легкое или умеренное учащение стула, как правило, не приводящее к выраженным водно–электролитным нарушениям.
Симптомы Псевдомембранозного колита у детей обычно развиваются остро и характеризуются отсутствием аппетита, лихорадкой, интоксикацией, диареей, отрыжкой, вздутием и спастическими болями в животе (абдоминальные колики). Пальпация живота по ходу толстого кишечника болезненна.
Стул частый, в каловых массах – примесь слизи и крови (реже). Иногда бoльшая часть испражнений представлена густой белесоватой слизью и обрывками фибринозных наложений.
При многократной диарее развивается эксикоз с нарушениями кровообращения, значительно реже отмечается коллапс без предшествующей диареи.
Течение псевдомембранозного колита может осложниться кишечным кровотечением, перфорацией и развитием перитонита.
Поэтому при тяжелых формах клостридиоза должно проводиться совместное наблюдение педиатра и хирурга.
Встречаются рецидивирующие (повторяющиеся) формы клостридиоза с развитием колита при неполном излечении клостридиоза и реинфекции.
Клостридиоз может развиться спустя 1–2 недели после отмены антибактериальной терапии.
Клинические Симптомы и Течение при CLostridium perfringens.
Заболевание начинается с болей в животе, преимущественно в пупочной области.
Быстро нарастает общая слабость, понос, стул становится обильным, водянистым, иногда принимает вид рисового отвара, учащается до 20 раз в сутки, бывает обильная рвота.
Начинается выраженное обезвоживание (судороги, характерное лицо, морщинистая кожа кистей, нерасправляющиеся складки кожи, цианоз, афония, сухость слизистых оболочек и др.).
При отравлениях, вызванных токсинами клостридий типов Е и F, может развиться Некротический энтерит (сильные боли в животе, тошнота, рвота, жидкий стул с примесью крови). Заболевание протекает очень тяжело. Помимо дегидратации и гиповолемического шока может развиться острая почечная недостаточность, инфекционно-токсический шок.
Диагностика.
В первую очередь необходимо провести Бактериологичекое исследование кала.
Для этого используются метод иммуно–ферментного анализа (ИФА) и цитотоксический тест на культурах клеток с использованием специфических антисывороток.
Но «золотым стандартом» лабораторной диагностики Cl. difficile – инфекции является цитотоксический тест, направленный на обнаружение токсина В.
При эндоскопическом обследовании толстого кишечника при развитии наиболее тяжелой формы заболевания (псевдомембранозный колит) на фоне резко выраженных воспалительно–геморрагических изменений слизистой кишечника обнаруживают небольшие по размеру (чаще - до 2-5 мм, реже - до 20 мм и более в диаметре) возвышающиеся желтоватые бляшки.
Бляшки образованы скоплением фибрина, муцина и клеток, участвующих в воспалении. Сливаясь, бляшки образуют псевдомембраны. Пленки могут отторгаться, обнажая изъязвленную поверхность кишечной стенки.
Результаты анализа крови: нейтрофильный лейкоцитоз, сдвигом лейкоцитарной формулы влево, ускорение СОЭ.
При подозрении на пищевое отравление, вызванное токсинами CL perfringens., берут подозрительные продукты и материал от больных (рвотные массы или промывные воды, кровь, испражнения).
Диагноз ставится также с учетом анамнеза, эпидемиологических факторов, клинических проявлений.
- При Бессимптомном бактерионосительстве Cl. difficile лечение не проводится.
При манифестных формах Cl. difficile нужно срочно отменить Антибиотик!!
- Назначение Этиотропной терапии необходимо при:
-- при тяжелых формах заболевания;
-- продолжающейся диарее после отмены антибиотика;
-- при рецидиве диареи на фоне повторного приема антибиотиков.
- Препараты выбора для этиотропной терапии при клостридиозе:
-- Препарат 1-ой линии -- Метронидазол:
Суточная доза – 30мг/кг, дозу разделить на 3-4 приема в сутки, перорально или в/в. Курс лечения -- 7-10 дней.
-- Препарат 2 -ой линии -- Ванкомицин (при Cl. difficile):
Суточная доза – 40мг/кг(но не более 2г в сутки), дозу разделить на 4 приема в сутки, перорально. Курс лечение 7-10 дней.
- При отравлении CL perfringens для удаления токсинов из организма проводят как можно раньше промывание желудка водой или 5% раствором натрия гидрокарбоната.
- При отравлении CL perfringens назначают антибиотики широкого спектра действия (Тетрациклин, левомицетин, эритромицин).
- Энтеросорбенты назначаются только в легких случаях и при внутривенном введении метронидазола.
При пероральном введении этиотропных лекарственных средств нельзя одновременно применять энтеросорбенты (холестирамин, активированный уголь и др.),так как возможно снижение терапевтического эффекта антибиотиков из–за их связывания с энтеросорбентами в просвете кишечника.
- Противопоказаны препараты, снижающие кишечную моторику.
- После отмены антимикробных препаратов для полной санации кишечника от спор возбудителя назначаются Пробиотики.
Clostridioides difficile — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 10 января 2018; проверки требуют 10 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 10 января 2018; проверки требуют 10 правок.| Clostridioides difficile | |||
|---|---|---|---|
| |||
| Clostridioides difficile (Hall and O'Toole 1935) Lawson and Rainey 2016 | |||
| |||
Clostridioides difficile (лат.) — вид анаэробных спорообразующих грамположительных бактерий из семейства Peptostreptococcaceae класса Clostridia[1]. До 2016 года был отнесён к роду клостридий под названием Clostridium difficile[2].
C. difficile является главным возбудителем псевдомембранозного колита[3], тяжёлого инфекционного заболевания прямой кишки, часто возникает в случае уничтожения флоры кишечника из-за использования антибиотиков.
В случае возникновения, заболевание лечат антибиотиками, такими как метронидазол, при полном устранении всех других антибиотиков. Бактерия подразделяется на шесть штаммов, пять из которых содержат патогенные подтипы[4]/ C. difficile спорулирующая бактерия, поэтому псевдомембранозный колит может легко возобновиться после курса антибиотиков. Бактерия является также резистентной к таким антибиотикам, как эритромицин, хлорамфеникол и тетрациклин из-за транспозонов в геноме бактерии[4]. Симптомы заболевания могут варьироваться от легкой диареи и болей в животе до опасных для жизни воспалительных процессов, перфорации кишечника, а в тяжелых случаях - сепсиса и смерти. Эти симптомы вызваны двумя сильными цитотоксинами, TcdA и TcdB. Бактерия прикрепляется к эпителию кишечника и начинает производить эти токсины. Токсины проходят в клетки эпителия и в цитозоле клетки инактивируют небольшие GTP-молекулы, такие как Rho, Rac и Cdc42. Токсины TcdA и TcdB вызывают распад цитоскелета и гибель клеток[4]. Данные токсины находятся на особом патогенном локусе в геноме бактерии. Этот локус также содержит дополнительные гены для производства этих токсинов.
Было показано, что ректальное введение больным людям фекалий, взятых от здоровых доноров, вылечивает системную инфекцию C. difficile[5]. При применении фекальной трансплантации микробиоты, 90 % трансплантаций прошли успешно без серьезных побочных эффектов[6]
- ↑ Classification of domains and phyla - Hierarchical classification of prokaryotes (bacteria) : Version 2.2 : [англ.] // LPSN. — 2019. — 22 June.
- ↑ Genus Clostridioides : [англ.] // LPSN[en]. (Проверено 17 марта 2020).
- ↑ Pseudomembranous Colitis (неопр.). eMedicine. WebMD (1 июля 2005). Дата обращения 11 января 2007. Архивировано 26 июня 2013 года.
- ↑ 1 2 3 Mónica Oleastro, Adriano O. Henriques, Mónica Serrano, Aristides L. Mendes, Joana Isidro. Overview of Clostridium difficile Infection: Life Cycle, Epidemiology, Antimicrobial Resistance and Treatment (англ.) // Clostridium Difficile - A Comprehensive Overview. — 2017. — 27 September. — doi:10.5772/intechopen.69053.
- ↑ Джонатан Эйзен. Знакомьтесь, ваши микробы (неопр.). TED Talks (июль 2012).
- ↑ Michael H. Woodworth, Cynthia Carpentieri, Kaitlin L. Sitchenko, Colleen S. Kraft. Challenges in fecal donor selection and screening for fecal microbiota transplantation: A review (англ.) // Gut Microbes. — 2017. — 27 January (vol. 8, iss. 3). — P. 225—237. — ISSN 1949-0976. — doi:10.1080/19490976.2017.1286006.
Clostridium botulinum — Википедия
Clostridium botulinum (лат.) (ботулина) — анаэробная грамположительная бактерия рода клостридий[1], возбудитель ботулизма — тяжёлой пищевой интоксикации, вызываемой ботулиническим токсином и характеризуемой поражением нервной системы.
Впервые эти бактерии выявил в 1895 году бельгийский микробиолог Эмиль ван Эрменгем, ученик Роберта Коха. Однако первые упоминания о вызываемом ими ботулизме относятся ещё к 1793 году, когда в Германии после употребления в пищу копчёной кровяной колбасы заболели 13 человек, 6 из которых скончались. Аналогичные пищевые отравления колбасой с гибелью большого числа людей наблюдались в Германии во время войны с Наполеоном в 1795–1813 годах. Тогда считалось, что эта смертность связана с отсутствием гигиены питания в деревнях в связи с войной[2].
Первым учёным, который занялся сбором статистики по случаям подобных отравлений и их симптомов, был Генрих Фердинанд Аутенрит из Тюбингенского университета. Опубликованный им в газете в 1817 году список симптомов включал желудочно-кишечные нарушения, двоение в глазах и расширение зрачка. Также Аутенрит обнаружил связь между силой действия яда и степенью прожарки колбасы.
Одним из медиков, представивших профессору описания случаев отравления, был врач и литератор Юстинус Кернер. В дальнейшем Кернер значительную часть своей жизни посвятил изучению ботулинического токсина и считается крестным отцом его исследований. Проводя испытания на животных и на самом себе, он пытался выделить из колбасы неизвестный токсин, который сам называл «колбасный яд», «жирный яд» или «жировая кислота». Результаты этих исследований были опубликованы им в 1822 году в монографии, описывавшей 155 случаев отравления у человека и эксперименты на животных, в соответствии с которыми делался вывод о том, что действие токсина заключается в нарушении передачи импульса в волокнах периферической и автономной нервных систем. Кернер также предположил биологическое происхождение данного яда на основании сходства действия токсина с действием атропина и змеиного яда.
В дальнейшем заболевание, возникающее в результате отравления описанным им токсином получило название «ботулизм» от лат. botulus, что означает «колбаса».
C. botulinum обитает в почве. Заболеваемость ботулизмом повсеместна. Наиболее распространены бактерии типа A и B. В природных условиях бактерии колонизируют ил на дне водоёмов, инфицируют рыб. При пересыхании водоёмов рост C. botulinum стимулируется. Таким образом, естественный резервуар для этих бактерий — почва и различные животные. Тёплый климат создаёт условия для длительного сохранения спор в почве, а также для прорастания и размножения вегетативных форм.
Попадание в человеческий организм как вегетативных форм C. botulinum, так и спор обычно не вызывает заболевания, так как для продуцирования токсина нужны строго анаэробные условия. Исключения составляют раневой ботулизм (развивается при загрязнении почвой раны, в которой создаются условия, необходимые для прорастания попавших из почвы C. botulinum и последующего токсинообразования), а также ботулизм новорождённых до 6 месяцев, в кишечнике которых также возможно размножение C. botulinum и токсинообразование из-за особенностей кишечной микрофлоры.
Возбудители ботулизма имеют форму палочек длиной 3-9 мкм, шириной 0,6-1 мк с закругленными концами. Палочки образуют субтерминально расположенные споры и имеют вид теннисной ракетки. Капсулы не образуют. Подвижны в результате перитрихиально расположенных жгутиков. Грамположительны.
Строгий анаэроб, срок культивирования 48–72 ч. На мясо-пептонном бульоне — помутнение среды с газообразованием, характерный запах прогорклого масла. На кровяном МПА — колонии крупные с корневидными отростками и зоной гемолиза. Оптимальная кислотность для роста 7,3–7,6 (для прорастания спор 6,0–7,2).
Вид C. botulinum образует экзотоксины, различающиеся по антигенным свойствам и по этому признаку подразделяются на серотипы. Ботулотоксины всех типов обладают сходной биологической активностью, являясь вариантами одного нейротоксина. Кроме нейротоксического действия, ботулотоксин обладает лейкотоксической, гемолитической и лецитиназной активностью.
Ботулотоксин[править | править код]
Известны 7 антигенных вариантов ботулотоксина: A, B, C (подтипы C1 и C2), D, E, F, G. Токсинообразование типов C, D, E закодировано в геноме конвертируемых бактериофагов и проявляется при интеграции профага в бактериальную хромосому; у остальных типов генетический контроль осуществляет непосредственно хромосома клетки.
Заболевания человека вызывают ботулотоксины типов A, B, E, а также F. В организме человека C. botulinum размножаются слабо и не продуцируют токсина за редким исключением. Ботулотоксин накапливается в пищевых продуктах, инфицированных спорами C. botulinum, при их прорастании, если созданы анаэробные условия (например, при консервировании). Для человека ботулотоксин — самый сильнодействующий бактериальный яд, губительно действующий в дозе 10−8 мг/кг. Споры C. botulinum выдерживают кипячение в течение 6 часов, стерилизация при высоком давлении разрушает их через 20 минут, 10%-ная соляная кислота — через 1 час, 50%-ный формалин через 24 часа[3]. Ботулинический токсин типа A (B) полностью разрушается при кипячении в течение 25 минут.
Токсин представляет собой полипептидную цепь с одной или несколькими внутримолекулярными связями, его молекулярная масса равна 150 000, он относится к бинарным токсинам.
Ботулотоксины всех типов продуцируются в виде токсичных белковых комплексов, состоящих из нейротоксина и нетоксичного белка. Белок является стабилизатором токсина, защищает его от разрушающего действия протеолитических ферментов и HCl.
Ботулотоксин в виде высокомолекулярного комплекса малотоксичен и является прототоксином. В результате мягкого протеолиза, осуществляемого у большинства типов токсина собственными эндогенными протеазами, а у типа E экзогенными протеазами (например трипсином), прототоксин распадается на 2 субкомпонента: L-лёгкий и H-тяжёлый. Между ними сохраняется дисульфидная связь. L-суб-компонент соответствует фрагменту A (активатор) и оказывает токсическое действие на клетку-мишень (мотонейрон). H-субкомпонент соответствует фрагменту В (акцептор) и осуществляет прикрепление к рецептору клетки-мишени.
Применение ботулотоксина[править | править код]
Ботулинический нейротоксин типа A-гемагглютинин комплекс используется в современной косметологии под торговыми названиями «Ботокс», «Диспорт», «Релатокс» и «Лантокс».
Попав вместе с пищей в желудочно-кишечный тракт, ботулотоксин прикрепляется к клеткам эпителия кишечника и путём пиноцитоза попадает в лимфатические сосуды, затем в кровь и далее проходит гематоэнцефалический барьер. В организме он распадается на 2 субкомпонента: L-лёгкий и Н-тяжёлый. Н-субкомпонент связывается с ганглиозидами пресинаптической мембраны мотонейронов. L-субкомпонент, действуя как эндопротеаза, блокирует секрецию ацетилхолина, тем самым прерываются нервные импульсы, идущие от мотонейрона к мышце, что приводит к развитию вялых параличей. Ботулотоксин поражает мотонейроны спинальных моторных центров, продолговатого мозга и периферической нервной системы.
В результате опытов, проведённых в различных условиях, выявлено, что ботулотоксин приводит к угнетению как спонтанного, так и вызванного возбуждением выброса нейромедиаторов в нервных окончаниях. При этом чувствительность рецепторов к ацетилхолину не изменяется, процессы синтеза и хранения нейромедиаторов не страдают. В результате экспериментов установлено, что в среднем для блокирования одного синапса достаточно 10 молекул ботулотоксина. Также отмечается, что более высокая нервная активность ускоряет возникновение синаптического блока. Предполагается, что поражающее действие токсина обусловлено поражением Ca² (кальциевых потенциал-зависимых ионных каналов) зависимого механизма экзоцитоза в пресинаптической мембране. В настоящее время это поражение считается необратимым, а восстановление двигательной активности происходит за счёт образования новых синаптических связей[4].
C. botulinum является сапронозом и вегетирует в почве, часто обнаруживается в кишечнике лошадей и других животных, реже встречается в кишечнике человека. Из почвы или испражнений споры возбудителя попадают на различные объекты и могут загрязнять пищевые продукты. В анаэробных условиях споры прорастают, вегетативные клетки продуцируют ботулотоксин. Чаще всего заболевание возникает при употреблении в пищу консервированных продуктов домашнего приготовления, что связано с их недостаточной стерилизацией.
Инкубационный период при ботулизме колеблется от нескольких часов до 2—5 дней (редко до 10 дней). В первые сутки отмечается тошнота, рвота, диарея. Далее преобладают нейросимптомы, связанные с поражением бульбарных нервных центров: нарушение аккомодации, двоение в глазах, затрудненное глотание, афония. При тяжёлых формах ботулизма смерть наступает от паралича дыхания, иногда от внезапной остановки сердца.
Классический способ — биологическая проба на мышах. Для опытов подбирают партию из 5 мышей. Первую заражают только исследуемым материалом, остальных — исследуемым материалом с введением 2 мл 200 МЕ антитоксической сыворотки типов A, B, C и E. При наличии в материале токсина выживает животное, получившее антитоксическую сыворотку, нейтрализовавшую токсин соответствующего типа. Для идентификации токсинов также используют РПГА с антительным диагностикумом (эритроциты, сенсибилизированные антитоксинами соответствующих типов). Серологических исследований не проводят, так как заболевание не сопровождается выработкой выраженных титров антител, что связано с незначительной дозой токсина, вызвавшей поражение.
Поскольку основной причиной возникновения заболевания является употребление различных продуктов домашнего приготовления (консервированные, маринованные, копчёные, вяленые (рыба, мясо) и др.), то в профилактике ботулизма большое значение имеет разъяснительная работа с населением. Знание оптимальных условий прорастания спор, токсинообразования, устойчивости к термическому воздействию спор позволяет определить адекватные технологические условия обработки пищевых продуктов, исключающие накопление ботулинического токсина.
Опасны не только герметично закрытые консервы, но и те продукты, в кишечнике, тканях мышц которых также созданы анаэробные условия. C. botulinum погибают в очень кислой среде, но создать такие условия в пищевых продуктах нельзя (невкусно). C. botulinum — анаэроб, то есть не размножается в присутствии кислорода, поэтому консервы, приготовленные в открытых условиях, безопасны (например, грибы, засоленные в открытых вёдрах, бочках). Вместе с тем, описаны случаи ботулизма при поедании рыбы (омуля), засоленного в бочках, хранившегося в ненадлежащих температурных условиях (т. н. "омуль с душком"), а также копчёной рыбы, хранившейся также в ненадлежащих температурных условиях.
Как быть с герметично закатанными консервами? Можно бороться с уже имеющимся токсином. Он термолабилен. При длительном (более получаса) кипячении токсин разрушается, следовательно, прошедшие такую термообработку продукты безопасны (в случае приобретения продукта, например, копчёной рыбы, и транспортировке его в теплых условиях, перед употреблением такого продукта необходимо прогреть на сковороде с обеих сторон - каждую сторону - минимум по 15 минут).
Споры C. botulinum находятся в земле. Из этого следует, что продукты перед консервированием надо тщательно мыть. Споры очень живучи: они выживают даже при кипячении. При промышленном производстве применяют стерилизацию в автоклавах при 120 °C[5]
Рост бактерий может быть предотвращен высокой кислотностью, высоким содержанием сахара, высоким уровнем кислорода, очень низким уровнем влажности или хранением при температуре ниже 3 °C для типа A. Например, при низкой кислотности, консервированные овощи, такие как зелёный горошек, которые не были нагреты достаточно, чтобы убить споры, могут обеспечить бескислородную среду для развития спор и производства токсина. С другой стороны, маринованные огурцы являются достаточно кислыми, чтобы предотвратить рост, и даже если споры присутствуют, они не представляют никакой опасности для потребителя. Мед, кукурузный сироп и другие сладкие продукты могут содержать споры, но они не могут расти в высококонцентрированном растворе сахара. Однако, в пищеварительной системе младенцев, когда эти продукты разбавляются пищеварительным соком с низким содержанием кислоты и низким содержанием кислорода, споры могут расти и производить токсин. Поэтому детям до 1 года не рекомендуется мёд. Как только дети начинают есть твёрдую пищу, пищеварительные соки становятся слишком кислыми для роста бактерий.
В случае применения ботулотоксина в качестве оружия выделяют общие методы профилактики, направленные на предотвращение попадания токсина в организм, такие, как своевременная медицинская экспертиза употребляемой воды и пищи, обеспечение личного состава индивидуальными средствами защиты органов дыхания, создание коллективных убежищ, оснащённых системами фильтрации воздуха. К специальным методам защиты относят вакцинопрофилактику. При подозрении на поражение ботулотоксином производится введение противоботулинистической сыворотки в дозе 1000—2000 МЕ внутримышечно. Следует отметить, что вакцинопрофилактика может оказаться неэффективной из-за несовпадения типа токсина и антитоксической сыворотки. Штатных антидотов и средств профилактики в настоящее время не существует. Эксперименты на животных показали некоторую эффективность 4-амлопиридина. У животных, получивших летальную дозу ботулотоксина, на 1—2 часа частично восстанавливалась двигательная активность, но впоследствии паралич дыхательной мускулатуры развивался в полном объёме. В связи с краткосрочностью действия и высокой токсичностью препарата данное вещество не рекомендовано в качестве табельного средства при поражении ботулотоксином.
- Ботокс — очищенный нейротоксиновый комплекс ботулотоксина типа A.
- Ботулизм — заболевание, вызываемое C. botulinum
- Поздеев О. К. Медицинская микробиология. — М.: ГЭОТАР-Медиа, 2007. — 768 с. — ISBN 978-5-9704-0385-3.
- Sherris, John C. Медицинская микробиология = Medical Microbiology. — 4-е изд. — McGraw-Hill Medical Publishing Division, 2004. — ISBN 0-8385-8529-9.
- Куценко С. А. Бутомото Н. В. Гребенюк А. Н. Военная токсикология, радиобиология и медицинская защита / Иванов В. Б. — Фолиант, 2004. — 528 с. — ISBN 5-93929-082-5.
Клостридии и клостридиозы - Симптомы и лечение. Журнал Медикал
Клостридии – это достаточно обширная группа микроорганизмов, представители которой являются не только причиной незначительного нарушения здоровья, но и серьезных инфекций, одно только упоминание о которых вызывает тревогу – это столбняк, ботулизм, газовая гангрена. Причем специфическая профилактика, а именно вакцинация, разработана только при столбняке, тогда как остальные болезни, вызванные клостридиями, могут поражать различные слои населения, встречаясь преимущественно в виде спорадических случаев.
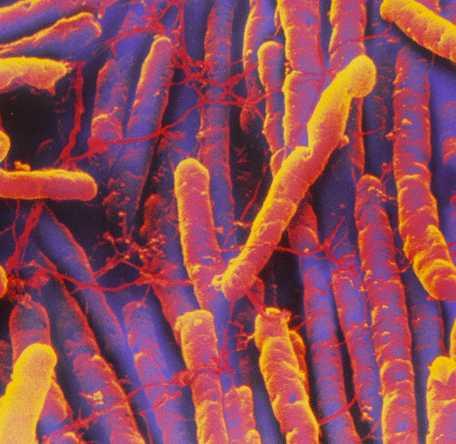
Клостридии
Описание клостридий
Клостридии (Clostridium) – это грамположительные микроорганизмы (при окраске по Грамму приобретают сине-фиолетовый цвет), относящиеся к семейству Clostridiacae, роду Clostridium. Первое описание клостридий датировано 1880 годом польским ученым микробиологом А. Пражмовским. Представляют собой палочки размером от 0,5 до 20 мкм, подвижные, обладают различной протеолитической активностью (способностью вырабатывать ферменты) в зависимости от вида. Способны образовывать споры, в результате которых приобретают форму «веретена» в связи с тем, что раздуваются в центре за счет образования эндоспоры (именно от греческого слова «веретено» и произошло их название). Особенность образовывать эндоспоры позволяет клостридиям выдерживать кипячение и быть малодоступными для антибиотиков. Иногда эндоспоры располагаются терминально, что придает клостридиям форму «теннисных ракеток». Клостридии являются анаэробами (размножаются при отсутствие кислорода).
К роду Clostridium относятся 100 и более видов бактерий. Наиболее известные из них C. botulinum (возбудитель ботулизма), C. tetani (возбудитель столбняка), C. septicum, C. perfringens, C. oedematiens, C. novyi (возбудители газовой гангрены), C. difficile, C. hystoliticum, C. sporogenes, C. clostridioforme, C. acetobutylicum, C. colicanis, C. aerotolerans, C. bifermentans, C. tertium, C. piliforme, C. laramie, C. ramosum, C. fallax, C. formicaceticum и другие.
Клостридии широко распространены в природе, могут обнаруживаться в почве, в водоемах. Некоторые клостридии (например, C. difficile) являются представителями нормальной микрофлоры некоторых систем организма человека, то есть являются сапрофитами. Чаще всего они обнаруживаются в кишечнике, на коже, слизистой оболочке ротовой полости, женской половой системы, респираторного тракта. Но все же основное место обитания – кишечник. В норме у совершенно здоровых людей количество клостридий зависит от возраста и составляет: у детей до 1 года – до 103 КОЕ/г (колониеобразующих единиц в грамме фекалий), у детей с 1 года и взрослых до 60 лет – до 105 КОЕ/г, старше 60 лет – до 106 КОЕ/г. C. difficile нередко высевают из почвы и воды, в которых, благодаря образованию эндоспор, она может сохраняться до 2х и более месяцев.
Факторы патогенности клостридий
Особенность клостридий и заболеваний, вызванных ими, это выработка токсинов и симптомы, связанные с ними, то есть клостридиозы - токсикоинфекции.
1) Токсинообразование – это фактор патогенности клостридий. Некоторые виды клостридий (C. botulinum, C. tetani, C. perfringens) продуцируют одни из самых сильных бактериальных экзотоксинов (ботулотоксин, столбнячный токсин – тетаноспазмин, ε-токсин, разрушающий эритроциты). Экзотоксины обладают нейротоксичностью (действие на нервную систему), гемотоксичностью (на эритроциты и лейкоциты), некротоксичностью (вызывает некроз тканей).
2) Другим фактором патогенности является инвазивность – способность локального повреждения тканей за счет выработки ряда протеолитических ферментов. В частности, C. perfringens способна вырабатывать протеиназу (расщепляющую белки), коллагеназу, гиалуронидазу. Такие факторы агрессии, как протеиназа, лецитиназа, гиалуронидаза, коллагеназа, являются результатом жизнедеятельности многих видов клостридий.
Главной особенностью патогенного действия клостридий является преобладание некротических процессов в тканях над воспалительными, выраженность которых минимальна. Итак, жизнедеятельность клостридий осуществляется в анаэробных (без кислорода) условиях и сопровождается выработкой токсинов, ферментов и белков, который определяют газообразование и некроз в тканях, а также общее токсическое влияние на организм больного (чаще это нейротоксическое влияние).
Общие причины заражения инфекциями, вызванными клостридиями
Источником инфекции может быть больной и носитель как человек, так и животное, с испражнениями которого клостридии попадают в почву, на дно водоемов, где могут сохраняться несколько месяцев. Механизмы заражения – алиментарный (пищевой), контактно-бытовой. В зависимости от вида клостридий и симптомов болезни заражение здорового человека происходит через определенные факторы передачи. Факторами передачи пищевого пути служат пищевые продукты (мясные продукты, фрукты и овощи, молоко и молочные продукты), для ряда болезней, как ботулизм например, это продукты с созданием анаэробных условий без предварительной термической обработки (консервы, соления, копчености, вяленые продукты, колбасы домашнего приготовления). Контактно-бытовой механизм реализуется через раневой путь инфицирования, когда споры клостридий определенных видов попадают на поврежденные кожные покровы. Также описаны случаи болезней новорожденных (в условиях нарушения правил стерильности), что бывает при столбняке, ботулизме и других клостридиозах.
Заболевания, вызванные клостридиями
Ботулизм (С. botulinum)
Столбняк (С. tetani)
Газовая гангрена (С.perfringens тип А, С.septicum, C.oedematiens, C.novyi)
Псевдомембранозный колит (C.difficile, С.perfringens тип А)
Антибиотикоассоциированные диареи (C.difficile)
Некротический энтерит, пищевая токсикоинфекция (С.perfringens тип А)
Ботулизм (возбудитель С. botulinum) – острое инфекционное заболевание, характеризующееся поражением нервной системы с развитием парезов и параличей гладкой и поперечнополосатой мускулатуры. Главная особенность возбудителя – способность вырабатывать один из сильнейших микробиологических ядов – ботулотоксин, который и запускает развитие всех симптомов болезни. Более подробно по поводу данного заболевания в статье «Ботулизм».
Столбняк (возбудитель С. tetani) – также острая инфекционная болезнь с поражением нервной системы и тоническим сокращением мышц поперечнополосатой группы. Данный возбудитель также имеет отличительную особенность – выработку сильного токсина – столбнячного экзотоксина, обуславливающего тяжелую клинику заболевания. Подробнее о столбняке в статье «Столбняк».
Газовая гангрена (возбудители С.perfringens тип А, С.septicum, C.oedematiens, C.novyi) – инфекция, которая развивается в анаэробных условиях при активном участии некоторых видов клостридий, которая развивается на обширных участках поврежденных тканей. Развивается после обширных ранений, травм, травматических ампутаций, огнестрельных ранений. Сроки появления газовой гангрены – первые 2-3 дня с момента ранения или другой тяжелой травмы. В очаге инфекции клостридии находят благоприятные условия для размножения (отсутствие кислорода, омертвевшие клетки и ткани), выделяют токсины, вызывая интоксикацию всего организма и возможное поражение токсинами других органов и систем. У пациента в местном очаге наблюдается отек тканей, газообразование, омертвление тканей, распространение процесса на здоровые участки. Выделяют несколько форм – классическая, отечно-токсическая, гнилостная и флегмонозная. Помощь пациенту нужно оказывать как можно скорее, иначе распространение процесса может стоить больному жизни.
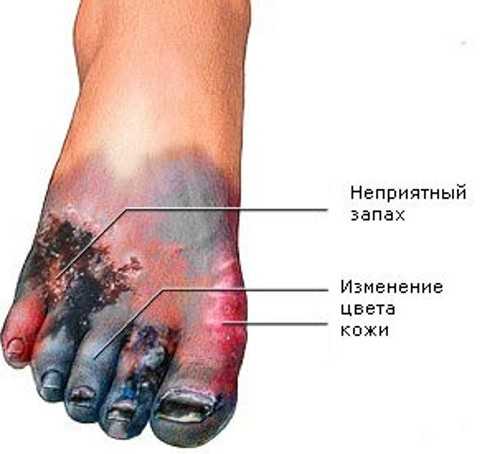
Газовая гангрена
Псевдомембранозный колит или ПМК (вызывается чаще C.difficile, но может играть роль и С.perfringens тип А). ПМК также развивается вследствие антибиотикотерапии, частыми виновниками которой являются линкомицин, ампициллин, тетрациклин, левомицетин, клиндамицин, реже цефалоспорины. Следствием такого лечения является грубый дисбактериоз кишечника с выраженной активностью одного из рассматриваемых нами микробов - C.difficile. Жизнедеятельность клостридии вызывает воспаление слизистой оболочки кишечника, в основном дистального его отдела, образованием так называемых «псевдомембран» - фибринозных налетов на слизистой оболочке. Такие нарушения грозят развитием осложнения – прободения стенки кишечника, что может привести к летальному исходу. Группы риска по развитию ПМК: лица преклонного возраста (старше 65 лет), а также лица с сопутствующими заболеваниями (онкология, пациенты после оперативных вмешательств и другие). У пациента развивается температура и интоксикация (слабость, головная боль), однако эти симптомы необязательны. Также характерно расстройство стула, который становится частым, водянистым. У ослабленных пациентов могут возникнуть симптомы обезвоживания. Стул может напоминать изменения при холере (водянистый беловатого цвета, частый и обильный), однако в тяжелых случаях при сильном болевом синдроме может появиться стул с примесью крови.
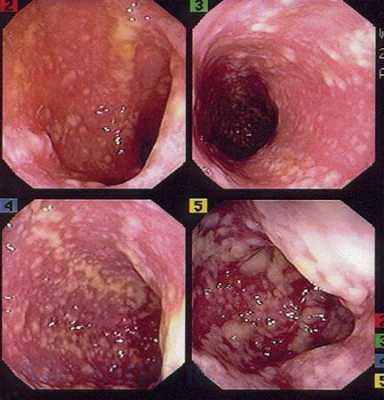
Эндоскопическая картина ПМК
Антибиотикоассоциированные диареи или ААД (вызываются C.difficile, С.perfringens), однако может быть микробная ассоциация с грибами рода Candida, клебсиеллой, стафилококком и другими. Чаще регистрируются в условиях лечебных учреждений среди пациентов, требующих антибиотикотерапии в силу того или иного заболевания. Именно в этих условиях и формируются устойчивые к лекарственным препаратам виды клостридий. Наблюдаются чаще при назначении препаратов широкого спектра (цефалоспорины, ампициллин и других). Возникают антибиотикоассоциированные диареи за счет сочетанного подавления роста как патогенной, так и сапрофитной (вполне нормальной) микрофлоры пищеварительной системы человека. Риск возникновения такой диареи не связан напрямую с количеством антибиотика в организме (она может возникнуть и при первом приеме, и при повторных введениях лекарства). Группы риска по развитию ААД – пациенты, принимающие цитостатики и имеющие иммунодефицит.
Симптомами ААД являются высокая температура и интоксикация (слабость, недомогание), появление водянистого стула с патологическими примесями (слизь, иногда кровь), боли в околопупочной области, а затем по всему животу. При заражении C.difficile нередки случаи повторной клиники (рецидива) через 4-6 дней в силу устойчивости спор клостридий к лечению. У детишек первых 3х месяцев, учитывая малую обсемененность кишечника и находящихся на грудном вскармливании ААД возникает редко.
Некротический энтерит (причиной является С.perfringens типа F). Некротоксин клостридии вызывает некроз стенки кишечника и образованием эррозированных поверхностей и язв (то есть разрушение стенки кишечника). В месте поражения наблюдаются воспалительные изменения с отеком слизистой. Есть опасность кровотечения и прободения язвы, а также развития тромбоза мелких сосудов. Пациенты жалуются на температуру, рвоту и жидкий стул с кровью и обилием пены.
Пищевая токсикоинфекция, вызванная С.perfringens длится несколько дней. Клинически мало отличий от токсикоинфекции другой этиологии. Симптомы болезни обусловлены токсином клостридии и появляются через несколько часов (чаще это 6-12 часов) с момента употребления в пищу недоброкачественных продуктов питания ( чаще мясные продукты). Пациенты предъявляют жалобы на жидкий стул, тошноту, редко рвоту, болезненность в животе.
Поражение мочеполовой системы. В некоторых случаях клостридии могут явиться первопричиной развития острого простатита.
Клостридиальный сепсис может развиться при распространении большого количества токсинов по организму и токсического поражения различных органов и систем, в том числе и жизненноважных (почки, головной мозг, печень).
Диагностика клостридиозов
Предварительный диагноз ставится на основании симптомов конкретной клинической картины, связи заболевания с какой-либо обширной травмой, назначением антибиотиков, употреблением в пищу характерных продуктов питания и тому подобное. Диагноз подтверждается после лабораторной и инструментальной диагностики.
Лабораторная диагностика включает в себя:
1) Бактериоскопия первичная материалов для исследования.
2) Бактериологический метод, при котором происходит идентификация возбудителя. Материалом для исследования служит отделяемое из ран, испражнения и другие в зависимости от клинической формы. При сепсисе это может быть кровь, моча. Материал засевают на селективные питательные среды (например, среда Кита-Тароцци) и выращивают в анаэробных условиях.
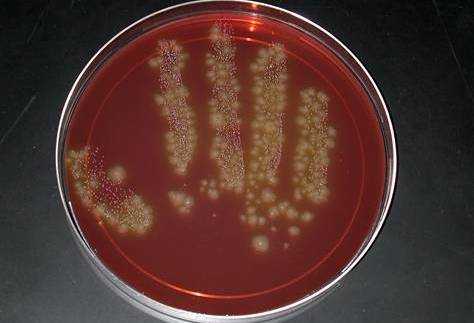
Клостридии при бакпосеве
3) Биологическая проба для выявления токсинов клостридий, с целью которой применяется реакция нейтрализации специфическими антитоксическими сыворотками.
4) Параклинические методы исследования (общий анализ крови, мочи, копрограмма, биохимические исследования крови).
5) Инструментальная диагностика. При рентгенологическом исследовании можно обнаружить скопление газа в подкожном пространстве и мышечной ткани, что наведен на предварительные выводы о клостридиях (газ можно обнаружить и при других анаэробных инфекциях). При ПМК проводят эндоскопическое исследование, при котором видна картина очагового или диффузного (распространенного) колита с образованием псевдомембран.
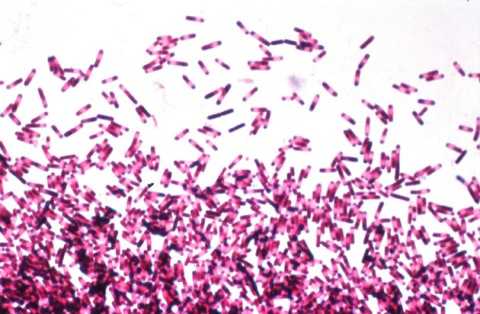
clostridium difficile под микроскопом
Лечение клостридиозов
Пациенты с клостридиозными инфекциями подлежат госпитализации по показаниям и тяжести.
Такие заболевания, как ботулизм, столбняк, газовая гангрена лечатся только в стационаре и требуют немедленной помощи с целью спасения жизни пациента. Некоторые виды диарей являются госпитальными, поэтому также лечатся в стационаре.
Медикаментозная помощь включает в себя:
1) Введение специфических препаратов с целью нейтрализации токсинов при ботулизме (противоботулиническая сыворотка, иммуноглобулин) и столбняке (противостолбнячная сыворотка, иммуноглобулин). Эти препараты подлежат тщательному расчету и постановке строго под наблюдением врача в больнице. Сыворотки чужеродные, поэтому должна быть готовность к возможному проведению противошоковых мероприятий.
2) Антибактериальная терапия, с целью которой назначаются антибиотики, к которым клостридии имеют чувствительность. К ним относятся: нифуроксазид, метронидазол, рифаксимин, тинидазол, доксициклин, тетрациклин, клиндамицин, кларитромицин, пенициллин, левофлоксацин. Выбор препарата остается только за лечащим доктором, который заподозрил и подтвердил диагноз определенной клинической формы клостридиозной инфекции. Для лечения антибиотикассоциированных поражений кишечника лекарственный препарат, вызвавший данное состояние, отменяют. Для этиотропной терапии может быть рекомендован ванкомицин для приема внутрь, метронидазол.
3) Хирургический метод лечения (актуален при газовой гангрене) и сводится к иссечению поврежденных участков раны с последующей антибактериальной санацией.
4) Симптоматическое лечение в зависимости от клинического синдрома (это могут быть пробиотики, уросептики, гепатопротекторы, жаропонижающие, противовоспалительные и другие группы препаратов).
Профилактика клостридиозов
Одно из важных правил – тщательное соблюдение правил личной гигиены в домашних условиях и в социальной среде: обработка рук после туалета, тщательная обработка продуктов питания, в том числе и термическая. Профилактические меры относятся и к медицинским работникам: контроль и динамическое наблюдение за назначением антибактериальных препаратов, особенно ослабленным пациентам отделений реанимации, онкогематологических стационаров, реципиентам органов и тканей.
Врач инфекционист Быкова Н.И.
Clostridium perfringens — Википедия
Материал из Википедии — свободной энциклопедии
| Clostridium perfringens | |||
|---|---|---|---|
| Clostridium perfringens, окраска по методу Грама | |||
| |||
| Clostridium perfringens (Veillon and Zuber 1898) Hauduroy et al. 1937 | |||
Clostridium perfringens (лат.) — вид грамположительных, облигатно (строго) анаэробных (за исключением C. perfringens типа A) спорообразующих бактерий рода клостридий. Возбудитель пищевых отравлений человека, один из возбудителей газовой гангрены. Является санитарно-показательным организмом. Открыта в 1892 году Уэлчем и Нетталом.
Морфология[править | править код]
Крупные (0,8—1,5 × 4—8 мкм) полиморфные палочковидные грамположительные бактерии. Споры овальные, расположены центрально либо субтерминально. Неподвижны, в организме человека образуют капсулу. Образуют стабильные L-формы, способные расти на поверхности стекла[1].
Культуральные свойства[править | править код]
Зоны преципитации вокруг колоний C. perfringens на желточном агареХемоорганогетеротроф, облигатный анаэроб. Растёт на простых питательных средах в анаэробных условиях. На агаризованных средах образуются круглые колонии 1—2 мм в диаметре с гладким или зубчатым краем. Колонии, выросшие в толще агара, имеют чечевицеобразную форму. В жидкой среде — помутнение с дальнейшим просветлением среды и образованием беловатого хлопьевидного осадка. На среде Китт-Тароцци — помутнение с обильным газообразованием. На кровяном агаре образуются круглые гладкие сероватые колонии, постепенно зеленеющие и окружённые зоной гемолиза β-типа. На желточном агаре ввиду образования лецитиназы образуются зоны преципитации. Сбраживают с активным газообразованием глюкозу, лактозу, мальтозу и сахарозу. Образует масляную кислоту в ходе ацетобутиратного брожения, способен восстанавливать нитраты[2].
Геном[править | править код]
В 1989 году было проведено физическое картирование генома C.perfringens с использованием метода пульс-электрофореза[3], в 2001 году была определена нуклеотидная последовательность всего генома C.perfringens штамма 13, этот геном представлен одной кольцевой двуцепочечной молекулой ДНК размером 3031430 п.н. Доля пар Г+Ц составляет 28,6%. Количество открытых рамок считывания составляет 2660. Также имеется плазмида pCP13 размером 54310 п.н., которая содержит 63 открытые рамки считывания[4]. Геном C.perfringens ATCC13124 представлен кольцевой двуцепочечной молекулой ДНК размером 3256683 п.н. и содержит 3015 генов, из них 2899 кодируют белки. Доля пар Г+Ц составляет 28,37%[5]. У C. perfringens штамма E88 геном размером 2799250 п.н. и содержит 2372 открытых рамок считывания[6]. Охарактеризованы гены энтеротоксинов C. perfringens[7], гены токсинообразования могут находиться как на хромосоме, так и на плазмидах[8] и являются транспозибельными элементами[9].
C. perfringens является возбудителем пищевых отравлений человека и одним из возбудителей газовой гангрены. Синтезируют протеиназы, лецитиназу, коллагеназу, гиалуронидазу и другие ферменты агрессивности. Продуцируют также токсины[10][11][12]. α-токсин является фосфолипазой С, обладающей гемолитическими свойствами[13], ε-токсин является белком размером 300 аминокислот, образующий поры в мембранах эпителиоцитов кишечника человека и вызывающий выход ионов K+ и воды из клетки, LD50 для мышей составляет 0,1 мкг на кг веса[14].
Клостридии
СТАЙЛАБ предлагает комплексные тест-системы для анализа клостридий в пищевых продуктах и продовольственном сырье методом ПЦР.
Клостридии – это анаэробные спорообразующие грамположительные бактерии. Они способны жить и размножаться только в отсутствие кислорода. Некоторые из этих бактерий входят в состав нормальной микрофлоры кишечника человека и животных, другие обитают в почве. Клостридии используются для производства спиртов и органических кислот.
Среди патогенных клостридий – возбудители таких заболеваний, как газовая гангрена, столбняк, ботулизм, псевдомембранозные колиты, некротические энтериты. Белковые токсины клостридий – ботулотоксины, тетаноспазмин (тетанотоксин, столбнячный токсин) и ε-токсин относятся к сильнейшим ядам органического происхождения, известным в настоящее время. В пищевых продуктах чаще всего встречаются два представителя клостридий: Clostridium botulinum и Clostridium perfringens.
Clostridium botulinum – это подвижная палочковидная бактерия, обитающая в иле и почве, иногда в организмах рыб. Она не размножается в присутствии кислорода. Однако бескислородная среда консервированных продуктов позволяет Clostridium botulinum размножаться и вырабатывать ботулотоксины. Эти яды разрушаются при кипячении в течение получаса и в щелочной среде (например, в растворе пищевой соды) в течение 1 часа, но проявляют устойчивость к желудочному соку. Наиболее токсичный из ботулотоксинов – ботулотоксин А. Его молекула имеет два связанных между собой домена. После попадания в организм одна часть молекулы превращается в канал в мембране нервной клетки. Вторая часть молекулы отделяется от первой и проникает в клетку по этому каналу, где необратимо препятствует выделению нейромедиатора ацетилхолина. Это приводит к нарушению нервной и нервно-мышечной передаче сигнала и, как следствие, расслаблению мышц. Пострадавшие умирают от остановки дыхания. Скрытый период отравления, во время которого не проявляются никакие его симптомы, зависит от дозы токсина и составляет от нескольких часов до нескольких суток. Отравление ботулотоксином не всегда приводит к смерти, однако противоядия против этого яда не существует. Лечением является симптоматическая и поддерживающая терапия в условиях больницы.
Clostridium botulinum попадает в продукты при нарушении правил их переработки, чаще всего, с землей. Заражены ей могут быть колбасные изделия, консервы из мяса, рыбы, овощей и грибов. Кроме того, иногда эта бактерия встречается в меде. Clostridium botulinum может выжить в пищеварительной системе маленьких детей (до 1 года). В этом случае она становится причиной детского ботулизма. Скрытый период заболевания длится несколько недель, после чего наступает отравление ботулотоксином. У взрослых людей со сниженным иммунитетом, после операций на брюшной полости и с некоторыми другими состояниями также может встречаться такой тип ботулизма.
Ботулизм может возникать не только у людей, но и у животных, зачастую приводя к их гибели. Помимо употребления продуктов, зараженных Clostridium botulinum, отравление ботулотоксином может наступать в результате попадания этого вещества на слизистые оболочки, роговицу глаз, в раны, а также при его вдыхании.
Ботулотоксин А используют в медицине и косметологии в качестве миорелаксанта.
Clostridium perfringens патогенна для человека и животных и является возбудителем пищевых токсикоинфекций, некротических энтеритов, а также газовой гангрены. Эти бактерии обитают в почве и воде, в том числе, в сточных водах. Они способны выживать в кишечнике человека и животных, и их присутствие не всегда приводит к заболеваниям. Clostridium perfringens типа А, в отличие от других бактерий этого вида, относительно устойчива к воздействию кислорода.
Clostridium perfringens выделяет множество ядов с некротическим и гемолитическим (вызывает разрушение клеток крови) действием. Наиболее токсичным из них является выделяемый сероварами B и D ε-токсин (эпсилон-токсин), образующий в клетках каналы, по которым из них выходят ионы калия. Это приводит к отеку различных органов, в том числе, мозга и нарушению их работы. Clostridium perfringens серовара A вызывают относительно легкие пищевые токсикоинфекции.
Clostridium perfringens нередко встречается в сыром мясе животных и птицы и консервах из него. С загрязненной водой эта бактерия может попадать в овощи и фрукты.
В Российской Федерации и странах Таможенного Союза содержание клостридий в пищевых продуктах регламентировано Техническим Регламентом Таможенного Союза ТР ТС 021/2011 «О безопасности пищевой продукции», ТР ТС 034/2013 "О безопасности мяса и мясной продукции" и другими законодательными документами. С актуальной информацией можно ознакомиться на сайте compact24.com
Микробиологические методы анализа клостридий и других анаэробов довольно трудоемки: в присутствии кислорода эти организмы не размножаются, потому необходимо создать им бескислородные условия. Для этого используют различные подходы: культивирование в жидких средах в специальных высоких пробирках или посев внутрь столбика агара, замена воздуха в пробирке углекислым газом, добавка в среды веществ, поглощающих кислород, запаивание пробирок, культивирование под вазелиновым маслом и др. После выделения культуры микроорганизма необходимо определить его биологическими методами, оценив биохимические свойства бактерий или иным методом. Определение ДНК с помощью ПЦР является самым точным способом определения микроорганизма.
Литература
- О.К. Поздеев. Медицинская микробиология. Москва, ГЭОТАР-МЕД, 2001.
- Clostridium botulinum. International Program on Chemical Safety. Poisons Information Monograph 858 Bacteria. World Health Organization.
- Shukla, HD; Sharma, SK. Clostridium botulinum: a bug with beauty and weapon. Crit Rev Microbiol 31 (1): 11–8. 2005
- Knapp O, Maier E, Benz R, Geny B, Popoff MR. Identification of the channel-forming domain of Clostridium perfringens Epsilon-toxin (ETX). Biochim Biophys Acta. 2009 Dec;1788(12):2584-93.
- Epsilon Toxin of Clostridium perfringens. The Center for Food Security and Public Health. Iowa State University. 2004.
возбудители газовой гангрены. Пути передачи. Clostridium perfringens, novyi, septicum. Таксономия. Микробиология. Фото
Клостридии - возбудители газовой гангрены. Пути передачи. Clostridium perfringens, novyi, septicum. Таксономия. Микробиология. ФотоГазовая гангрена (газовая флегмона) — это чрезвычайно тяжелый инфекционный процесс, развивающийся при инфицировании ран анаэробными патогенными бактериями рода Clostridium. Заболевание сопровождается тяжелой интоксикацией, быстро прогрессирующим омертвением (некрозом) тканей, отеком и газообразованием.
Клостридии обитают в земле, их много в уличной пыли. Предрасположены к заболеванию травмированные люди с обширными участками размозжения мышечной ткани, где резко снижено кровоснабжение и образуется множество «карманов». Бактерии размножаются только в среде, где отсутствует кислород. При попадании в кислородную среду микроорганизмы образуют споры и в таком состоянии сохраняются многие десятилетия. Они обитают в кишечнике человека и травоядных животных, с калом попадают в грунт, и далее с уличной пылью распространяются по объектам внешней среды. При благоприятных условиях клостридии активизируются и начинают интенсивно размножаться. Из множества видов клостридий, в основном, только 7 вызывают газовую гангрену. 70-80% всех заболеваний приходится на Clostridium perfringens. Основной метод лечения заболевания — хирургический. Производятся вскрытие раны лампасными разрезами. При прогрессировании заболевания конечность ампутируется.
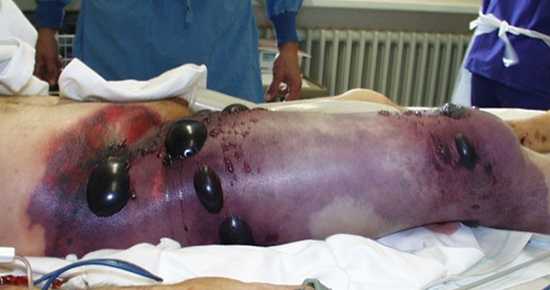
Рис. 1. На фото газовая гангрена нижней конечности.
Эпидемиология
На сегодняшний день описано около 80 видов бактерий рода Clostridium. Причиной газовой гангрены у человека являются лишь патогенные виды клостридий: Clostridium perfringens (70 — 80% всех случаев заболевания), Clostridium novi и Clostridium septicum. Описаны также другие виды патогенных бактерий рода Clostridium, но они встречаются значительно реже. Все микроорганизмы являются облигатными анаэробами — растут и размножаются в условиях отсутствия доступа кислорода.
При неблагоприятных условиях бактерии образуют споры. В таком состоянии они могут пребывать значительное количество времени. Споры устойчивы к солнечному свету, высушиванию и высокой температуре. Рост и развитие клостридий происходит только в анаэробных условиях. Восприимчивы к заболеванию человек и все виды животных.
Источники инфекции
Клостридии постоянно присутствуют в почве, кишечнике человека и травоядных животных, в ряде случаев при плохой гигиене бактерии можно обнаружить на кожных покровах.
Пути передачи
Газовая гангрена развивается при инфицировании клостридиями обширных размозженных ран (огнестрельных, рвано-ушибленных), чаще нижних конечностей и туловища, ранениях толстого кишечника. Бактерии проникают в поврежденные ткани с землей, пылью, через обрывки одежды, осколки снарядов, при оперативных вмешательствах, инъекциях лекарственных препаратов, внебольничных абортах. При шахтных и транспортных травмах ранения чаще возникают в области ягодиц и бедер. Подвержены заболеванию лица, травмированные крупным рогатым скотом, свиньями, овцами и козами. Раны при этом загрязняются навозом животных. В некоторых случаях заболевание развивается при небольших, но загрязненных порезах. Заболевание развивается быстро. Первые его признаки появляются уже с первых суток травмирования.
Рис. 2. 90% всех случаев заболевания газовой гангреной приходится на Clostridium perfringens.
к содержанию ↑Клостридии
Клостридии — факультативные анаэробы (бактерии растут и размножаются при отсутствии доступа кислорода). Являются сапрофитами. Освобождают природу от мертвого органического материала через процессы брожения и гниения. Они присутствуют в кишечнике животных и человека, где питаются органическими остатками, но не инвазируют (проникают) в живые здоровые ткани.
Клостридии — это бактерии палочковидной формы (бациллы), продуцирующие целый ряд токсинов и ферментов, образующие при неблагоприятных условиях споры. Патогенные формы возбудителей вызывают такие грозные заболевания, как столбняк, ботулизм и газовую гангрену. Они вырабатывают самые сильные из известных ядов — тетаноспазмин (Clostridium tetani), ботулотоксин (Clostridium botulinum) и а-токсин (Clostridium perfringens).
Основными возбудителями газовой гангрены являются Clostridium perfringens (70 — 80% случаев), Clostridium novyi (20 — 43%) и Clostridium septicum (5 — 18%). Значительно реже встречаются такие виды клостридий, как Clostridium histolyticum, Clostridium sordellii, Clostridium difficile, Clostridium fallax и др.
Газовая гангрена практически всегда является смешанной инфекцией. Часто при инфицировании к клостридиям присоединяются аэробные микроорганизмы: стрептококки, стафилококки, кишечная палочка, протей и др.
Таксономия клостридий
Возбудители газовой гангрены относятся к семейству Bacillaceae, роду Clostridium. К роду Clostridium относятся многочисленные (около 80) видов клостридий.
Морфология
Возбудитель газовой гангрены — грамположительная палочка. Бактерии обычно подвижны, имеют капсулу. некоторые виды клостридий лишены капсулы, но имеют жгутики. Самая большая по размеру из всех клостридий является С. novyi. Все остальные бактерии значительно меньших размеров.
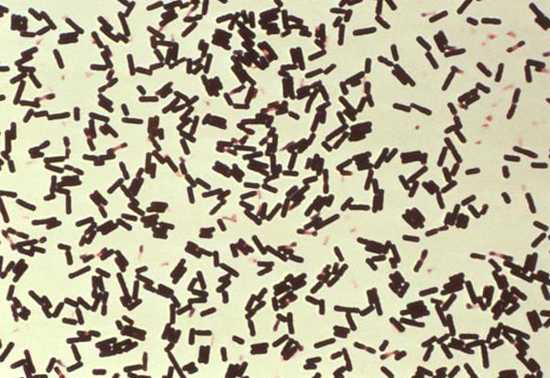
Рис. 3. Возбудители газовой гангрены Clostridium perfringens (мазок чистой культуры) под микроскопом.
Спорообразование клостридий
Клостридии при неблагоприятных условиях образуют споры, расположенные центрально или субтерминально. При центральном расположении спор палочка становится похожей на веретено (closter — веретено).
Споры клостридий устойчивы к высушиванию, высокой температуре и солнечному свету. Они способны выживать в солевых растворах, переносить длительное кипячение, промораживание, ультрафиолетовое облучение, радиацию и вакуум. Споры проявляют устойчивость к целому ряду токсических и дезинфицирующих веществ.
В спорообразном состоянии бактерии могут находиться сотни лет. При благоприятных условиях внешней среды споры прорастают. Процесс прорастания длится 4 — 5 часов.
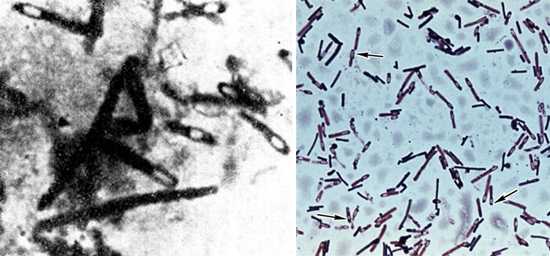
Рис. 4. Споры Clostridium perfringens.
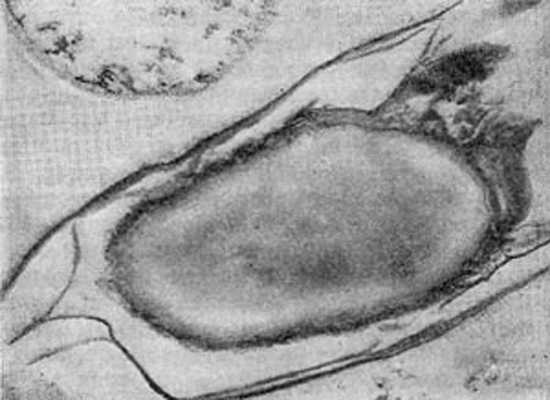
Рис. 5. На фото спора клостридии. В ее сердцевине находится покоящаяся вегетативная клетка.
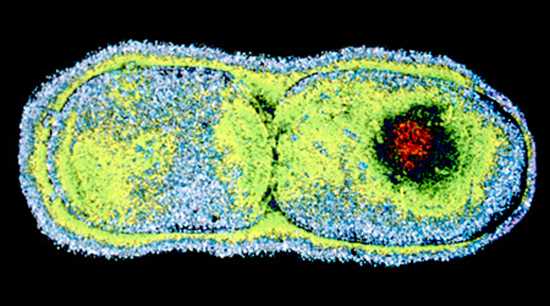
Рис. 6. Деление вегетативной клетки после прорастания споры.
Биохимические свойства и токсины клостридий
Возбудители газовой гангрены ферментируют углеводы с образованием газа и кислоты, образуют сложные экзотоксины — 12 ферментов (токсинов) и энтеротоксин, вызывающий воспаление кишечника. Бактерии делятся на шесть сероваров (А, В, С, D, E, F), каждый из которых имеет свои некротические характеристики. Серовар А является основным возбудителем газовой гангрены. Он формирует до 90% всех случаев заболевания. Основные мишени для токсинов являются мембраны клеток. Ферменты способствуют их расщеплению с последующим за этим отеком и аутолизом (саморастворением).
Бактерии типов А и С выделяют энтеротоксины, являющихся причиной пищевых токсикоинфекций и некротического энтерита.
к содержанию ↑Clostridium perfringens — основной возбудитель газовой гангрены
Газовую гангрену, пищевые токсикоинфекции и некротический энтерит у человека и животных вызывают Clostridium perfringens типов А, С и D. Аналогичные заболевания, но только у животных вызывают Clostridium perfringens типов В, С, D и Е.
Возбудитель впервые был открыт Уэлчем и Нетталом в 1892 году.
Морфология Clostridium perfringens
Бактерии имеют вид палочек с закругленными концами. Они крупные, имеют размер 3-9 × 0,9-1,2 мкм. Неподвижные. Располагаются поодиночке. Выделенные из чистых культур клостридии имеют капсулу. Окрашиваются по Граму в фиолетовый цвет. Старые культуры утрачивают эту способность. Образуют споры, сохраняющие в окружающей среде многие десятилетия.
Рис. 7. Мазок из чистой культуры Clostridium perfringens (фото слева). Спора бактерии (фото справа).
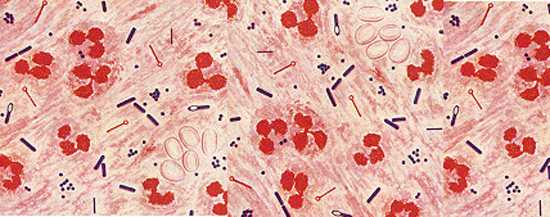
Рис. 8. На фото бактерии клостридий перфингенс и споры.
Культивирование Clostridium perfringens
Clostridium perfringens являются строгими облигатными анаэробами, хемоорганогетеротрофами. Растут на простых питательных средах — сахарно-кровяном агаре и среде Китта-Тароцци. Рост бактерий сопровождается газообразованием и снижением рН в кислую сторону.
- На сахарно-кровяном агаре бактерии образуют гладкие, блестящие, округлой формы (S-колонии), либо колонии сероватого цвета, плоские, шероховатые с зазубренными краями (R-колонии). Вокруг колоний образуется зона гемолиза. При контакте с воздухом колонии приобретают зеленоватую окраску. Колонии в толще агара приобретают чечевицеобразную форму.
- При росте в жидких средах (среда Китта-Тароцци) образуется помутнение с интенсивным газообразованием. В последующем среда просветляется и на дно выпадает беловатого цвета пластиноподобный осадок.
- При росте на желчном агаре образуются зоны преципитации.
- При росте на молоке уже через 4 часа отмечается его интенсивное сворачивание, а сгусток из-за газообразования приобретает дырчатую структуру и часто подпрыгивает вверх. Подобная реакция используется в лабораториях для проведения экспресс-диагностики.
- При росте на мясном бульоне бактерии образуют уксусную и масляную кислоты, а также большое количество таких газов, как H2S, NH3 и CО.
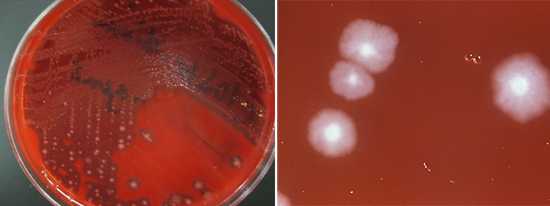
Рис. 9. Колонии Clostridium perfringens на кровяном агаре.
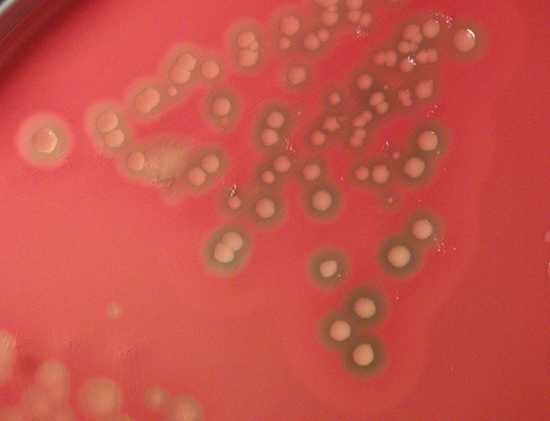
Рис. 10. C. perfringens идентифицируют по характерной «двойной зоне» гемолиза.
Биохимические свойства клостридий
Мощная ферментативная активность бактерий послужила присуждению им эпитета perfringens, что обозначает разламывающий, прорывающий. Благодаря интенсивному газообразованию происходит отек поврежденных тканей и разрывы питательных сред. Clostridium perfringens вырабатывают огромное число сахаролитических ферментов, сбраживающих глюкозу, лактозу, мальтозу и сахарозу с последующим образованием кислоты и газа. Они интенсивно створаживают молоко с последующим образованием губчатого крупноячеистого сгустка («штормовая реакция»).
Бактерии разлагают желатин, яичный белок, свернувшуюся сыворотку и коллаген. Не разлагает казеин.
В ходе ацетобутиратного брожения Clostridium perfringens синтезируют масляную кислоту, восстанавливают нитраты в нитриты, образуют лецитиназу.
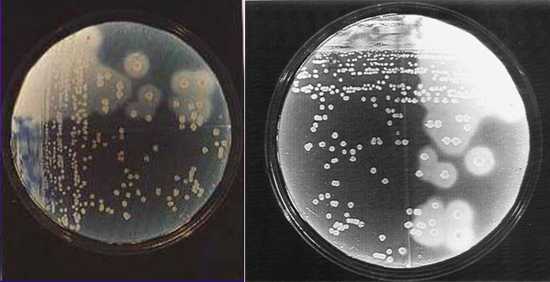
Рис. 11. Определение лецитиназной активности. Вокруг колоний отчетливо видны зоны мутного ореола, состоящие из преципитированных липидов.

Рис. 12. В левой пробирке культура Clostridium perfringens на сахарном агаре. В результате интенсивного газообразования в гелиевоподобной среде образовались зоны разрывов.
Токсинообразование
Бактерии Clostridium perfringens по спектру продуцируемых ими токсинов (ферментов) подразделяются на типы A, B, C, и Е. Газовая гангрена и пищевые токсикоинфекции чаще связаны с типом А, некротизирующий энтероколит — с типом С. Понятие «токсин» объединяет около 12 идентифицированных сегодня токсинов (ферментов) и энтеротоксин. Выброс ферментов в области поврежденных тканей приводит к расщеплению сложных веществ и нарушению клеточной проницаемости, в результате чего клетки отекают и расплавляются.
Основные экзотоксины клостридий
- а-токсин (фосфолипаза С). Более интенсивно продуцируется клостридиями типа А. Является основным и самым мощным токсином. Фермент гидролизирует (расщепляет) фосфолипиды клеточных мембран, что приводит к разрушению (лизису) клеток. Оказывает дерматонекротическое и летальное действие, является главным фактором внутритканевой инвазии и внутрисосудистого гемолиза — символа смертельной клостридиальной токсинемии. Обладает лецитиназной активностью.
- b-токсин (цитотоксин). В основном, продуцируется клостридиями типов В и С. Оказывает дерматонекротическое и летальное действие, не вызывает гемолиз. Является причиной развития некротического энтерита.
- Тета-токсин. Обладает гемолитическим и дерматонекротическим действием. Чувствителен к кислороду. Имеет схожесть с О-стрептолизином стрептококков.
- v-токсин (протеиназы). Нарушают реакции белкового синтеза путем расщепления нуклеиновых кислот.
- р-токсин (коллагеназа и желатиназа). Продуцируется клостридиями типов А, С и Е, а также некоторыми штаммами бактерий типа D. Ферменты расщепляют желатин и коллагеновые волокна соединительной ткани. Оказывают некротизирующее и летальное действие.
- Мю-токсин (гиалуронидаза). Является фактором проникновения клостридий. Ферменты расщепляют кислые мукополисахариды и гиалуроновую кислоту.
- Ню-токсин (ДНК-за). Разрушает клеточную ДНК.
- q-гемолизин. При участии комплемента разрушает мембраны эритроцитов.
- Фибринолизин. Растворяет волокна фибрина.
- Гемагглютинин. При его участии происходит реакция агглютинации эритроцитов.
- у-токсин (протеиназа). По своему действию напоминает фибринолизин. Не расщепляет нативный (природный) коллаген, но разрушает азоколл (денатурированный коллаген), казеин и желатин.
- Дельта -токсин (эластаза). Является протеолитическим ферментом. Расщепляет белки и пептиды.
- Сигма-токсин. Продуцируют клостридии типа В и С. Оказывает летальное действие, проявляет гемолитическую активность.
- Омега-токсин. Продуцируется, в основном, клостридиями типа С. Оказывает дерматонекротическое и летальное действие.
- Эпсилон -токсин. Продуцируется клостридиями типовВ и D, l-токсин — клостридиями типа Е. Проявляют летальное и дерматонекротизирующее действие.
- у- и n-токсины. Биохимическая природа этих токсинов остается неизвестной.
- р-токсин. Является фактором проницаемости тканей.
Энтеротоксин возбудителя газовой гангрены
Энтеротоксин продуцируют клостридии типов А и С.
- Энтеротоксин Clostridium perfringens штамма А представляет собой термолабильный белок, выделяющийся в тонком кишечнике в процессе образования спор. При его воздействии капилляры расширяются, повышается их проницаемость, усиливается секреция воды, ионов натрия и хлора, повреждаются мембраны энтероцитов.
- Энтеропатогенность Clostridium perfringens типа С связана с b-токсином. Заболевание протекает по типу некротизирующего энтерита.
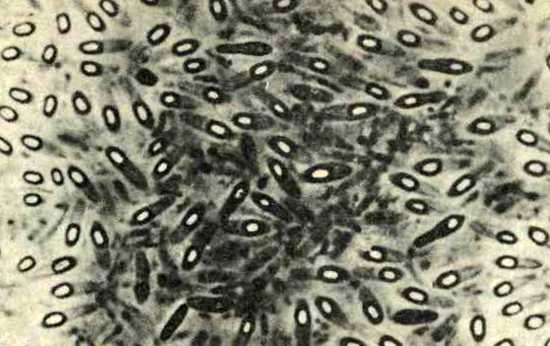
Рис. 13. При неблагоприятных условиях некоторые бактерии образуют споры. Они помогают выжить микроорганизму в неблагоприятных условиях много десятилетий. На фото споры бактерий рода Clostridium.
к содержанию ↑Clostridium novyi
Clostridium novyi являются одним из основных возбудителей газовой гангрены. В годы Великой Отечественной войны причиной газовой гангрены в 42% случаев были бактерии этого вида. Впервые выделили возбудитель и дали ему название Clostridium oedematiens Э. Сэген и М. В. Вейнберг в 1891 году. Позже более полно этот вид клостридий был описан американским бактериологом Ф. Нови, чьим именем в дальнейшем стали называть этот вид бактерий.
Морфология Clostridium novyi
Клостридии представляют собой палочки, крупные, иногда слегка изогнутые, размером 4 — 22 х 1,4 — 2 мкм, подвижные, имеют до 25 жгутиков, располагаются часто цепочками. Возбудитель, как и все клостридии, являются облигатными анаэробами. Капсулу не образуют. Окрашиваются по Граму в фиолетовый цвет (грамположительные). Старые культуры утрачивают эту способность. Образуют овальной формы споры, располагающиеся центрально и субтерминально.
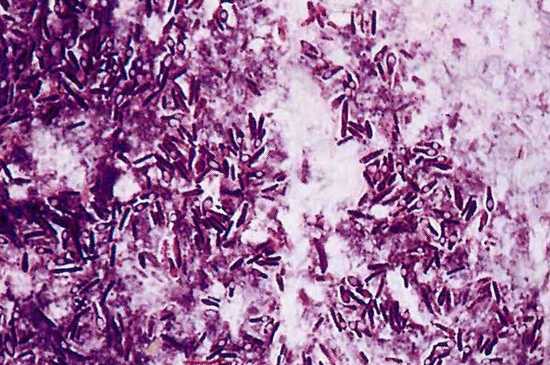
Рис. 14. Clostridium novyi. Крупные палочки, располагаются одиночно или цепочками.
Культивирование
Clostridium novyi являются строгими анаэробами. Высокочувствительны к кислороду. Растут на простых средах: углеводных, казеиновых и мясопептонных.
- При росте на плотных средах через 48 часов образуются полупрозрачные, сочные колонии сероватого цвета. Края неровные. Поверхность зернистая. Клостридии типов А, В и С иногда образуют дочерние колонии. Колонии окружены зоной гемолиза. Клостридии типа D эритроциты не разрушают.
В глубине агара колонии напоминают комочки ваты или снежные хлопья, часто окрашенные в коричневый или желтый цвет.
- При росте на жидких средах образуется газ и помутнение питательной среды, на дно выпадает осадок. рН сдвигается в кислую сторону за счет образования H2S и органических кислот.
Антигенная структура
Clostridium novyi идентифицируются по выявлению соматических антигенов. Существует 4 серовара, различные по антигенным характеристикам и синтезируемых токсинов — серовары А, В, С и D.
Биохимические свойства
Серовары типов А, В и С ферментируют фруктозу, глюкозу и мальтозу, серовары типа D ферментируют только глюкозу. Серовары типов А, С и D разлагают глицерин. Все штаммы свертывают молоко и разлагают желатин. Клостридии типа D образуют сероводород и индол, остальные типы бактерий — нет.
Токсины Clostridium novyi
Clostridium novyi продуцируют такой фермент патогенности, как фосфолипазу (а-токсин), а также b, у, сигма, е и n — токсины, обладающие некротическим, гемолитическим и летальным действиями. Нарушая проницаемость сосудов, они приводят к развитию желеобразного отека.
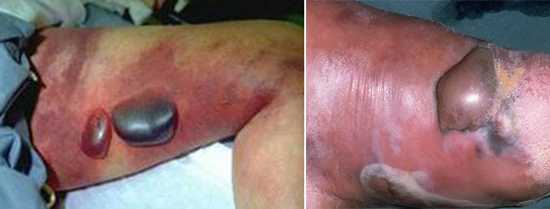
Рис. 15. На фото газовая гангрена.
к содержанию ↑Clostridium septicum
Clostridium septicum впервые были описаны в 1877 году Л. Пастером. Эти бактерии являются условно-патогенными. В обычных условиях они пребывают в кишечнике человека и не вызывают заболевание. В случае дефектов кишечника, например при колоректальном раке, инфекция повреждает кишечник и с кровью (гематогенным путем) распространяется по организму. В отличие от Clostridium perfringens газовая гангрена может возникнуть без предварительных травм и повреждений. Инфекция чаще встречается у людей с травмами и ожогами кожи, после хирургических вмешательств и септических абортах, заболеваниях периферических сосудов, сахарном диабете, раке толстой кишки.
Заболевание развивается быстро. До 80% взрослых погибает в течение первых 2-х суток. Выживаемость повышается у лиц без сопутствующих заболеваниях нижних конечностей.
Clostridium septicum поражают как человека, так и домашних животных: крупный и мелкий рогатый скот.
Морфология
Clostridium septicum представляет собой бактерию палочковидной формы. с размерами 3 — 4 х 1,1 — 1,6 мкм. В культурах иногда образуются нитевидные формы бактерий, имеющие в длину до 50 мкм в длину. Подвижны (имеют жгутики). Капсулу не образуют. Грамположительны. Со временем клостридии теряют эту особенность. Являются строгими анаэробами.
Clostridium septicum образуют споры. Споры чаще всего располагаются субтерминально, реже — центрально.
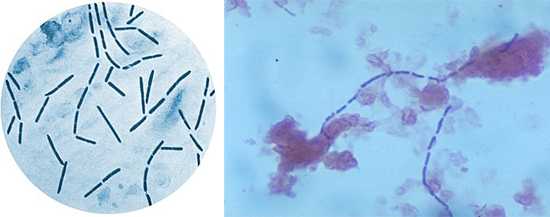
Рис. 16. Clostridium septicum под микроскопом.
Культуральные свойства
Clostridium septicum хорошо растут на казеиновых и мясных средах с добавлением глюкозы.
- На поверхности глюкозокровяного агара бактерии образуют полупрозрачные колонии, блестящие, состоящие из переплетающихся нитей с зоной гемолиза по периферии.
- При росте на 2% агаре колонии имеет вид дисков.
- При росте на агаре Цейсслера по истечении 48 часов образуется сплошной нежный налет с зоной гемолиза по периферии.
- При росте в 1% сахарном агаре колонии образуются в глубине. У них уплотненный центр, от периферии отходят переплетающиеся нити.
- При росте на мясопептонном бульоне образуется равномерное помутнение. Далее отмечается выпадение рыхлого осадка и газообразование.
- При росте на среде Китта-Тароцци бактерии растут с интенсивным газообразованием.

Рис. 17. При росте в 1% сахарном агаре колонии образуются в глубине. У них уплотненный центр, от периферии отходят переплетающиеся нити.
Антигенная структура
Clostridium septicum имеют Н и О антигены. По антигенам Н определяется 6 сероваров: А, В, С, D, E и F.
Биохимические свойства
Clostridium septicum синтезируют ряд ферментов. Они живут на различных органических субстратах, в том числе содержащих сахара и аминокислоты с выделением углекислого газа и молекулярного водорода.
Бактерии ферментируют некоторые углеводы: глюкозу, мальтозу и лактозу с образованием газа и кислоты. Нитраты переводят в нитриты. Расщепляют белки с выделением аммиака и сероводорода. Молоко под действием бактерий свертывается медленно. Не разлагают сахарозу, глицерин и маннит. Не образуют индол.
Токсины
Clostridium septicum выделяют 4 экзотоксина: а, р, у и s. обладающие некротическим, гемолитическим и летальным действиями.
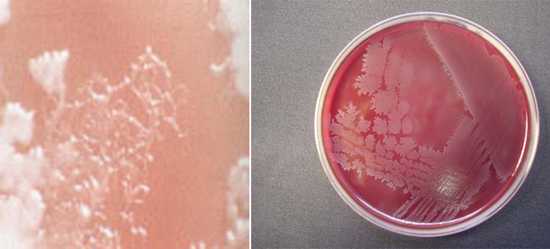
Рис. 18. Рост Clostridium septicum на питательных средах.
Что такое газовая гангрена
ПОНРАВИЛАСЬ СТАТЬЯ?
Подпишитесь на нашу рассылку!
Статьи раздела "Газовая гангрена" Новые статьи Популярные статьи Похожие статьи О микробах и болезнях © 2020 НаверхClostridium histolyticum — Википедия
| Clostridium histolyticum | |||
|---|---|---|---|
| |||
| Clostridium histolyticum (Weinberg and Séguin 1916) Bergey, Harrison, Breed, Hammer and Huntoon 1923 | |||
| |||
Clostridium histolyticum (лат.) — вид грамположительных, факультативно анаэробных, спорообразующих палочковидных бактерий рода Clostridium. Является одним из возбудителей газовой гангрены у человека и млекопитающих. Её разрушающие способности, воздействующие на мягкие ткани так велики, что по истечении 12 часов после заражения, могут просматриваться кости.
Впервые была описана в 1916 году Вайнбергом и Сегеном, которые выделили эту бактерию из субстрата больных газовой гангреной. Они назвали бактерию Bacillus histolyticus.
С греческого histolyticum переводится, как «растворяющая ткань». Ими была обнаружена высокая патогенность для морских свинок, мышей и кроликов, но в меньшей степени, для крыс. Внутримышечные инъекции бактериальной культуры вызвали сильное разрушение близлежащих тканей, внутримышечные геморрагии, расщепление кожи, обнажение костей, а иногда и автоампутацию. В 1922 году Хеллером была переименована в бактерию Weinbergillus histolyticus, а год спустя Бергей, Харрисон и др. переклассифицировали её как Clostridium histolyticum[2].
Представляет собой грамположительную спорообразующую подвижную палочковидную бактерию длиной от 3 до 5 мкм. и диаметром от 0,5 до 0,8 мкм. Относится к факультативным анаэробам[3]. Clostridium histolyticum продуцирует большие эндоспоры.
Clostridium histolyticum трудно культивировать, потому что рост ингибируется сахарами, а споры термолабильны (не устойчивы к нагреванию)[4]. В мазках раны C. histolyticum очень напоминает C. perfringens, но без капсулы. Это свойство может помешать диагностике инфекции, вызванной C. histolyticum.
Исследования показали, что токсигенность штамма Clostridium histolyticum непосредственно связана с его спорообразующей потенцией: чем выше спорообразующая потенция, тем более токсикогенным является штамм. Кроме того, токсигенные штаммы обладают более сильным потенциалом к росту, чем менее токсигенные или нетоксигенные штаммы. Гладкие субштаммы С. histolyticum, кажется, выражают более высокую токсигенность нежели, чем шероховатые субштаммы[5].
Clostridium histolyticum продуцирует 5 видов серологически идентифицируемых токсинов, часть из которых (β—δ) являются ферментами.
α-токсин[править | править код]
Альфа-токсин является главным фактором токсигенности C. histolyticum. При введении в мышцы, вызывает гибель лабораторных животных в течение нескольких часов. Обладает некротическими свойствами.
β-токсин[править | править код]
Бета-токсин — коллагеназы, разрушают связывающую ткань мышц. Коллагеназы представляют собой металлопротеазы цинка, которые расщепляют коллаген и желатин на небольшие фрагменты. Семь коллагеназ представляют собой альфа, бета, гамма, дельта, эпсилон, дзета и эта. Они далее идентифицируются по их молекулярным массам (68, 115,79,110, 125 и 130 кДа соответственно), чтобы отличить их от пяти токсинов. Бета-токсин играет важную роль в патогенности C. histolyticum, благодаря его способности разрушать коллагеновые волокна в организме и вызывать некроз. Было показано, что бета-токсин вызывает кровоизлияние при помещении на поверхность лёгких животных, кровоизлияния и отёки при введении в крысиные лапы и летальные внутрилёгочные кровоизлияния при внутривенном введении животным.
γ-токсин[править | править код]
Гамма-токсин — протеиназы, вызывают деструкцию (разрушение) и омертвение (некроз) внутренних органов, в особенности мышц.
δ-токсин[править | править код]
Дельта-токсин или эластаза, активируется ионами Ca2+. Является протеолитическим ферментом. Ингибируется цистеином. Имеет молекулярную массу в промежутке от 10 до 50 кДа[4].
ε-токсин[править | править код]
Эпсилон-токсин проявляет кислород-зависимую гемолитическую активность (лабилен к кислороду), подобно θ-токсину C. perfringens и δ-токсинам C. septicum, и C. novyi[4].