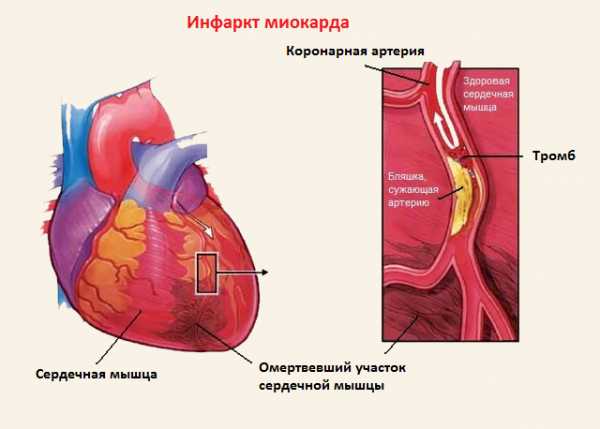
Миокардиопатия что это такое
Кардиомиопатия, или миокардиопатия – серьезная болезнь, которой на самом деле нет
Рассматриваемая патология представляет собой не до конца изученные нарушения в строении и функционировании сердечной мышцы. Пару десятков лет назад данную патологию именовали миокардиопатией, но на сегодняшний день в официальных медицинских источниках подобное название не используются.
Кардиомиопатия не имеет ограничений в возрасте и половой принадлежности, и является крайне неблагоприятной в отношении прогнозов.
Что за болезнь кардиомиопатия – механизм возникновения патологии
Для того, чтобы разобраться в сути данного заболевания, следует начать с анализа самого термина:
- «Кардио» (cardio) в переводе с греческого означает сердце.
- «Мио» — все, что связанно с мышечным слоем.
- «Патия» (pathos) – страдание.
Таким образом, разбор указанного термина практически не вносит ясности в общую картину. Любой сердечный недуг провоцирует у больного мучительные ощущения.
Видео: Кардиомиопатии — общая характеристика
Абстрагирование названия рассматриваемой болезни связано с тем, что на сегодняшний день причины кардиомиопатии точно не установлены. Это определение является собирательным для ряда признаков, которые вызывают дегенеративные процессы в сердечной мышце и желудочках сердца. Все это, в конечном счете, заканчивается сердечной недостаточностью либо нарушениями сердечного ритма.
Исследования выявляют нарушение метаболических процессов в клетках сердца. В последующем, это может стать причиной усыхания мышечных волокон, а также замещение патологических участков соединительной тканью.
Виды кардиомиопатии и причины заболевания – кто в группе риска?
В зависимости от природы возникновения данного недуга, различают:
- Идиопатическую или первичную кардиомиопатию. Что именно вызывает сердечную патологию, — в этом случае до сих пор не известно.
- Вторичную. Предполагаемыми причинами развития указанной кардиомиопатии являются:
- Наследственная предрасположенность. Человек может унаследовать генетическую аномалию, которая вызывает погрешности в структуре и функциях мышечных волокон. Исход заболевания при наследственной кардиомиопатии предугадать невозможно.
- Вирусы. В эту группу причисляют возбудителей гриппа, герпеса и пр.
- Наличие в анамнезе сведений о перенесенных ранее миокардитах.
- Сбои в функционировании эндокринной системы. Это касается пагубного влияния катехоламинов и соматропного гормона на анатомические структуры сердечной мышцы.
- Неспособность защитных сил организма полноценно выполнять свою работу.
- Вредоносное влияние на сердечную мышцу разнообразных токсинов и аллергенов. В качестве раздражителей могут выступать тяжелые металлы, некоторые медицинские средства, алкоголь, а также наркотики.
В крайне редких случаях рассматриваемый недуг диагностируют на последних месяцах беременности, либо в первое полугодие послеродового периода.
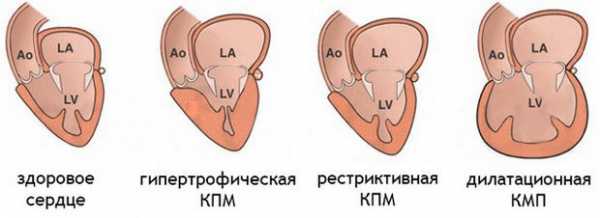
Различают 4 основных вида указанной сердечной патологии:
1. Дилатационная, или застойная
При данной форме недуга клетки миокарда на разных участках начинают отмирать. Причиной подобного явления зачастую служат воспалительные процессы.
Поврежденные вирусными агентами клетки организм воспринимает, как чужеродные тела — и старается избавиться от них. Некогда здоровая мышечная ткань замещается соединительной, которая не отличается пластичностью.
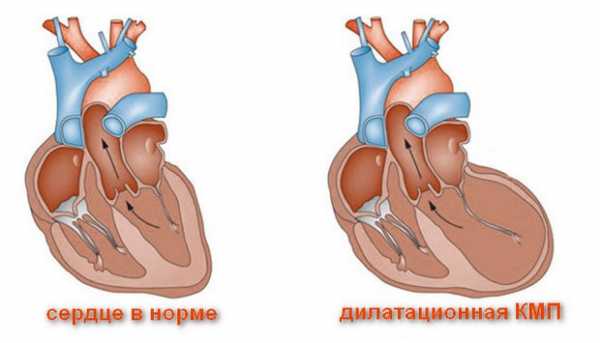
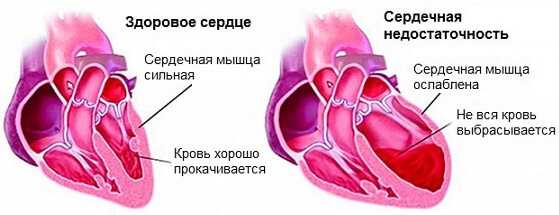
В попытках справиться со своей работой по перекачиванию крови, камеры сердца увеличиваются в параметрах. Поврежденный желудочек сердца (либо оба сразу) не способен полноценно выталкивать кровь. Это приводит к развитию застойных процессов в желудочках, что является следствием появления сердечной недостаточности.
Кроме того, сердце работает в сверхрежиме, пытаясь обеспечить кислородом все органы и системы, что ведет к развитию аритмии.
2. Гипертрофическая
Характеризуется утолщением и увеличением массы миокарда. Как правило, в дегенеративный процесс вовлекается левый желудочек, намного реже – правый желудочек и перегородка.
- Если патологические изменения затрагивают все секции сердечной мышцы, говорят о симметрической кардиомиопатии.
- При деформировании мышечной ткани в области межжелудочковой перегородки диагностируют асимметричную кардиомиопатию.
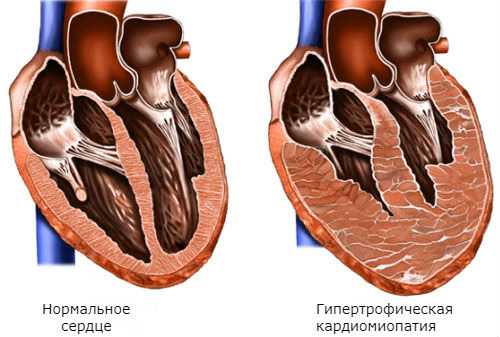
При указанной форме заболевания происходит уменьшение объемов пораженного желудочка. Из-за этого кровь не способна поместиться в желудочке, и основная ее масса сосредотачивается в предсердии, что вызывает его расширение. На фоне застойных процессов происходит кислородное голодание миокарда, что негативно сказывается на насосной функции сердца.
Видео: Гипертрофическая кардиомиопатия. Болезнь большого сердца
3. Рестриктивная
При данной разновидности рассматриваемого недуга миокард сохраняет свои размеры и толщину, однако его стенки утрачивают свою эластичность. Это приводит к неспособности полноценно перекачивать кровь.
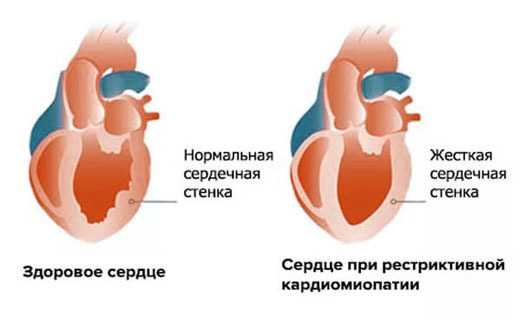
Ученные выдвигают теорию о том, что данная форма кардиомиопатии является осложнением иных патологий, но не отдельным заболеванием.
Причиной потери эндокардом своей эластичности зачастую являются воспалительные процессы. Нередко рестриктивную кардиомиопатию связывают с гормональными сбоями, а также нарушением липидного обмена.
4. Аритмическая
Центром патологических процессов в данном случае выступает правый желудочек: мышечная ткань замещается на соединительную, либо жировую. Левый желудочек также может вовлекаться в подобные деструктивные процессы.
Опасность аритмической кардиомиопатии заключается в ее последствиях: она нередко приводит к смерти больного.
Данный недуг встречается крайне редко (1 случай из 5000). Однако в зону риска попадают молодые люди, которые активно занимаются спортом.
С полученных за все годы сведений известно, что, в ряде случаев, болезнь передается по наследству (хотя и не всегда). Поэтому людям в возрасте до 40 лет, у которых близкие родственники умерли в молодом возрасте от указанного недуга, следует регулярно проходить обследование.
В некоторых медицинских источниках отдельной группой классифицируют специфические формы указанной сердечной болезни:
- Алкогольная кардиомиопатия. Под вредоносным влиянием этанола, который содержится в спиртных напитках, происходит нарушение работы полостей сердца, что с течением времени прогрессирует. Любители пива пребывают в двойной опасности. Производители добавляют в этот алкогольный продукт химическое вещество кобальт, благодаря чему образуется пышная пена. Но, по своей сути, кобальт является ядом, который провоцирует более выраженную интоксикацию, нежели этанол. При лечении алкогольной кардиомиопатии в первую очередь полностью исключают алкоголь, иначе изменения будут необратимыми.
- Ишемическая кардиомиопатия. Связана со сбоями в кровоснабжении сердечной мышцы. Симптоматическая картина проявляется не всегда, из-за чего люди редко обращаются за медицинской помощью. Однако отсутствие адекватных лечебных мероприятий может привести к обширному инфаркту миокарда. В группе риска пребывают люди преклонного возраста с начальной стадией развития атеросклероза.
- Метаболическая. Связана со сбоями в обменных процессах миокарда на клеточном уровне. Причинами подобного явления зачастую выступают интенсивные физические нагрузки, дефицит витаминов и микроэлементов, серьезные погрешности в работе почек.
- Дисгормональная. Чаще всего, диагностируются у женщин, переживающих климакс, а также у подростков в период полового созревания. Серьезных поражений сердечной мышцы в подобном случае не происходит. Лечебные мероприятия сводятся к минимизации физических нагрузок и приема седативных средств.
Видео: Кардиомиопатия
Первые признаки и симптомы миокардиопатии – как вовремя заметить?
Симптоматическая картина рассматриваемой патологии будет определяться ее разновидностью, а также степенью поражения сердечной мышцы.
При дилатационной форме наблюдаются следующие негативные явления:
- Бледность кожных покровов.
- Отечность нижних конечностей. На запущенных стадиях жидкость скапливается в легких и брюшине.
- Синюшность лица в районе ногтевой пластины пальцев.
- Сложности с дыханием даже при минимальной физической нагрузке.
- Боли в груди, которые можно устранить посредством приема нитроглицерина.
- Увеличения диаметра вен на шее.
- Повышение артериального давления. Подобным образом организм пытается компенсировать дефицит оксигена в крови.
Аналогичные жалобы присутствуют при алкогольной кардиомиопатии. Боли в груди, однако, снять при помощи нитроглицерина не удается. Симптоматика приобретает выраженные черты по мере увеличения количества алкогольных эксцессов. Жалобы не прекращаются в течение нескольких дней — либо недели — после последнего приема алкоголя.
Рестриктивная кардиомиопатия характеризуется аналогичной симптоматикой, что и у предыдущей формы заболевания. Однако по мере прогрессирования дегенеративных явлений печень увеличивается в размерах – ее можно прощупать. Сбои в сердцебиении становятся частыми и выраженными, что нередко заканчивается обмороком.
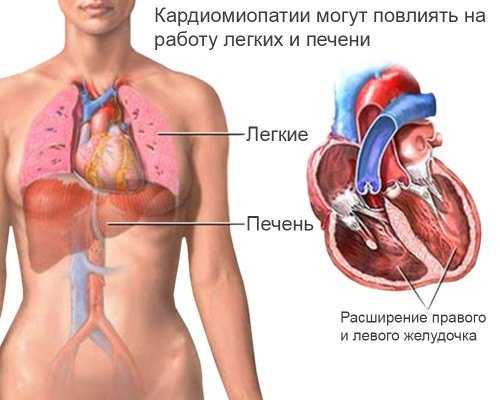
При гипертрофической кардиомиопатии жалобы у пациентов могут отсутствовать годами. К врачу обращаются, зачастую, на последних стадиях болезни, когда развивается сердечная недостаточность. Общая картина может дополняться головокружениями и обмороками.
Аритмогенная форма заболевания сопровождается сбоями в сердцебиении, что имеют приступообразную природу. Подобные патологические состояния зачастую дают о себе знать в периоды интенсивных физических нагрузок. Рассматриваемый вид кардиомиопатии считается одним из самых опасных.
Чем опасна кардиомиопатия – основные риски и прогноз
Опасность рассматриваемого недуга заключается в том, что на тех моментах, когда излечение возможно, болезнь практически никак себя не проявляет. Редко возникающие симптомы больные игнорируют, связывая их с усталостью на работе либо с определенной стрессовой ситуацией.
На запущенных стадия кардиомиопатии возникают следующие осложнения:
- Сердечная недостаточность, которая с течением времени становится все более выраженной.
- Закупорка легочных артерий тромбами, что может нарушить кровообращение и стать причиной внезапной смерти.
- Тяжелые аритмии. Также могут спровоцировать печальный для больного исход.
Дилатационная кардиомиопатия считается одной из самых редких, но в то же время — самых тяжелых форм данной патологии. Согласно статистическим данным, только в 30% случаев после установления точного диагноза наблюдается 5-летняя выживаемость.
Виды и степени блокады сердца – причины и симптомы кардиоблокады
Как бы то ни было, диагностирование указанного недуга не является поводом для паники и уныния. В первую очередь, больным следует прилежно придерживаться рекомендаций, данных кардиологом, и своевременно проходить необходимый курс лечения.
что это, виды, чем опасна, прогноз
Кардиомиопатия представляет собой недоизученную патологию сердечной мышцы. Раньше можно было услышать и такое название – миокардиопатия (от сочетания слов: миокард и патология). Но эта вольная трактовка на сегодня не применяется, поскольку в МКБ-10 кардиомиопатия занимает два раздела – I 42 и I 43.
Логичней применять название кардиомиопатии, то есть во множественном числе, поскольку даже в МКБ-10 в двух разделах приведены полтора десятка разновидностей, которые различаются как по признакам, так и по причинам возникновения.
Заметим, что патология крайне неблагоприятна в прогнозе. Высока вероятность осложнений, которые могут привести к внезапной смерти.
Содержание статьи
Что такое кардиомиопатия
Ввел термин кардиомиопатия в 1957 году британский кардиолог Уоллес Бригден (Wallace Brigden (1916 – 2008)), которому принадлежат многие новшества в лечении заболеваний сердечно-сосудистой системы. Этот термин определял группу заболеваний, причины которых не имели четких определений.Важно. Группа кардиомиопатии объединяет в себе патологии, представляющие собой избирательную деформацию сердечной мышцы (миокарда).
Суть избирательности в том, что структурно и функционально изменяется только сердечная мышца, а вот сопряженные с ней важные части организма, например, коронарные артерии, клапанный аппарат сердца, изменениям не подвергаются.
Продвижение в понимании сути кардиомиопатий было отмечено классификацией 1980 года, в которой была ссылка на неизвестное происхождение патологий сердечной мышцы. И только в 1996 году решением международного общества кардиологом была поставлена точка в определении кардиомиопатий как различных болезней миокарда, для которых характерны нарушения сердечной деятельности.
Для заболеваний характерны патологические изменения миокарда, которые проявляются сердечной недостаточностью, аритмией, быстрой утомляемостью, отечностью ног, общим ухудшением функционирования организма. Существует немалый риск развития серьезных сбоев сердечного ритма с летальным исходом.
Заболеванию подвержены люди любой возрастной категории независимо от пола. Кардиомиопатии разделены на несколько типов в зависимости от специфики влияния на мышцу сердца:
- гипертрофическая,
- дилатационная,
- аритмогенная,
- поджелудочковая,
- рестриктивная.
Все типы заболевания можно разделить на первичную (причина неизвестна) и вторичную кардиомиопатию (наследственная предрасположенность или наличие ряда заболеваний, нарушающих защитную силу организма). По статистике больше всего распространены дилатационная и рестриктивная кардиомиопатии.
Гипертрофическая кардиомиопатия – утолщение стенок левого желудочка (поражение миокарда), при этом полости остаются прежними или уменьшаются в объеме, что существенно влияет на ритмы сердца.
Дилатационная кардиомиопатия
При данном поражении сердечной мышцы, происходит расширение камеры преимущественно левого (реже обоих) желудочка сердца без утолщения сердечных стенок. За счет дилатации (растяжения) всех четырех камер, сердце увеличивается в объеме, образуются пристеночные тромбы. Эти изменения влекут за собой снижение способности желудочков к сокращению и уменьшению выброса крови в аорту (систолическая дисфункция).Снижение сократительной функции происходит по причине утолщения стенок камер за счет вкраплений рубцовой ткани, которая не имеет функциональности клеток сердечной мышцы. В результате уменьшения выброса крови в желудочках накапливаются ее остатки. Возникает застой, который приводит к сердечной недостаточности. ДКМП по причине застоя получила еще одно название – застойная кардиомиопатия.
Считается, что генетическими факторами развития дилатационной кардиомиопатии обуславливаются до 30% случаев заболеваний. Вирусная природа фиксируется статистикой в 15% случаев.
Ситуация с неравномерным утолщением стенок полостей сердца имеет и собственное название – кардиомегалия. Иначе эта патология называется “огромное сердце”. Как вариант этой формы патологии диагностируется ишемическая кардиомиопатия. Характерно что при этом диагнозе имеют место множественные атеросклеротические поражения сосудов и возможно были перенесены инфаркты (ведь рубцовая ткань в сердечной мышце откуда-то взялась).
Важно. Ишемическая кардиомиопатия не похожа на ИБС с ее загрудинными болями, а основана на расширении стенок и на ранней сердечной недостаточности. Основной удар (девять из десяти!) приходится на мужчин в возрасте до 50-ти лет или около того.
В дополнение следует отметить, что сердечная недостаточность, вызванная застоем крови (то есть застойной кардиомиопатией), часто является причиной внезапной смерти.
Статистика утверждает, что по гендерным основаниям ДКМП на 60% чаще поражает мужчин, чем женщин. Особенно это касается возрастных групп от 25-ти до 50-ти лет.
В общем случае причиной заболевания может быть:
- любое токсическое воздействие – алкоголь, яды, наркотики, противоонкологические препараты;
- вирусная инфекция – обычный грипп, герпес, вирус Коксаки и др.;
- нарушение гормонального фона – дефицит белка, витамин и т.д.;
- заболевания, вызывающие аутоиммунный миокардит – красная волчанка или артрит.
- наследственность (семейная предрасположенность) – до 30 %.
Особо стоит обратить внимание на подвид ДКМП, который называется алкогольная кардиомиопатия. Причиной развития этого специфического подвида является воздействие яда этанола. Хотя этот факт касается злоупотребления алкоголем, но само понятие “злоупотребление” не имеет четких границ. Для одного организма достаточно ста граммов, чтобы определить злоупотребление. А для другого этот объем “что слону дробина”.
Внимание! Статистика утверждает, что алкогольная форма дилатации в общем объеме всех случаев дилатационной кардиомиопатии занимает 50%. Причем хронические алкоголики никогда не признают пагубную привычку в качестве причины заболевания.
Кроме общих симптомов, для алкогольной формы характерны:
- изменение цвета лица и носа в сторону красного,
- пожелтение склер,
- возникновение бессонницы,
- ночные удушья,
- тремор рук,
- повышение возбудимости.
Рестриктивная кардиомиопатия
Этот вид заболевания носит первичный или вторичный характер поражения сердца. Это редкое заболевание миокарда (и, в редких случаях, эндокарда), проявляется в уменьшении камер сердца, не уплотняя при этом стенок и нарушая диастолическую функцию желудочков. Размеры сердца при этом не увеличиваются, или происходят лишь незначительные изменения. Увеличениям подвергаются одно или оба предсердия. В полости перикарда часто наблюдается появление жидкости.В большом круге кровообращения образуется застой крови в венах, даже при минимальной физической нагрузке появляются одышка и слабость, отечность, появляется тахикардия и парадоксальный пульс. Нарушается кардиогемодинамика (эластическая жесткость желудочков резко увеличивается) вследствие чего, внутрижелудочковое давление в венах и легочной артерии резко увеличивается.
Причины первичной кардиомиопатии
Причины, провоцирующие развитие этого заболевания, довольно разные. Первичная патология зачастую вызывается следующими факторами:
- аутоиммунные процессы, которые приводят к самоуничтожению организма. Клетки по отношению друг к другу выступают в роли «киллеров». Этот механизм запускается как при помощи вирусов, так и некоторыми патологическими явлениями, которые прогрессируют;
- генетика. На уровне развития эмбриона происходит нарушение закладки тканей миокарда, вызванное нервозностью, неправильным питанием или курением, или алкоголизмом матери. Болезнь развивается без симптомов других заболеваний за счет кардиомиоцитов, действующих на белковые структуры, принимающие участие в сокращении сердечной мышцы;
- наличие в организме большого количества токсинов (в том числе никотин и алкоголь) и аллергенов;
- плохая работа эндокринной системы;
- любые вирусные инфекции;
- кардиосклероз. Соединительные волокна постепенно заменяют клетки сердечной мышцы, лишая стенок эластичности;
- ранее перенесенные микрокардиты;
- общее заболевание соединительной ткани (заболевания, которые развиваются при слабом иммунитете, вызывая воспалительные процессы с появлением рубцов в органах).
- накопительная, которая характеризуется образованием патологических включений в клетках или между ними;
- токсическая, возникающая при взаимодействии сердечной мышцы с противоопухолевыми препаратами и получая при этом поражения; частое употребление алкоголя на протяжении длительного времени. Оба случая могут вызвать тяжелую сердечную недостаточность и смерть;
- эндокринная, которая появляется в процессе нарушения обмена в сердечной мышце, теряющее сократительные свойства, возникает дистрофия стенок. Возникает во время климакса, болезни желудочно-кишечного тракта, сахарного диабета;
- алиментарная, возникающая от неправильного питания при диетах, голодании и вегетарианском меню.
Кардиомиопатия. Симптомы и признаки
Симптомы зависят от вида самого заболевания. При развитии дилатационной КМП происходит увеличение всех четырех полостей сердца, расширение желудочков и предсердий. От этого сердечная мышца не может справляться с нагрузками.
Признаки ДКМП. Даже при минимальном физическом напряжении возникает одышка; ноги приобретают отечность, появляется чувство усталости; область вокруг рта, крылья носа, мочки ушей, пальцы на руках, лодыжки и стопы приобретают синюшный оттенок.
При гипертрофической КМП, происходит утолщение стенок сердца, что влечет за собой уменьшение в размерах самих полостей сердца. Это влияет на выброс крови при каждом сокращении. Ее количество гораздо меньше, чем необходимо для нормального кровообращения организма.
Признаки гипертрофической кардиомиопатии. Появляется тахикардия, боли в области сердца, бледный цвет лица, постоянные обмороки, слабость и одышка.
При развитии рестриктивной КМП, происходит рубцевание сердечной мышцы. Сердце никогда не может расслабиться, нарушается его работа.
Признаки рестриктивной кардиомиопатии. Кожа приобретает синюшный цвет, учащаются приступы одышки, отечность возникает не только в конечностях, но и в животе, печень подвергается увеличению в размерах. Этот тип кардиомиопатии считается самым тяжелым и редким.
Диагностика кардиомиопатии
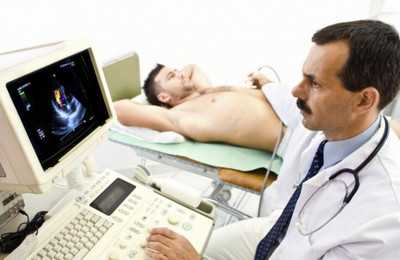 Любая диагностика – трудная и важная процедура. Диагностика сердечных заболевании не представляет собой исключение. Используются различные методы диагностирования в комплексе, так как часто на начальной стадии не предоставляется возможным сразу определить тип заболевания.
Любая диагностика – трудная и важная процедура. Диагностика сердечных заболевании не представляет собой исключение. Используются различные методы диагностирования в комплексе, так как часто на начальной стадии не предоставляется возможным сразу определить тип заболевания.Применяют рентгенографию, ЭхоКГ, холтеровское монтирование, электрокардиографию и физикальное обследование. У каждого из этих способов, есть свои плюсы и особенности. Все процедуры абсолютно безболезненны и не представляют опасности. К сожалению, насколько точным будет диагноз, зависит от квалификации специалиста, так как из-за схожести симптомов могут возникать сомнения по поводу вида КМП.
Чтобы понять степень повреждения сердца, чаще всего применяется физикальное обследование (пальпация, перкуссия, процедуры диагностики). Но, за частую, этого мало для постановки диагноза, поэтому в комплекс обследования включают дополнительные методы.
Электрокардиограмма – это графическое изображение работы сердца. При детальном изучении опытным врачом, его расшифровка дает возможность поставить точный диагноз.
Самым современным методом является диагностика с помощью ЭхоКГ. Данный метод дает четкую видимость состояния сердца, что позволяет без дополнительных исследований поставить четкий диагноз – какая именно кардиомиопатия у пациента. Метод подходит абсолютно всем, даже беременным женщинам и детям. Повторять его можно многократно.
Рентгенография заключает в себе использование рентгеновских лучей. Не нуждается в подготовке и стоит относительно дешево. Но диагностика данным методом не всем показана из-за воздействия лучей на организм человека. Да и полученная информация является неполной и сжатой, поэтому назначают дополнительное обследование.
Холтеровское мониторирование – это обследование с помощью аппарата, который нужно носить на теле целые сутки не снимая. Он не причиняет неудобств, так как весит менее килограмма. Диагностирование, по большому счету, зависит от самого пациента. Он должен письменно вести отчет о всех физических нагрузках, приеме лекарственных препаратов, возникающих болях и т.д. Помимо этого, забыть на время обследования о гигиенических процедурах. Но этот метод – самый точный. В течение суток просматривается подробная работоспособность сердечной мышцы.
Лечение
Приемы терапии относительно одинаковы, сфокусированы на ликвидации основного заболевания.
Специалист может назначить курс терапии, которая поддержит общую работу сердца, притормозит дальнейшее развитие и улучшит состояние миокарда. Больному необходимо постоянное наблюдение кардиолога, периодически стационарное лечение и соблюдение правил здорового образа жизни (умеренная физическая активность, правильное питание, отказ от вредных привычек и т.д.).
Терапевтическое лечение напрямую зависит от стадии развития болезни. Если это первичный недуг, необходимо восстановление нормализации работы сердечной мышцы и исключение сердечной недостаточности. При вторичном заболевании – главной задачей является лечение основной болезни. Например, при поражении инфекцией первоначально назначаются антибиотики и противовоспалительное медикаментозное лечение. И только после этого – восстановление деятельности сердца.
Если болезнь слишком запущена, требуется хирургическое вмешательство (трансплантация сердца). Операционное вмешательство при лечении кардиомиопатии относительно редкое явление. Применяется только в случае вторичной формы недуга, при устранении основной болезни. Примером служит порок сердца.
Прогноз
Кардиомиопатии с точки зрения прогноза крайне неблагоприятны. Возникшая сердечная недостаточность будет неуклонно прогрессировать. Опасность в том, что патология долгое время может никак себя не проявлять. Да, вроде возникают некие неприятные ощущения, однако их часто можно списать на бытовые стрессы, усталость в процессе работы и пр.
Тем не менее, постепенно возникают аритмические либо тромбоэмболические осложнения, которые могут привести к внезапной смерти в достаточно молодом возрасте.
Статистика неумолима по дилатационной кардиомиопатии. После постановки диагноза пятилетней выживаемости достигает лишь 30%. Хотя планомерное лечение позволяет стабилизировать состояние на неопределенный срок.
Крайне важно! Даже при постановке диагноза ДКМП не пускайте лечение на самотек! Можно достаточно долго жить и в условиях планомерного лечения.
Трансплантация сердца может дать хорошие результаты по выживаемости. Зафиксированы случаи превышения 10-летней выживаемости после таких операций.
Не очень хорошо зарекомендовал себя субаортальный стеноз при гипертрофической кардиомиопатии. Его хирургическое лечение имеет высокие риски. По статистике каждый шестой пациент умирает либо во время, либо после операции в короткие сроки.
Очень важно! Женщинам с диагнозом кардиомиопатия противопоказана беременность по причине высокого риска материнской смертности.
Кардиомиопатия: причины, признаки, симптомы, лечение
Кардиомиопатии – группа недугов, которых объединяет то, что во время их прогрессирования наблюдаются патологические изменения в структуре миокарда. Как следствие, эта сердечная мышца перестаёт полноценно функционировать. Обычно развитие патологии наблюдается на фоне различных внесердечных и сердечных нарушений. Это говорит о том, что факторов, которые могут послужить своеобразным «толчком» для прогрессирования патологии, довольно много. Кардиомиопатия может быть первичной и вторичной.
Распространённость данной патологии в мире довольно высокая. Её диагностируют в среднем у трёх человек из 1000. Чаще симптомы болезни проявляются у взрослых людей, но не исключено возникновение кардиомиопатии у детей.
Этиология
Причины прогрессирования первичной кардиомиопатии:
- нарушения на генном уровне;
- вирусная инфекция;
- аутоиммунные нарушения;
- фиброз миокарда не уточнённой этиологии.
Спровоцировать прогрессирование вторичной кардиомиопатии могут такие недуги:
Разновидности
Виды первичной кардиомиопатии:
- гипертрофическая кардиомиопатия;
- рестриктивная кардиомиопатия;
- дилатационная кардиомиопатия.
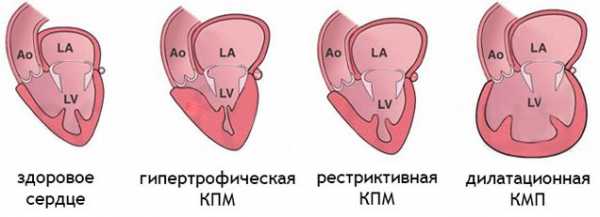
Виды первичной кардиомиопатии
Вторичная кардиомиопатия подразделяется на такие подвиды:
- дисгормональная кардиомиопатия. В медицинской литературе её также именуют климактерической кардиомиопатией, так как чаще она прогрессирует у представительниц прекрасного пола в климактерический период;
- дисметаболическая кардиомиопатия;
- токсическая кардиомиопатия;
- ишемическая кардиомиопатия;
- алкогольная кардиомиопатия.
Дилатационная форма
Характерная особенность дилатационной кардиомиопатии – нарушение сократительной способности сердечной мышцы с расширением камер сердца. Большинство учёных уверены в том, что недуг передаётся на генетическом уровне, так как встречается семейный характер патологии.
Симптомы дилатационной кардиомиопатии:
- повышенная утомляемость;
- при дилатационной кардиомиопатии у больного часто отмечается повышение артериального давления до высоких цифр;
- бледность кожи;
- на ногах появляются отеки;
- кончики пальцев приобретают цианотичный оттенок;
- одышка при дилатационной кардиомиопатии проявляется даже при небольшой физ. нагрузке.
Указанные симптомы обусловлены нарастающей сердечной недостаточностью. Прогноз при дилатационной кардиомиопатии довольно серьёзен. В первые 5 лет после диагностирования патологии умирает до 70% больных. Но если вовремя начать проводить адекватное лечение, то срок жизни пациента можно продлить. Представительницам прекрасного пола с диагнозом «дилатационная кардиомиопатия» следует избегать беременности, так как риск смерти во время родов очень велик.
Лечение
Лечение этой формы патологии в первую очередь направлено на борьбу с прогрессирующей сердечной недостаточностью. В план лечения врачи включают такие препараты:
- ингибиторы АПФ;
- бета-блокаторы;
- бета-адреноблокаторы;
- мочегонные фармацевтические препараты.
Стоит также отметить, ввиду того, что прогноз недуга неблагоприятный, единственным методом, который может продлить жизнь пациенту, является трансплантация сердца.
Гипертрофическая форма
Гипертрофическая кардиомиопатия – патология, основным проявлением которой является утолщение стенки левого желудочка. При этом полость желудочка не увеличивается в размерах. Специалисты считают, что основная причина прогрессирования гипертрофической кардиомиопатии – генетические нарушения.
Симптомы гипертрофической кардиомиопатии:
- аритмия;
- одышка;
- общая слабость;
- бледность кожных покровов;
- нарушение сознания;
- боль в груди;
- тахикардия.
Стоит отметить, что при гипертрофической кардиомиопатии часто возникают различные нарушения сердечного ритма. Иногда они становятся причиной внезапной смерти пациента. У людей с данным диагнозом постепенно прогрессирует сердечная недостаточность.
Прогноз недуга относительно благоприятен по сравнению с другими формами недуга. Пациенты с гипертрофической кардиомиопатией долгое время остаются трудоспособными, но им следует выбирать профессии, где не требуется чрезмерная физическая активность. С таким диагнозом можно планировать беременность и роды.
Лечение
Основная цель терапии – улучшить сократительную способность гипертрофированного желудочка. План лечения включает в себя:
- верапамил;
- дилтиазем;
- бета-блокаторы;
- применение пейсмекера для электростимуляции.
Рестриктивная форма
В случае прогрессирования рестриктивной формы эластичность стенок сердца снижается. Частой причиной развития такого состояния является массивный фиброз миокарда или же его инфильтрация различными веществами.
В результате прогрессирования рестриктивной формы проявляются такие нарушения в работе органа:
- предсердия расширяются, ведь в них повышается давление;
- ткани миокарда утолщаются;
- диастолический объем желудочков уменьшается.
Симптомы рестриктивной кардиомиопатии:
- выраженная одышка;
- отеки.
Лечение
Лечение рестриктивной формы – довольно сложная задача, так как больные обычно обращаются за медицинской помощью на поздней стадии прогрессирования патологии. Диагностика также доставляет трудности. Трансплантация сердца является неэффективной, так как этот патологический процесс может вновь начать прогрессировать в пересаженном сердце.
Если было точно установлено, что рестриктивная форма недуга носит вторичный характер, то план лечения дополняется кровопусканием и кортикостероидами. Прогноз неблагоприятный. Высока вероятность летального исхода.
Алкогольная форма
Алкогольная кардиомиопатия – патология, развивающаяся из-за чрезмерного употребления алкогольных напитков.
Симптомы алкогольной кардиомиопатии:
- аритмия;
- головная боль;
- тахикардия;
- у пациента появляется ощущение нехватки воздуха;
- чувство жара;
- отеки;
- при алкогольной кардиомиопатии у человека появляется одышка даже при незначительной физ. нагрузке;
- нарушение сна;
- повышение АД до высоких цифр;
- повышенная потливость;
- боль в груди.
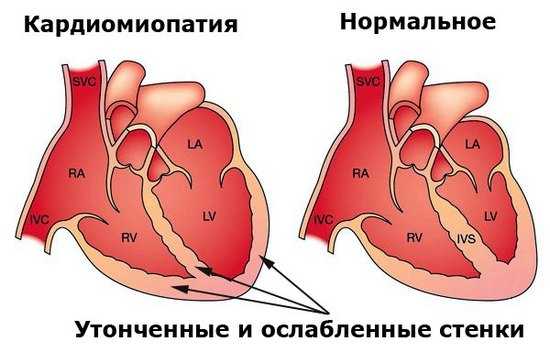
Алкогольная кардиомиопатия
При прогрессировании алкогольной кардиомиопатии изменяется и внешний вид пациента. Проявляются такие характерные признаки:
- желтеют склеры;
- кожный покров на лице гиперемирован;
- нос имеет сине-багровый оттенок;
- глаза краснеют;
- тремор конечностей.
Лечение
Важно полностью исключить употребление алкогольных напитков. Лечение проводится на протяжении нескольких месяцев. В план лечения включают такие препараты:
- бета-адреноблокаторы;
- сердечные гликозиды;
- мочегонные средства;
- антиаритмические фармацевтические препараты;
- аминокислоты;
- анаболические стероиды;
- витамин С;
- витамины из групп В;
- фосфокреатин;
- триметазидин;
- левокарнитин.
Дисгормональная форма
Дисгормональная кардиомиопатия прогрессирует на фоне различных гормональных нарушений. На фоне гормонального сбоя в миокарде нарушается метаболизм, и его механическая деятельность нарушается.
Симптомы дисгормональной кардиомиопатии:
- нервное возбуждение;
- боль в области проекции сердца;
- головокружение;
- аритмия;
- нестабильность АД;
- повышается потоотделение.
Терапия
Прогноз при этой форме недуга благоприятный. Возможно снижение трудоспособности, но при правильно подобранной терапии её можно восстановить. Консервативная терапия включает в себя:
- приём бета-блокаторов;
- приём седативных препаратов;
- гормональную терапию.
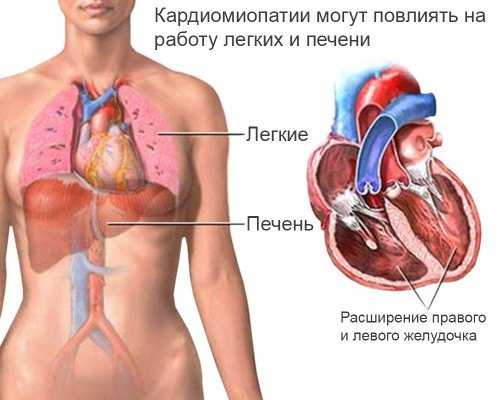
Влияние кардиомиопатии на другие органы
Дисметаболическая форма
При дисметаболической кардиомиопатии нарушается метаболизм непосредственно в тканях миокарда. Из-за этого работа органа нарушается, и его стенки подвергаются дистрофии. Возможными причинами этого патологического процесса являются:
Симптомы дисметаболической кардиомиопатии:
- частые головокружения;
- отеки ног;
- увеличение живота в размерах;
- боль в груди;
- слабость;
- приступы удушья;
- нарушение сна;
- одышка;
- нарушение сознания.
Возникает такая кардиомиопатия у детей и взрослых. На ранних стадиях своего развития может совершенно себя никак не проявлять. Но по мере прогрессирования патологии проявляется симптоматика, указанная выше.
Лечебные мероприятия
Лечение кардиомиопатии этого типа направлено, в первую очередь, на устранение истинной причины, которая спровоцировала прогрессирование недуга. Также специалисты проводят лечебные мероприятия, которые помогут предотвратить дальнейшее ухудшение состояния миокарда.
Ишемическая форма
Ишемическая кардиомиопатия протекает в двух формах:
- асимметричная;
- симметричная.
Спровоцировать развитие патологии могут такие факторы:
- наследственность;
- ИБС;
- недуги щитовидной железы;
- гипертония;
- повышенная концентрация инсулина в крови.
Симптомы ишемической кардиомиопатии:
- одышка;
- тахикардия;
- слабость;
- кашель;
- отеки на ногах;
- снижение или полное отсутствие аппетита;
- аритмия.
Также по мере прогрессирования ишемической кардиомиопатии наблюдается возрастание массы сердца.
Терапия
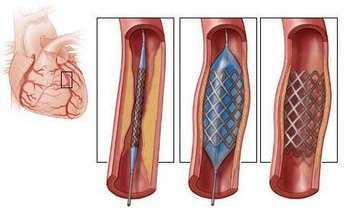
Коронарное шунтирование сосудов сердца
Для лечения кардиомиопатии этого типа задействуют:
- имплантацию дефибриллятора;
- применение лекарственных препаратов;
- кардиостимулятор. Его используют для нормализации сердечного ритма;
- коронарное шунтирование;
- пересадку сердца.
Прогноз ишемической кардиомиопатии неблагоприятный.
Токсическая форма
Токсическая кардиомиопатия может начать развиваться вследствие длительного воздействия на организм некоторых фармацевтических препаратов или алкоголя. Обычно у человека проявляется такая симптоматика:
- аритмия;
- одышка;
- повышенное АД;
- боль в области проекции сердца;
- отёчность;
- похолодание ног;
- тремор.
Важно своевременно провести лечение кардиомиопатии, чтобы не развились опасные осложнения. Важно сначала устранить провоцирующий фактор – перестать принимать лекарственные препараты, отказаться от алкоголя. Далее проводится симптоматическая терапия.
Дилатационная кардиомиопатия - причины, симптомы, диагностика и лечение
Дилатационная кардиомиопатия – это миокардиальное поражение, характеризующееся расширением полости левого или обоих желудочков и нарушением сократительной функции сердца. Дилатационная кардиомиопатия проявляется признаками застойной сердечной недостаточности, тромбоэмболическим синдромом, нарушениями ритма. Диагностика дилатационной кардиомиопатии основывается на данных клинической картины, объективного обследования, ЭКГ, фонокардиографии, ЭхоКГ, рентгенографии, сцинтиграфии, МРТ, биопсии миокарда. Лечение дилатационной кардиомиопатии проводится ингибиторами АПФ, β-адреноблокаторами, диуретиками, нитратами, антикоагулянтами и антиагрегантами.
Общие сведения
Дилатационная кардиомиопатия (застойная, конгестивная кардиомиопатия) – клиническая форма кардиомиопатии, в основе которой лежит растяжение полостей сердца и систолическая дисфункцией желудочков (преимущественно левого). В современной кардиологии на долю дилатационной кардиомиопатии приходится около 60% всех кардиомиопатий. Дилатационная кардиомиопатия чаще манифестирует в возрасте 20-50 лет, однако встречается у детей и пожилых людей. Среди заболевших преобладают лица мужского пола (62-88%).
Дилатационная кардиомиопатия
Причины дилатационной кардиомиопатии
В настоящее время существует несколько теорий, объясняющих развитие дилатационной кардиомиопатии: наследственная, токсическая, метаболическая, аутоиммунная, вирусная. В 20–30 % случаев дилатационная кардиомиопатия является семейным заболеванием, чаще с аутосомно-доминантным, реже – с аутосомно-рецессивным или Х-сцепленным (синдром Барта) типом наследования. Синдром Барта, кроме дилатационной кардиомиопатии, характеризуется множественными миопатиями, сердечной недостаточностью, фиброэластозом эндокарда, нейтропенией, задержкой роста, пиодермиями. Семейные формы дилатационной кардиомиопатии и имеют наиболее неблагоприятное течение.
В анамнезе у 30% пациентов с дилатационной кардиомиопатией отмечается злоупотребление алкоголем. Токсическое воздействие этанола и его метаболитов на миокард выражается в повреждении митохондрий, уменьшении синтеза сократительных белков, образовании свободных радикалов и нарушении метаболизма в кардиомиоцитах. Среди других токсических факторов выделяют профессиональный контакт со смазочными материалами, аэрозолями, промышленной пылью, металлами и пр.
В этиологии дилатационной кардиомиопатии прослеживается влияние алиментарных факторов: недостаточного питания, дефицита белка, гиповитаминоза В1, нехватки селена, дефицита карнитина. На базе этих наблюдений основывается метаболическая теория развития дилатационной кардиомиопатии. Аутоиммунные нарушения при дилатационной кардиомиопатии проявляются наличием органоспецифических кардиальных аутоантител: антиактина, антиламинина, антимиозина тяжелых цепей, антител к митохондриальной мембране кардиомиоцитов и др. Однако аутоиммунные механизмы являются лишь следствием фактора, который пока не установлен.
С помощью молекулярно-биологических технологий (в т. ч. ПЦР) в этиопатогенезе дилатационной кардиомиопатии доказана роль вирусов (энтеровируса, аденовируса, вируса герпеса, цитомегаловируса). Часто дилатационная кардиомиопатия служит исходом вирусного миокардита.
Факторами риска послеродовой дилатационной кардиомиопатии, развивающейся у ранее здоровых женщин в последнем триместре беременности или вскоре после родов, считаются возраст старше 30 лет, негроидная раса, многоплодная беременность, наличие в анамнезе более 3-х родов, поздний токсикоз беременности.
В некоторых случаях этиология дилатационной кардиомиопатии остается неизвестной (идиопатическая дилатационная кардиомиопатия). Вероятно, дилатация миокарда возникает при воздействии ряда эндогенных и экзогенных факторов, преимущественно у лиц с генетической предрасположенностью.
Патогенез
Под действием причинных факторов уменьшается количество функционально полноценно кардиомиоцитов, что сопровождается расширением камер сердца и снижением насосной функции миокарда. Дилатация сердца приводит к диастолической и систолической дисфункции желудочков и обусловливает развитие застойной сердечной недостаточности в малом, а затем и в большом круге кровообращения.
На начальных стадиях дилатационной кардиомиопатии компенсация достигается благодаря действию закона Франка–Старлинга, увеличению ЧСС и уменьшению периферического сопротивления. По мере истощения резервов сердца прогрессирует ригидность миокарда, нарастает систолическая дисфункция, уменьшается минутный и ударный объем, нарастает конечное диастолическое давление в левом желудочке, что приводит к еще большему его расширению.
В результате растяжения полостей желудочков и клапанных колец развивается относительная митральная и трикуспидальная недостаточность. Гипертрофия миоцитов и формирование заместительного фиброза приводят к компенсаторной гипертрофии миокарда. При уменьшении коронарной перфузии развивается субэндокардиальная ишемия.
Вследствие снижения сердечного выброса и уменьшения почечной перфузии активизируются симпатическая нервная и ренин-ангиотензиновая системы. Выброс катехоламинов сопровождается тахикардией, возникновением аритмий. Развивающиеся периферическая вазоконстрикция и вторичный гиперальдостеронизм приводят к задержке ионов натрия, увеличению ОЦК и развитию отеков.
У 60 % пациентов с дилатационной кардиомиопатией в полостях сердца формируются пристеночные тромбы, вызывающие в дальнейшем развитие тромбоэмболического синдрома.
Симптомы дилатационной кардиомиопатии
Дилатационная кардиомиопатия развивается постепенно; длительное время жалобы могут отсутствовать. Реже она манифестирует подостро, после ОРВИ или пневмонии. Патогномоничными синдромами дилатационной кардиомиопатии являются сердечная недостаточность, нарушения ритма и проводимости, тромбоэмболии.
Клинические проявления дилатационной кардиомиопатии включают быструю утомляемость, одышку, ортопноэ, сухой кашель, приступы удушья (сердечная астма). Около 10 % пациентов предъявляют жалобы на ангинозные боли - приступы стенокардии. Присоединение застойных явлений в большом круге кровообращения характеризуется появлением тяжести в правом подреберье, отеков ног, асцита.
При нарушениях ритма и проводимости возникают пароксизмы сердцебиения и перебоев в работе сердца, головокружение, синкопальные состояния. В некоторых случаях дилатационная кардиомиопатия впервые заявляет о себе тромбоэмболией артерий большого и малого кругов кровообращения (ишемический инсульт, ТЭЛА), что может послужить причиной внезапной смерти больных. Риск эмболии увеличивается при мерцательной аритмии, которая сопутствует дилатационной кардиомиопатии в 10—30% случаев.
Течение дилатационной кардиомиопатии может быть быстро прогрессирующим, медленно прогрессирующим и рецидивирующим (с чередованием обострений и ремиссий заболевания). При быстро прогрессирующем варианте дилатационной кардиомиопатии терминальная стадия сердечной недостаточности наступает в течение 1,5 лет от появления первых признаков заболевания. Чаще всего встречается медленно прогрессирующее течение дилатационной кардиомиопатии.
Диагностика
Диагностика дилатационной кардиомиопатии представляет существенные трудности ввиду отсутствия специфических критериев. Диагноз устанавливается путем исключения других заболеваний, сопровождающихся дилатацией полостей сердца и развитием недостаточности кровообращения.
Объективными клиническими признаками дилатационной кардиомиопатии служат кардиомегалия, тахикардия, ритм галопа, шумы относительной недостаточности митрального и трикуспидального клапанов, увеличение ЧД, застойные хрипы в нижних отделах легких, набухание вен шеи, увеличение печени и др. Аускультативные данные подтверждаются с помощью фонокардиографии. Инструментальная диагностика:
- Электрокардиография. На ЭКГ выявляются признаки перегрузки и гипертрофии левого желудочка и левого предсердия, нарушения ритма и проводимости по типу фибрилляции предсердий, мерцательной аритмии, блокады левой ножки пучка Гиса, АВ – блокады. С помощью ЭКГ-мониторирования по Холтеру определяются угрожающие для жизни аритмии и оценивается суточная динамику процессов реполяризации.
- УЗИ сердца. Эхокардиография позволяет обнаружить основные дифференциальные признаки дилатационной кардиомиопатии – расширение полостей сердца, уменьшение фракции выброса левого желудочка. При ЭхоКГ исключаются другие вероятные причины сердечной недостаточности - постинфарктный кардиосклероз, пороки сердца и т. д.; обнаруживаются пристеночные тромбы и оценивается риск развития тромбоэмболии.
- Радиологическая диагностика. Рентгенологически может выявляться увеличение размеров сердца, гидроперикард, признаки легочной гипертензии. Для оценки структурных изменений и сократительной способности миокарда выполняются сцинтиграфия, МРТ, ПЭТ сердца.
- Биопсия миокарда. Используется для дифференциальной диагностики дилатационной кардиомиопатии с другими формами заболевании.
Лечение дилатационной кардиомиопатии
Лечебная тактика при дилатационной кардиомиопатии заключается в коррекции проявлений сердечной недостаточности, нарушений ритма, гиперкоагуляции. Больным рекомендуется постельный режим, ограничение потребления жидкости и соли.
Медикаментозная терапия сердечной недостаточности включает назначение ингибиторов АПФ (эналаприла, каптоприла, периндоприла и др.), диуретиков (фуросемида, спиронолактона). При нарушениях ритма сердца используются b-адреноблокаторы (карведилол, бисопролол, метопролола), с осторожностью – сердечные гликозиды (дигоксин). Целесообразен прием пролонгированных нитратов (венозных вазодилататоров - изосорбида динитрата, нитросорбида), снижающих приток крови к правым отделам сердца.
Профилактика тромбоэмболических осложнений при дилатационной кардиомиопатии проводится антикоагулянтами (гепарин подкожно) и антиагрегантами (ацетилсалициловая кислота, пентоксифиллин, дипиридамол). Радикальное лечение дилатационой кардиомиопатии подразумевает проведение трансплантации сердца. Выживаемость свыше 1 года после пересадки сердца достигает 75–85 %.
Прогноз и профилактика
В целом течение дилатационной кардиомиопатии неблагоприятное: 10-летняя выживаемость составляет от 15 до 30%. Средняя продолжительность жизни после появления симптомов сердечной недостаточности составляет 4–7 лет. Гибель пациентов в большинстве случаев наступает от фибрилляции желудочков, хронической недостаточности кровообращения, массивной легочной тромбоэмболии.
Рекомендации кардиологов по профилактике дилатационной кардиомиопатии включают медико-генетическое консультирование при семейных формах заболевания, активное лечение респираторных инфекций, исключение употребления алкоголя, сбалансированное питание, обеспечивающее достаточное поступление витаминов и минералов.
Гипертрофическая кардиомиопатия - причины, симптомы, диагностика и лечение
Гипертрофическая кардиомиопатия – первичное изолированное поражение миокарда, характеризующееся гипертрофией желудочков (чаще левого) при уменьшенном или нормальном объеме их полостей. Клинически гипертрофическая кардиомиопатия проявляется сердечной недостаточностью, болью в грудной клетке, нарушениями ритма, синкопальными состояниями, внезапной смертью. Диагностика гипертрофической кардиомиопатии включает проведение ЭКГ, суточного ЭКГ-мониторирования, ЭхоКГ, рентгенологического исследования, МРТ, ПЭТ сердца. Лечение гипертрофической кардиомиопатии проводится b-адреноблокаторами, блокаторами кальциевых каналов, антикоагулянтами, антиаритмическими препаратами, ингибиторами АПФ; в ряде случаев прибегают к кардиохирургической операции (миотомии, миоэктомии, протезированию митрального клапана, двухкамерной электрокардиостимуляции, имплантации кардиовертер-дефибриллятора).
Общие сведения
В кардиологии различают первичные (идиопатические) кардиомиопатии (гипертрофическую, констриктивную, дилатационную, рестриктивную, аритмогенную дисплазию правого желудочка) и специфические вторичные кардиомиопатии (алкогольную, токсическую, метаболическую, климактерическую и ряд других).
Гипертрофическая кардиомиопатия – самостоятельное, не зависящее от других сердечно-сосудистых заболеваний, значительное утолщение миокарда левого (реже правого) желудочка, сопровождающееся уменьшением его полости, нарушением диастолической функции с развитием нарушений сердечного ритма и сердечной недостаточности.
Гипертрофическая кардиомиопатия развивается у 0,2-1,1% населения, чаще мужского пола; средний возраст пациентов составляет от 30 до 50 лет. Коронарный атеросклероз среди больных гипертрофической кардиомиопатией встречается в 15-25 % случаев. Внезапная смерть, вызванная с тяжелыми желудочковыми аритмиями (пароксизмальной желудочковой тахикардией), наступает у 50% пациентов с гипертрофической кардиомиопатией. У 5-9 % больных заболевание осложняется инфекционным эндокардитом, протекающим с поражением митрального или аортального клапана.
Гипертрофическая кардиомиопатия
Причины гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия – заболевание с аутосомно-доминантным типом наследования, поэтому обычно носит семейный характер, что не исключает, однако, возникновение спорадических форм.
В основе семейных случаев гипертрофической кардиомиопатии лежат передаваемые по наследству дефекты генов, кодирующих синтез сократительных белков миокарда (гена тяжелой цепи b-миозина, гена сердечного тропонина Т, гена а-тропомиозина, гена, кодирующего сердечную изоформу миозин-связывающего белка). Спонтанные мутации этих же генов, происходящие под воздействием неблагоприятных факторов среды, обусловливают развитие спорадических форм гипертрофической кардиомиопатии.
Гипертрофия миокарда левого желудочка при гипертрофической кардиомиопатии не связана с врожденными и приобретенными пороками сердца, ИБС, гипертонической болезнью и другими заболеваниями, которые обычно приводят к подобным изменениям.
Патогенез
В патогенезе гипертрофической кардиомиопатии ведущая роль принадлежит компенсаторной гипертрофии сердечной мышцы, обусловленной одним из двух возможных патологических механизмов - нарушением диастолической функции миокарда или обструкцией выходного тракта левого желудочка. Диастолическая дисфункция характеризуется поступлением в желудочки недостаточного количества крови в диастолу, что связано с плохой растяжимостью миокарда, и обусловливает быстрый подъем конечного диастолического давления.
При обструкции выходного отдела левого желудочка имеет место утолщение межжелудочковой перегородки и нарушение движения передней створки митрального клапана. В связи с этим в период изгнания возникает перепад давления между полостью левого желудочка и начальным отрезком аорты, что сопровождается повышением конечного диастолического давления в левом желудочке. Возникающая в этих условиях компенсаторная гиперфункция сопровождается гипертрофией, а затем и дилатацией левого предсердия, в случае же декомпенсации развивается легочная гипертензия.
В ряде случаев гипертрофической кардиомиопатии сопутствует ишемия миокарда, обусловленная снижением вазодилататорного резерва коронарных артерий, увеличением потребности гипертрофированного миокарда в кислороде, сдавлением во время систолы интрамуральных артерий, сопутствующим атеросклерозом венечных артерий и т. д.
Макроскопическими признаками гипертрофической кардиомиопатии служит утолщение стенок левого желудочка при нормальных или уменьшенных размерах его полости, гипертрофия межжелудочковой перегородки, дилатация левого предсердия. Микроскопическая картина гипертрофической кардиомиопатии характеризуется беспорядочным расположением кардиомиоцитов, замещением мышечной ткани на фиброзную, аномальным строением интрамуральных венечных артерий.
Классификация
В соответствии с локализацией гипертрофии выделяют гипертрофическую кардиомиопатию левого и правого желудочков. В свою очередь, гипертрофия левого желудочка может быть асимметричной и симметричной (концентрической). В большинстве случаев выявляется асимметричная гипертрофия межжелудочковой перегородки на всем протяжении или в ее базальных отделах. Реже встречается асимметричной гипертрофия верхушки сердца (апикальная гипертрофическая кардиомиопатия), задней или переднебоковой стенки. На долю симметричной гипертрофии приходится около 30 % случаев.
С учетом наличия градиента систолического давления в полости левого желудочка различают обструктивную и необструктивную гипертрофическую кардиомиопатию. Симметричная гипертрофия левого желудочка, как правило, представляет собой необструктивную форму гипертрофической кардиомиопатии.
Асимметричная гипертрофия может являться как необструктивной, так и обструктивной. Так, синонимом асимметричной гипертрофии межжелудочковой перегородки служит понятие «идиопатический гипертрофический субаортальный стеноз», гипертрофии средней части межжелудочковой перегородки (на уровне папиллярных мышц) – «мезовентрикулярная обструкция». Верхушечная гипертрофия левого желудочка, как правило, представлена необструктивным вариантом.
В зависимости от степени утолщения миокарда выделяют умеренную (15-20 мм), среднюю (21-25 мм) и выраженную (более 25 мм) гипертрофию.
На основании клинико-физиологической классификации выделяют IV стадии гипертрофической кардиомиопатии:
- I - градиент давления в выходном тракте левого желудочка (ВТЛЖ) не более 25 мм рт. ст.; жалобы отсутствуют;
- II - градиент давления в ВТЛЖ возрастает до 36 мм рт. ст.; появляются жалобы при физической нагрузке;
- III - градиент давления в ВТЛЖ увеличивается до 44 мм рт. ст.; появляются стенокардия, одышка;
- IV - градиент давления в ВТЛЖ выше 80 мм рт. ст.; развиваются выраженные нарушения гемодинамики, возможна внезапная сердечная смерть.
Симптомы гипертрофической кардиомиопатии
Длительное время течение гипертрофической кардиомиопатии остается бессимптомным, клиническая манифестация чаще происходит в возрасте 25–40 лет. С учетом преобладающих жалоб выделяют девять клинических форм гипертрофической кардиомиопатии: малосимптомную, вегетодистоническую, кардиалгическую, инфарктоподобную, аритмическую, декомпенсационную, псевдоклапанную, смешанную, молниеносную. Несмотря на то, что каждый клинический вариант характеризуется определенными признаками, всем формам гипертрофической кардиомиопатии присущи общие симптомы.
Необструктивная форма гипертрофической кардиомиопатии, не сопровождающаяся нарушением оттока крови из желудочка, обычно малосимптомна. В этом случае жалобы на одышку, перебои в работе сердца, неритмичный пульс могут отмечаться при выполнении физической нагрузки.
Типичными симптомами обструктивной гипертрофической кардиомиопатии служат приступы ангинозных болей (70%), выраженная одышка (90%), головокружения и обморочные состояния (25-50%), преходящая артериальная гипотензия, нарушения ритма сердца (пароксизмальная тахикардия, фибрилляция предсердий, экстрасистолия). Возможно возникновение приступов сердечной астмы и отека легких. Нередко первым эпизодом проявления гипертрофической кардиомиопатии служит внезапная смерть.
Диагностика
При диагностическом поиске обнаруживается систолический шум, высокий, скорый пульс, смещение верхушечного толчка. Инструментальные методы обследования при гипертрофической кардиомиопатии включают ЭхоКГ, ЭКГ, ФКГ, рентгенографию грудной клетки, холтеровское мониторирование, поликардиографию, ритмокардиографию. С помощью эхокардиографии выявляется гипертрофия МЖП, стенок миокарда желудочка, увеличение размеров левого предсердия, наличие обструкции ВТЛЖ, диастолическая дисфункция левого желудочка.
ЭКГ-признаки гипертрофической кардиомиопатии малоспецифичны и требуют дифференциальной диагностики с очаговыми изменениями миокарда, гипертонической болезнью, ИБС, аортальным стенозом и другими заболеваниями, осложняющимися гипертрофией левого желудочка. Для оценки тяжести гипертрофической кардиомиопатии, прогноза и выработки рекомендаций по лечению используются нагрузочные пробы (велоэргометрия, тредмил-тест).
Суточное мониторирование ЭКГ позволяет документировать пароксизмальные эпизоды желудочковой экстрасистолии и тахикардии, фибрилляции и трепетания предсердий. На фонокардиограмме регистрируется систолический шум различной степени выраженности, сохранность амплитуды I и II тонов. Сфигмография демонстрирует двухвершинную кривую каротидного пульса, характеризующуюся дополнительной волной на подъеме.
При рентгенологическом исследовании изменения контуров сердца (увеличение левых отделов сердца, расширение восходящей части аорты, выбухание ствола и расширение ветвей легочной артерии) обнаруживаются только в развернутой стадии гипертрофической кардиомиопатии. Для получения дополнительных данных за гипертрофическую кардиомиопатию прибегают к проведению зондирования левых отделов сердца, вентрикулографии, коронарографии, сканированию сердца с радиоизотопом таллия, МРТ, ПЭТ сердца.
Лечение гипертрофической кардиомиопатии
Пациентам с гипертрофической кардиомиопатией (особенно с обструктивной формой) рекомендуется ограничение физических нагрузок, которые могут спровоцировать увеличение градиента давления «левый желудочек-аорта», аритмии сердца и обмороки.
При умеренно выраженных симптомах гипертрофической кардиомиопатии назначают b-адреноблокаторы (пропранолол, атенолол, метопролол) или блокаторы кальциевых каналов (верапамил), уменьшающие ЧСС, удлиняющие диастолу, улучшающие пассивное наполнение левого желудочка и снижающие давление наполнения. В связи с наличием высокого риска развития тромбоэмболий необходим прием антикоагулянтов. При развитии сердечной недостаточности показаны диуретики, ингибиторы АПФ; при нарушениях желудочкового ритма - антиаритмические препараты (амиодарон, дизопирамид).
При обструктивной гипертрофической кардиомиопатии проводится профилактика инфекционного эндокардита, т. к. в результате постоянной травматизации передней створки митрального клапана на ней могут появляться вегетации. Кардиохирургическое лечение гипертрофической кардиомиопатии целесообразно при градиенте давления между левым желудочком и аортой >50 мм рт.ст. В этом случае может выполняться септальная миотомия или миоэктомия, а при структурных изменениях митрального клапана, вызывающих значительную регургитацию, - протезирование митрального клапана.
Для уменьшения обструкции ВТЛЖ показана имплантация двухкамерного электрокардиостимулятора; при наличии желудочковых нарушений ритма - имплантация кардиовертер-дефибриллятора.
Прогноз гипертрофической кардиомиопатии
Течение гипертрофической кардиомиопатии вариабельно. Необструктивная форма гипертрофической кардиомиопатии протекает относительно стабильно, однако при длительном стаже заболевания все же развивается сердечная недостаточность. У 5–10% пациентов возможен самостоятельный регресс гипертрофии; у такого же процента больных отмечается переход гипертрофической кардиомиопатии в дилатационную; еще столько же пациентов сталкивается с осложнением в виде инфекционного эндокардита.
Без лечения летальность при гипертрофической кардиомиопатии составляет 3–8 %, при этом в половине подобных случаев возникает внезапная смерть вследствие фибрилляции желудочков, полной атриовентрикулярной блокады, острого инфаркта миокарда.
Перипартальная кардиомиопатия - причины, симптомы, диагностика и лечение
Перипартальная кардиомиопатия – это редкое жизнеугрожающее заболевание сердца, возникающее во время беременности или в течение нескольких месяцев после родов. Клинически болезнь проявляется классическими симптомами застойной сердечной недостаточности: затруднением дыхания при физической нагрузке или ходьбе, учащенным сердцебиением, отеками на ногах. Отличительная особенность ХСН при перипартальной КМП – быстрое нарастание. Диагноз ставится на основании жалоб, анамнестических данных, лабораторно и инструментально подтвержденной сердечной недостаточности. Лечение проводится по общим принципам терапии ХСН с добавлением агонистов дофаминовых рецепторов.
Общие сведения
Перипартальная кардиомиопатия (перипартальная болезнь, кардиомиопатия Мидоуса) в подавляющем большинстве случаев развивается после родов (в течение 5-6 месяцев), реже – во II или III триместре беременности. Заболевание впервые было описано французским врачом Ц. Рицше в 1849 году. Средняя распространенность составляет 1 случай на 10 000 родов. Перипартальная КМП чаще возникает у лиц негроидной расы, поэтому в африканских странах ее встречаемость намного выше (1:100).
Перипартальная кардиомиопатия
Причины
Несмотря на многочисленные исследования, точный этиологический фактор патологии не установлен. Предполагается роль вирусов, вызывающих миокардит (вируса Коксаки А и В, Эпштейн-Барра), и аутоантител к белкам сердечной мышцы. Перипартальная КМП более часто наблюдается у ближайших родственников, что свидетельствует о генетической предрасположенности. Существуют факторы, увеличивающие вероятность развития ПКМП:
Патогенез
Неизвестный фактор стимулирует оксидативный стресс, который, в свою очередь, активирует в кардиомиоцитах катепсин D – белок, расщепляющий гормон пролактин на фрагменты. Один из них, 16кДа фрагмент, обладает кардиотоксическим эффектом, вызывает вазоконстрикцию, дисфункцию и запрограммированную гибель клеток миокарда, подавляет пролиферацию эндотелиальных клеток сосудов.
Все это приводит к расширению полостей сердца, ухудшению насосной функции миокарда правого и левого желудочка. Патоморфологические изменения при перипартальной кардиомиопатии неспецифичны и схожи с таковыми при миокардитах. Выявляется диффузная дегенерация, очаги миоцитолиза, некроза, фиброза, умеренная гипертрофия волокон миокарда.
Симптомы перипартальной кардиомиопатии
Временной промежуток возникновения признаков заболевания – от конца II триместра беременности до 6 месяца после родов. Наиболее часто клиническая картина начинает разворачиваться в течение первого месяца после рождения ребенка. Трудность распознавания ПКМП заключается в том, что ее ранние симптомы имитируют физиологические изменения при беременности.
К таким признакам можно отнести повышенную утомляемость, ухудшение переносимости физических нагрузок, небольшое затруднение дыхания, усиливающееся в лежачем положении (ортопноэ). Из-за быстрого прогрессирования ХСН симптомы усугубляются. Одышка присутствует даже в покое. Появляются ноющие боли в области сердца, головокружение, отеки на стопах и голенях, учащенное сердцебиение. Начинают беспокоить тянущие боли в правом подреберье из-за увеличения размеров печени.
Осложнения
Перипартальная кардиомиопатия является тяжелым состоянием с большим количеством осложнений, в том числе фатальных. При быстропрогрессирующем течении возможно развитие острой сердечной недостаточности с отеком легких или кардиогенным шоком. Резкая дилатация камер сердца способствует возникновению жизнеугрожающих нарушений ритма сердца.
Из-за вихревого движения крови в расширенных полостях сердца легко образуются тромбы, поэтому у больных ПКМП существует высокий риск кардиоэмболического инсульта и ТЭЛА. Ухудшение систолической функции миокарда неблагоприятно сказывается на плацентарном кровообращении, что приводит к внутриутробной гипоксии плода, задержке развития или антенатальной гибели.
Диагностика
Чаще всего больных курируют врачи-кардиологи. Беременные пациентки с перипартальной кардиомиопатией находятся под совместным наблюдением кардиолога и акушера-гинеколога. При физикальном осмотре обращают внимание на набухание шейных вен, усиливающееся при надавливании на печень (гепатоюгулярный рефлюкс), влажные хрипы в легких, глухость тонов сердца. ПКМП дифференцируют с приобретенными пороками сердца, дилатационной кардиомиопатией, миокардитами и пр.
Поскольку преобладающее число случаев ПКМП приходится на послеродовый период, большое значение имеет уточнение факта беременности у пациентки с быстропрогрессирующей ХСН. Отсутствие каких-либо кардиологических заболеваний (ИБС, пороки сердца) до начала гестации свидетельствует в пользу ПКМП. Для уточнения диагноза проводится дополнительное обследование, включающее:
- Лабораторные исследования. В крови обнаруживается повышение фрагмента пролактина 16кДа и маркера сердечной недостаточности – мозгового натрийуретического пептида (NT-proBNP).
- ЭКГ. На электрокардиограмме отмечаются признаки гипертрофии левого и правого желудочков, различные нарушения ритма: фибрилляция предсердий, желудочковая экстрасистолия, блокада левой ножки пучка Гиса.
- Эхо-КГ. Эхокардиография считается основным методом исследования. Выявляется расширение всех камер сердца, особенно левого желудочка, выраженное снижение фракции выброса (45-50%), относительная атриовентрикулярная недостаточность. Иногда встречаются пристеночные тромбы, умеренный перикардиальный выпот.
- МРТ сердца. Магнитно-резонансная томография позволяет провести детальную оценку структуры миокарда. Назначается при неоднозначных результатах Эхо-КГ.
- Рентгенография ОГК. На рентгенограмме органов отмечается расширение тени сердца, усиление сосудистого рисунка за счет венозного полнокровия сосудов малого круга кровообращения.
Лечение перипартальной кардиомиопатии
Консервативная терапия
После подтверждения диагноза больных обязательно госпитализируют в кардиологический стационар. При тяжелой недостаточности кровообращения показан перевод в отделение реанимации и интенсивной терапии для проведения внутриаортальной балонной контрпульсации. Несмотря на быстропрогрессирующее течение, почти у половины пациенток наблюдается спонтанное выздоровление.
Немедикаментозное лечение включает ограничение приема жидкости до 2 литров в сутки и поваренной соли до 3-4 граммов в сутки. При назначении лекарственной терапии беременным необходимо учитывать потенциальный нежелательный эффект некоторых медикаментов на плод. Рекомендованы:
- Агонисты дофаминовых рецепторов. Препараты действуют на главное патогенетическое звено ПКМП. Подавляя выработку пролактина, они снижают образование его кардиотоксического фрагмента (16кДа). У беременных применяется бромокриптин, после родов возможен перевод на каберголин или хинаголид.
- Ингибиторы АПФ. Основные лекарственные средства, замедляющие прогрессирование сердечной недостаточности.
- Бета-адреноблокаторы. Назначаются как альтернатива ингибиторам АПФ беременным женщинам, а также при наличии тахиаритмий.
- Вазодилататоры. Сосудорасширяющие медикаменты используются для снятия вазоспазма при систолическом давлении более 110 мм рт. ст.
- Диуретики. С целью уменьшения застойных явлений в легких и выведения жидкости применяются тиазидные и петлевые мочегонные препараты.
- Сердечные гликозиды. Для поддержания адекватного сердечного выброса при артериальной гипотензии показаны дигоксин, левосимендан.
- Антикоагулянты. Так как дилатация сердечных полостей сопровождается высоким риском тромбообразования, пациенткам рекомендован прием антикоагулянтов (варфарина, ривароксабана). Беременным разрешен только гепарин.
Хирургическое лечение
При выраженной ХСН (фракция выброса левого желудочка достигает менее 40%), развившейся у беременных, требуется прерывание беременности путем кесарева сечения. Крайне тяжелая, резистентная к консервативной терапии перипартальная кардиомиопатия служит показанием к трансплантации сердца. При устойчивых тахиаритмиях, сопровождающихся грубыми гемодинамическими нарушениями (критическое падение артериального давления), прибегают к имплантации кардиовертера-дефибриллятора.
Прогноз и профилактика
Перипартальная кардиомиопатия – жизнеугрожающее состояние с высоким процентом летальности. В зависимости от своевременности диагностирования и начала грамотной терапии частота летальных исходов составляет от 7 до 56%. Основными причинами смерти выступают нарушения ритма и проводимости сердца, тромбоэмболические осложнения, недостаточность кровообращения.
Полное восстановление насосной функции сердечной мышцы после лечения наблюдается в 50-65% случаев. У 30-50%, перенесших перипартальную КМП, при повторной беременности происходит рецидив заболевания, поэтому им рекомендуется применение различных методов контрацепции. Эффективных методов профилактики не существует.
что это такое, лечение и прогноз жизни
Дилатационная кардиомиопатия — это клинический вариант врожденного или чаще приобретенного порока сердца, характеризуется расширением камер при неизменном объеме миокарда.
Более того, мышечный слой может истончаться по причине компрессии, растяжения и последующего нарушения питания.
Проявляется болезнь не сразу, спустя годы возникают какие-то симптомы. Но они неспецифичны. Человек может списывать отклонения на проблемы с желудком и пищеварительной системой, погоду, на что угодно, но не подозревать о проблеме.
Драгоценное время утекает, органический дефект оказывается все стабильнее и больше, угнетая кардиальную деятельность. Итог — внезапная смерть от остановки сердца.
Всегда ли сценарий столь пессимистичен? Конечно, нет. Все зависит от пациента и его отношения к собственному здоровью.
Механизм развития патологии
Суть анатомического дефекта кроется в расширении одной, но чаще сразу нескольких камер.
В ходе развития отмечается скопление крови в кардиальных структурах. Отсюда возникновение постепенного застоя и растяжения предсердий и/или желудочков.
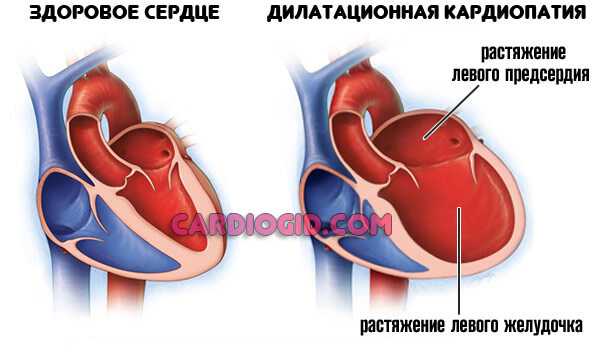
Основной процесс имеет свойство прогрессировать, обычно это недостаточность аортального, митрального клапана, бывает, что в сочетании. Объем жидкой соединительной ткани, остающейся в кардиальных структурах, увеличивается постепенно.
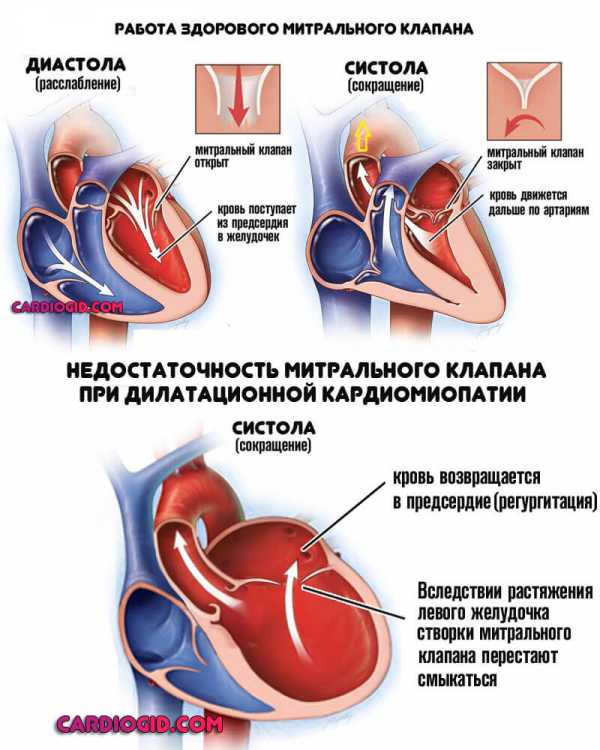
Сердце растет дальше, однако объем мышечной массы сохраняется прежним, поскольку сократительная способность до определенного момента не страдает (это главное отличие кардиомиопатии дилатационной от прочих форм).
Более того, слой функциональных клеток истончается. Рост объема органа приводит к растяжению ткани, возникновению хронической сердечной недостаточности, третичной ишемии и постепенной дистрофии.
В конечном итоге падает объем выброса, страдают все системы, само же сердце перестает работать достаточно активно по причине слабости миокарда, что только усугубляет процессы.
Исход — смерть от остановки работы мышечного органа или полиорганной недостаточности. Что наступит раньше — большой вопрос, но в отсутствии терапии летальный исход неминуем.
От момента появления первых симптомов до фатального результата проходит 5-15 лет.
Процесс прогрессирует постепенно, время на диагностику и лечение есть. Исключения составляют возможные неотложные состояния, спровоцированные гипоксией (кардиогенный шок, асистолия, инфаркт, инсульт).
Причины расширения камер
Дилатационная кардиомипатия (сокращенно ДКМП) имеет собственный код по МКБ-10: I42.1. Факторы развития патологического процесса всегда кардиальные. Состояние не бывает первичным почти никогда, оно вторично, то есть, обусловлено прочими заболеваниями.
Среди возможных:
- Врожденные и приобретенные аномалии развития сердца. Существуют десятки генетических и фенотипических синдромов, обусловленных нарушениями перинатального периода.
Закладывание сердечнососудистой системы происходит на 2 неделе беременности, уже тогда возможны проблемы. Задача матери — обеспечить нормальную среду для развития эмбриона, а потому и плода. Первый триместр особенно ответственный.
Приобретенные патологии определяются неправильным образом жизни, перенесенными болезнями. Симптомами часто не проявляются ни те, ни другие (не считая генетических отклонений).
Залог сохранения здоровья и жизни — регулярный скрининг по определенной индивидуальной программе. Достаточно 1-2 раза в год проходить профилактическое обследование.
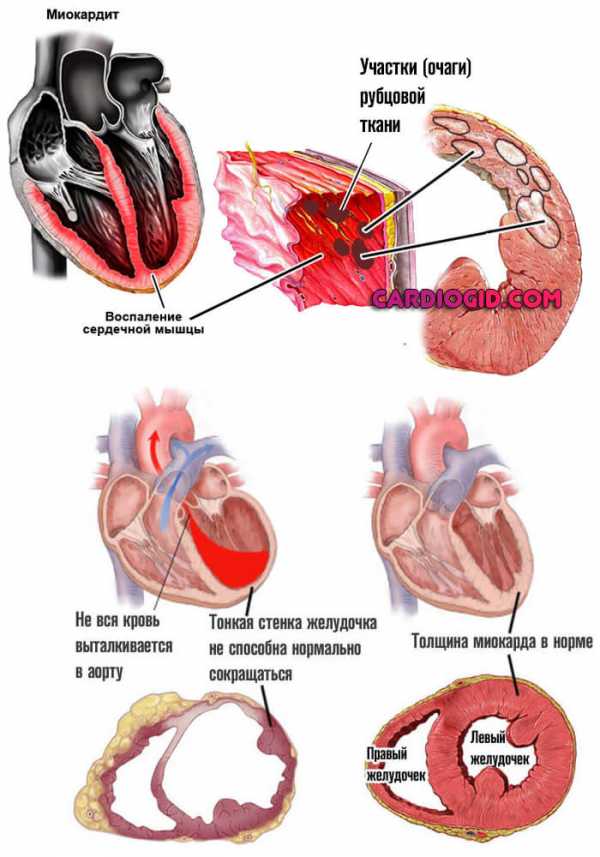
- Миокардит. Воспаление сердечных структур инфекционного (грибкового, вирусного, бактериального) происхождения. Симптомы достаточно специфичны и интенсивны, чтобы побудить человека отправиться к врачу.
Восстановление проводится в стационаре с применением антибиотиков, кортикостероидов и протекторных препаратов. В отсутствии терапии возникает деструкция мышц, предсердий, что снижает сократительную способность.
- Генетический фактор. Если в роду был человек, страдавший какой-либо формой кардиомиопатии, присутствует риск, что патологическое отклонение проявится в фенотипе у потомка.
Для более конкретных выводов рекомендуется опросить старших членов семьи и обратиться за консультацией к генетику. Вероятность варьируется в широких пределах.
По разным оценкам, наличие одного родственника определяет риск в 25%, двух — в 40%. Но это не приговор.
Если соблюдать профилактические меры, есть шансы не встретиться с проблемой. С другой стороны, даже диагностированный процесс не гарантирует летального исхода.
На ранних этапах патологию можно обуздать и прожить долго, без какой либо симптоматики и существенных ограничений.
- Аутоиммунные процессы. Ревматизм, системная красная волчанка, тиреоидин Хашимото и прочие. В определенный момент влекут генерализованные поражения всех систем.
- Метаболические нарушения в результате диет, анорексии и осознанного голодания. Возникают в рамках длительного процесса. Примерные сроки — 1-2 месяца с начала изнурения организма. Восстановление проводится осторожно, тело ослаблено, возможны непредсказуемые последствия, вплоть до остановки сердца или же разрыва истонченного желудка при обильном потреблении пищи.
- Длительно текущая артериальная гипертензия. На первой стадии ГБ осложнения крайне редки, возникают не более, чем в 3-7% случаев. 2 и 3 этапы особенно опасны. Показатели тонометра закрепляются на высоких уровнях, повышается нагрузка на сердце, миокард.
Расширение камер — компенсаторный механизм, когда кардиальные структуры не справляются с сократительным объемом, жидкая соединительная ткань застаивается, возникает расширение.
- Ишемическая болезнь длительного характера. Приводит к выраженным дистрофическим процессам в мышечном слое сердца. Следующий эволюционный шаг развития патологии — инфаркт.
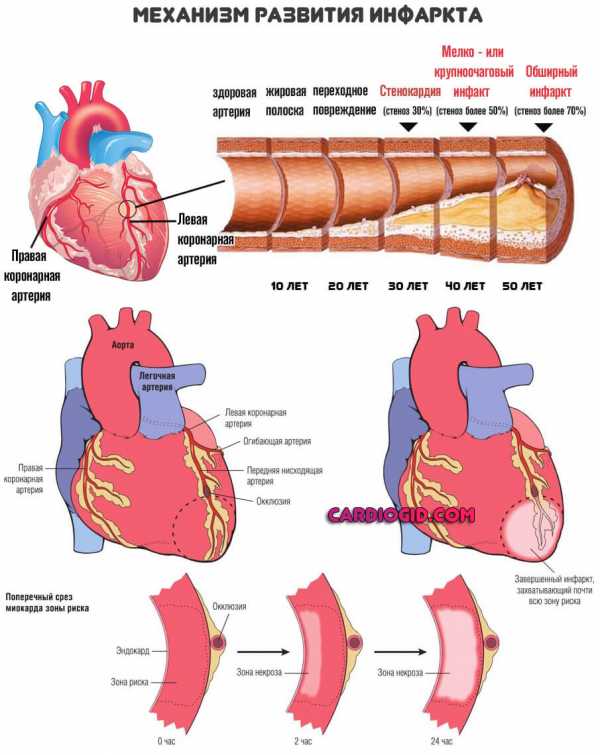
- Инфаркт. Крайняя степень коронарной недостаточности. Отмечается некроз клеток-миоцитов, замещение последних рубцовой, не активной тканью.
- Токсические поражения в результате злоупотребления алкоголем, контакте с солями тяжелых металлов, опасных ядовитых веществ. Также сказывается постоянный прием гликозидов (они подстегивают сократительную активность миокарда без оглядки на функциональный запас органа).
В отсутствии данных за органические патологии констатируют идиопатическую дилатационную кардиомиопатию. В таком случае лечение симптоматическое, направлено на поддержание работы сердца, также приостановку прогрессирования.
Как уже сказано, первичной патология бывает только в случае врожденного порока, либо генетического заболевания. Все прочие ситуации — вторичны.
Симптомы
Перечень проявлений зависит от степени тяжести процесса. Общепринятой классификации и стадирования, однако, не существует. Потому определение запущенности явления проводится по интенсивности признаков и характеру органических дефектов.
Примерная клиническая картина выглядит следующим образом:
- Боли в грудной клетке неясного происхождения. Диффузные, точная локализация пациенту не понятна. Отдают в живот, спину, руки, лицевую область. Интенсивность разнится от незначительного покалывания до невыносимого, мучительного приступа. Симптом неспецифичен, также по силе болевого синдрома невозможно судить о характере процесса. Диагностической роли этот признак не играет.
- Одышка. При интенсивных физических нагрузках (бег, поднятие тяжестей в течение длительного времени) на первой стадии. Затем же нарушение становится постоянным спутником человека. Больной не может подняться по лестнице, а затем и вовсе не способен даже встать с постели без одышки. Это качественный признак, указывающий на степень нарушения газообмена.
- Аритмия. По типу тахикардии, либо обратного явления. Ускорение или замедление сердечной деятельности может сочетаться с отклонениями в интервалах между сокращениями. Экстрасистолия, фибрилляция предсердий как возможные варианты. Несут опасность для жизни.
- Слабость, чувство отсутствия сил, апатичность, снижение работоспособности. На поздних стадиях нет возможности выполнять трудовые обязанности, что сказывается на социальной жизни пациента.
- Цианоз носогубного треугольника. Посинение области вокруг рта.
- Повышенная потливость. Особенно в ночное время.
- Бледность кожных покровов.
- Головная боль. В затылке или темени. Тюкающая, стреляющая, длительно текущая. Проявляется регулярно, периодически проходит или затихает.
- Вертиго. Нарушения нормальной ориентации в пространстве.
- Психические расстройства: от нервозности, раздражительности, тревожности до галлюцинаторно-бредовых вариантов, онейроидных сосудистых эпизодов, депрессий.
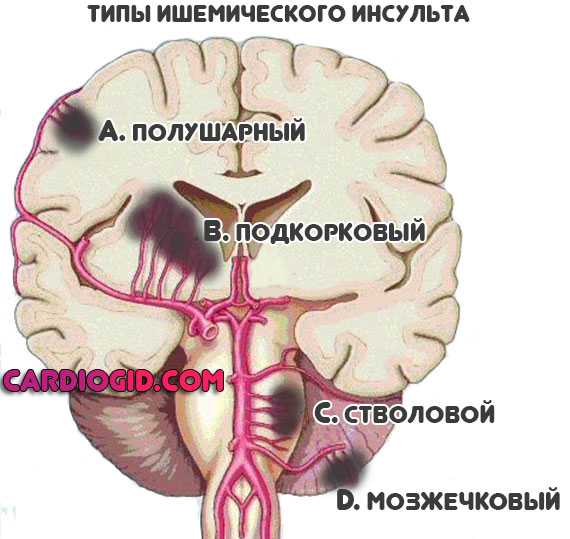
Последние три симптома говорят об ишемии церебральных структур. Это опасно, вероятен инсульт.
Диагностика
Проводится под контролем кардиолога. Участки профильного хирурга возможно, но показано в крайних случаях. Оперативным путем кардиомиопатия не лечится, устраняются таким способом этиологические факторы (пороки).
Примерная схема:
- Устный опрос, объективизация жалоб, симптомов.
- Сбор анамнеза. Учитывается образ жизни, давность течения болезни, наличие соматических патологий, семейная история, лечение (определенное влияние на сердце оказывают кортикостероиды, антипсихотики, транквилизаторы и нормотимики).
- Измерение артериального давления. Также частоты сердечных сокращений. Для выявления возможных отклонений функциональных показателей.
- Суточное мониторирование по Холтеру. Используется для динамического наблюдения за теми же уровнями. Однократного измерения недостаточно. Назначается как в амбулаторных условиях (предпочтительно), так и в стационаре.
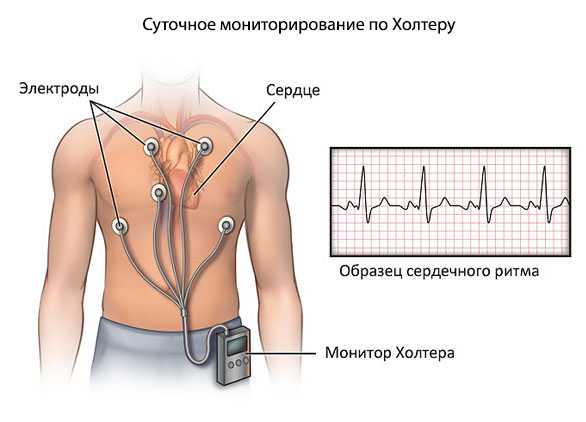
- Электрокардиография. Методика оценки функциональной активности сердца. Показывает малейшие отклонения в ритме. Важно, чтобы врач имел достаточную квалификацию для расшифровки.
- Эхокардиография. Профильный диагностический способ. Показывает все органические (анатомические) дефекты даже незначительного характера. Подходит для ранней оценки состояния сердца, также степени отклонений в поздний период и прогнозирования.
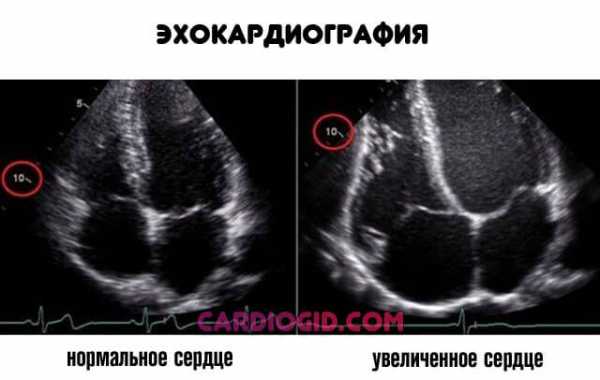
- КТ или МРТ для более детального рассмотрения анатомических структур.
- Коронография.
- Анализ крови.
Возможно проведение не всех представленных исследований, вопрос решается на усмотрение специалиста. Установление происхождения процесса относительно трудно.
Лечение
Имеет двойственный характер. Требуется этиотропное воздействие, то есть устранение основного заболевания, влекущего анатомические дефекты.
Симптоматическая терапия направлена на редукцию проявлений и приостановку патологического процесса. Такая схема может проводиться на протяжении многих лет и даже всей жизни. Основу мероприятий составляет консервативная методика.
Применяются препараты нескольких фармацевтических типов:
- Антиаритмические на фоне нарушения сократительной способности миокарда. Хиндин или Амиодарон. Возможно использование аналогов.
- Противогипертонические. Существует несколько групп медикаментов. Ингибиторы АПФ, бета-локаторы, антагонисты кальция как основных. Классическая схема: Верапамил или Дилтиазем + Периндоприл в разных торговых формах + Моксонидин или Физиотенз.
- Противотромбические. Одна из основных причин смерти пациентов с дилатационной кардиомиопатией — эмболия сгустками крови. Легочная артерия закупоривается, летальный исход вероятен в течение 2-3 минут или считанных секунд. Применяется Аспирин Кардио для восстановления реологических свойств крови.
- Статины. Для лечения атеросклероза на ранних стадиях.
- Витаминно-минеральные комплексы и средства на основе калия, магния (Аспаркам и прочие).
- Кардиопротекторы.
Гликозиды используются редко ввиду возможности спровоцировать остановку сердца или инфаркт.
Хирургическое лечение проводится по показаниям. Для восстановления анатомической целостности сердечных структур (воспаления, ревматизм, пороки) — протезирования, установки кардиостимулятора.
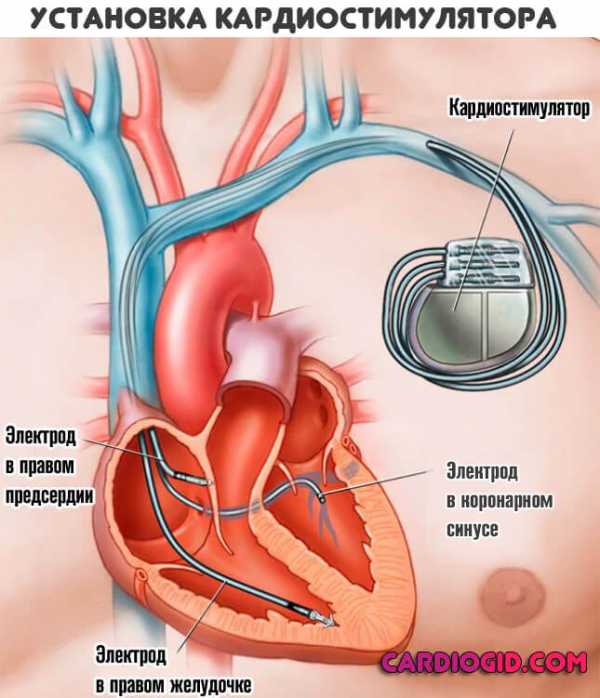
Крайняя мера — трансплантация органа. Проводится редко ввиду сложности найти донора, опасности методики. Назначается, если другого выхода нет и это реальный шанс на выживание (не всегда даже столь радикальным методом можно решить вопрос).
На протяжении периода терапии, а значит, скорее всего, жизни, показано изменение бытовых и прочих привычек.
- Нужно отказаться от курения, алкоголя, психоактивных веществ.
- Сон 8 часов минимум, больше 10 также не рекомендуется, возможны застойные процессы.
- Минимальная полезная физическая активность. Прогулки или ЛФК. Не более. Изнурение для здоровых людей опасно, стоит ли говорить, какие последствия ждут сердечника?
- Питьевой режим — 1.5-2 литра в сутки.
- Соль — 7 граммов, не свыше того.
- Коррекция рациона. Больше витаминов, минералов, белка, меньше углеводов, никакого фаст-фуда, консервов и полуфабрикатов. Также жирного, жареного, копченостей.
При успешном лечении есть шансы на долгую жизнь. Но ограничения станут непременным условием, хотя изменив к ним отношение, возможно переносить новую парадигму с радостью, а не как тяжелую повинность.
Шансы и осложнения
Прогноз жизни при дилатационной кардиомиопатии на ранних стадиях условно-благоприятный. В отсутствии органических причин продолжительность неопределенно долгая.
Неблагоприятные факторы:
- Старческий возраст.
- Наличие семейного компонента.
- Генетические патологии в анамнезе.
- Вредные привычки.
- Повышенная масса тела.
- Недостаточный отклик на лечение.
- Артериальная гипертензия, сахарный диабет в качестве сопутствующих проблем.
Вероятность летального исхода без медицинской помощи — 60% в перспективе пары лет. При условии терапии — 10-20%.
Осложнения:
- Внезапная смерть в результате остановки сердца.
- Кардиогенный шок.
- Инфаркт.
- Инсульт.
- Полиорганная недостаточность.
- Тромбоэмболия.
В заключение
Дилатационная кардиомиопатия — расширение камер органа по врожденным или приобретенным причинам. При постоянных профилактических осмотрах пропустить начало болезни невозможно, что ассоциировано с хорошим общим прогнозом.
Диагностика минимальна, проблем с верификацией обычно нет. Лечение консервативное, на протяжении всей жизни.
Хирургическая методика применяется редко, только по показаниям. На фоне кардиомиоапатии вмешательство несет большие риски. Все решается на усмотрении специалиста при учете мнения человека.
Гипертрофическая кардиомиопатия (ГКМП): диагностика и лечение
Патологии сердечнососудистой системы многообразны по своему характеру, численность самостоятельных единиц в классификаторе достигает сотен. Они разнятся как по течению, так и по происхождению, но многие рано или поздно приводят к летальным последствиям. Без лечения — таких абсолютное большинство.
Ряд процессов вообще не подлежат какой-либо коррекции, возможно лишь продление жизни. Согласно статистическим данным, смертность от кардиальных проблем в мире находится на первом-втором местах по количеству ситуаций.
Гипертрофическая кардиомиопатия — это врожденный или приобретенный порок развития сердца, когда объем мышечного слоя левого, реже правого желудочка спонтанно растет.
Заболевание спорное. Ученые до сих пор не могут придти к единому мнению относительно генеза состояния.
Одни указывают на чисто генетический характер (то есть явление сопряжено только с семейным фактором), иные же говорят о высокой вероятности спорадических моментов (возможно спонтанное, вторичное развитие).
Истина находится где-то посредине. В любом случае, болезнь без должного лечения на ранних стадиях несет колоссальную опасность.
Механизм развития патологии
В основе генеза состояния лежат два противоположных процесса.
Первый — это так называемая слабость миокарда. Она обуславливает недостаточную сократимость кардиальных структур в систолу, также малый объем поступающей крови в момент полного расслабления органа.
Отсюда нарушение нормального снабжения кислородом и необходимыми веществами тканей. На ранних этапах это малозаметный процесс, по мере усиления ишемии растут органические отклонения.
Тело, стремясь скомпенсировать функциональную несостоятельность, наращивает объем мышечной ткани. Но это бесполезно, поскольку значительные объемы сердца не равны адекватной активности.
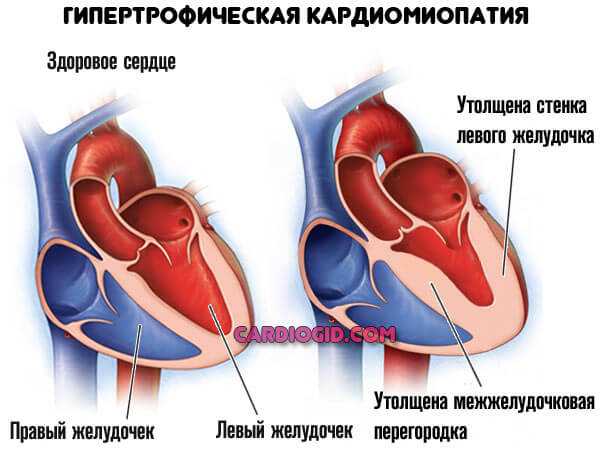
Напротив, происходит еще большее расслабление миокарда, поскольку нарушается проводимость пучков Гиса. Как итог пациент имеет существенное разрастание тканей органа, его патологическое увеличение с падением гемодинамического потенциала.
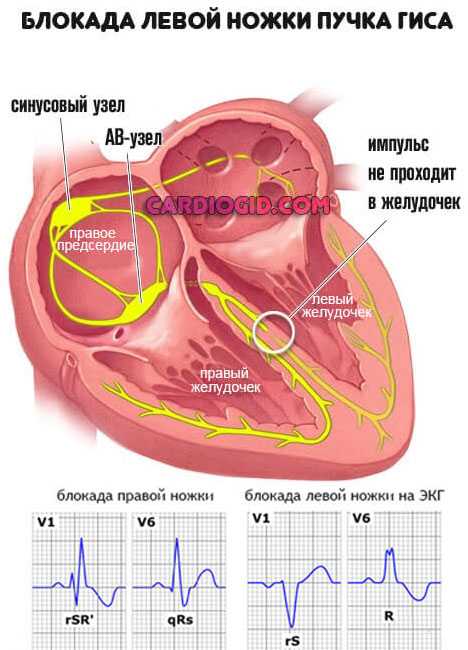
В перспективе нескольких лет запущенный вариант приводит к смерти от остановки сердца. Реанимационные мероприятия смысла не имеют, поскольку анатомический дефект слишком выражен.
Второй клинический вариант кардимиопатии — гипертрофия межжелудочковой перегородки. Он встречается на фоне стеноза митрального клапана, его пролапса или заращения в результате первичных патологических процессов.
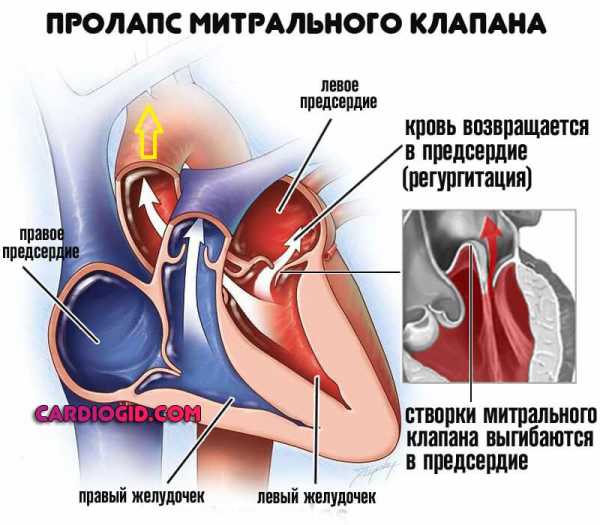
Как следствие опять же падает количество крови, которая транспортируется по камерам органа. Дальнейшая схема развития идентична.
В редких случаях, например, на фоне врожденных генетических синдромов или фенотипических отклонений во внутриутробный период, встречается сочетанный процесс. Когда работают сразу оба механизма. Это потенциально более опасно и труднее устранимо.
Перспективы развития летальных осложнений при изолированных дефектах первого или второго вида составляют от 5 до 20 лет, на фоне лечения и того больше.
Если же присутствуют сразу два порока (говоря условно), сроки сокращаются до 2-5 лет, даже медицинская помощь не гарантирует стабилизации состояния.
Потому необходимо проходить профилактические осмотры каждые полгода-год, если в анамнезе есть патологии кардиальных структур — еще чаще.
Классификация
Разграничение гипертрофической кардиомиопатии (сокращенно ГКМП) проводится по нескольким основаниям. Болезнь имеет собственный код по МКБ-10: I42.2, но шифр не отражает всей полноты процесса.
Исходя из распространенности явления, выделяют:
- Поражение левого желудочка. Потенциально летальное состояние. Поскольку нарушается нормальное движение крови по большому кругу. Это значит, что с течением времени нарастают явления гипоксии всех тканей. Особенно выражены признаки со стороны головного мозга, печени, почек.
- Разрастание правого желудочка. Считается относительно менее опасным. По мере развития, клиническая картина проявляется дыхательной недостаточностью и общими проблемами с легкими. Страдает малый круг.
- Двустороннее отклонение. Вбирает в себя типичные признаки одного и другого, существенно ухудшая прогноз.
В зависимости от объемов циркулирующей крови называют:
- Разновидность с обструкцией выносящего тракта.
- Тип без такового.
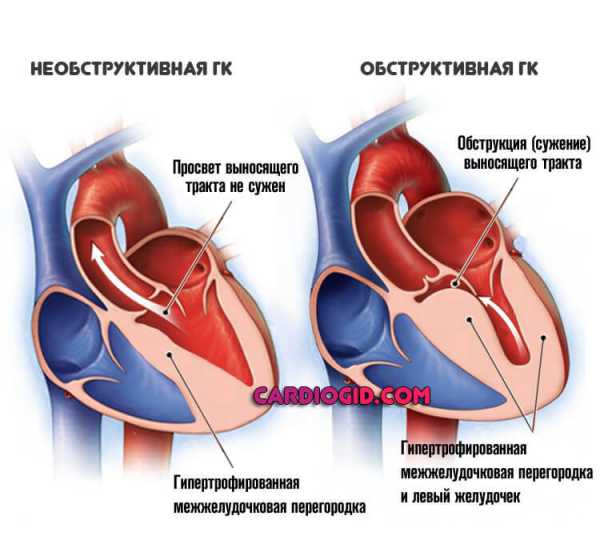
Клиническое значение данная классификация имеет только для врачей. В первой ситуации количество жидкой соединительной ткани, выбрасывающейся в систолу, падает за счет сужения кардиальных структур.
Сама по себе гипертрофическая кардиомиопатия левого желудочка имеет две основных формы:
- Симметричную. Когда поражение затрагивает в равной мере все отделы. Встречается, примерно, в 25% случаев, считаясь менее распространенной разновидностью. Дает знать о себе тяжелыми отклонениями в работе кардиальных структур. Вероятность успешного лечения падает.
- Асимметричную. Когда миокард поражен на отдельных участках либо на нескольких, но неравномерно.
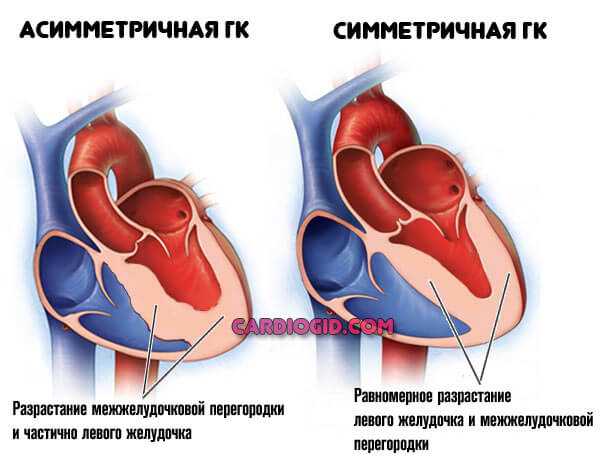
Наконец, в зависимости от характера патологического процесса, степени отклонения от нормы можно назвать:
- Гипертрофическую кардиомиопатию легкую. Когда мышца утолщена до размеров 15-20 мм.
- Среднюю. Характеризуется разрастанием анатомического образования до 25 мм.
- Тяжелую. Более указанного значения.
Соответственно, протекают подобные типы неодинаково. Чем крупнее сердце, тем хуже оно сокращается, перекачивает кровь, снабжает себя. К тому же растет вероятность внезапной остановки.
Указанные классификации играют большую роль в определении диагностической и терапевтической тактики на любом этапе. Прогнозы благоприятны только на ранних стадиях и то не во всех случаях.
Причины
Факторы развития можно подразделить на две группы. Первая касается врожденных моментов.
Крупная категория ученых и кардиологов практиков указывает на преимущественно генетическую этиологию процесса. Так это или нет — сказать сложно. Но наследственный фактор имеет большое клиническое значение.
Доказано, если в роду был человек, страдавший рассматриваемым состоянием, риск проявления у потомка растет на 25-30%.
Также играет роль нарушение нормального генотипа. Характер наследования — аутосомно-доминантный. То есть достаточно, чтобы поврежденный участок присутствовал хотя бы у одного родителя, что обуславливает значительную распространенность процесса.
Другая группа ученых и практиков говорит о преимущественно приобретенных причинах складывания патологического явления, а факт наличия подобного состояния у новорожденных объясняется нарушением внутриутробного развития плода.
По всей видимости, имеет место как то, так и другое в разных клинических случаях. Также известно, что кардиомиопатия гипертрофическая — не чисто генетическое заболевания. Она может обуславливаться сторонними отклонениями.
Среди которых:
- Воспалительные процессы в сердце. Особенно часто встречается миокардит, поражение мышечного слоя. Возникает на фоне инфекций, аутоиммунных явлений. Сопровождается длительными болями в грудной клетке, одышкой и ускорением ритма. Лечится в стационаре, с применением антибиотиков. Риск развития порока на фоне перенесенного воспаления высок. Во многом это обусловлено рубцеванием кардиальных структур. Наращивание массы — компенсаторный механизм, изначально ущербный.
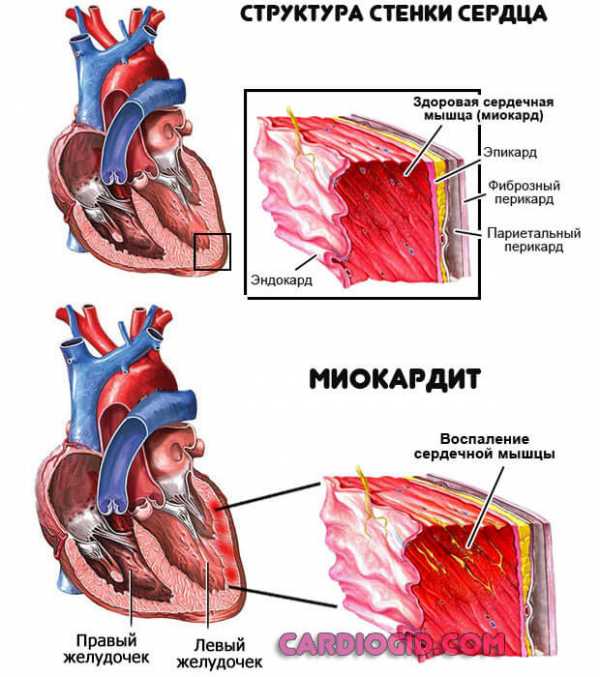
- Врожденные и приобретенные пороки сердца. Точно не известно, могут ли они непосредственно детерминировать кардиомиопатию гипертрофического типа. Но часто данное состояния встречается у пациентов с прочими отклонениями анатомического развития. Исследования в этой сфере ведутся, конкретных выводов пока недостаточно для обобщенного понимания проблемы.
- Ревматизм. Системное аутоиммунное заболевание с рецидивирующим течением. Имеет деструктивно-воспалительный характер. Лечение длительное, порой пожизненное. Качество восстановления зависит от момента начала терапии, особенностей организма пациента. На формирование кардиомиопатии потребуется не один год.
- Стеноз митрального клапана. Также пролапс и прочие варианты. Единственные пороки, которые доказано влияют на возможность развития кардиомиопатии гипертрофического типа. Характеризуется регургитацией (обратным током крови в предсердия), нарушением гемодинамики, порой фатальным. На фоне длительного вялого течения порока происходит параллельное формирование иных дефектов.
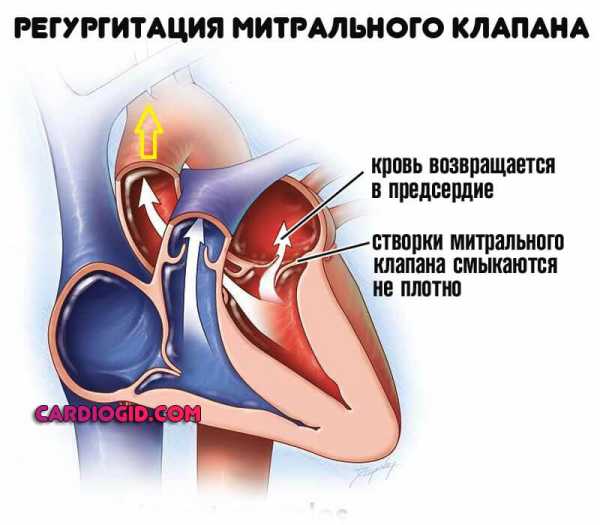
- Инфаркт в анамнезе. Острое нарушение трофики мышечного слоя. Как итог — резкое падение сократительной способности, гемодинамики. Без своевременной помощи неминуема смерть больного. Даже при успешном лечении образуются участки замещения функциональных тканей рубцовыми. Они не способны сокращаться, выступают заполнителями нарушенного пространства. Отсюда необходимость наращивания объемов миокарда, это также компенсаторный механизм.
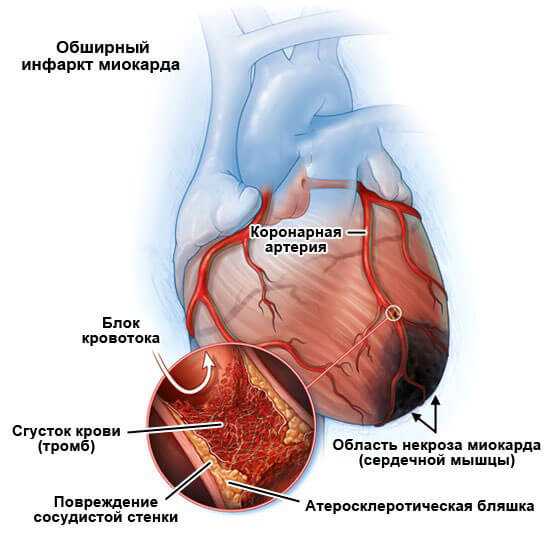
- Воспаление околосердечной сумки. Относительно редкое состояние (3-5% случаев всех первичных патологий подобного рода). Имеет инфекционное, реже иммунное происхождение. Характеризуется стремительным агрессивным течением, выраженной клиникой. Нередко осложняется воспалением миокарда (сказать точно, обуславливает ли первое второе или наоборот трудно). Лечение в стационаре под наблюдением врача.
Травмы грудной клетки с повреждением кардиальных структур.
Факторы риска
Большое значение имеют и так называемые факторы риска. Они предрасполагают к формированию опасных состояний. Среди таковых:
- Гиподинамия. Или недостаточная физическая активность пациента. По причине быта, профессиональной деятельности, длительного нахождения в постели.
- Курение. Продолжительное. Особенно рискуют пациенты с приличным стажем потребления табачной продукции.
- Ожирение. Опасно не само по себе. Все пациенты с избыточной массой тела имеют проблемы с метаболизмом и обменом липидов.
- Чрезмерная физическая нагрузка. Формируется гипертрофия миокарда так называемого естественного типа. Назвать таковой ее можно с большой долей условности. Пациент действительно не испытывает дискомфорта, но в определенный момент анатомические изменения, необходимые для обеспечения уровня механической активности, обернутся против человека.
- Алкоголизм.
- Потребление наркотических веществ.
- Длительное применение препаратов, оказывающих воздействие на сердце и сосуды.
- Артериальная гипертензия в анамнезе.
- Ишемическая болезнь.
Типичные симптомы
Признаки патологического процесса на ранних стадиях отсутствуют полностью. По мере прогрессирования, возникают следующие проявления:
- Одышка. Сначала в момент интенсивной физической нагрузки. Поскольку мало кто обеспечивает себя таким уровнем активности, проявления нет. Позже в состоянии покоя. Пациент не может подняться по лестнице, затем пройти по улице, а потом и вовсе встать с постели. Обнаружение отклонения возможно с помощью специальных тестов (велоэргометрия как щадящий вариант).
- Боли в груди. Ненадежный диагностический признак. Могут иметь внекардиальное происхождение. Текут приступообразно, развиваются спонтанно. Особенно на фоне стресса, активности, потребления спиртного, табака, препаратов.
- Сонливость, слабость, ощущение ватности тела, снижение работоспособности.
- Повышенная потливость в ночное время.
- Цианоз носогубного треугольника.
- Головные боли.
- Вертиго. Оба признака отмечаются на поздних стадиях, когда падает гемодинамика.
- Тошнота, рвота (редко).
- Бледность кожных покровов.
- Выраженные аритмии по типу тахикардии, брадикардии, экстрасистолии или фибрилляции. Протекают приступами или на постоянной основе.
Симптомы неспецифичны. Определить патологию по ним невозможно. При обнаружении хотя бы одного описанного явления стоит обращаться к докторам.
Показания к госпитализации
Перечень таковых относительно широк. Специальных клинических рекомендаций не разработано. Ориентируясь на опыт лечащих врачей можно говорить о следующих моментах:
- Снижение частоты сердечных сокращений до 60 ударов в минуту и менее. Критические состояния требуют вызова скорой помощи для решения вопроса транспортировки в профильный стационар.
- Тахикардия на уровне свыше 120 ударов, при условии, что длится она более 2 часов подряд.
- Выраженная степень гипертрофической кардиомиопатии (средняя по указанной выше классификации и далее).
- Аритмия иного типа (экстрасистолия, фибрилляция). Субъективно ощущается как резкий толчок в груди, переворачивания сердца, неправильное, неравномерное биение.
- Интенсивный болевой синдром. До выяснения причины.
- Сильная одышка, вплоть до невозможности выполнения простых бытовых обязанностей.
- Неврологические нарушения дефицитарного плана (речевая, зрительная, слуховая, прочие дисфункции).
В любом спорном случае, при подозрениях нужно обращаться к докторам. Также вызывать скорую помощь. Решение вопроса о госпитализации — прерогатива квалифицированного персонала.
Что необходимо обследовать?
Диагнотику проводят специалисты по кардиологии. Первичные мероприятия направлены на определение вероятной болезни. Только затем показана верификация, уточнение версии.
Полный перечень мероприятий таков:
- Устный опрос пациента о его жалобах.
- Сбор анамнестических данных.
- Измерение артериального давления, также частоты сердечных сокращений.
- Суточное мониторировние с применением автоматического тонометра программируемого типа.
- Электрокардиография для оценки функциональной активности сердечной мышцы, выявления аритмии.
- Эхокардиография. Основная методика в диагностике. Применяется чаще всего в первый же момент. Позволяет визуализировать ткани, хотя требуется значительная квалификация от медицинского персонала.
- Анализ крови общий и биохимический.
- Сцинтиграфия по показаниям.
- МРТ. Используется в крайних случаях, как способ детального отображения кардиальных структур. Считается относительно дорогим и малодоступным методом, по крайней мере, в реальности стран СНГ.
Основные мероприятия направлены на установление диагноза, его верификацию и определение причины проблемы.
Лечение
Лечение гипертрофической кардиомиопатии заключается в устранении симптомов и первопричины состояния. Терапия систематическая, назначается в момент обнаружения патологического процесса. Имеет две плоскости.
Первая — этиотропное воздействие. Возможно при приобретенном характере кардиомиопатии. В случае с генетическими дефектами смысла не имеет.
Вторая — симптоматическая. Купирование проявлений и повышение качества жизни. Используются консервативные и оперативные методики.
Среди первых, применяются такие препараты:
- Антигипертензивные. Классическая схема — Дилтиазем или Верапамил, Периндоприл и Моксонидин в комплексе.
- Противоаритмические. Хиндин, Амиодарон.
- Кардиопротекторы.
- Средства на основе калия и магния (Аспаркам и прочие).
Гликозиды противопоказаны. Возможны другие типы на усмотрение врача.
Хирургическое лечение показано в крайних случаях. В основном это мера борьбы с приобретенным процессом.
Методики различны. Так, гипертрофическая обструктивная кардиомиопатия устраняется путем протезирования аортального клапана или стентирования. Возможна установка кардиостимулятора, восстановление анатомической целостности органа и пр. Вариантов масса.
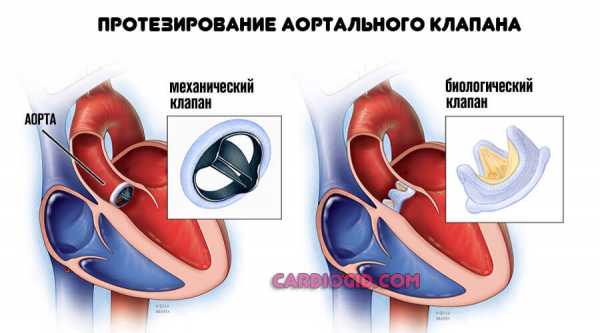
Применение народных рецептов не имеет смысла. Требуется изменить образ жизни (см. пункт профилактика).
Прогноз и возможные осложнения
Определить исход на раннем этапе ведения пациента сложно. Сказать стоит одно. Начальные стадии патологического процесса относительно благоприятны, поскольку выживаемость составляет 85-90%.
По мере прогрессирования цифры становятся все более пессимистичными. В любом случае, полное излечение невозможно. Дефект в какой-то степени останется все равно.
Но, при минимальных отклонениях вероятна стабилизация состояния и увеличение продолжительности жизни. До каких пределов — сказать трудно. Обычно не меньше, чем у среднестатистического человека.
Осложнения развиваются на любой стадии, но риски выше при запущенном процессе.
Среди последствий:
- Остановка сердца.
- Кардиогенный шок.
- Гипертонический криз.
- Инсульт.
- Инфаркт.
- Полиорганная недостаточность.
- Сосудистая деменция.
Также существенно снижается качество жизни. Все указанные осложнения рано или поздно ведут к смерти пациента.
Предотвращение возможно, но требуется приложить усилия. Как самому больному, так и его врачу.
Профилактика
Как в момент лечения гипертрофической кардиомиопатии, так и в рамках предотвращения таковой показаны специальные действия.
Меры превенции представляют определенные сложности. В первую очередь в полевом отношении. Трудно изменить образ мышления, привычки. Но здоровье того требует.
Среди рекомендаций:
- Полный отказ от курения, спиртного, наркотических веществ.
- Нормализация физической активности. Никаких перегрузок, но и гиподинамия недопустима. Примерно час-два прогулок в день, ЛФК, плавания, этого достаточно.
- Питьевой режим. 1.5-2 литра в сутки. Если есть артериальная гипертензия — по нижней границе.
- Соль в пределах разумного (7 граммов вполне хватит). Радикального исключения из рациона быть не должно.
- Пересмотр подхода к питанию. Больше витаминов, белка, меньше углеводов, жиров, никаких жареных, копченых блюд, фаст-фуда, полуфабрикатов, консервов. Рекомендуемый лечебный стол — №10.
- Полноценный сон не менее 8 часов.
- Избегание стрессов по возможности.
- Постоянный контроль артериального давления и частоты сердечных сокращений.
Также стоит своевременно лечить все выявленные заболевания, независимо от типа. В определенный момент они могут неожиданным образом проявить себя. Каждые полгода-год посещать кардиолога — это хорошая практика.
В заключение
Гипертрофическая форма кардиомиопатии представляет собой вариант патологического процесса потенциально летального рода.
Прогрессирование процесса неминуемо, формирование осложнений — вопрос времени.
Чтобы предотвратить пессимистичный итог нужно лечить патологию с первых же дней. Прогноз благоприятен только на ранней стадии.
Восстановление проводится медикаментозными, реже хирургическими методами под постоянным контролем врача-кардиолога. Рекомендуемая частота посещения специалиста — раз в три месяца.
Кардиомиопатия такоцубо - причины, симптомы, диагностика и лечение
Кардиомиопатия такоцубо — это преходящая острая сердечная недостаточность, сопровождающаяся расширением верхушки левого желудочка. Основные клинические проявления включают резкую загрудинную боль, одышку, тахикардию. Иногда развиваются пресинкопальные состояния и обмороки. Для диагностики назначают лабораторные анализы (определение уровня креатинкиназы, тропонина, ПНП), инструментальные неинвазивные (ЭКГ, ЭхоКГ, МРТ сердца) и инвазивные методы (коронарография, сцинтиграфия). При синдроме такоцубо показано медикаментозное лечение — гипотензивные средства, антикоагулянты, транквилизаторы. При кардиогенном шоке проводится внутриаортальная контрпульсация.
Общие сведения
Кардиомиопатия такоцубо имеет множество синонимов: синдром «разбитого сердца» (СРС), стресс-индуцированная кардиомиопатия, синдром верхушечного баллонирования. Необычное название «такоцубо» происходит от японского слова tako-tsubo, что в переводе означает «ловушка для осьминога». Это приспособление имеет широкое основание и узкое горлышко — похожую форму приобретает левый желудочек во время приступа. Кардиомиопатия такоцубо выявляется у 1-2% пациентов с острым коронарным синдромом. Более 90% больных — женщины в постменопаузальном периоде.
Кардиомиопатия такоцубо
Причины
Точные этиологические факторы развития кардиомиопатии такоцубо неизвестны. В качестве ведущих рассматриваются две рабочие гипотезы:
- Стрессовая. Основная теория заключается во влиянии стрессовых ситуаций на выработку гормонов, что приводит к транзиторным нарушениям работы миокарда. Триггерами начала болезни «разбитого сердца» бывают как эмоциональные потрясения (смерть близких, насилие, попадание в чрезвычайную ситуацию), так и медицинские причины — операция, астматический приступ.
- Наследственная. В последние годы разрабатывается теория о генетической предрасположенности к синдрому такоцубо. Описано несколько случаев появления кардиомиопатии у близких родственников. Предположительно, такие эпизоды вызваны наличием мутаций в генах, которые отвечают за чувствительность рецепторов к катехоламинам и эстрогенам. У страдающих стресс-индуцированной кардиомиопатией наблюдается функциональный полиморфизм этих генов.
Факторы риска
Среди способствующих факторов наиболее важны неуправляемые — пол и возраст. Кардиомиопатии такоцубо преимущественно встречается у женщин после 60 лет, что обусловлено большей чувствительностью к эмоциональным стрессам и гормональными перестройками в периоде постменопаузы. Фактором риска является наличие хронической сердечно-сосудистой патологии, которая увеличивает процент осложненного течения синдрома такоцубо. К управляемым факторам принадлежат: избыточный вес, частые стрессы дома или на работе, вредные привычки.
Патогенез
В клинической кардиологии выделяют несколько патогенетических механизмов развития синдрома. Характерное расширение верхушки сердца обусловлено аномальным расположением левой нисходящей артерии, которая кровоснабжает этот отдел сердца. Переходящий сбой в сократительной способности миокарда, вероятно, связан с одновременным вазоспазмом нескольких коронарных артерий и транзиторной ишемией сердечной стенки.
Другая патогенетическая теория предполагает множественную дисфункцию микрососудистого русла. Мелкие ветви коронарных артерий подвергаются спазму или дегенеративно-дистрофическим изменениям, в результате чего нарушается оксигенация миокарда левого желудочка. Важную роль в патогенезе кардиомиопатии играет чрезмерная активация симпатической системы и выделение катехоламинов, которые влияют на состояние сосудистого русла.
Классификация
Заболевание подразделяется на варианты в зависимости от локализации анатомических изменений. В 75-80% случаев развивается апикальное расширение желудочка, у 10-15% больных диагностируют срединно-левожелудочковый вариант кардиомиопатии. Более редкие разновидности поражения: инвертированный (менее 5%), бивентрикулярный (до 0,5%), правожелудочковый. Кардиологи чаще пользуются классификацией по клиническому течению, которая включает:
- Первичный синдром такоцубо. Расстройство возникает у здорового человека и зачастую имеет конкретные триггерные факторы. Тяжелые клинические симптомы служат причиной для обращения за экстренной медицинской помощью.
- Вторичный синдром такоцубо. Состояние наблюдается у пациентов, которые госпитализированы по поводу хирургической, акушерской или другой патологии. Кардиомиопатия осложняет течение основного заболевания, что обуславливает особые подходы к диагностике и лечению.
Симптомы
Основное проявление стресс-индуцированной формы кардиомиопатии — внезапная загрудинная боль. Приступ кардиалгии чаще возникает на фоне сильного эмоционального потрясения или испуга. Человек испытывает сжимающую или острую боль в области проекции сердца, которая может иррадиировать в плечо, лопатку. Характерным признаком синдрома такоцубо является «волна давления», которая поднимается от груди к шее и голове.
Болевой синдром обычно сопровождается повышенной потливостью, тревожностью. Одновременно с болью появляются одышка, чувство нехватки воздуха. Человек ощущает сильное сердцебиение, слабость в ногах. При этом кожа бледнеет, становится холодной и влажной. Часто появляется головокружение, потемнение в глазах. Тяжело протекающий приступ кардиомиопатии заканчивается обмороком вследствие снижения сердечного выброса.
Осложнения
Ранее кардиомиопатия такоцубо рассматривалась как доброкачественное заболевание без последствий. Но при несвоевременном обращении или неправильной лечебной тактике осложнения возникают у 52% больных. Среди острых последствий синдрома «разбитого сердца» выделяют: поражение правого желудочка (18-34%), митральную регургитацию (14-25%), обструкцию выходного тракта левого желудочка (10-25%).
В первые дни после манифестации кардиомиопатии сохраняется высокий риск фибрилляции предсердий (5-15%). У пациентов с отягощенным преморбидным фоном в 4% случаев наблюдаются желудочковые аритмии, в 1,5% — кардиогенный шок. Летальность при тяжелом течении синдрома составляет около 1%. У 5% больных, перенесших острый приступ, наступает рецидив, обусловленный теми же пусковыми механизмами.
Диагностика
По клинической картине индуцированная стрессом кардиомиопатия напоминает приступ стенокардии или инфаркт миокарда, что требует от врача-кардиолога проведения дифференциальной диагностики. Обследование необходимо выполнить в максимально короткие сроки. Диагностическая программа включает ряд лабораторно-инструментальных исследований:
- Электрокардиографию. Типичные изменения на ЭКГ регистрируют у 95% пациентов в острой фазе СРС. Основные признаки заболевания: изменение положения сегмента ST относительно изоэлектрической линии, блокада ножки пучка Гиса. Через сутки после развития кардиомиопатии наблюдается удлинение интервала QT.
- Определение биомаркеров. Первично определяются уровни сердечного тропонина и креатинкиназы, количество которых незначительно повышено. В остром периоде кардиомиопатии выявляют увеличение концентрации предсердного натрийуретического пептида (ПНП).
- Эхокардиография. Трансторакальная ЭхоКГ выполняется всем больным с предположительным диагнозом стресс-индуцированной кардиомиопатии. При УЗИ сердца выявляют большую площадь дисфункции миокарда, симметричные нарушения сокращения стенок левого желудочка.
- Коронарная ангиография. Назначение исследования в ургентном порядке целесообразно для исключения инфаркта миокарда. При кардиомиопатии такоцубо визуализируются неизмененные коронарные сосуды с сохраненным кровотоком. Для уточнения диагноза рекомендована левожелудочковая вентрикулография.
- Высокоспециализированные методы. Для разграничения кардиомиопатии такоцубо и других кардиологических болезней применяется МРТ сердца, отображающая участки поражения миокарда в трехмерном режиме. При невозможности проведения исследования показана перфузионная сцинтиграфия миокарда.
Вентрикулография. Типичная для кардиомиопатии такоцубо форма расширения верхушки левого желудочка.
Лечение
Консервативная терапия
Кардиомиопатия такоцубо относится к неотложным состояниям, поэтому медицинскую помощь оказывают в условиях специализированного кардиологического стационара или в отделениях интенсивной терапии. Обычно назначается поддерживающая лечебная схема, которая обеспечивает постепенное восстановление функциональной активности миокарда. Для лечения используют следующие группы лекарственных препаратов:
- Кальциевые сенсибилизаторы. Рекомендованы при резком снижении фракции выброса и динамической обструкции кровотока из левого желудочка. Медикаменты (в основном — левосимендан) улучшают показатели перфузии и микроциркуляции, предотвращают развитие кардиогенного шока.
- Гипотензивные препараты. Средства из этой группы используются при легком варианте течения кардиомиопатии для устранения возможных провоцирующих факторов. Назначаются бета-адреноблокаторы, антагонисты кальция, диуретики.
- Антикоагулянты. Применяются для профилактики образования апикальных тромбов и растворения уже имеющихся кровяных сгустков. Показано профилактическое введение низкомолекулярных гепаринов в терапевтических дозах, прием ацетилсалициловой кислоты.
- Транквилизаторы. Препараты целесообразно использовать, если появлению симптомов кардиомиопатии такоцубо предшествовал сильный стресс. Помимо влияния на психоэмоциональное состояние транквилизаторы обладают дополнительным анальгетическим эффектом.
Хирургическое лечение
Если кардиомиопатия такоцубо осложняется кардиогенным шоком, используют современный малоинвазивный метод — внутриаортальную баллонную контрпульсацию. Процедура предполагает механическое нагнетание крови в большой круг кровообращения с помощью небольшого медицинского насоса, установленного в аорте. Методика внутриаортальной контрпульсации улучшает гемодинамические показатели.
Прогноз и профилактика
При своевременной медицинской помощи большинство пациентов переживают острый приступ кардиомиопатии без отдаленных осложнений. Долгосрочный прогноз, как правило, благоприятный. Даже у больных с хроническими сердечно-сосудистыми заболеваниями сократительная способность миокарда после приступа индуцированной стрессом кардиомиопатии восстанавливается почти полностью. Специфическая профилактика патологии не разработана.
Кардиомиопатия такоцубо — Википедия
 Японские ловушки осьминогов, в честь которых названо заболевание.
Японские ловушки осьминогов, в честь которых названо заболевание. Кардиомиопа́тия такоцу́бо (от яп. 蛸壺, такоцубо — ловушка для осьминога), транзито́рное шарообра́зное расшире́ние верху́шки ле́вого желу́дочка[2], стре́ссовая кардиомиопа́тия — вид неишемической кардиомиопатии, при котором развивается внезапное преходящее снижение сократимости миокарда (сердечной мышцы). В связи с тем, что слабость миокарда может вызываться эмоциональным стрессом, например, смертью любимого человека, состояние также называется «синдромом разбитого сердца»[3].
Стрессовая кардиомиопатия — хорошо распознаваемая причина острой сердечной недостаточности, летальных желудочковых аритмий и разрыва стенки желудочка.[4] В типичных случаях кардиомиопатия такоцубо проявляется внезапным развитием сердечной недостаточности или болей в груди, сочетающихся с изменениями на ЭКГ, характерными для переднего инфаркта миокарда.
В ходе наблюдения за пациентами, часто отмечается выбухание верхушки левого желудочка с гиперкинезом его основания. Картина выбухания верхушки сердца, сочетающегося с сохранённой функцией его основания, дала синдрому японское название тако цубо («ловушка осьминога»).[5]
В качестве причины рассматривается повышение содержания в крови катехоламинов (преимущественно адреналина). В план обследования пациентов включается коронарография, при которой не выявляется гемодинамически значимых стенозов, способных привести к левожелудочковой дисфункции. При благоприятном исходе начального приступа функция левого желудочка восстанавливается в течение 2 месяцев. Обычно кардиомиопатия такоцубо наблюдается у женщин в постменопаузе. [6] Часто в анамнезе больных отмечается недавний тяжёлый эмоциональный или физический стресс.[6]
Вентрикулограмма левого желудочка во время систолы, демонстрирующая характерное шарообразное расширение и неподвижность верхушки сердца у пациента с кардиомиопатией такоцубо.Этиология кардиомиопатии такоцубо ясна не полностью, однако предполагается несколько механизмов.
- Заворачивающаяся левая передняя нисходящая артерия (англ. wraparound LAD). Левая передняя нисходящая артерия кровоснабжает переднюю стенку левого желудочка у большинства пациентов. Если эта артерия заворачивается вокруг верхушки сердца, она может отвечать также за кровоснабжение верхушки и нижней стенки сердца. Некоторые исследователи отмечали корреляцию между кардиомиопатией такоцубо и этим типом левой передней нисходящей артерии.[7] Вместе с тем, другие исследователи показали, что этот анатомический вариант недостаточно типичен для объяснения причины кардиомиопатии такоцубо.[8] Эта теория также не объясняет встречающиеся случаи акинеза межжелудочковой перегородки и основания сердца.
- Транзиторный вазоспазм. Некоторые первые исследователи кардиомиопатии такоцубо предполагали, что множественные одновременные спазмы коронарных артерий способны вызывать снижение кровотока, достаточное для развития преходящего сбоя в работе миокарда.[9] Другие исследования показали, что вазоспазм значительно менее распространён, чем считалось первоначально.[10][11][12] Также было отмечено, что вазоспазмы, даже многих артерий, не коррелировали по расположению с зонами гипокинеза миокарда.[13]
- Микрососудистая дисфункция. Эта теория предполагает, что развивается дисфункция мелких ветвей коронарных артерий, которые невозможно визуализировать посредством коронарографии. Изменения могут проявляться как микрососудистым вазоспазмом, так, возможно, и микроангиопатией, подобной наблюдаемой при сахарном диабете. В этих условиях мелкие артерии неспособны обеспечивать адекватную оксигенацию миокарда.
Вероятно, в развитии стрессовой кардиомиопатии имеют значение многие факторы — вазоспазм, недостаточность микроциркуляции и патологический катехоламиновый ответ.[14] При наблюдении больших групп пациентов указывается, что у некоторых из них кардиомиопатия такоцубо развивалась после эмоционального стресса или, в иных случаях, после предшествующего физического стресса (астматического статуса или внезапного заболевания). Примерно у одной трети пациентов стрессовый фактор отсутствовал.[15] Наблюдение больших групп пациентов в Европе показало, что кардиомиопатия такоцубо имеет несколько бо́льшую частоту встречаемости в зимнее время. Это может быть обусловлено двумя возможными патофизиологическими причинами: спазмом мелких ветвей коронарных артерий, преобладающим в холодную погоду, и вирусными инфекциями, например Parvovirus B19, которые чаще наблюдаются в зимний сезон.[16]
(A) Эхокардиограмма, демонстрирующая дилятацию левого желудочка в острую стадию. (B) Восстановление функции левого желудочка при повторной эхокардиографии через 6 дней.Кардиомиопатия такоцубо обнаруживалась у 1,7—2,2 % пациентов с острым коронарным синдромом.[16] Хотя первые случаи описаны у пациентов в Японии, кардиомиопатия такоцубо в последнее время отмечалась и у пациентов в США и Западной Европе. Вероятно, синдром не диагностировался до тех пор, пока не был детально описан в японской литературе.
Диагностика кардиомиопатии такоцубо может быть затруднена клинической картиной. Изменения на ЭКГ часто ошибочно трактуют как проявления переднего инфаркта миокарда.[6][17] Картина описывается острым началом преходящей дисфункции подвижности верхушки (выбухание) в сочетании с болью в груди, диспноэ, элевацией ST-сегмента, инверсией T-зубца или удлинением QT-интервала на ЭКГ. Подъём ферментов миокарда в худшем случае умеренный; отсутствует выраженная коронарная недостаточность.[16]
Диагноз устанавливается на основании патогномоничных изменений подвижности сердечной стенки — нормального сокращения или гиперкинеза основания левого желудочка в сочетании с акинезом или дискинезом остальных его отделов. Это сопровождается отсутствием признаков выраженной коронарной недостаточности, которая могла бы объяснить указанные нарушения сократимости. Хотя классическое ангиографическое описание кардиомиопатии такоцубо включает шарообразное расширение верхушки, встречаются и другие варианты — выбухание межжелудочковой перегородки или, в более редких случаях, выбухание других сегментов.[16][18][19][20][21]
Паттерны выбухания были классифицированы Симидзу и др. как тип такоцубо с апикальной акинезией и базальной гиперкинезией; обратная такоцубо с базальной акинезией и апикальной гиперкинезией; перегородочный тип с перегородочным выбуханием в сочетании с базальной и апикальной гиперкинезией; локальный тип с выбуханием других сегментов левого желудочка и клинической картиной такоцубоподобной левожелудочковой дисфункции.[19]
Есть сообщения, что патоморфологические изменения при этом виде кардиомиопатии представлены фокальным миоцитолизом; ассоциированных микробиологических агентов не выявляется. В некоторых случаях обнаруживалась инфильтрация малыми мононуклеарами; эти патологические находки позволяют предположить, что стрессовая кардиомиопатия является вариантом воспалительного заболевания сердца, а не коронарной патологией. Также имеются сообщения о гистологическом повреждении миокарда без ишемической болезни сердца.[22]
Терапия кардиомиопатии такоцубо в большинстве случаев поддерживающая. У пациентов с артериальной гипотензией используется поддержка инотропными препаратами или внутриаортальная баллонная контрпульсация. Стандартно назначают ацетилсалициловую кислоту[23], ингибиторы АПФ или антагонисты рецепторов ангиотензина I с целью снижения артериального давления, а также β-адреноблокаторы для контроля ЧСС и нитраты для устранения спазма коронарных артерий.[24] У многих пациентов функция левого желудочка восстанавливается в течение 2 месяцев.[25][26]
Несмотря на грозные исходные клинические проявления у некоторых больных, большинство пациентов переживают начальный приступ с очень низким уровнем больничной летальности или осложнений. После перенесённой острой стадии заболевания пациентов ожидает благоприятный исход с хорошим долгосрочным прогнозом.[5][16][18] Даже при тяжёлой систолической дисфункции в начале заболевания, сократительная способность миокарда начинает восстанавливаться уже в первые несколько суток и нормализуется в течение нескольких месяцев.[16][10][11][12] В 5 % случаев[24] возникает рецидив заболевания, вероятно, провоцируемый ассоциированным пусковым механизмом.[15][16]
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ Eshtehardi P., Koestner S.C., Adorjan P., Windecker S., Meier B., Hess O.M., Wahl A., Cook S. Transient apical ballooning syndrome--clinical characteristics, ballooning pattern, and long-term follow-up in a Swiss population (англ.) // International Journal of Cardiology (англ.)русск. : journal. — 2009. — July (vol. 135, no. 3). — P. 370—375. — PMID 18599137.
- ↑ Mayo Clinic Research Reveals 'broken Heart Syndrome' Recurs In 1 Of 10 Patients
- ↑ Akashi Y.J., Nef H.M., Mollmann, H., Ueyama T. Stress Cardiomyopathy (англ.) // Annual Reviews. — 2010. — Vol. 61. — P. 271—286. — doi:10.1146/annurev.med.041908.191750.
- ↑ 1 2 Gianni, M; Dentali F., Grandi AM et al. Apical ballooning syndrome or takotsubo cardiomyopathy: a systematic review (англ.) // European Heart Journal (англ.)русск. : journal. — Oxford University Press, 2006. — December (vol. 27, no. 13). — P. 1523—1529. — doi:10.1093/eurheartj/ehl032. — PMID 16720686.
- ↑ 1 2 3 Azzarelli S., Galassi A.R., Amico F., Giacoppo M., Argentino V., Tomasello S.D., Tamburino C., Fiscella A. Clinical features of transient left ventricular apical ballooning (англ.) // Am J Cardiol. : journal. — 2006. — Vol. 98, no. 9. — P. 1273—1276. — doi:10.1016/j.amjcard.2006.05.065. — PMID 17056345.
- ↑ Ibáñez B., Navarro F., Farré J., et al. [Tako-tsubo syndrome associated with a long course of the left anterior descending coronary artery along the apical diaphragmatic surface of the left ventricle.] (Spanish; Castilian) // Revista española de cardiología. — 2004. — Т. 57, № 3. — С. 209—216. — doi:10.1016/S1885-5857(06)60138-2. — PMID 15056424.
- ↑ Inoue, M; Shimizu M., Ino H et al. Differentiation between patients with takotsubo cardiomyopathy and those with anterior acute myocardial infarction (англ.) // Circ. J. : journal. — 2005. — Vol. 69, no. 1. — P. 89—94. — doi:10.1253/circj.69.89. — PMID 15635210.
- ↑ Kurisu S., Sato H., Kawagoe T et al. Tako-tsubo-like left ventricular dysfunction with ST-segment elevation: a novel cardiac syndrome mimicking acute myocardial infarction (англ.) // American Heart Journal (англ.)русск. : journal. — 2002. — Vol. 143, no. 3. — P. 448—455. — doi:10.1067/mhj.2002.120403. — PMID 11868050.
- ↑ 1 2 Tsuchuhashi K et al. JACC 2001
- ↑ 1 2 Kawai et al. JPJ 2000
- ↑ 1 2 Desmet et al. Heart 2003
- ↑ Abe et al. JACC 2003
- ↑ Wittstein I.S., Thiemann D.R., Lima J.A., et al. Neurohumoral features of myocardial stunning due to sudden emotional stress (англ.) // The New England Journal of Medicine : journal. — 2005. — February (vol. 352, no. 6). — P. 539—548. — doi:10.1056/NEJMoa043046. — PMID 15703419.
- ↑ 1 2 Elesber, A.A. Four-Year Recurrence Rate and Prognosis of the Apical Ballooning Syndrome (англ.) // J Amer Coll Card : journal. — 2007. — July (vol. 50, no. 5). — P. 448—452. — doi:10.1016/j.jacc.2007.03.050.
- ↑ 1 2 3 4 5 6 7 Eshtehardi P., Koestner S.C., Adorjan P., Windecker S., Meier B., Hess O.M., Wahl A., Cook S. Transient apical ballooning syndrome--clinical characteristics, ballooning pattern, and long-term follow-up in a Swiss population (англ.) // International Journal of Cardiology (англ.)русск. : journal. — 2009. — July (vol. 135, no. 3). — P. 370—375. — PMID 18599137.
- ↑ Bybee K.A., Motiei A., Syed I.S., Kara T., Prasad A., Lennon R.J., Murphy J.G., Hammill S.C., Rihal C.S., Wright R.S. Electrocardiography cannot reliably differentiate transient left ventricular apical ballooning syndrome from anterior ST-segment elevation myocardial infarction (англ.) // Journal of Electrocardiology (англ.)русск. : journal. — 2006. — PMID 17067626.
- ↑ 1 2 Pilgrim T.M., Wyss T.R. Takotsubo cardiomyopathy or transient left ventricular apical ballooning syndrome: A systematic review (англ.) // International Journal of Cardiology (англ.)русск. : journal. — 2008. — March (vol. 124, no. 3). — P. 283—292. — PMID 17651841.
- ↑ 1 2 Shimizu M., Kato Y., Masai H., Shima T., Miwa Y. Recurrent episodes of takotsubo-like transient left ventricular ballooning occurring in different regions: a case report (англ.) // J. Cardiol. : journal. — 2006. — August (vol. 48, no. 2). — P. 101—107. — PMID 16948453.
- ↑ Hurst R.T., Askew J.W., Reuss C.S., Lee R.W., Sweeney J.P., Fortuin F.D., Oh J.K., Tajik A.J. Transient midventricular ballooning syndrome: a new variant (англ.) // Journal of the American College of Cardiology (англ.)русск. : journal. — 2006. — August (vol. 48, no. 3). — P. 579—583. — PMID 16875987.
- ↑ Yasu T., Tone K., Kubo N., Saito M. Transient mid-ventricular ballooning cardiomyopathy: a new entity of Takotsubo cardiomyopathy (англ.) // International Journal of Cardiology (англ.)русск. : journal. — 2006. — June (vol. 110, no. 1). — P. 100—101. — PMID 15996774.
- ↑ Dhar S., Koul D., Subramanian S., Bakhshi M. Transient apical ballooning: sheep in wolves' garb (англ.) // Cardiology in Review (англ.)русск.. — 2007. — Vol. 15, no. 3. — P. 150—153. — PMID 17438381.
- ↑ Medics can 'mend a broken heart'
- ↑ 1 2 A. John Camm, Thomas F. Luscher, Patrick Serruys. The ESC Textbook of Cardiovascular Medicine. — Wiley-Blackwell, 2006. — 1136 с.
- ↑ Akashi Y.J., Nakazawa K., Sakakibara M., Miyake F., Koike H., Sasaka K. The clinical features of takotsubo cardiomyopathy (англ.) // QJM: An International Journal of Medicine (англ.)русск.. — 2003. — Vol. 96, no. 8. — P. 563—573. — doi:10.1093/qjmed/hcg096. — PMID 12897341.
- ↑ Nyui N., Yamanaka O., Nakayama R., Sawano M., Kawai S. 'Tako-Tsubo' transient ventricular dysfunction: a case report (неопр.) // Jpn Circ J. — 2000. — Т. 64, № 9. — С. 715—719. — doi:10.1253/jcj.64.715. — PMID 10981859.