Нр ассоциированный что это такое
НР-ассоциированные болезни ЖКТ
Что собой представляют недуги желудочно-кишечного тракта? Современная медицина выделяет целый комплекс постоянных или периодических признаков, которые нельзя отнести к биохимическим изменениям или каким-либо нарушениям органического характера.
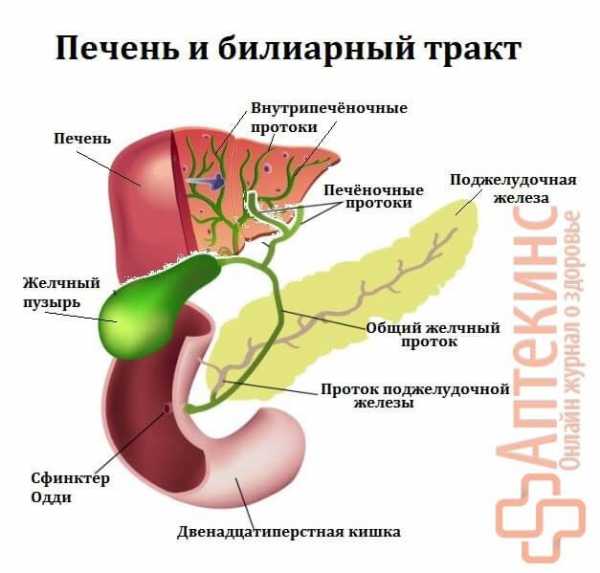
История болезни: хронический гепатит с ассоциированным циррозом печени
Основным симптомом патологий ЖКТ является болевой синдром в области живота. Самыми распространенными недугами являются: язвы, гастриты, дуоденит, панкреатит, холецистит,гепатит, колит и т.д.
Каждое в отдельности заболевание имеет свои особенные признаки и требует индивидуального лечения. Так, например, история болезни: хронический гепатит с ассоциированным циррозом печени прослеживается часто. Как утверждает практика 20% всех больных гепатитом С имеют проблемы с печенью. Скорость формирования цирроза может быть разной, все зависит от индивидуальных особенностей каждого человека в отдельности.
История болезни: хронический НР-ассоциированный гастрит (педиатрия)
Поверхностное воспаление стенки желудка называют гастритом. Страдают такой патологией почти половина всего взрослого населения планеты. Выделяют хронический гастрит и острый. Острая проблема появляется вследствие раздражителей – из-за бактерий, механических повреждений, на фоне приема лекарств или из-за обжигающего вещества.
В свою очередь хронический НР-ассоциированный гастрит в педиатрии – это постоянный воспалительный процесс на слизистой части желудка. Патология может наблюдаться на разной глубине.
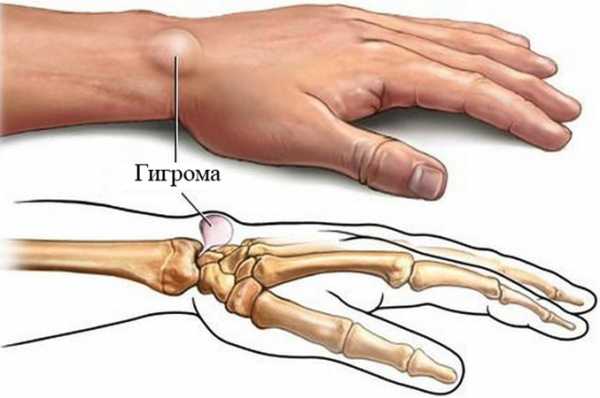
Хеликобактер, ассоциированный с язвенной болезнью
Человеческое тело наполняют разнообразные микроорганизмы. Можно выделить три основных вида таких «обитателей». Сразу стоит упомянуть безвредных «помощников», которые во всем помогают человеку, а также нейтральных «личностей», которые ни вред, ни пользу не приносят.
Но существует и третий подвид микроорганизмов – это скрытые паразиты, которые отравляют организм изнутри и вызывают различные недуги.
Схема лечения язвенной болезни, не ассоциированной с хеликобактер
Хеликобактер – это спиралевидная грамотрицательная бактерия, поражающая желудок и двенадцатиперстную кишку. Язвенная болезнь желудка часто появляется на фоне заражения вышеупомянутой инфекцией, но так бывает не всегда. Провоцирующими факторами также выступают: вредные привычки, неправильное питание, повышенная нервозность и т.д.
Хеликобактер, ассоциированный с язвенной болезнью, проявляется явно. Диагностируют такую проблему при помощи лабораторных и микробиологических исследований. Схема лечения язвенной болезни, не ассоциированной с хеликобактер, составляется только врачом.
Особенности гастрита, ассоциированного с Helicobacter pylori
Прошло совсем немного времени с того периода, когда никто и не думал искать причину гастритов среди микроорганизмов. Поверить было тяжело, что в агрессивной желудочной среде можно жить и размножаться. Но некоторые ученые все же стали подробнее изучать палочкообразные существа, обнаруживаемые в слизистой желудка людей, умерших от осложнений язвенной болезни. Так мир узнал о кислотоустойчивой бактерии Helicobacter pylori (Хеликобактер пилори, HP) — виновнике таких заболеваний желудка, как гастрит, эрозии и язвы.
Хронический гастрит и странная бактерия — где связь?

Поначалу врачи не обращали внимания на странные палочки и спирали в слизистой желудка. Появление гастритов долгое время связывали с погрешностями в диете, стрессами, вредными привычками, наследственностью, группой крови и пр. Однако, изучив подробно бактерий, заселявших желудки многих пациентов, мнение ученых кардинально изменилось. Выяснилось, что эти микроорганизмы не такие уж и безобидные. Большая часть заболеваний желудка спровоцирована именно деятельностью Helicobacter pylori.
Первые сведения о наличии странной бактерии в желудке датированы 1875 годом, когда хеликобактер был обнаружен немецкими докторами во время исследования тканей у скончавшихся пациентов от язвенной болезни желудка. Потребовалось достаточно много времени на изучение и доказательства вины HP, так как медицине о нем было известно очень мало: не было знаний о способах его культивирования вне организма, об особенностях строения бактерии, сыграло роль и отсутствие оснащенных лабораторий и т. д.
Затем было еще несколько публикаций различных авторов, которые обнаруживали спиралевидную бактерию в желудках людей и животных, но особого значения этим исследованиям не придавалось.
В начале 80-х годов двадцатого столетия за исследования взялись два австралийских ученых Уоррен и Маршал. Именно они смогли выделить хеликобактера и культивировать его на искусственной среде. Они высказали мнение о том, что большинство болезней, таких как гастрит и язва спровоцированы этим микроорганизмом. Но это революционное заявление медицинское сообщество не приняло с овациями. Тогда Маршал решил привести доказательства: он выпил культуру бактерии, выращенную в лаборатории, и через некоторое время продемонстрировал свой гастрит посредством гастроскопии, а также выделил Хеликобактера из собственного желудка. Далее была проведена антибактериальная терапия препаратами висмута и метронидазолом. Произошло чудо — гастрит излечился! Таким образом ученые доказали, что Helicobacter pylori вызывает воспалительные заболевания в желудке, а лечение гастритов, ассоциированных с HP нужно проводить антибактериальными препаратами.
За открытие австралийские врачи были удостоены Нобелевской премии (2005 г).
Особенности течения гастрита, асоциированного с HP
Главными симптомами хронического гастрита являются диспепсические расстройства. Пациенты предъявляют жалобы на тошноту, тяжесть в области желудка после приема пищи, отрыжку, изжогу, урчание в животе. Характерным симптомом для гастрита, ассоциированного с HP, является расстройство стула: кашицеобразный стул, императивные позывы к дефекации. Нарушения стула носят непостоянный характер, но дают о себе знать.
Реже отмечается горечь и жжение во рту, отрыжка воздухом.
Хронический гастрит может вызывать такие симптомы, как слабость, раздражительность, повышенная утомляемость, потеря интереса к происходящему. Такие симптомы зовутся «общими» и характерны для многих инфекционных заболеваний.
Диагностика хеликобактерного гастрита: гастроскопия, биопсия, хелик-тест

Помимо стандартных методов обследования больного (анализы крови, мочи, кала, УЗИ внутренних органов), при подозрении на хронический гастрит бактериальной природы в обязательном порядке проводится гастроскопия. Желудок осматривается через зонд, на конце которого находится камера с подсветкой. Оценивается изменение слизистой желудка, его поверхность осматривают на наличие эрозий, язв, новообразований.
Во время гастроскопии проводится биопсия тканей из разных отделов желудка. Полученные образцы направляют на микроскопическое исследование. Используя специальную окраску препаратов, доктор под микроскопом может определить присутствие Helicobacter pylori в желудке пациента.
Более простым и доступным методом является проведение хелик-теста (уреазный дыхательный тест). Это абсолютно безболезненное исследование, основанное на способности бактерии HP проявлять уреазную активность. Пациент выпивает раствор мочевины, а затем дышит через специальную трубку с индикатором. В результате реакции гидролиза идет выделение газа, которое отмечается в трубке изменением окраски.
Осложнения: гастрит и язва желудка, рак желудка
Хронический гастрит редко протекает без существенных изменений стенки желудка. Длительный воспалительный процесс и повышенная кислотность создают почву для развития осложнений. Гастрит и язва — верные спутники. Клетки желудка начинают вырабатывать большее количество кислоты для того, чтобы уничтожить бактерию. Так устроен наш желудок, − обезвреживание многих микроорганизмов происходит под действием соляной кислоты. Но хеликобактер не боится кислоты, а вот сама стенка желудка повреждается от избытка кислотности. Возникает воспаление, эрозии, язвы.
Рак желудка не принято ассоциировать с Helicobacter pylori, но в то же время он никогда не развивается на неизмененной стенке желудка. Раку обычно предшествуют предраковые изменения — хронический гастрит, эрозии, язвы, полипы. То есть связь рака желудка и HP не прямая, но есть.
Подход современных врачей-гастроэнтерологов к эрадикации HP

Избавление пациента с гастритом от бактерии хеликобактер пилори, вызвавшей заболевание, зовется эрадикацией. Это стандартизированный план лечения, одобренный Всемирной организацией здравоохранения. Решения подобного уровня принимаются на специальных конференциях с участием ведущих гастроэнтерологов мира.
Эрадикация Helicobacter pylori состоит из трех компонентов:
Может быть применен и четвертый компонент этой схемы — препарат висмута (Де-нол).
Схемы имеют несколько вариантов, которые зовутся линиями. Выбор остается за врачом в зависимости от тяжести заболевания, сопутствующих патологий, региона проживания и т. д. В каждой стране сообщества гастроэнтерологов вносят в схему свои коррективы относительно выбора препарата, его дозировки и продолжительности курса. Ведь чувствительность к антибиотикам в различных регионах проживания может отличаться. То, чем лечат в Америке, может не дать эффекта для россиянина.
Гастродуоденит ассоциированный с нр: лечение, симптомы
Болезни пищеварительного тракта нарушают нормальное функционирование организма. Желудочно-кишечный тракт имеет большое значение для организма, а воспаление может привести к осложнениям, если не началось своевременное лечение. Крайне важно вовремя обратиться к врачу, чтобы провести необходимый лечебный комплекс. Одним из часто встречаемых заболеваний является ассоциированный гастродуоденит, являющийся одним из видов гастроэнтерита. Частое диагностирование ассоциированного гастродуоденита связано с постоянным контактом двенадцатиперстной кишки и желудка. При возникновении недуга у пациента воспаляется слизистая оболочка двенадцатиперстной кишки.
Описание
Болезнь может возникать в острой или хронической форме. Учитывая факторы, вызывающие ассоциированные недуги в хронической стадии, выделяют первичный и вторичный тип ассоциированной болезни. Появление первичного типа характерно при нарушенном пищеварении, возникнем при неправильном рационе. Вторичный тип может появиться как следствие других заболеваний, например, гастритов, панкреатитов и т. д.
Существует несколько классификаций нр ассоциированного гастродуоденита. При наличии определенного уровня кислотности выделяют такие виды, как нормальный гастродуоденит, ассоциированная болезнь с пониженным или повышенным уровнем секреторной функции.
Появление гастродуоденита связано с размножением бактерии helicobacter pylori. Хеликобактер является причиной появления недуга в 80% случаев.
При запущенных стадиях невозможно определить наличие хеликобактера, потому что пищеварительная среда становится непригодной для его существования. Правильно составленный рацион, активный образ жизни, отказ от вредных привычек – это основные пункты, необходимые для сохранения здоровья и предотвращения появления воспалительных процессов в пищеварительном тракте. При появлении неприятных признаков при ассоциированном гастродуодените нужно немедленно обращаться к врачу, чтобы не появились осложнения.
Вернуться к оглавлениюСимптомы
Воспалительные процессы на начальной стадии могут характеризоваться такими признаками, как:
- появление изжоги, отрыжки с кислым запахом;
- повышение аппетита;
- болевые ощущения в области под ложечкой, которые появляются через 2 часа после приема пищи;
- возможно возникновение запоров.
 Бактерии Хеликобактер пилори.
Бактерии Хеликобактер пилори.Начальная стадия характеризуется чаще всего повышенным уровнем кислотности. Но при последних стадиях заболевания у пациента возникает атрофия слизистой оболочки желудочной среды. Это проявляется в развитии таких симптомов, как:
- ухудшение аппетита;
- чувство тяжести в желудочной области, возникающее вследствие непереваренной пищи;
- болевые ощущения в желудочной зоне, имеющие тупой характер;
- пониженная барьерная функция соляной кислоты ведет к появлению поносов;
- появление металлического привкуса;
- проявление отрыжки, которая может иметь запах употребленной пищи, а иногда имеет тухлый характер;
- резкая потеря веса;
- могут появляться трещины в ротовых уголках, которые называют заедами;
- появление тошноты.
Если хеликобактер распространилась в область двенадцатиперстной кишки, у пациента начинаются такие признаки:
- чувство горечи во рту, которое может сопровождаться отрыжкой желчи;
- появление тошноты и рвоты;
- болевые ощущения в области правого подреберья.
Диагностика
Для постановки диагноза врачу следует провести комплексную диагностику пациента, чтобы исключить развитие других заболеваний. Диагностический комплекс включает такие методы:
- проведение эндоскопического обследования, с помощью которого можно определить отечность слизистой оболочки, определить нахождение очага воспаления;
- гистологическая диагностика, которая позволяет определить степень протекания воспалительного процесса;
- электрогастрография и ультразвуковое исследование дают возможность исследовать моторную функцию;
- при проведении рентгена можно оценить эвакуаторную функцию, которая необходима при дифференциации с другими недугами со схожими по симптомам.
Лечение гастродуоденита ассоциированного с нр
Рацион должен быть легким, можно употреблять супы и каши на воде.Любой лечебный комплекс, направленный на лечение пищеварительной системы, подразумевает введение диеты, состоящее из нескольких пунктов:
- Пациенту разрешается употребление супов и каш, сваренных на воде или мясном бульоне, но без добавления масла.
- Мясные и рыбные продукты рекомендуется употреблять в вареном виде.
- Применение молока разрешено в случае отсутствия поносов и аллергических реакций. Рекомендуется употреблять нежирный кефир, сметану, творог и протертый сыр, не содержащий вкусовых добавок.
- Можно употреблять черствые виды хлеба, несдобные сухарики, но другие сдобные продукты полностью запрещены.
- Фрукты и овощи можно употреблять в вареном или сыром виде, но главное – их перетереть перед употреблением.
- Разрешено употребление натуральных соков, компотов, несладких чаев.
Необходимо помнить, что рацион должен состоять из 5 приемов пищи, при этом еда должна быть нормальной температуры, чтобы не обжигать воспаленную оболочку. Кроме того, люди, у которых диагностировали развитие ассоциированных гастродуоденитов, должны соблюдать постельный режим как минимум 8 дней.
Чтобы уничтожить хеликобактер, пациенту назначают специальный медикаментозный лечебный комплекс, включающий прием антибиотиков. Такие препараты назначают в зависимости от стадии развития заболевания. Запрещен самостоятельный подбор и лечение антибиотиками, потому что можно нарушить микрофлору пищеварительного тракта. Вместе с антибиотиками назначают препараты, в которых содержатся полезные бактерии, необходимые для нормальной работы тракта. Кроме того, врач может назначить комплекс витаминов и минералов, необходимый для поддержания тонуса организма.
Вернуться к оглавлениюВывод
Хронический гастродуоденит может быть ассоциирован с другими заболеваниями, у которых схожий симптоматический ряд. Однако у больных ассоциированным гастродуоденитом заболевание чаще всего возникает из-за бактерии Helicobacter pylori.
При своевременных лечебных мероприятиях пациенту удастся избежать осложнений.
Эволюция в эрадикационной терапии НР-ассоциированных заболеваний. Выход за рамки стандартов? | Успенский Ю.П., Фоминых Ю.А., Иванов С.В., Менакер И.О.
Статья посвящена эрадикационной терапии НР-ассоциированных заболеваний
ВведениеОдним из наиболее «популярных» в гастроэнтерологии микроорганизмов, своего рода «притчей во языцех», является Helicobacter pylori. Установлено, что H. pylori выявляется приблизительно у 30–35% населения в детском возрасте и у 50–85% во взрослой популяции [1–5]. В то же время необходимо отметить, что H. pylori-ассоциированные заболевания развиваются не чаще 10–20% случаев [6]. Это наблюдение объясняется тем, что популяция H. pylori отличается крайне высокой генетической гетерогенностью, а ее штаммы значительно отличаются по вирулентности, следовательно, не все из них способны вызвать клинические проявления заболеваний [7]. Следует сказать, что даже инфицирование цитопатогенными штаммами отнюдь не означает фатальной неизбежности развития заболевания, существенное значение принадлежит особенностям макроорганизма, реализации других патогенетических факторов. Тем не менее уверенно доказано, что данный микроорганизм увеличивает риск развития язвенной болезни (ЯБ) и гастрита, является канцерогеном первого порядка и может способствовать формированию новообразований желудка (MALT-лимфома, аденокарцинома). И, несмотря на то, что микробная теория развития поражений гастродуоденальной области как уникальная и единственная не выдерживает критики с позиций классического учения о развитии болезни (в отношении H. pylori не выполняются такие постулаты Коха, как 100% инфицированность заболевших, отсутствие развития заболевания при заражении микробной культурой в эксперименте), суждения о протективной роли бактерии также остаются бездоказательными. Вполне обоснованным является высказывание одного из ведущих хеликобактериологов мира Д. Грэхема: «Хороший хеликобактер – мертвый хеликобактер» (разумеется, в рамках применения данной максимы у больных и в группах лиц повышенного риска, а не у всей человеческой популяции в целом). Таким образом, клиническая и научная составляющие диктуют необходимость проведения эрадикационной терапии.
Принято подразделять показания к проведению эрадикационной терапии на абсолютные и относительные (табл. 1). Традиционно в клинической практике используются стандартные схемы антихеликобактерной терапии (АХБТ), в состав которых входят ингибиторы протонной помпы (ИПП) и антибактериальные препараты.
Как известно, эрадикацию инфекции H. pylori более 80% принято считать успешной. Зачастую данного положительного и эффективного результата практикующим врачам удается достичь не после первого и порой даже не после второго курса АХБТ. По-прежнему существует ряд проблем, приводящих к снижению эффективности АХБТ. К основным причинам, способствующим уменьшению процента успешной эрадикации, относятся:
1. Рост резистентности H. pylori к антибиотикам.
2. Побочные эффекты ИПП и антибактериальных препаратов.
3. Низкий уровень комплаентности и нежелание пациента принимать антибиотики.
Отмечено, что повышение резистентности H. pylori к антибиотикам приводит к катастрофическому уменьшению эффективности эрадикации – с 80–90% до 30–60% [9]. Одним из основных факторов, оказывающих негативное влияние на успех АХБТ, является характерная для многих стран тенденция к росту резистентности микроорганизма к кларитромицину – важнейшему компоненту стандартной тройной схемы эрадикации 1-й линии. Рекомендации III Маастрихтского консенсуса предписывают использование кларитромицина в схемах эрадикационной терапии 1-й линии, если резистентность H. pylori к этому антибиотику в данном регионе не превышает 15–20% [10]. Суммируя результаты 20 европейских исследований, в которых проведена оценка результатов стандартной тройной терапии 1-й линии, включавшей ИПП, амоксициллин и кларитромицин у 2751 пациента, можно заключить, что в случае чувствительности штаммов эрадикация достигается в среднем у 87,8%, а при устойчивости к кларитромицину – только у 18,3% пациентов [11], а по данным некоторых авторов, в условиях резистентности к кларитромицину процент эрадикации снижается даже до 14,3% [12]. В рекомендациях IV Маастрихтского консенсуса определено, что для регионов с высокой и низкой резистентностью H. pylori к кларитромицину рекомендованы разные схемы терапии как 1-й, так и 2-й линии (табл. 2).
Резистентность H. pylori к антибиотикам в России также активно изучается. В большинстве отечественных исследований прослеживается тенденция к росту резистентности микроорганизма к кларитромицину, что согласуется с известными общемировыми данными (табл. 3).
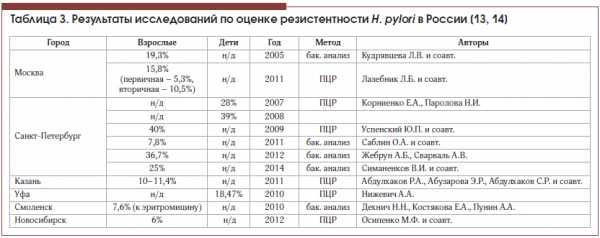
В связи с нарастающей устойчивостью H. pylori к кларитромицину и другим антибиотикам, а также с наличием риска развития резистентности к новым антибактериальным препаратам, использующимся в лечении хеликобактериоза, поиск и разработка новых схем терапии очень актуальны.
Одним из наиболее перспективных направлений оптимизации схем эрадикационной терапии является дополнительное использование в ее составе пробиотиков, возможность применения которых указана в общепринятых стандартах лечения инфекции H.pylori: IV Маастрихтское соглашение, рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению H. pylori у взрослых (2013), V Московское соглашение – Стандарты диагностики и лечения кислотозависимых и ассоциированных с Helicobacter pylori заболеваний (2013) [8, 15–17].
Дополнительное к стандартной эрадикационной терапии назначение пробиотиков повышает комплаентность, снижает частоту и выраженность побочных эффектов (дисбиоз кишечника, антибиотик-ассоциированная диарея), повышает эффективность эрадикации бактерии за счет прямого антагонистического влияния на H. pylori и повышения иммунного ответа организма человека [18–21].
В последнее время особое значение стало придаваться поиску принципиально нового решения по оптимизации эрадикационной терапии. Группой немецких исследователей был разработан препарат на основе инактивированных клеток пробиотических бактерий Lactobacillus reuteri DSMZ 17648 (Pylopass™), выделенных и переработанных биотехнологическим путем. Важно подчеркнуть, что Lactobacillus reuteri DSMZ 17648 – специально подобранный штамм лактобацилл, обладающий уникальной способностью специфично связываться с H. pylori и образовывать коагрегаты, не влияя на другие бактерии и нормальную кишечную флору. Данное специфическое связывание снижает подвижность Helicobacter, а агрегаты патогенов перестают связываться со слизистой ЖКТ и «вымываются» из желудка, что в результате приводит к уменьшению колонизации H. pylori в слизистой оболочке желудка, снижая риск развития гастрита и ЯБ [21, 22]. Исследования эффективности препарата показали, что имеет место снижение уровня H. pylori после 2х-недельного курса приема по данным дыхательного уреазного теста. В качестве критерия оценки эффективности элиминации H. pylori использовался мочевинный дыхательный тест (МДТ): нагрузка H. pylori после 2 нед. приема Pylopass™. Установлено, что на фоне приема плацебо отмечено изменение МДТ на 3% по сравнению с исходным, а при использовании Pylopass – на 16% по сравнению с исходным [21, 23].
В России данный продукт зарегистрирован под торговым названием Хелинорм, является инновационным безрецептурным антихеликобактерным средством с принципиально новым механизмом действия [21].
Цель исследования: изучить эффективность и безопасность использования продукта Хелинорм, назначаемого с целью терапии пациентов с HP-ассоциированной ЯБ двенадцатиперстной кишки (ДПК).
Задачи исследования:
Выявить влияние продукта Хелинорм в составе комплексной эрадикационной терапии на:
– клиническую картину заболевания;
– эндоскопическую картину;
– обсемененность HP-инфекцией;
– качество жизни пациентов, принимающих Хелинорм;
– обосновать назначение Хелинорма в составе комплексной терапии.
Материал и методы
Тип исследования – проспективное когортное открытое сравнительное рандомизированное. Для распределения пациентов по группам была использована фиксированная блоковая рандомизация с переменным размером блока (Randomly Mixed Permuted Blocks). Выбор данного метода рандомизации был обусловлен необходимостью обеспечения одинакового размера групп сравнения – 1:1:1 (в процессе процедуры рандомизации использовался простой генератор случайных чисел).
В исследование включались пациенты с ЯБ ДПК, ассоциированной с инфекцией H. pylori. Согласно критериям включения, представленным ниже, пациенты имели либо ЯБ ДПК в фазе рецидива язвообразования, либо рубцовую деформацию луковицы ДПК, на фоне эрозивного бульбита или иных эндоскопических проявлений воспалительного процесса в слизистой оболочке.
Критерии включения:
– подписание информированного согласия;
– отсутствие психических расстройств и интеллектуально-мнестических нарушений;
– наличие ЯБ ДПК, ассоциированной с инфекцией H. pylori, в фазе обострения на момент включения в исследование;
– отсутствие других острых заболеваний на момент включения в исследование.
Критерии исключения:
– наличие тяжелых органических заболеваний органов пищеварения или их осложнений, например, ЯБ (признаки кровотечения из ЖКТ, перфорация, пенетрация, стеноз пилородуоденальной зоны, малигнизация), органических поражений кишечника (опухоли, дивертикулез), ОКИ, воспалительных заболеваний кишечника (болезнь Крона, язвенный колит и пр.) на момент включения в исследование;
– наличие выраженной сопутствующей патологии: недостаточность кровообращения, ХОБЛ с проявлениями дыхательной недостаточности, хроническая почечная недостаточность, хронические гепатиты различной этиологии, хроническая печеночная недостаточность;
– целиакия;
– системные заболевания соединительной ткани;
– прием стероидных препаратов;
– наличие аллергических реакций или непереносимость компонентов препарата;
– злоупотребление алкоголем;
– беременность или кормление грудью;
– невозможность или нежелание дать информированное согласие на участие в исследовании или на выполнение требований исследования;
– психические заболевания, в т. ч. ранее перенесенные, которые, по мнению исследователя, делают неприемлемым участие пациента в исследовании;
– наркомания в течение 1 года до включения в исследование;
– тяжелые судорожные расстройства в анамнезе;
– пациенты, склонные к отказу от исследования и выполнению предписаний врача;
– пациенты, участвующие в других клинических испытаниях.
В исследование были включены 60 пациентов (средний возраст – 36 лет), которые были разделены на 3 сходные по возрастному и гендерному составу группы по 20 человек.
Пациенты группы 1 (группа активного контроля) принимали следующую терапию в течение 10 дней:
– омепразол 20 мг 2 р./сут;
– кларитромицин 500 мг 2 р./сут;
– амоксициллин 1000 мг 2 р./сут;
– Де-нол 240 мг 2 р./сут.
Режим дозирования на протяжении всего периода терапии был неизменным.
Пациенты группы 2 (группа активного контроля) принимали эрадикационную терапию в течение 10 дней:
– омепразол 20 мг 2 р./сут;
– кларитромицин 500 мг 2 р./сут;
– амоксициллин 1000 мг 2 р./сут.
Режим дозирования на протяжении всего периода терапии также был неизменным.
Пациенты группы 3 (основная группа) принимали эрадикационную терапию в течение 10 дней:
– омепразол 20 мг 2 р./сут;
– кларитромицин 500 мг 2 р./сут;
– амоксициллин 1000 мг 2 р./сут;
– продукт Хелинорм по 1 капсуле 2 р./сут во время еды в течение 28 дней (начало приема исследуемого препарата, таким образом, совпадало с основным стартом терапии с применением стандартного эрадикационного комплекса и продолжалось еще 18 дней после окончания базисного курса).
В течение периода лечения проводилось динамическое наблюдение за пациентами. По окончании курса терапии всем пациентам были повторно проведены клиническое обследование, стандартизированный опрос, оценка качества жизни. Через 2 мес. от начала наблюдения пациентам выполнялось эндоскопическое исследование верхних отделов пищеварительного тракта с забором гистологического материала и уреазным тестом. Дизайн исследования представлен в таблице 4.
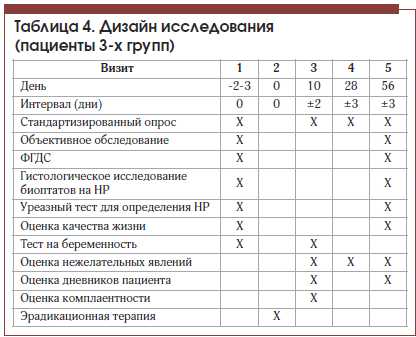
Конечными точками исследования были следующие: частота жалоб пациентов, частота положительных тестов на H. pylori, частота эндоскопических и гистологических изменений по данным ФГДС, значения показателей по шкалам качества жизни опросника SF-36.
Анализ полученных в результате исследования данных был проведен с помощью пакета статистических программ SPSS 17.0 (SPSS Inс., США) с использованием методов параметрической и непараметрической статистики [24–26]. Определение типа распределения данных проводилось с использованием критериев Шапиро – Уилка и Колмогорова – Смирнова. Так как фактические данные имели распределение, отличное от нормального, для статистического описания средних тенденций вариационных была использована медиана.
Для сравнения количественных признаков в динамике использовался парный критерий Вилкоксона (в зависимости от типа распределения данных). Сравнение групп наблюдения проводилось с помощью непараметрического дисперсионного анализа (критерий Краскела – Уоллиса).
Для сравнения качественных признаков в динамике использовался критерий Мак-Нимара, для сравнения частоты исходов в группах наблюдения – критерий χ2 Пирсона и его вариации (поправка Йейтса на непрерывность и точный критерий Фишера).
Уровень статистической значимости p<0,05 считался достаточным для отклонения нулевой статистической гипотезы и вывода о статистической значимости различий данных, полученных в исследовании. При проведении множественных сравнений для коррекции критического уровня статистической значимости использовалась поправка Бонферрони.
Результаты исследования
Все пациенты завершили исследование в соответствии с протоколом.
Оценка жалоб пациентов
У включенных в исследование пациентов на момент начала наблюдения наиболее распространенными жалобами были боли в животе, отрыжка, тошнота, чувство горечи во рту, урчание в животе и вздутие живота. Динамика частоты гастроинтестинальных жалоб после курса терапии представлена в таблице 5.
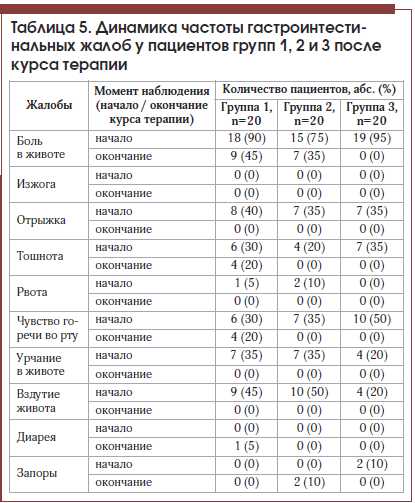
Среди жалоб наибольший интерес представлял болевой синдром как наиболее существенно влиявший на качество жизни пациентов.
При сравнении момента окончания наблюдения и момента начала терапии во всех 3-х группах наблюдалось статистически значимое уменьшение частоты встречаемости болей в животе: уровень статистической значимости составил 0,004, 0,008 и <0,001 для групп 1, 2 и 3 соответственно.
При попарном сравнении групп между собой в отношении снижения частоты встречаемости болевого синдрома статистически значимые различия были выявлены между группами 3 и 1 (χ2=12,554, p< 0,001) и между группами 3 и 2 (χ2 = 11,165, p=0,001), в то время как между группами 1 и 2 статистических различий выявлено не было (χ2=0,036, p=0,849).
Оценка качества жизни пациентов
После курса терапии статистически значимое улучшение качества жизни наблюдалось у пациентов группы 2 по шкалам GH, VT и MH и у пациентов группы 3 по шкалам GH, BP, VT и MH, в то время как у пациентов группы 1 статистически значимого изменения качества жизни не наблюдалось ни по одной из шкал. Динамика показателей качества жизни пациентов представлена в таблице 6 и на рисунках 1–3.
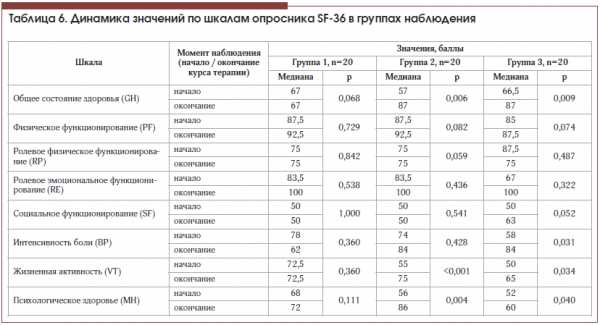
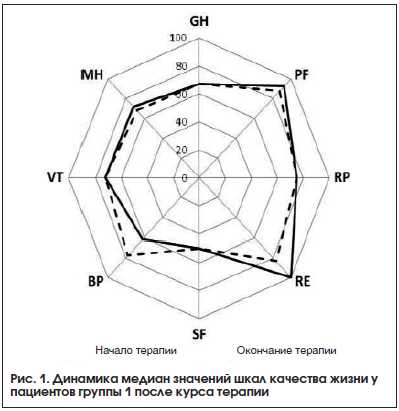
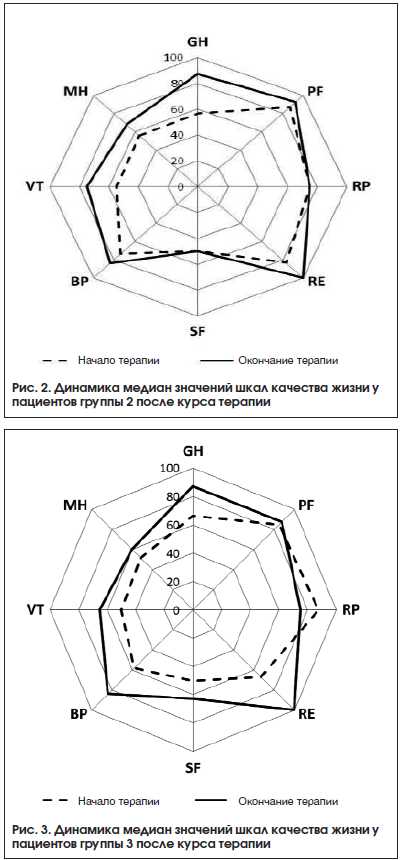
Сравнение динамики показателей шкал качества жизни выявило статистически значимые различия между группами только в отношении шкалы «интенсивность боли» BP (χ2=2,920, p=0,012). Близкими к статистически значимым оказались различия между группами и в отношении шкалы жизненной активности VT (χ2=5,942, p=0,051). Попарные межгрупповые сравнения значения показателя качества жизни по шкале «интенсивность боли» показали статистически значимые различия между группами 3 и 1 (U=111,5, p=0,015) и между группами 3 и 2 (U=106,0, p=0,010), в то время как группы 1 и 2 статистически не различались (U=179,5, p=0,583).
Оценка данных ФГДС
По данным ФГДС у всех включенных в исследование пациентов был диагностирован хронический H. pylori-ассоциированный гастродуоденит. У 7 (12%) пациентов имелась рубцовая деформация луковицы ДПК, у 13 (22%) пациентов имелись эрозии в луковице ДПК, у всех пациентов отмечались отечность и гиперемия слизистой ДПК.
У 22 (37%) пациентов была выявлена язва ДПК, у 14 (23%) пациентов имелся эрозивный бульбит, у остальных 24 (40%) пациентов имел место катаральный дуоденит.
На фоне проводимой терапии во всех группах пациентов отмечено улучшение эндоскопической картины – язвенный дефект зарубцевался у всех пациентов, имевших язву ДПК на момент начала наблюдения, у пациентов с эрозивным дуоденитом имевшиеся эрозии на фоне терапии эпителизировались.
При этом гиперемия и отечность слизистой оболочки желудка и ДПК сохранялись у 5 (25%) пациентов группы 1, 2 (10%) пациентов группы 2 и у 2 (10%) пациентов группы 3.
Оценка результатов гистологического метода диагностики H. pylori и уреазного теста
На момент начала исследования положительный результат гистологического исследования для диагностики H. pylori и положительный уреазный тест были выявлены у всех включенных в исследование пациентов (согласно критериям включения в исследование).
После курса лечения во всех 3-х группах отмечено статистически значимое снижение частоты выявления положительного итога диагностики H. pylori по результатам как гистологического исследования, так и уреазного теста (табл. 7, рис. 4). Тем не менее в группе, получавшей Хелинорм, после окончания курса терапии только у 1 пациента гистологическое исследование показало наличие H. pylori, в противоположность 6 и 3 пациентам групп активного контроля с добавлением Де-Нола и просто эрадикационной терапии соответственно.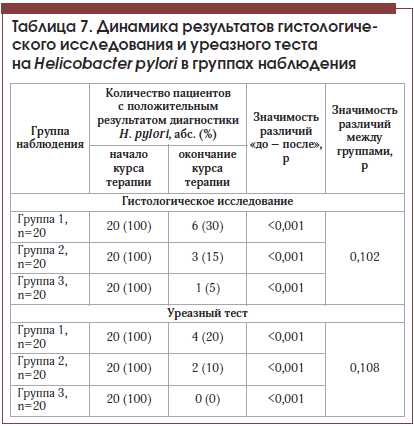
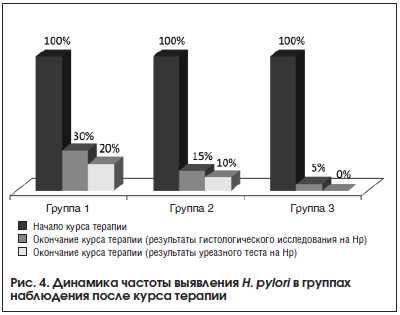
Как видно из полученных данных, у включенных в исследование пациентов результаты выявления H. pylori при использовании гистологического метода и уреазного теста не имели существенных расхождений.
Обсуждение результатов
По результатам анализа исследовательских данных, после курса эрадикационной терапии положительная клиническая динамика наблюдалась во всех 3-х группах пациентов, но при этом болевой синдром достоверно более эффективно элиминировался у пациентов группы 3, получавших исследуемый Хелинорм в дополнение к эрадикационной терапии. Также обратило на себя внимание отсутствие нежелательных явлений в группе исследуемого продукта Хелинорм, что позволяет сделать благоприятное заключение в отношении профиля его безопасности.
После использования продукта Хелинорм в комплексе с эрадикационной терапией отмечено более выраженное улучшение качества жизни по сравнению с обычно используемыми схемами эрадикации H. pylori, в первую очередь улучшение качества жизни пациентов было связано со снижением выраженности болевого синдрома.
Элиминация H. pylori по данным обоих использованных тестов (гистологического и уреазного) была более эффективной в группе пациентов, принимавших Хелинорм (95 и 100% соответственно), при этом эндоскопическая динамика была сходной во всех 3-х группах наблюдения.
Полученные результаты позволяют предположить, что включение продукта Хелинорм в стандартную эрадикационную схему лечения может повысить эффективность терапии Helicobacter pylori-ассоциированных заболеваний. По эффективности такая комбинация сравнима с группой, получавшей эрадикационную терапию + Де-Нол, а благоприятный профиль безопасности средства Хелинорм выгодно выделяет продукт среди препаратов для борьбы с H. pylori.
Заключение
Прием продукта Хелинорм вместе со стандартной эрадикационной терапией:
– повышает эффективность эрадикации H. pylori на 10%;
– оказывает положительное влияние на клиническую картину заболевания Helicobacter pylori-ассоциированной ЯБ ДПК и, в частности, способствует купированию абдоминального болевого синдрома;
– имеет хорошую переносимость и безопасность;
– улучшает показатели качества жизни, что свидетельствует о высокой медико-экономической эффективности данного подхода к лечению.
Таким образом, Хелинорм может быть рекомендован для применения у пациентов с Helicobacter pylori-ассоциированными заболеваниями.
Рекомендуемая схема приема продукта Хелинорм – по 1 капсуле 2 р./сут в течение 28 дней, на фоне эрадикационной терапии.