Остеокласты что это такое
Остеокласты - это разрушители костной ткани
Тело человека состоит из множества клеток. Все они имеют разную структуру и выполняют разные функции. Но есть нечто, объединяющее все их разнообразие – это постоянный процесс обновления. Его можно рассмотреть на примере костных структур. Клетки остеокласты и остеобласты подобны бригадам по укладке асфальта: одни снимают старый асфальт, другие укладывают новый. Костная ткань непрерывно обновляется, и мозг контролирует эту работу.
Когда возникает сбой, всегда есть причина: или мозг дал не ту команду, или строительного материала не хватило, или остеобласты (клетки, строящие ткань) уменьшились в количестве. А остеокласты (разрушители) остались в прежнем числе. Это приводит к различным болезням, в частности, остеопорозу.
Как устроена костная ткань
Кость – это орган тела, который постоянно обновляется. Он состоит из нескольких видов тканей, важнейшей из которых является костная. В развитом межклеточном веществе кости, богатом солями, работает три вида клеток:
- Остеоциты.
- Остеобласты.
- Остеокласты.
Если охарактеризовать их коротко, это хранители, созидатели и разрушители.
Остеобласты
Название этих клеток произошло от древнегреческих слов «кость» и «росток». Это молодые клетки, которые формируют костную ткань. Сначала они создают матрикс, сетку межклеточного вещества. После этого этапа остеобласты производят кальцификацию матрикса, сами при этом превращаясь в остеоциты.
Остеобласты имеют кубическую или пирамидальную форму. В них развита гранулярная эндоплазматическая сеть, синтезирующая белки. Комплекс Гольджи выводит их в строящуюся кость. Митохондрии обеспечивают нормальную жизнедеятельность клетки, обеспечивая ее энергией. Остеобласты могут делиться митозом.
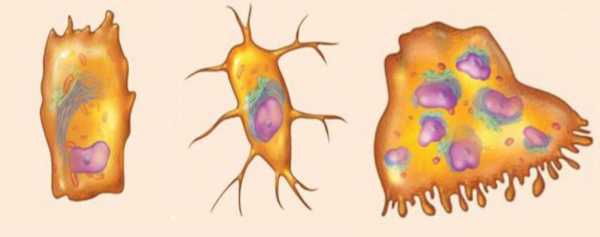
Главная задача остеобластов — образование белков матрикса, к которым относятся коллаген, остеокальцин и остеопонтин. После их синтеза начинается откладывание в матриксе минеральных веществ. Также они выделяют оссеин, который склеивает соли кальция. В результате кость становится минерально-органической структурой.
Остеобласты помогают транспортировке кальция и фосфатов, что помогает в ощелачивании организма. При формировании кости они находятся на всей поверхности костных балок, а после – в местах разрушения и регенерации после травмы, а также в надкостнице.
Остеоциты
Остеоцит называют клеткой зрелой костной ткани. Это дефинитивная клетка, то есть пришедшая к конечной форме. Она не имеет способности делиться путем митоза. Когда структура матрикса полностью заполнена минеральным веществом, остеобласт прекращает работу и клетка становится остеоцитом. Функция остеоцитов – обеспечить поддержание и регенерацию костей, а также регулирование минерального состава.
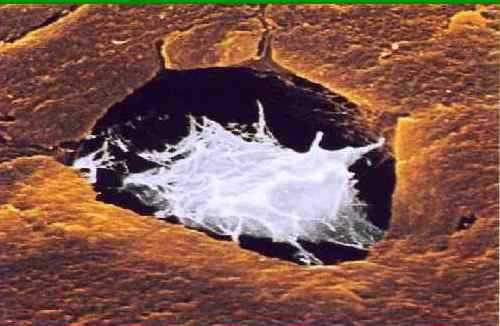
В структуре кости есть лакуны, в которых и находятся остеоциты. В процессе замуровывания остеобласты создают длинные отростки остеоцитов, которые соприкасаются друг с другом нексусами. Находящиеся около сосуда отростки получают питание и кислород от него. Количество таких отростков может быть очень большое, до нескольких сотен. Остеоцит имеет форму звезды из-за множества отростков, которые находятся в костных канальцах. После старения и апоптоза (самоуничтожения) канальцы пустеют.
Клетки остеокласты
Остеокласты представляют собой гигантские (диаметром 40 мкм) многоядерные клетки. Они разрушают кость путем растворения минеральных солей и разрушения коллагенового матрикса. Они имеют несколько ядер (от 5 до 20), много комплексов Гольджи, митохондрий и лизосом. Из лизосом выделяются ферменты, которые инициируют резорбцию кости.
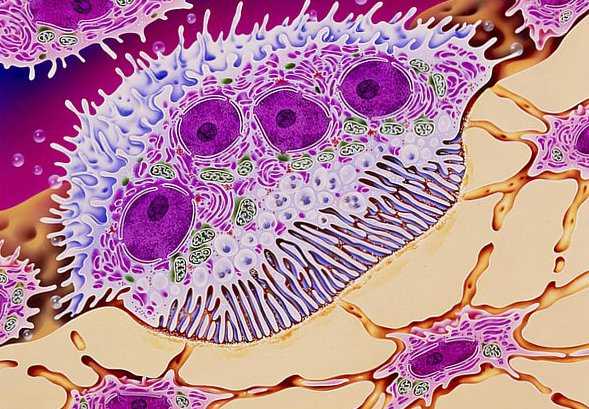
Иначе говоря, остеокласт – это костный макрофаг. Он подходит к кости, прикрепляется к ней гофрированной каемкой и формирует мембрану, которая защищает окружение остеокласта от действия гормонов. Затем он продуцирует кислую среду, которая растворяет минеральные соли. После с помощью ферментов лизосом старые клетки перевариваются. Часть веществ уходит в кровь, остальная используется для поддержания процесса уничтожения кости.
Работа в тандеме
Остеокласты работают группой. Они въедаются в старую кость и прокладывают в ней туннель. Ежедневный проход такой группы – 50 мкм. После прохода первой группы начинает движение вторая, состоящая из остеобластов. Они располагаются по стенкам туннеля и заполняют их поверхность. После этого они начинают синтезировать матрикс со скоростью 1 мкм в день. Одновременно с этим по оси тоннеля начинают прорастать капилляры.
Выстроив матрикс, остеобласты начинают замуровываться, создавая минерально-белковую структуру вокруг себя. По достижении цели, когда кость уже выстроена, в лакунах остаются остеоциты. Они живут некоторое время, после чего кончают жизнь самоуничтожением (апоптозом).
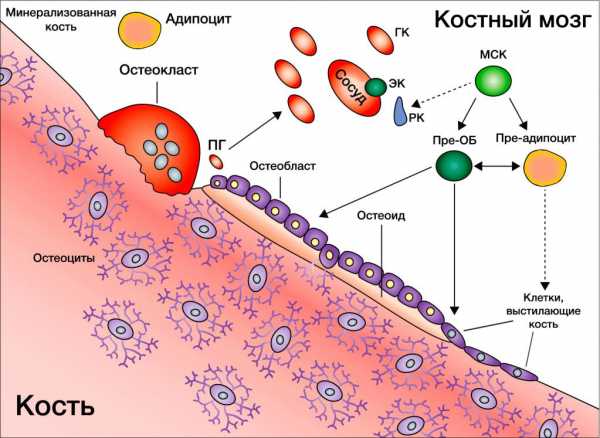
Процесс работы в тандеме двух видов костных клеток называется ремоделированием. Регулируется он гормонами паратиреоидных желез, активирующих остеокласты. Это паратиреоидный гормон. Щитовидая железа вырабатывает кальцитонин, который стимулирует образование костей. Кроме этих, в ремоделировании участвуют много других гормонов, которые вырабатывают половые железы, гипофиз и поджелудочная железа.
При нарушении работы гормонов может наблюдаться недостаток остеобластов или их угнетение. Вместе с активностью остеокластов это может привести к болезням. Например, остеопорозу и его последствиям: переломам и повреждениям суставов.
Заключение
Для жизни необходима правильная работа всех частей организма, даже таких маленьких структур, как остеокласты. Это позволяет всем органам тела человека, от щитовидной железы до костей, взаимодействовать друг с другом. Вот почему нужны знания о здоровом образе жизни, правильном питании и сохранении здоровья. Тогда преждевременный остеопороз будет не страшен.
Остеобласт — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 8 ноября 2018; проверки требует 1 правка. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 8 ноября 2018; проверки требует 1 правка.Остеобла́сты (от др.-греч. ὀστέον — «кость» + др.-греч. βλάστη — «росток, отпрыск, побег») — молодые клетки костной ткани (диаметром 15-20 мкм), которые синтезируют межклеточное вещество — матрикс. По мере накопления межклеточного вещества остеобласты замуровываются в нём и становятся остеоцитами. Остеобласты богаты элементами зернистой эндоплазматической сети, рибосомами, имеют хорошо развитый комплекс Гольджи. Их многочисленные отростки контактируют между собой и с отростками остеоцитов. Вспомогательной функцией остеобластов является участие в процессе отложения солей кальция в межклеточном веществе (кальцификации матрикса) благодаря высокому содержанию щелочной фосфатазы, что свидетельствует о высокой синтетической активности остеобластов. При этом происходит образование полостей (лакун), в которых они и залегают, превращаясь в остеоциты.
Остеобласты возникают из мезенхимальных стволовых клеток[1]. По форме остеобласты делятся на три группы: кубические, пирамидальные и угловатые (многоугольные).
В сформировавшейся кости остеобласты встречаются только в местах разрушения и восстановления костной ткани, тогда как в развивающейся кости они непрерывным слоем покрывают почти всю поверхность формирующейся костной балки. Остеобласты располагаются вокруг первичных костных перекладин, образованных коллагеновыми волокнами. Оказавшись между ними, многие остеобласты замуровываются в межклеточном веществе и становятся остеоцитами. Так возникает костная ткань.
Остеобласты также в большом количестве находятся в надкостнице и в эндосте.
Остеобласты отделяют кость от внеклеточной жидкости. Фосфат и кальций из костной ткани и в нее не могут перемещаться пассивной диффузией, потому что плотные остеобластные соединения изолируют внутреннее пространство кости. Кальций транспортируется через остеобласты пассивным транспортом (то есть транспортерами, которые не нагнетают кальций против градиента). Напротив, фосфат активно перемещается сочетанием секреции фосфатсодержащих соединений, включая АТФ расщепления фосфата фосфатазами на фронте минерализации. Щелочная фосфатаза — это мембранный белок, который является характерным маркером остеобластов, он находится в больших количествах на апикальной (секреторной) поверхности активных остеобластов.
В замкнутой системе при минерализации накапливается фосфорная кислота, быстро понижая рН и останавливая дальнейшее выпадение осадка. Хрящ не препятствует диффузии, поэтому кислота рассеивается, что позволяет осадку выпадать. В остеоне, где матрикс отделен от внеклеточной жидкости плотными соединениями, этого не происходит. В контролируемом закрытом отсеке удаление H+ приводит к выпадению осадка в широком диапазоне внеклеточных условий, если кальций и фосфат доступны в отсеке матрикса[2]. Остеобласты обладают способностью к обмену Na+ / H+ через обменники Na/H, NHE1 и NHE6[3]. Этот обмен Н+ является основным способом удаления кислоты, хотя механизм, с помощью которого Н+ переносится из матричного пространства в барьерный остеобласт, неизвестен.
Остеобласты также соединены щелевыми контактами, что позволяет клеткам в одной когорте функционировать совместно. Это было продемонстрировано путем введения флуоресцентных красителей с низким молекулярным весом в остеобласты; показано, что краситель диффундирует в окружающие и более глубокие клетки в костных блоках[4]. Десмосомы также соединяют более глубокие слои клеток с поверхностным слоем. Кость состоит из многих таких блоков, которые разделены непроницаемыми зонами без клеточных соединений, называемых цементными линиями.
- ↑ M. F. Pittenger, A. M. Mackay, S. C. Beck, R. K. Jaiswal, R. Douglas. Multilineage potential of adult human mesenchymal stem cells // Science (New York, N.Y.). — 1999-04-02. — Т. 284, вып. 5411. — С. 143–147. — ISSN 0036-8075.
- ↑ S. Schartum, G. Nichols. Concerning pH gradients between the extracellular compartment and fluids bathing the bone mineral surface and their relation to calcium ion distribution // The Journal of Clinical Investigation. — May 1962. — Т. 41. — С. 1163–1168. — ISSN 0021-9738. — doi:10.1172/JCI104569.
- ↑ Li Liu, Paul H. Schlesinger, Nicole M. Slack, Peter A. Friedman, Harry C. Blair. High capacity Na+/H+ exchange activity in mineralizing osteoblasts // Journal of Cellular Physiology. — June 2011. — Т. 226, вып. 6. — С. 1702–1712. — ISSN 1097-4652. — doi:10.1002/jcp.22501.
- ↑ C. E. Yellowley, Z. Li, Z. Zhou, C. R. Jacobs, H. J. Donahue. Functional gap junctions between osteocytic and osteoblastic cells // Journal of Bone and Mineral Research: The Official Journal of the American Society for Bone and Mineral Research. — February 2000. — Т. 15, вып. 2. — С. 209–217. — ISSN 0884-0431. — doi:10.1359/jbmr.2000.15.2.209.
Остеопороз – что это такое: причины, остеобласты и остеокласты
Остеопороз – это состояние косной системы, характеризующееся значительным уменьшением плотности костной ткани, что в результате приводит к хрупкости костей. При остеопорозе увеличивает риск возникновения переломов и трещин костей при незначительных ушибах, таких как падение человека, когда он поскользнулся на льду.
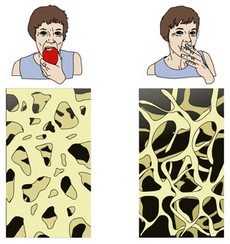 К сожалению, можно сказать, что большинство людей даже не подозревают о возможном наличии у них остеопороза, пока не произойдет перелом или лечащий врач не назначит прохождение скрининг-теста.
К сожалению, можно сказать, что большинство людей даже не подозревают о возможном наличии у них остеопороза, пока не произойдет перелом или лечащий врач не назначит прохождение скрининг-теста.
Хрупкостью костей или остеопорозом страдают около 44 миллионов человек. Из этого числа десять миллионов уже имеют остеопороз, а у тридцати четырех миллионов выявлена хрупкость костей, что говорит о наличии серьезного риска возможного развития остеопороза.
У женской половины человечества в четыре – пять раз больше вероятность заболеть остеопорозом, чем у мужской половины. К факторам риска провоцирующим развитие этого заболевания в зрелом возрасте можно причислить хрупкое телосложение, ведение пассивного образа жизни, прием алкоголя и курение, прием определенного набора медицинских препаратов, а также стероидов.
Однако, остеопороз сегодня поражает и молодых. Причины – значительное снижение физической активности, неприспособленность к физическому труду, неправильный рацион питания, состоящий в большей степени из «мертвых» продуктов и полуфабрикатов, раннее курение и потребление пива.
Возникновение остеопороза

Чтобы понять определение минеральной плотности кости и ее роль, важно знать причины возникновения остеопороза.
Во время жизни, костная ткань человека постоянно обновляется. Этот процесс является нормальным, тем самым происходит усвоение старых клеток и появление новых. Данный цикл является важным процессом в человеческом организме, и он нужен для поддержания нормального состояния костной системы, а также для ее восстановления в случае повреждения.
Клетки ответственные за воспроизводство новой костной ткани называются остеобластами, а клетки, отвечающие за рассасывание устаревшей костной ткани, называются остеокластами.
Возникновение остеопороза обусловлено нарушением баланса между действием остеобластов и остеокластов. Этот дисбаланс может быть вызван различными факторами, такими как, гормональные нарушения или инфекционные заболевания.
Такое не соответствие, также может быть вызвано возрастными изменениями, изменениями гормонального фона в период менопаузы, при долговременном соблюдении различных диет, которые содержат малое количество кальция и недостаток витамина D. При остеопорозе, количество остеокластов превышает количество остеобластов, а следовательно, костная ткань истощается, что приводит к истончению костей и как следствие потери костной силы. В итоге такого поражения вероятность переломов и трещин костей при незначительной травме резко увеличивается.
Риск остеопороза
Скелет человека состоит из двух основных типов костей.
- Трубчатая кость или кортикальная по своей структуре более твердая,
- другая – губчатая кость, также называемая трабекулярной, является более мягкой.
В конечном итоге, если действие остеобластов и остеокластов не сбалансировано, то кости имеющие губчатую структуру поражаются на много быстрее.
Основная и большая часть костной системы формируется примерно к 25-27 годам и после этого начинается снижение костной массы на всем протяжении жизненного цикла человека. Существует нормальный уровень снижения костной массы, как у женского населения, так и мужского.
Для примера, помимо возрастных изменений у женщин, существуют физиологические – после менопаузы, которые вызывают перестроения в организме, что способствует серьезному уменьшению костной массы. Потеря костной массы бывает значительной и через 3-5 лет достигает двадцати процентов.
Поскольку у женщин костная масса на много меньше, чем у мужчин изначально, это увеличивает риск возникновения у них трещин и переломов по сравнению с мужчинами того же возраста. Мужчины, также как и женщины, подвержены серьезным рискам возникновения остеопороза, особенно если они страдают определенными видами заболевания, имеют низкий уровень тестостерона, принимают лекарственные препараты, курят и если образ жизни не отличается подвижностью.
Наиболее лучшим способом предотвращения остеопороза является наращивание костной массы в более раннем возрасте, применяя при этом правильное питание и регулярные физические нагрузки. К большому сожалению остеопороз в зрелом возрасте не воспринимается как серьезное заболевание. При сенильном остеопорозе, уменьшение плотности костей происходит медленно. Поэтому это заболевание, на начальной стадии, протекает бессимптомно и при его выявлении не имеется ни каких жалоб на состояние здоровья.
Последствия
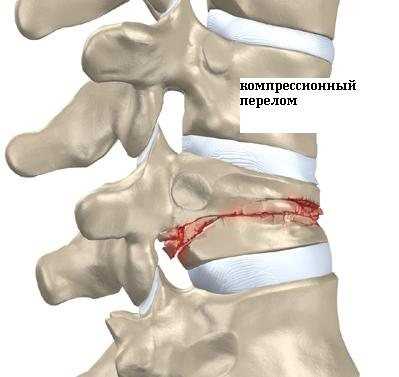
Деформация кости и последующие болевые ощущения появляются лишь тогда, когда плотность уменьшилась на столько, что произошел перелом, вызвавший небольшую травму кости.
Компрессионный перелом позвонка может привести к хроническим болям в поясничной области. Прелом позвонка происходит непроизвольно или во время небольшого травматического воздействия. Возникает резкая боль в спинной области, и она усиливается при движении.
Область перелома может быть болезненна на ощупь, но по прошествии нескольких месяцев болезненные ощущения проходят. Если произойдет перелом нескольких позвонков, то в этом случае может развиться искривление позвоночника, которое будет вызвать постоянное напряжение мышц и боли.
Переломы и трещины других костей обычно возникают в результате небольшого падения или нагрузки. Одним из самых серьезных переломов является перелом шейки бедра, так как он обычно приводит к инвалидности в пожилом возрасте.
Распространенным явлением при остеопорозе является перелом костей предплечья в месте соединения с запястьем. Такой перелом называют перелом Коллеса (перелом лучевой кости в типичном месте). Следует добавить, что заживление переломов у людей, страдающих остеопорозом, происходят медленно и болезненно. Человеку, с высокой степенью остеопороза необходимо постоянное соблюдение специализированной диеты.
Остеокласт - это... Что такое Остеокласт?
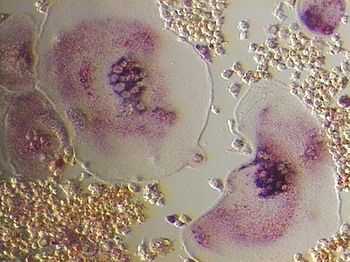
Остеокласты и остеобласты на трабекуле нижней челюсти коровьего эмбрионаОстеокласты — гигантские многоядерные клетки позвоночных животных, появляющиеся в местах рассасывания костных структур.[1] Диаметр остеокласта около 40 мкм, они содержат 15-20 близко расположенных ядер. Функция их заключается в растворении кости. В сочетании с остеобластами, остеокласты контролируют количество костной ткани (остеобласты создают новую костную ткань, а остеокласты разрушают старую).
Остеокласты обычно имеют множество лизосом. При выделении содержащихся в лизосомах гидролитических ферментов происходит резорбция основного вещества кости и обызвествленного хряща.[2]
Примечания
| Опорно-двигательная система, соединительная ткань: костная и хрящевая | |
|---|---|
| Хрящи | |
| Хрящевой рост | надхрящница, костная мозоль, эпифизарная пластинка |
| Клетки | хондробласт, хондроцит |
| Типы хрящевой ткани | гиалиновая, эластическая, волокнистая |
| Кости | |
| Оссификация | эндесмальная, эндохондральная |
| Клетки | остеобласт, остеоцит, остеокласт |
| Типы костной ткани | губчатая, компактная |
| Отделы | субхондральная кость, эпифиз, метафиз, диафиз |
| Структура | остеон, гаверсовы каналы, фолькмановские каналы, эндост, надкостница, костный мозг, пневматизация |
| Форма | длинные, короткие, плоские, сесамовидные, смешанные |
Взаимодействие остеокластов и остеобластов
Статья была опубликована в: Lietal. (2016)
Osteoclast-Derived Exosomal miR-214-3p Inhibits Osteoblastic Bone Formation.
Источник:
University of Western Australia; Photo: Shutterstock.
Предупреждение:
Открытый профессором Струковым В.И. анаболический способ лечения остеопороза с помощью препаратов «Остеомед», «Остео-вит» согласуется с физиологией человека. Профессор Струков В.И. выступает против применения бисфосфонатов при лечении остеопороза, так как бисфосфонаты тормозят функцию остеокластов и тем самым грубо вмешиваются в физиологию человека. Профессор Струков В.И. считает, что костная система человека построена очень разумно, и остеокласт никогда не разрушает остеоциты, если того не требует организм (процесс ремоделирования кости). Поэтому мешать работе остеокласта ни в коем случае нельзя. Исследования австралийских ученых подтверждают правоту профессора Струкова и показывают, что между остеокластами и остеобластами существует сигнальный обмен. И повышение активности остеокластов повышает и активность остеобластов. Поэтому применение бисфосфонатов, тормозящих функцию остеокластов приводит также к подавлению и функции остеобластов.
Блокирование микро-РНК для предупреждения остеопороза.
Ориентация (на мишень) микро-РНК (RNA — miR-214-3p), повышенный уровень которой обнаруживается у пожилых женщин, мог бы помочь в лечении остеопороза.
МикроРНК (microRNA, miRNA) — «малые» некодирующие молекулы РНК длиной 18-25 нуклеотидов (в среднем 22), обнаруженные у растений, животных и некоторых вирусов, принимающие участие в транскрипционной и посттранскипционной регуляции экспрессии генов путем РНК-интерференции. – Прим.перев.
Исследователи из Гонконгского Баптистского университета определили микро-РНК (miRNA), вырабатываемые костными клетками естественным путем, которые стимулируют рост костей. Их открытия, опубликованные в «NatureCommunications», могли бы привести к новым методам лечения остеопороза.
Остеопороз является распространенным заболеванием, которое делает кость ломкой и приводит к повышенному риску переломов. Главная причина переломов костей у пожилых людей — так называемая «молчаливая болезнь»: вы редко знаете о ней, пока у вас не произойдет перелома кости. Остеопороз возникает, когда кости теряют минералы, в частности кальций, гораздо быстрее, чем организм может заменить их, вызывая тем самым потерю плотности кости.
Чтобы лучше понять клеточный механизм потери костной массы, группа исследователей сосредоточила свое внимание на двух типах клеток: остеокластах, отвечающих за костную резорбцию и вызывающих переломы кости, и остеобластах, формирующих кости и регулярно создающих перекрестные помехи (cross-talk) в организме.
“Ремоделирование костей регулируют два типа клеток, причем каждая – разными путями,” – говорит соавтор XuJiake, профессор Университета Западной Австралии (University of Western Australia).
“Один классический путь, который они проделывают, это путь производства белков, затем выработка и связывание его с рецептором другой клетки или же через межклеточных контакт”.
Кроме клеточного сигнализирования, основанного на белках, исследователи обнаружили, что остеокласты могли бы также производить «малые» smallsac-ikestructurescontainingmiRNAsthatcouldcommunicatewithothercells.
“Мы открыли, что остеокласты могут посылать сигнал остеобластам о стимуляции костного роста, так что если мы нашли бы способ манипулировать этим, то вместо способствования росту костной массы, это приводило бы к новому методу лечения остеопороза,” – сказал он.
Читать больше в «Asian Scientist Magazine»: http://www.asianscientist.com/2016/03/in-the-lab/osteoporosis-microrna-mir-214-3p/
остеокласт - Osteoclast - qwe.wiki
Остеокластов (от древнегреческого ὀστέον (Остеон) , что означает «кость», и κλαστός (clastos) , что означает «разбитый») является одним из видов костных клеток , который разрушает костную ткань . Эта функция имеет решающее значение в обслуживании, ремонте и реконструкции из костей в позвоночном скелета . Остеокластов разбирает и переваривает композит гидратированного белка и минеральных веществ на молекулярном уровне путем секреции кислоты и коллагеназы , процесс , известный как резорбции кости . Этот процесс также помогает регулировать уровень крови кальция .
Одонтокласт (/ Odon · с · кластов /; о-don'to-klast) является остеокластов , связанный с поглощением корней молочных зубов .
Состав
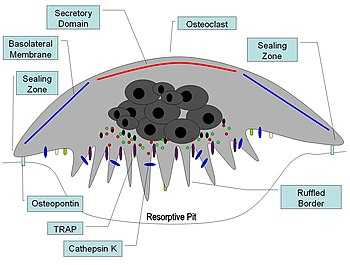 Иллюстрированное поперечное сечение активированных остеокластов
Иллюстрированное поперечное сечение активированных остеокластов Остеокластов является большой многоядерные клетки и остеокласты человека на кости , как правило , имеют пять ядер и 150-200 мкм в диаметре. Когда остеокластов индуцирующих цитокины используются для преобразования макрофагов в остеокласты, очень большие клетки , которые могут достигать 100 мкм в диаметре происходит. Они могут иметь множество ядер, и , как правило , выражают основные остеокластов белков , но имеют существенные отличия от клеток в живых костях из-за не-природный субстрат. Размер многоядерных собранных остеокластов позволяет ему сосредоточиться перенос ионов, белок секреторных и везикулярных транспортных возможности многих макрофагов на локализованную области кости.
Место нахождения
В кости, остеокласты находятся в ямках на поверхности кости , которые называются резорбции бухт или Хаушип в лакуны . Остеокластов характеризуются цитоплазмами с однородным «пенным» внешним видом. Это явление происходит из - за высокой концентрации везикул и вакуолей . Эти вакуоли включают лизосомы , наполненные кислой фосфатазы . Это позволяет охарактеризовать остеокластов их окрашивания для высокой экспрессии в тартратрезистентной кислой фосфатазы (TRAP) и катепсина K . Остеокласты шероховатая эндоплазматическая сеть редка, и комплекс Гольджи обширен.
На участке активной резорбции кости, остеокласты образуют специализированную клеточную мембрану , на «трепала границу», которая противодействует поверхность костной ткани. Это широко сложить или взъерошенные границы облегчает удаление костей за счет резкого увеличения поверхности клеток для секреции и поглощения содержимого резорбции отсека и является морфологической характеристикой остеокластов, активно резорбции кости.
развитие
С момента своего открытия в 1873 году там было много споров об их происхождении. Три теории были доминирующими: с 1949 по 1970 год ткани происхождения соединительно был популярен, в котором говорилось , что остеокласты и остеобласты одного и того же рода, и остеобласты соединяются вместе , чтобы сформировать остеокластов. После нескольких лет споров теперь ясно , что эти клетки развиваются из себя слияния макрофагов. Это было в начале 1980 - х годов , что моноциты система фагоцитоза была признана в качестве предшественника остеокластов. Образование остеокластов требует присутствия RANKL (рецептор активатора ядерного фактора Кв лиганда) и M-CSF (макрофагальный колониестимулирующий фактор) . Эти связанные с мембранами белки получают путем соседних стромальные клетки и остеобласты , таким образом , требует непосредственного контакта между этими клетками и остеокластов прекурсоров .
М-CSF , действует через его рецептор на остеокласты, C-FMS (колониестимулирующий фактор 1 рецептор), трансмембранная тирозинкиназу -рецептор, что приводит к вторичной матричной активации тирозинкиназы Src. Обе эти молекулы необходимы для остеокластогенеза и широко участвует в дифференциации моноцитов / макрофагов клеток , полученных.
RANKL является членом семейства некроза опухоли ( TNF ), и имеет важное значение в остеокластогенезе. RANKL нокаутных мышей проявляют фенотип остеопетроза и дефектов прорезывания зубов, наряду с отсутствием или дефицитом остеокластов. RANKL активирует NF-κβ (ядерный фактор-κβ) и NFATc1 (ядерный фактор активированных Т - клетки, цитоплазматический, кальциневрин-зависимый 1) через RANK . Активация NF-κβ стимулируется почти сразу после того, как взаимодействие RANKL-RANK происходит и не повышалась. NFATc1 стимуляция, однако, начинается ~ 24-48 часов после связывания происходит и его выражение было показано, что RANKL зависит.
Дифференцировку остеокластов ингибируется Остеопротегерин (OPG), который получают с помощью остеобластов и связывается с RANKL тем самым предотвращая взаимодействие с RANK. Это может быть важно отметить , что в то время как остеокласты являются производными от гемопоэтической линии, остеобласты получают из мезенхимных стволовых клеток.
функция
После активации остеокластов перейти к областям микротрещин в костях хемотаксиса . Остеокласты лежат в небольших полостях называются лакуной Хаушипа, в образованной из переваривания основной кости. Уплотнительная зона прикрепления остеокластов в плазматической мембране к подлежащей кости. Уплотнительные зоны ограничены поясами специализированных адгезионных структур , называемых podosomes . Приложение к костной матрицы облегчается за счет рецепторов интегрина, такие как v 3, с помощью специфического мотива аминокислоты Arg-Gly-Asp в матричных белков костной ткани, таких как остеопонтина . Остеокластов высвобождает ионы водорода под действие карбоангидразы ( H 2 O + CO 2 → HCO 3 - + Н + ) через взъерошенные границы в резорбтивную полость, подкисление и помогающего растворение минерализованной костной матрицы в Ca 2+ , H 3 PO 4 , H 2 CO 3 , вода и другие вещества. Дисфункция карбоангидразы была задокументирована , чтобы вызвать некоторые формы остеопетроза. Ионы водорода закачивает против высокого градиента концентрации с помощью протонных насосов , в частности , уникальной вакуольной-АТФаза . Этот фермент был мишенью в профилактике остеопороза . Кроме того, несколько гидролитические ферменты , такие как члены катепсина и матричной металлопротеиназы (ММР) группы, освобождаются , чтобы переварить органические компоненты матрицы. Эти ферменты высвобождаются в отсек с помощью лизосом . Из этих гидролитических ферментов, катепсина К имеет наибольшее значение.
Катепсина K и другие катепсины
Катепсина К является коллагенолитической, папаин -как, цистеин протеаза , который в основном выражается в остеокластах и секретируются в резорбтивную яму. Катепсина К основным протеазы участвуют в деградации коллагена I типа и других noncollagenous белков. Мутации в гене катепсина K связаны с пикнодизостоз , наследственной osteopetrotic болезни, которая характеризуется отсутствием функциональной экспрессии катепсина К. Нокаут исследования катепсина К у мышей приводит к osteopetrotic фенотипа, который, частично компенсируется увеличением экспрессии других , что катепсин К и усиливается остеокластогенез протеаз.
Катепсина К имеет оптимальную ферментативную активность в кислых условиях. Он синтезируется в виде профермента с молекулярным весом 37kDa, и после активации аутокаталитического расщепления, превращается в зрелую, активную форму с молекулярной массой ~ 27kDa.
При поляризации остеокластов над местом резорбции, катепсин К выделяются из трепали границ в резорбтивную яму. Катепсина K переселяется через трепали границу межклеточных везикулы и затем высвобождают функциональным секреторным домен . В пределах этих межклеточных везикул, катепсина К, наряду с активными формами кислорода , генерируемых TRAP , дополнительно ухудшает костный внеклеточный матрикс.
Несколько других катепсины выражены в остеокластов , включая катепсины В , C , D, E, G и L. Функция этих цистеина и аспарагиновой протеазы , как правило , неизвестны в пределах кости, и они выражены в гораздо более низких уровнях , чем катепсина К.
Исследования катепсина L мышей с неоднозначны, отчетом с пониженной губчатой костью в гомозиготном и гетерозиготном катепсине L мышей с по сравнению с диким типом и другим отчетом не находя скелетные аномалий.
Матричные металлопротеиназы
В матричных металлопротеиназ (ММР) включают семейство более чем 20 цинк-зависимой эндопептидаз. Роль матричных металлопротеиназ (ММР) в остеокластах биологии плохо определена, но и в других тканях они были связаны с опухолевым содействием деятельностью, такие как активация факторов роста и необходимы для метастазирования опухоли и ангиогенеза.
ММР9 связан с костной микросреде. Это выражается остеокластами, и , как известно, требуется для остеокластов миграции и является мощной желатиназой. Трансгенные мыши , лишенные MMP-9 развиваются дефекты развития костей, внутрикостного ангиогенеза и репарации переломов.
MMP-13 , как полагают, участвуют в резорбции костной ткани и дифференцировки остеокластов, а нокаутные мыши Выявленные уменьшилось число остеокластов, остеопетроз и снижение резорбции кости.
ММР, выраженные остеокластов, включают ММР-9, -10, -12, -14 и. помимо ММР-9, мало что известно о их значимости для остеокластов, однако, высокие уровни ММР-14 находятся в зоне герметизации.
остеокластов физиология
В 1980 - х и 90 - х годах была изучена физиология типичных остеокластов в деталях. С выделением трепали границ изучался транспорт ионов через него непосредственно в биохимических подробно. Энергия-зависимый транспорт кислоты был проверен и постулировали протонный насос очищает. При успешной культуре остеокластов, стало очевидно , что они организованы так, чтобы поддерживать массовый перенос протонов для подкисления резорбции отсека и солюбилизаций костного минерала. Это включает в себя Раффлед границы Cl - проницаемость для контроля мембранного потенциала и базолатеральная Cl - / HCO 3 - . Обмен поддерживать цитозольный рН в физиологически приемлемом диапазоне>
Эффективность его секреции ионов зависит от остеокластов , образуя эффективное уплотнение вокруг резорбции отсека. Расположение этой «зона герметизации» по- видимому, опосредовано интегрины экспрессируются на поверхности остеокластов. С уплотнительной зоной на месте, многоядерные остеокласты реорганизуют себя. Развитие высоко инвагинированная трепала мембрану соединяющей всасывающий отсек позволяет массивную секреторную активность. Кроме того, она позволяет везикулярный трансцитоз минерала и деградированного коллаген от взволнованной границы к свободной мембране клетки, и его высвобождения в внеклеточный. Эта активность завершает резорбцию кости, и оба минеральные компоненты и фрагменты коллагена выходят в общий кровоток.
регулирование
Остеокласты регулируется несколько гормонов , в том числе паратиреоидного гормона (ПТГ) из паращитовидной железы, кальцитонина из щитовидной железы, а также фактор роста интерлейкина 6 (IL-6). Этот последний гормон, ИЛ-6 , является одним из факторов заболевания остеопороза , который является дисбаланс между костной резорбцией и образованием костной ткани. Остеокластов активность также опосредованы взаимодействием двух молекул , полученных остеобластов, а именно остеопротегерина и RANK - лиганда . Обратите внимание , что эти молекулы также регулируют дифференцировку остеокластов.
одонтокласт
Одонтокласт (/ Odon · с · кластов /; о-don'to-klast) является остеокластов , связанный с поглощением корней молочных зубов .
Альтернативное использование термина
Остеокластов может также быть инструментом для разрушения и восстановить кости (происхождение гречески остеон : кости и klastos : сломаны). Чтобы избежать путаницы, ячейка была первоначально называется osotoclast. Когда хирургический инструмент вышел из употребления, клетка стала известна своим настоящим именем.
Клиническое значение
Гигантские остеокласты могут возникать в некоторых заболеваниях, включая болезнь Педжета костной и бисфосфонаты токсичности.
У кошек, ненормальное одонтокласт активность может привести к кошачьему odontoclastic резорбции поражения , что вызывает необходимость извлечения пораженных зубов.
история
Остеокласты были обнаружены Kolliker в 1873 году.
Смотрите также
Рекомендации
внешняя ссылка
Костная резорбция — Википедия
Ко́стная резо́рбция (от англ. bone resorption), или резорбция костной ткани, — медико-биологический термин, в целом обозначающий процесс разрушения (рассасывания, деградации) костной ткани при непосредственном участии остеокластов.
Следует отделять костную резорбцию от самой по себе резорбции (от лат. resorbere — поглощать) — многозначного научного термина, в зависимости от области применения имеющего несколько различных значений. Ниже приведены основные из них:
1) повторное поглощение или всасывание (в биологии и физиологии)
2) рассасывание и растворение (в медицине и патологической анатомии).
Резорбция костной ткани (разрушение, рассасывание кости, остеолиз) происходит при участии гигантских многоядерных клеток, так называемых остеокластов, которые также имеют большое количество лизосом, митохондрий и вакуолей.
Остеокласт — это основная клетка, участвующая в процессе резорбции кости. Характерной особенностью остеокласта является появление некоей функциональной зоны — «гофрированного края», или «щёточной каёмки», — при активизации этих клеток. Гофрированный край представляет собой спирально-скрученную мембрану клетки с множественными цитоплазматическими складками, который обращён в сторону развивающегося процесса резорбции, и является местом активного окисления тканей.[1]:26-28 Группа остеокластов растворяет минеральный компонент кости, а также гидролизует органический матрикс. Разрушение кости начинается с прикрепления остеокласта к минерализованной костной поверхности «гофрированным краем», через который выделяются гидролитические ферменты и протоны, а также различные интегрины (α₁, αᵥ, β₁, β₃), участвующие в растворении кости.[1]:28 Другие клетки, принимающие участие в резорбции костной ткани — это моноциты и макрофаги. Они взаимодействуют с костной тканью посредством фагоцитоза и хемотаксиса, в большинстве случаев действуя как «уборщики мусора». Помимо фагоцитарной активности продуцируются цитокины (ИЛ-1, ИЛ-1α, ИЛ-1β, ФНО-α и др.) влияющие на активизацию коллагеназ, разрушающих белковый матрикс. Кроме того, моноциты и макрофаги рассматриваются многими учёными как предшественники остеокластов.[1]:31-32 Имеются сведения о влиянии лимфоцитов на резорбцию костной ткани посредством секреции ФНО-β, а также через 1,25-дигидроксивитамин D и ПТГ, к которым лимфоциты имеют рецепторы.[1]:32
Резорбция костной ткани является неотъемлемой частью как физиологического процесса, так и патологического. Прежде всего следует различать патологическую резорбцию и нормальный физиологический процесс.
Патологическая костная резорбция может быть ограниченной (локальной), которая спровоцирована местным воспалением, например, вследствие травмы или инфекции, при этом запускаются локальные факторы, активирующие резорбцию, такие как факторы роста, цитокины, простагландины и др. Повышенная костная резорбция может проявляться во многих областях скелета и тогда она имеет системный характер, в этих случаях задействованы системные факторы регуляции. Такая резорбция костной ткани наблюдается при многих метаболических заболевания скелета, особенно при остеопении и остеопорозе, заболеваниях эндокринной системы, ревматических заболеваниях, заболеваниях органов пищеварения, почек, крови и других состояниях, а также при генетических нарушениях и приёме некоторых медикаментов.[2]:12-29
Физиологическая костная резорбция является неотъемлемой частью функционирования кости, которая постоянно обновляется за счёт двух противоположных процессов — разрушения и образования костной ткани. Костная ткань —это динамическая система с активным метаболизмом. Последовательная цепь процессов удаления участков старого костного матрикса и замещение его новым носит название ремоделирования костной ткани или костное ремоделирование.[2]:10 В детском возрасте за счёт именно этих процессов происходит рост и увеличение скелета, в этот период образование костной ткани естественным образом преобладает над резорбцией. Локальным проявлением физиологической костной резорбции также может служить процесс прорезывания зубов, в котором продвижению зубного фолликула предшествует активная резорбция челюстной костной ткани. В сформировавшемся скелете (зрелый возраст) процессы рассасывания старой кости и образования новой в целом уравновешены. Однако с возрастом процессы ремоделирования постепенно смещаются в сторону резорбции, и количество рассосавшейся костной ткани начинает преобладать над вновь образованной, в результате чего и происходит постепенная потеря костной массы, что может приводить сначала к возрастной остеопении, а затем и к — остеопорозу.
Ремоделирование кости не только обеспечивает сохранность и обновление скелета, но и играет важную роль в минеральном обмене, так как кость является естественным резервуаром микроэлементов (кальция, магния и фосфатов), которые в период резорбции постепенно высвобождаются и поступают в кровоток.
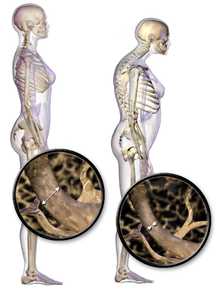 Видимые возрастные изменения
Видимые возрастные измененияв костной ткани (остеопороз)
Процесс перестройки (ремоделирования) костной ткани происходит в отдельных участках кости, которые носят название «единицы ремоделирования» или базисной многоклеточной единицы (БМЕ). В этих участках локально протекают сопряжённые процессы резорбции и образования кости. Активизация процесса начинается с запуска неких сигналов-стимулов, по которым остеокласты и другие мононуклеарные клетки мигрируют к определённому участку костной ткани и прикрепляются к костной пластине. Остеокласты продуцируют протеолитические ферменты, лактат, ионы водорода, которые разрушают (гидролизуют) белковый матрикс и растворяют минеральную часть кости, при этом выделяется свободный кальций и другие компоненты.[1]:85—87 В результате такой активности в губчатой кости образуются углубления до 40 мкм, имеющие форму блюдца, а в кортикальной кости — конусовидные пустоты диаметром около 150 мкм и длиной до 2,5 мм. Продолжительность фазы резорбции длится от 27 дней в кортикальном слое кости и до 42 дней в губчатой ткани. Этот период резорбции включает в себя и фазу реверсии длительностью 4 дня в кортикальной и 9 дней в губчатой тканях кости. Фаза реверсии является переходным периодом, в который процесс резорбции сопряжён с процессом формирования кости. В период реверсии образуется цементирующая линия (или клей), которая соединяет новую и старую кость. Цикл ремоделирования завершается фазой формирования кости, которая длится от 95 до 130 дней. Вновь образующийся участок костной ткани носит название базисной структурной единицы (БСЕ) или остеона. Остеобласты образуют неминерализованный органический матрикс (остеоид), который через 25—35 дней начинает минерализоваться.[1]:87 Ремоделирование кости начинается ещё в пренатальном периоде и продолжается на протяжении всей жизни. Активность ремоделирования костной ткани и скорость костеобразования находятся на высоком уровне вплоть до достижения индивидом половой зрелости, затем этот уровень снижается. В среднем к 20—23 годам жизни достигается пик костной массы, который поддерживается на заданном уровне до 30—35 лет у женщин, а у мужчин — несколько дольше. В этот возрастной период ремоделирование кости имеет циклический равномерный характер, в котором процессы разрушения и образования кости уравновешены, что обеспечивает обновление кости и сохранение костной массы, а также поддерживает минеральный обмен. С возрастом интенсивность ремоделирования костной ткани резко снижается, это происходит после 35 лет у женщин и 50 лет у мужчин. Резорбция костной ткани идёт с бо́льшей скоростью, чем костеобразование, начинается постепенная потеря массы кости, что становится причиной возрастного уменьшения костного объёма и снижения минеральной плотности костной ткани (МПКТ).[2]:12
Без резорбции костной ткани не может происходить образование новой кости. Процесс ремоделирования идёт одновременно в нескольких отдельных участках скелета, где внеклеточный матрикс последовательно удаляется, а затем замещается новой тканью. В целом цикл ремоделирования схематично можно представить следующим образом: активизация → резорбция → реверсия → формирование → покой.[1]:85
Регулирование процессов ремоделирования костной ткани — это сложный механизм, который находится под контролем различных системных и локальных факторов. К системным факторам относятся: кальций-регулирующие гормоны (паратиреоидный гормон — ПТГ; кальцитонин; активные метаболиты витамина D₃ — кальцитриол), системные гормоны (половые гормоны — эстрогены, андрогены, прогестины, тестостерон; гормоны щитовидной железы — тироксин; глюкокортикоиды — ГК; соматотропный гормон — СТГ; инсулин). Местные регуляторы представляют: ростовые факторы (инсулиноподобные ростовые факторы — ИПРФ-1 и ИПРФ-2; ростовой фактор фибробластов; трансформирующий фактор роста β — ТФР-β; и др.), простагландины (простагландин Е₂ — ПГЕ₂), цитокины (интерлейкины — ИЛ-1, ИЛ-2, ИЛ-6, ИЛ-11 и др.; гранулоцитарно-макрофагальный колониестимулирующий фактор — ГМКГ; фактор некроза опухоли — ФНО-α; лимфотоксин-альфа — ФНО-β).[2]:13,22 Одни из этих гормонов и факторов, прежде всего, стимулируют костную резорбцию, другие оказывают преимущественно тормозящее действие, однако и те и другие действуют по принципу обратной связи.
Стимулируют костную резорбцию:
Паратиреоидный гормон (ПТГ) — важнейший регулятор кальциевого обмена и костного метаболизма. Его основное действие на костную ткань — это стимуляция костной резорбции через активацию остеокластов.[3]
Глюкокортикоиды (ГК) в избыточном количестве оказывают непрямое стимулирующее влияние на костную резорбцию. Они снижают абсорбцию кальция в кишечнике и реабсорбцию кальция в почках, что приводит к гипокальциемии, которая по принципу обратной связи стимулирует секрецию ПТГ. Кроме того, ГК подавляют функцию остеобластов и замедляют созревание клеток предшественников остеобластов. При гиперкортицизме отмечается снижение соматотропной функции гипофиза и уровня половых гормонов, что в свою очередь замедляет процессы костеобразования.[2]:46—48
Гормоны щитовидной железы. Тиреоидные гормоны оказывают как прямое, так и опосредованное действие на активизацию костного обмена и процессы ремоделирования. Тироксин (Т₄) и трийодтиронин (Т₃) необходимы для нормального роста и развития скелета, они увеличивают число и активность остеокластов, но также активизируют и функцию остеобластов. Избыток этих гормонов в организме (как эндогенный, так и экзогенный) приводит к резкой активизации процесса резорбции костной ткани.
Витамин D — холекальциферол в настоящее время считается компонентом гормональной системы и относится к прогормонам стероидной группы. Он регулирует фосфорно-кальциевый обмен, участвует в минерализации костной ткани и в то же время поддерживает гомеостаз кальция. Биологическое действие активных метаболитов этого витамина (кальцитриола) состоит в активизации костного обмена, повышении абсорбции кальция и фосфора в кишечнике и усилении экскреции кальция почками. Совместно с ПТГ Витамин D стимулирует костную резорбцию (как остеокластическую резорбцию, так и остеоцитарный остеолиз) за счёт увеличения количества остеокластов и активизации дифференциации клеток-предшественников.[2]:14—16
Локальные факторы, усиливающие костную резорбцию — интерлейкины (ИЛ-1, ИЛ-3, ИЛ-6, ИЛ-11), фактор некроза опухоли (ФНО-α), лимфотоксин-альфа (ФНО-β), гранулоцитарно-макрофагальный стимулирующий фактор, фактор стволовых клеток и простагландины.
Ингибируют костную резорбцию:
Кальцитонин-гипокальциемический гормон — продуцируется С-клетками щитовидной железы. Органом-мишенью для него служит костная ткань, а основным биологическим действием является торможение костной резорбции. Кальцитонин проявляет очень мощное прямое ингибирующее действие на остеокластическую активность и формирование остеокластов, чем провоцирует исчезновение функционально-активного гофрированного края клетки. Кроме того он подавляет распад коллагена. Кальцитонин является функциональным антагонистом ПТГ.[1]:34
Половые гормоны (эстрогены, андрогены, прогестины) — оказывают значительное влияние на скелет в течение всей жизни человека. Они непосредственно участвуют в формировании скелета и определяют его половой диморфизм, контролируют достижение пика костной массы и скорость её дальнейшего снижения, поддерживают минеральный гомеостаз. В этом ряду ведущую роль играют эстрогены, регулируя метаболизм костной ткани, как у женщин, так и у мужчин.[2]:19[2]:19
Эстрогены оказывают прямое действие на все костные клетки в силу того, что рецепторы к эстрогенам обнаружены на всех типах костных клеток. Они снижают костную резорбцию за счёт угнетения активности остеокластов, а также их дифференцирования на ранних стадиях из клеток предшественников. Опосредованное действие эстрогенов осуществляется через подавление местных резорбирующих факторов (ИЛ-1, ИЛ-6, ФНО-α, ГМКФ). Кроме того эстрогены проявляют защитное действие на костную ткань от резорбтивного влияния ПТГ.[2]:18—20
Дефицит эстрогенов у женщин репродуктивного возраста и в период менопаузы является ведущим фактором в развитии остеопении и остеопороза, в основе развития которых лежит нарушение равновесия в процессе ремоделирования костной ткани с преобладанием темпа резорбции кости. При этом также имеет место снижение синтеза кальцитриола [1,25(ОН)₂D₃], увеличение количества цитокинов (ИЛ-1, ИЛ-6) и факторов роста (ИПФР-I, ИПФР-II, ТФР-β и др.), продукция которых также регулируется эстрогенами.[1]:38—41
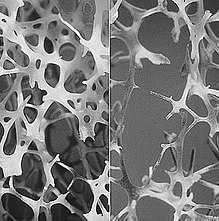
В общей диагностике заболеваний и непатологических состояний организма с проявлением костной резорбции (в первую очередь это остеопения и остеопороз), а также в оценке степени этой резорбции в настоящее время существуют три основных направления:
1. Лучевая диагностика — это рентгенография, радиография и остеоденситометрия.
Широкое распространение имеет обычная рентгенография. Однако визуальная оценка рентгенограмм скелета является субъективной и малоинформативной. Остеопороз по рентгенограммам выявляется лишь на поздних стадиях, когда происходит потеря уже 30 % костной массы и более. Существуют радиоизотопные методы исследования скелета — сцинтиграфия, которая также не способна выявить остеопенические состояния, как правило, предшествующие остеопорозу.[2]:67-73 Наиболее информативным методом костной денситометрии является двухэнергетическая рентгеновская абсорбциометрия (DEXA). Это низкоэнергетический метод с высокой точностью измерений и малой лучевой нагрузкой на пациента. Он позволяет количественно определить минеральную плотность костной ткани (МПК) в различных отделах скелета и общую костную массу, а также выявить их снижение уже при 2-5 % потери.[4]:45 Расчёт условных единиц и величины стандартного отклонения от среднестатистических показателей позволяет количественно различить как варианты нормы, так остеопению и остеопороз.[2]:81 Метод компьютерной томографии расширяет возможности исследования костной ткани. Его преимущества — это высокая воспроизводимость, меньшее облучение, высокая точность исследования и возможность раздельной оценки губчатой и компактной кости.[2]:82 В целом лучевая диагностика позволяет в большей степени оценить состояние костной ткани по минеральному компоненту, но является менее информативной в отношении органической составляющей. Кроме того к её недостаткам можно отнести облучение пациента и относительную дороговизну обследования.
2. Лабораторная диагностика включает исследование минерального обмена, гормональное обследование и определение биохимических маркёров костного метаболизма.
Минеральный гомеостаз оценивается по уровню общего и ионизированного кальция, фосфора и магния в крови, а также активных форм витамина D, которые позволяют косвенно судить об активности обменных процессов в костной ткани. Важным моментом в этой связи является исследование экскреции кальция и креатинина в утренней моче, проведённые натощак.[2]:87-89 Это наиболее дешёвый метод оценки резорбции кости, однако он малочувствителен, и может быть в достаточной мере информативным только при высокой скорости резорбции. Следующим шагом в оценки минерального обмена и установки диагноза служит определение уровня кальцийрегулирующих гормонов (ПТГ, кальцитонин).
Исследование системных гормонов является ключевым звеном в диагностике метаболических заболеваний скелета. Ведущими среди них являются половые гормоны (эстрогены, андрогены, тестостерон), при снижении уровня которых усиливается костная резорбция, что ведёт к развитию остеопении и остеопороза (гипогонадальный остеопороз, постменопаузальный остеопороз).[4]:33-35Тиреоидные гормоны в своём избытке также повышают костную резорбцию, а гипертиреоз приводит к усилению костного обмена, увеличению количества остеокластов и развитию остеопороза. В то же время при снижении функции щитовидной железы (гипотиреозе) нарушается обмен кальция с тенденцией снижения его концентрации в крови (особенно ионизированного кальция), значительно замедляется костное ремоделирование, что может приводить к развитию остеопении. Стероидный остеопороз возникает в результате воздействия на костную ткань избыточного количества гормонов коры надпочечников — глюкокортикоидов (ГК). Эндогенный гиперкортицизм (при болезни и синдроме Иценко-Кушинга) и экзогенный гиперкортицизм (в результате длительного терапевтического применения ГК) усиливают резорбцию костной ткани.[2]:46-49 Анализ гормонограмм необходим не только в диагностических целях для выявления причин остеопении и остеопороза, но и выбора адекватной терапии.
Биохимические маркёры костной резорбции
Наиболее полную информацию о процессах ремоделирования костной ткани представляют биохимические маркёры костного метаболизма. Это маркёры костной резорбции и маркёры формирования кости.[5] Резорбция костной ткани включает в себя разрушение минерального и органического комплексов. При разрушении костного матрикса происходит деструкция коллагена с образованием молекулярных фрагментов, это С- и N-телопептиды коллагена I типа, а также поперечных сшивок коллагена — пиридинолина и дезоксипиридинолина.[6] В норме эти производные пиридина образуют поперечные соединения в спиральной структуре коллагена, обеспечивая его стабильность за счет поперечных ковалентных связей между отдельными молекулами полипептидных цепей коллагена I типа. Повышается уровень лизосомальных ферментов остеокластов — кислой фосфатазы и особенно тартратрезистентной кислой фосфатазы (ТРКФ). Все эти компоненты преимущественно содержатся в костной ткани, в других органах и тканях они содержатся в минимальных количествах. Поэтому при резорбции кости эти продукты распада поступают в кровоток и затем выводятся с мочой, идеально играя роль биохимических маркёров костной резорбции.[4]:42-45 Определять маркёры можно как в моче, так и в сыворотке крови методом иммуноферментного анализа (ИФА или ELISA). С-концевые телопептиды коллагена I типа фрагментируются и отщепляются в самом начале деструкции кости, они получили название CrossLaps. Различают α- и β- изомеры CrossLaps. Выявление высоких концентраций β-CrossLaps свидетельствует о резорбции относительно старой кости, а повышение уровня α-изомеров характеризует усиление резорбции молодой или вновь образованной костной ткани. Иммунохимическое определение β-CrossLaps коррелирует с результатами гистоморфометрического исследования биоптатов кости. Однако точность метода в большой степени зависит от условий проведения, и качества используемых коммерческих наборов тест-реактивов.
Преимуществом биохимических методов исследования является неинвазивность проведения, доступность, особенно параметров определяемых в моче, поскольку моча является одним из самых удобных объектов исследования. Маркёры костной резорбции являются высокоспецифичными, они быстрее реагируют на изменения в ремоделировании кости и появляются в исследуемых жидкостях, предоставляя информацию об активности процесса.[6] В отличие от денситометрии, биохимические маркёры являются более ранними диагностическими критериями. Хотя денситометрия — весьма точный и нетравматичный метод исследования для оценки функционально-структурного состояния костной ткани и диагностики остеопороза, однако, с момента начала изменения в костной ткани и до момента получения достоверной информации необходим более длительный промежуток времени.[4]:72
При этом следует отчётливо понимать, что ни один из параметров и методов диагностики не является исчерпывающим или самодостаточным. У каждого метода есть свои преимущества и недостатки, а для получения более достоверной клинической картины необходимо — комплексное мультидисциплинарное обследование.
«Биохимические маркёры костной резорбции, показатели минеральной насыщенности крови, уровень остеотропных гормонов, а также данные денситометрии у одной пациентки не всегда однонаправлены и не во всех случаях соединяются в однородную клиническую картину. Этот факт лишь свидетельствует о дискретности данного патологического процесса и расхождении во времени биохимических и морфологических проявлений одного и того же заболевания, что нисколько не умаляет значимости этих диагностических критериев, но только указывает на необходимость комплексного обследования и системных выводов».[4]:72
Хотя не существует какого-либо единственного и специфического костного маркёра и невозможно поставить диагноз только на основании исследования биохимических маркёров костного ремоделирования, тем не менее, они позволяют проводить дифференциальную диагностику метаболических заболеваний скелета (особенно с остеомаляцией) и наблюдение за динамикой костного метаболизма при лечении остеопороза.[2]:106-107
Показатели костной резорбции:
Продукты остеокластов — кислая фосфатаза, тартратрезистентная кислая фосфатаза (ТРКФ) — определяются биохимическим анализом крови.
Продукты деградации коллагена — гидроксипролин (определяется в моче), пиридинолин и дезоксипиридинолин (могут определяться как в моче, так и в крови).[6] Коллагеновые перекрёстные группы: N-концевой телопептид, С-концевой телопептид (CrossLaps) — определяются в моче и крови.
Продукты распада минерального комплекса — уровень ионизированного кальция в крови, концентрация кальция и фосфора в моче по отношению к креатинину (утром натощак).
3. Биопсия костной ткани.
Гистоморфологическое исследование до сих пор остаётся единственным методом прямого и точного анализа ремоделирования кости на клеточном и тканевом уровне. Этот метод играет первостепенную роль в постановке диагноза, он достоверно позволяет дифференцировать заболевания характеризующиеся разрежением костной ткани и исключать остеомаляцию, а также определять скорость ремоделирования кости. Даёт возможность уточнять патогенез заболевания, выявляя анатомическую и гистопатологическую гетерогенность механизмов, ведущих к утрате костной ткани при остеопорозе. Кроме того он позволяет судить о качестве кости и оценивать эффективность лечения с позиции воздействия лекарственных средств на процессы ремоделирования (подавляющих резорбцию или стимулирующих образование костной ткани). В последнее время именно эта сфера применения гистоморфометрии кости занимает важное место в клинических и экспериментальных исследованиях.[1]:321 Однако далеко не все патоморфологические лаборатории оснащены соответствующим оборудованием для работы с недекальцинированной костью, кроме того проведение исследования является трудоёмким, длительным и дорогостоящим. При этом нельзя не учитывать, что получение любого биоптата связано с внедрением в организм, которое сопряжено с риском и дискомфортом для пациента.[2]:109
Факторы риска ускорения костной резорбции[править | править код]
Основные заболевания, характеризующиеся повышенной резорбцией и утратой костной ткани это остеопения и остеопороз. Как правило, они протекают медленно и бессимптомно, что затрудняет их диагностику в ранние сроки. Поэтому так важно знать те факторы, признаки и условия, которые способствуют развитию этих заболеваний или указывают на уже начавшиеся нарушения.
К таким факторам, прежде всего, относятся гормональные — это сам по себе факт принадлежности к женскому полу, низкий уровень эстрогенов, позднее начало менструаций, нестабильный цикл, длительный период аменорей до наступления менопаузы, бесплодие, ранняя менопауза (в том числе после хирургических или других вмешательств), частые беременности и роды, длительная лактация.
Следует особо отметить, что у женщин, имеющих в анамнезе какие-либо из перечисленных факторов, при снижении уровня эстрогенов развиваются некариозные поражения зубов (эрозии, клиновидные дефекты, повышенная стираемость). Эта патология характеризуется убылью (часто — видимой) твёрдых тканей зубов (эмали, дентина и цемента), которая часто сопровождается их повышенной чувствительностью (гиперестезией зубов).[4]:53
"Зубы являются составной частью костного скелета, к тому же единственной его видимой частью. Общие механизмы в развитии некариозных поражений зубов, остеопении и остеопороза возникают у женщин вследствие снижения базового уровня эстрогенов в крови. Однако остеопения и остеопороз развиваются медленно и бессимптомно, и зачастую диагностируются только в поздние сроки, а некариозные поражения имеют сигнальные симптомы в виде дефектов тканей и гиперестезии зубов, которые легко обнаруживаются и сами себя проявляют. Таким образом, они наглядны, — чем оказывают неоценимую помощь врачу в диагностике.[7]:153
— Г.Е. Соловьёва-Савоярова, «Некариозные поражения зубов у женщин как проявление остеопении и остеопороза»
В свете новейших отечественных научно-медицинских исследований на стыке стоматологии, эндокринологии и остеологии, некариозные поражения зубов могут выступать в качестве сигналов тревоги, предупреждающих о системных гормонально-метаболических нарушений, а также выявляющих на ранних стадиях риск развития остеопении и остеопороза у женщин. Кроме того их проявление следует расцениваться как ранний диагностический признак остеопении, а женщины, имеющие некариозные поражения зубов — автоматически входят в группу риска развития остеопороза.[7]:152-153
Другими факторами риска могут стать такие особенности жизни, как наступление менопаузы у женщин, пожилой возраст (как у женщин, так и у мужчин), низкая масса тела, неправильное питание (малое потребление кальция, непереносимость молочных продуктов, дефицит витамина D, избыточное потребление мяса, несбалансированная диета, голодание, злоупотребление кофе и алкоголем), курение, малоподвижный образ жизни (гиподинамия), избыточные физические нагрузки.
Сопутствующие заболевания и состояния, относящиеся к факторам риска, это эндокринные заболевания (гипогонадизм, болезнь Иценко-Кушинга, гипертиреоз, сахарный диабет I-го типа и др.), заболевания органов пищеварения, почек, крови, ревматические заболевания, нервная анорексия, хронические обструктивные заболевания лёгких, иммобилизация, лучевая терапия.[2]:175-176
Некоторые лекарственные препараты (кортикостероиды, тиреоидные гормоны, гепарин, циклоспорин, тетрациклины и др.) при длительном применении также могут провоцировать или усиливать костную резорбцию.
- ↑ 1 2 3 4 5 6 7 8 9 10 Риггз Б.Л., Мелтон III Л. Дж. «Остеопороз. Этиология, диагностика, лечение» / пер. с англ. под общей редакцией проф. Е. А. Лепарского, Москва — СПб.: «БИНОМ», «Невский диалект», 2000, ISBN 5-7989-0185-8 — 560 с.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Рожинская Л. Я., «Системный остеопороз: Практическое руководство для врачей».— Москва: Издатель Мокеев, 2000 г. издание 2-е, переработанное и дополненное — 196 с. ISBN 5-93135-003-9
- ↑ Lowik C. W. G. M., van der Pluijm G., Bloys H. et al. Parathyroid hormone and PTH-like protein stimulate interleukin-6 production by osteogenic cells: a possible // Res. Commun. — 1999. — No. 162. P. 1549
- ↑ 1 2 3 4 5 6 Соловьёва-Савоярова Г.Е., Дрожжина В.А. «Эстрогены и некариозные поражения зубов» / Силин А.В.. — СПб.: Издательство СЗГМУ им. И.И. Мечникова, 2012. — 140 с. — 700 экз. — ISBN 978-5-89588-049-4.
- ↑ McCormick R. Osteoporosis: Integrating biomarkers and other diagnostic correlates into the management of bone flagility // Alternative Medicine Review. — 2007. — Vol. 12, N 2. — P. 127
- ↑ 1 2 3 И. П. Ермакова, И. А. Пронченко, «Современные биохимические маркеры в диагностике остеопороза», Медицинский научно-практический журнал Остеопороз и остеопатии, № 1, 1998
- ↑ 1 2 Соловьёва-Савоярова Г.Е., Силин А.В., Дрожжина В.А. «Некариозные поражения зубов у женщин как проявление остеопении и остеопороза». Материалы конференции. XVIII Международная конференция челюстно-лицевых хирургов и стоматологов «Новые технологии в стоматологии». — СПб.: Министерства здравоохранения и соц. Развития РФ, 2013. — 152-153 с.
- Риггз Б. Л., Мелтон III Л. Дж. «Остеопороз» (перевод с английского) М. — СПб.: БИНОМ, Невский диалект, 2000.— 560 с. ISBN 5-7989-0185-8
- Рожинская Л. Я. «Системный остеопороз»: Практическое руководство для врачей.— М.: Издатель Мокеев, 2000.— 196 с. ISBN 5-93135-003-9
- Руденко Э. В. «Остеопороз: диагностика, лечение и профилактика». Практическое руководство для врачей.— Минск.: Белнаука, 2001.— 153 с. ISBN 985-08-0421-1
- Соловьёва-Савоярова Г. Е., Дрожжина В. А. «Эстрогены и некариозные поражения зубов». — СПб., Издательство СЗГМУ им. И. И. Мечникова, 2012. — 140 с. ISBN 978-5-89588-049-4
- Соловьёва-Савоярова Г. Е., Дрожжина В. А., Силин А. В., «Некариозные поражения зубов, этиопатогенетический подход к их реконструкции». Материалы IX научно-практической конференции "Современные методы диагностики, лечения и профилактики стоматологических заболеваний. Эндодонтия и реставрации. — СПб., СПбИНСТОМ, 2012, — 121 с. ISBN 978-5-88711-329-6
- Соловьёва-Савоярова Г. Е., Силин А. В., Дрожжина В. А. «Некариозные поражения зубов у женщин как проявление остеопении и остеопороза». Материалы конференции. XVIII Международная конференция челюстно-лицевых хирургов и стоматологов «Новые технологии в стоматологии». — СПб., издательство Министерства здравоохранения и соц. Развития РФ. — 188 с.
- Bettica P., Moro L. «Biochemical markers of bone metabolism in the assessment ofosteoporosis» JIFCC 1995. V. 7, issue 1, pp. 16-22
- Eriksen E.F., Colvald D.S., Berg N.J. et al. «Evidence of estrogen receptors in normal human osteoblast-like cells». — Science. 1988. vol. 241 (1), P.84-86
- Lowik CWGM., van der Pluijm G., Bloys H. et al. «Parathyroid hormone and PTH-like protein stimulate interleukin-6 production by osteogenic cells: a possible». Res. Commun. — 1999. — № 162. pp. 1546—1552.
- McCormick R. «Osteoporosis: Integrating biomarkers and other diagnostic correlates into the management of bone flagility». Alternative Medicine Review. — 2007. — Vol. 12, № 2. — pp. 113—145.
- Roodman G.D., «Advances in Bone Biology». — The Osteoclast Endocr. Rev. 1996. Vol.17 (4). pp.308-332
- Valimaki M. J., Tantela R., Jones J. D., Peterson J. M., Riggs BL. «Bone resorption in healthy and osteoporotic postmenopausal women: comparison markers for serum carboxy-terminal telopeptide of type I collagen and urinary pyridinium cross-links». Eur. Journal Endocrinol. 1994, v. 131, pp. 258—262.
ОСТЕОКЛАСТ
Остеокласт (osteoclastus) — клетка моноцитарно-макрофагальной природы, гигантская многоядерная клетка, способная резорбировать обызвествленный хрящ и межклеточное вещество в процессе перестройки и развития кости.
Остеокласты появляются в местах рассасывания костных структур, основная функция их – лизис минерализованных структур и удаление продуктов распада кости. Остеокласты совместно с остеобластами осуществляют контроль над количеством костной ткани, остеобласты отвечают за создание новой костной ткани путем откладывания костного матрикса, а остеокласты за разрушение старой. Остеокласты образуются в результате слияния гемопоэтических стволовых клеток моноцитарно-макрофагального ростка.
Остеокласты могут иметь от 3-ех до нескольких десятков ядер, число их может достигать ста, размер клетки составляет около 190 мкм, в цитоплазме содержится множество лизосом. В них содержатся гидролитические ферменты, которые, выделяясь из остеокластов, начинают процесс резорбции обызвествленного хряща и основного вещества кости. Остеокласты разрушают кость в тех местах, где она не находится под нагрузкой, ориентируются они на пьезоэлектрические эффекты, которые появляются в кости под нагрузкой. Остеокласты относятся к системе макрофагов, так как имеют моноцитарное происхождение, они не являются костными клетками. Как и другие макрофаги, они образуются из моноцитов, которые развиваются в костном мозге.
Кости способны перестраивать свою структуру так, чтобы приспособиться к испытываемым нагрузкам, следовательно, накопление и разрушение матрикса регулируется локальными механическими напряжениями. Эти механизмы определяют, должен ли матрикс откладываться остеобластами на поверхности кости, или напротив, разрушаться остеокластами, природа этих механизмов пока неизвестна. Важную роль в этом процессе играют факторы роста, их выделяют заключенные в толщу матрикса костные клетки, они выделяются при воздействии нагрузок или разрушении матрикса.
Костная ткань - строение, ремоделирование, резорбция, реверсия, клетки костной ткани
Скелет метаболически активен и постоянно обновляется, и оба процесса регулируются местными и системными факторами. Среди основных функций скелета выделяют структурные (опора, передвижение, дыхание и защита внутренних органов) и метаболические (хранилище для кальция, фосфора и карбоната; карбонатный костный буфер, связывание токсинов и тяжелых металлов). Тесная структурная связь с гемопоэтической системой определяет совместное использование клеток и локальных регулирующих факторов.При нормальном развитии скелета уже в эмбриональном периоде хрящевая ткань замещается более твердой костной тканью (новообразование кости или моделирование). После рождения рост скелета продолжается, но основная клеточная активность направлена на ремоделирование кости, т.е. перестройку уже имеющейся структуры кости. Вновь сформированная на ранних стадиях равития из мезенхимы кость и кость, образующаяся во время быстрого восстановления, могут иметь относительно дезорганизованную структуру коллагеновых волокон в матриксе. Такая кость называется "тканой" (woven) костью. В то же время все другие кости закладываются организованным способом с последовательными слоями хорошо организованного коллагена и называется пластинчатой костью.
Типы костной ткани.
У взрослого человека различают 2 главных типа кости (рисунок 1):
1. Кортикальная кость (плотная и компактная) составляет внешнюю часть всех скелетных структур. На поперечном срезе компактной кости можно видеть, что она состоит из многочисленных цилиндров, образованных концентрическими костными пластинками, в центре каждого такого цилиндра имеется гаверсов канал, вместе с которым он составляет гаверсову систему или остеон. Через каждый гаверсов канал проходят одна артерия, вена, лимфатический сосуд и нервные волокна. До 80 % скелета состоит из кортикальной кости, главной функцией которой является обеспечение механической силы и защиты, но она может участвовать и в метаболическом ответе при тяжелом или длительном минеральном дефиците.
2. Трабекулярная или губчатая кость находится внутри длинных костей, особенно в концевых частях, в телах позвонков и во внутренних частях таза и в других крупных плоских костях. Она представляет собой сеть из тонких анастомозирующих костных элементов, называемых трабекулами. В ее основном веществе содержится меньше неорганического материала (60-65 %), чем в основном веществе компактной кости. Органическое вещество состоит главным образом из коллагеновых волокон. Пространства между трабекулами заполнены мягким костным мозгом. Трабекулярная кость обеспечивает механическую поддержку, особенно в позвоночнике. Метаболически она более активна, чем кортикальная кость и обеспечивает начальные поставки солей в условиях их острого дефицита.
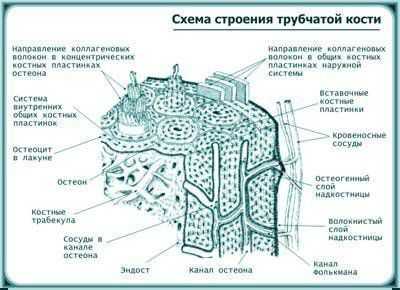
Рисунок 1. Анатомия кости.
Состав кости.
Кость - это обызвествленная соединительная ткань, состоящая из клеток, погруженных в твердое основное вещество. Около 30 % основного вещества составляют органические соединения, преимущественно в форме коллагеновых волокон, а остальные 70 % - неорганические. Главный неорганический компонент кости представлен гидроксиапатитом, т.е. 3[Ca3(PO4)] Ca(OH)2, образованным из кальция и фосфата; но в кости также содержатся в различных количествах натрий, магний, калий, хлор, фтор, карбонат и цитрат.
Костный матрикс.
Органический матрикс в свою очередь состоит из коллагеновых волокон (90-95 %) и основного вещества, которое контролирует отложение солей в кость. Костные соли представлены преимущественно кальцием и фосфатом. Коллагеновые волокна дают кости прочность на разрыв, а соли основного вещества - прочность на сжатие. Коллаген откладывается пластинчатым способом и усилен множественными поперечными связями ("прошивками") внутри и между трехспиральными молекулами коллагена (рисунок 2). Эти поперечные связи представляют собой трехвалентные пиридинолины, которые стойки к деградации и высвобождаются во время резорбции кости в свободной или пептидной форме и могут определяться в сыворотке и моче.
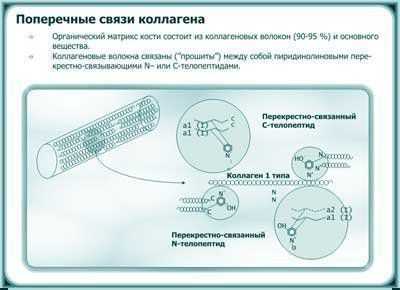
Рисунок 2. Схема коллагеновых поперечных связей в кости. Адаптировано из Eyre D.R., 1996.
Матрикс содержит также неколлагеновые белки, которые важны для регуляции минерализации и укрепления основы коллагена. Кальцийсвязывающие белки включают остеокальцин (костный Gla-протеин) и матриксный Gla-протеин, которые содержат γ-карбоксиглютаминовую кислоту и витамин К зависимы подобно многим факторам свертывающей системы крови. Эти белки могут задерживать минерализацию и позволяют созреть костному матриксу. Даже при том, что остеокальцин является наиболее специфическим белковым продуктом остеобластов, подавление гена остеокальцина не ухудшает рост и минерализацию скелета. Костный сиалопротеин и остеопонтин связываются с кальцием и коллагеном и могут играть роль в процессе прилипания остеокластов к поверхности кости. Неорганическая основа кости представлена кристаллами гидроксиапатита. Эти кристаллы могут содержать карбонат, фторид и различные другие минералы в следовых количествах в зависимости от окружающей среды.
Соли фосфата кальция в костях находятся в 2 формах:
1. Легко обмениваемый пул, который находится в равновесии с внеклеточной жидкостью. Этот запас обеспечивает легкий обмен между костями и внеклеточной жидкостью. Таким образом, если концентрация Ca или фосфата во внеклеточной жидкости увеличивается, соли легко откладываются или, если эти концентрации снижаются, тогда соли легко мобилизуются из этого запаса.
2. Старая структурная кость, где соли фосфата кальция находятся в виде кристаллов гидроксиапатита. Эти кристаллы с трудом мобилизуются или обмениваются с внеклеточной жидкостью и для их мобилизации - резорбции необходим паратгормон.
Клетки костной ткани.
Костные клетки - остеоциты, находятся в лакунах, распределенных по всему основному веществу. Лакуны соединяются между собой тонкими канальцами, содержащими отростки остеоцитов. Через эти канальцы проходят кровеносные сосуды. От каждой лакуны отходит наподобие лучей много тонких канальцев, содержащих цитоплазму (отростки остеоцитов), которые могут соединяться с центральным гаверсовым каналом, с другими лакунами или тянуться от одной костной пластинки к другой.
Остеобласты.
Остеобласты образуются из мезенхимальных стволовых клеток, изначально плюрипотентных, которые могут также дифференцироваться в клетки мышечной, хрящевой и фиброзной ткани, а также в адипоциты. Вероятно имеются клетки предшественники, которые могут далее дифференцироваться только в остеобласты. Эти клетки предшественники остеобластов присутствуют в надкостнице и строме костного мозга.
Как только продукция остеобластами коллагеновых и неколлагеновых белков завершается, некоторые остеобласты внедряются в толщу матрикса и становятся остеоцитами. Остеобласты и остеоциты соединяются друг с другом многими клеточными отростками, которые лежат в канальцах в пределах кости. Этот синцитий взаимосвязанных клеток вероятно важен для ощущения механических сил. Большинство остеобластов либо остается на поверхности кости и рассредоточивается в виде расплющенных клеток, либо подвергается запрограммированной клеточной смерти (апоптозу). Остеобласты сохраняют соединения с остеоцитами, которые могут быть необходимы для передачи сигналов активации во время ремоделирования.
Остеобласты функционально и морфологически гетерогенны. Они имеют рецепторы для факторов (ПТГ, кальцитриол, глюкокортикоиды, половые гормоны, соматотропин и тиреотропин, интерлейкин-1, фактор некроза опухоли альфа, простагландины, инсулиноподобные факторы роста, трансформирующий фактор роста бета, факторы роста фибробластов), которые влияют на ремоделирование кости, и сами продуцируют много регуляторов роста кости.
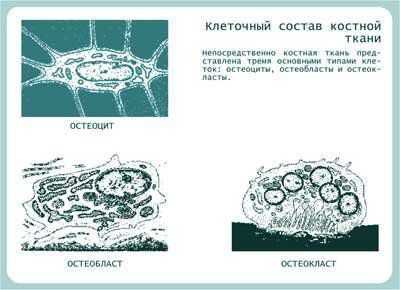
Рисунок 3. Клетки костной ткани. Адаптировано из Афанасьев Ю.И., Елисеев В.Г., 1989.
Остеокласты.
Остеокласты - это крупные многоядерные клетки, которые резорбируют кость, растворяя соли и разрушая матрикс. Активные остеокласты обычно имеют от 2 до 5 ядер, но могут иметь и больше. Они богаты цитоплазмой, имеют множество аппаратов Гольджи и много митохондрий и лизосом. Активно резорбирующие остеокласты крепко прикреплены к кости зоной мембраны, которая относительно лишена субклеточных частиц. Эта область называется "чистой" зоной, хотя лучший термин - зона "изолирования"; так как она как бы герметизирует область действия ферментов. Вторая (внутренняя) зона - наиболее обширная, богатая цитоплазматическими выростами (гофрированная каемка), является областью абсорбции и секреции гидролитических ферментов, где имеет место резорбция кости. В том месте, где остеокласт соприкасается с костным веществом, образуется лакуна. Часто наблюдаются группы остеокластов, которые либо располагаются на поверхности лакун Хоушипа, либо образуют туннели в кортикальной кости, формируя гаверсовы каналы. Продолжительность жизни остеокластов может составлять от 3 до 4 недель, затем они теряют ядро апоптозом и становятся неактивными. Остеокласты связаны с моноцитарно-макрофагальными клетками и образуются из гранулоцит - макрофагальных колониеобразующих единиц. Макрофагальный колониестимулирующий фактор необходим для начала дифференциации остеокластов. Клетки предшественники остеокластов присутствуют в костном мозге, селезенке, и в небольшом количестве в циркуляции. Во время развития предшественники остеокластов вероятно мигрируют в кость из экстрамедуллярных участков гемопоэза.
Ремоделирование кости.
В костной ткани в течение всей жизни человека происходят взаимосвязанные процессы разрушения и созидания, объединяемые термином ремоделирование костной ткани. Цикл ремоделирования кости начинается с активации, опосредованной клетками остеобластного происхождения (рисунок 15). Активация может включать остеоциты, "обкладочные клетки" (отдыхающие остеобласты на поверхности кости), и преостеобласты в костном мозге. Точно ответственные клетки остеобластного происхождения не были полностью определены. Эти клетки подвергаются изменениям формы и секретируют коллагеназу и другие ферменты, которые лизируют белки на поверхности кости; они также выделяют фактор, который назван остеокласт дифференцирующим фактором (ОДФ). Последующий цикл ремоделирования состоит из трех фаз: резорбция, реверсия и формирование (рисунок 4).
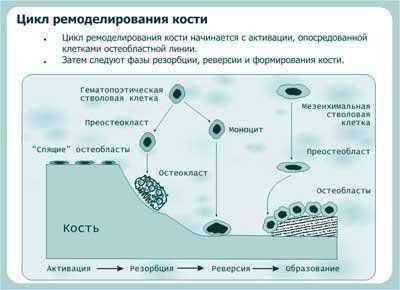
Рисунок 4. Схема ремоделирования кости. Адаптировано из Raisz L.G., 1999.
Резорбция кости.
Резорбция костной ткани связана с активностью остеокластов, которые являются фагоцитами для кости. Энзимы из остеокластов растворяют органический матрикс, а кислоты растворяют костные соли. Остеокласты регулируются ПТГ; увеличение ПТГ вызывает увеличение количества и активности остеокластов, и таким образом, увеличение костной резорбции; снижение ПТГ производит обратный эффект. Постоянный обмен костных солей обеспечивает ремоделирование кости для поддержания прочности ее на протяжении жизни. Остеокластическая резорбция per se может начинаться с миграции частично дифференцированных мононуклеарных преостеобластов к поверхности кости, которые затем сливаются с образованием крупных многоядерных остеокластов, которые требуются для резорбции кости. Остеокласты удаляют минералы и матрикс до ограниченной глубины на трабекулярной поверхности или в пределах кортикальной кости; в результате пластинки остеона разрушаются и на его месте образуется полость. Пока неясно, что останавливает этот процесс, но вероятно могут вовлекаться высокие местные концентрации кальция или веществ, высвобождаемых из матрикса.
Реверсия кости.
После завершения остеокластической резорбции имеется фаза реверсии, во время которой мононуклеарные клетки (МК), возможно моноцитарно/макрофагального происхождения, появляются на поверхности кости. Эти клетки готовят поверхность для новых остеобластов, чтобы начать образование кости ( остеогенез ). Слой богатого гликопротеидами вещества откладывается на резорбированной поверхности, так называемая "цементирующая линия", к которой могут приклеиваться новые остеобласты. Остеопонтин может быть ключевым белком в этом процессе. Клетки на месте реверсирования могут также обеспечивать сигналы для дифференциации и миграции остеобластов.
Образование кости.
Фаза формирования продолжается до полного замещения резорбированной кости и пока полностью не сформируется новая костная структурная единица. Когда эта фаза завершена, поверхность покрывается сглаженными выравнивающими клетками, и имеется длительный период отдыха с небольшой клеточной деятельностью на поверхности кости, пока новый цикл ремоделирования не начинается. Основные этапы образования кости представлены ниже:
Шаги кальцификации кости.
- Остеокласты секретируют молекулы коллагена и основного вещества.
- Молекулы коллагена образуют коллагеновые волокна, называемые остеоидом.
- Остеобласты секретируют энзим - щелочную фосфатазу (ЩФ), которая увеличивает локальную концентрацию фосфата, активирует коллагеновые волокна, вызывая отложение солей фосфата кальция.
- Соли фосфата кальция преципитируют на коллагеновых волокнах и окончательно становятся кристаллами гидроксиапатита.
Стадии цикла моделирования имеют различную продолжительность. Резорбция вероятно продолжается приблизительно две недели. Фаза реверсии может длиться до четырех или пяти недель, в то время как фаза формирования может продолжаться в течение четырех месяцев до тех пор пока новая структурная единица полностью не сформируется.
Регуляция функции костных клеток.
В норме процессы отложения и резорбции солей находятся в равновесии, и костная масса остается постоянной. Обычно процессы ремоделирования оккупируют 10-15 % поверхности кости. ПТГ является одним из важнейших факторов, влияющих на количество участков ремоделирования и может увеличивать оборот кости в 7-10 раз, увеличивая поверхность ремоделирования до 100 % всей поверхности кости.
Существует как системная, так и местная регуляция функции костной клетки. Главные системные регуляторы - кальций регулирующие гормоны, ПТГ и кальцитриол; в меньшей степени кальцитонин. Другие системные гормоны также оказывают влияние на скелет, особенно соматотропин, глюкокортикоиды, гормоны щитовидной железы и половые гормоны. Более того, некоторые факторы, такие как ИПФР, имеют, и системные и местные эффекты, а другие имеют главным образом или исключительно местные эффекты, особенно простагландины, ТФР-БЕТА, отдельные морфогенные белки, и цитокины.
Паратгормон (ПТГ) - наиболее важный регулятор гомеостаза кальция. Он поддерживает сывороточную концентрацию кальция, стимулируя резорбцию кости остеокластами, увеличивая почечную канальцевую реабсорбцию кальция, и увеличивая почечную продукцию кальцитриола. ПТГ также стимулирует экспрессию генов и увеличивает производство нескольких местных факторов, включая ИЛ-6, ИФР-1 и ИФР-связывающегоглобулина, IGF-BP-5, и простагландинов.
Кальцитриол - увеличивает кишечную абсорбцию кальция и фосфатов, таким образом поддерживая минерализацию кости. В высоких концентрациях, при условиях дефицита кальция и фосфора, он также стимулирует резорбцию кости, таким образом помогая поддерживать поставку этих ионов к другим тканям. Кальцитриол стимулирует остеокластогенез в культурах клеток, но животные, испытывающие недостаток витамина Д, имеют относительно нормальный рост костей и ремоделирование во время своего развития.
Кальцитонин - ингибирует остеокласты и поэтому резорбцию костей в фармакологических дозах. Однако, его физиологическая роль минимальна. Его эффекты являются преходящими, вероятно из-за сниженной регуляции рецепторов. В результате, он только кратковременно эффективен для коррекции гиперкальцемии из-за чрезмерной резорбции кости.
Соматотропин и ИФР - Системы Ст/ИФР-1 и ИФР-2 важны для роста скелета, особенно роста конечной пластинки хряща и эндохондрального остеогенеза . Действия ИФР определяются в частности наличием различных IGF-BP: IGF-BP-3 - главная детерминанта сывороточных концентраций ИФР, в то время как IGF-BP-5 может облегчать, а IGF-BP-4 может ингибировать локальные действия ИФР.
Глюкокортикоиды - имеют и стимулирующие, и подавляющие эффекты на клетки кости. Они важны для дифференцировки остеобластов, и они сенсибилизируют костные клетки к регуляторам ремоделирования кости, включая ИФР-1 и ПТГ. Ингибиция остеогенеза - главная причина индуцированного глюкокортикоидами остеопороза. Гормоны щитовидной железы - стимулируют и резорбцию, и формирование кости.
Таким образом, оборот кости увеличивается при гипертиреозе и могут происходить потери кости.
Половые гормоны - оказывают глубокое влияние на кость. Эстрогены влияют на развитие скелета как у мужчин, так и у женщин. В позднем пубертатном периоде эстрогены уменьшают оборот кости, ингибируя резорбцию кости; они необходимы для эпифизарного закрытия у юношей и девушек. Таким образом, мужчины с генетической потерей эстрогеновых рецепторов или фермента ароматазы, который преобразует андрогены в эстрогены, имеют задержку развития кости и остеопороз, и запаздывание эпифизарного закрытия. Многие местные факторы также находятся под влиянием эстрогенов, включая цитокины и простагландины. Андрогены могут стимулировать остеогенез как прямо, так и посредством их влияния на примыкающие мышечные ткани.
Цитокины - Как описано выше, цитокины, продуцируемые костными клетками и прилегающими гематопоэтическими и сосудистыми клетками, имеют множественные регулирующие эффекты на скелет. Многие из этих факторов вовлечены в потери кости, связанные с овариэктомией у грызунов. Регулирование может происходить в результате изменяющегося производства агонистов и изменений рецепторов или связывающих белков (антагонисты рецептора) для этих факторов.
Другие - Множество других факторов играет важную роль в метаболизме кости:
- Простагландины, лейкотриены и окись азота могут быть важны в быстрых ответах клеток кости на воспаление и механические силы. Простагландины имеют бифазные эффекты на резорбцию и образование кости, но доминирующими эффектами in vivo является стимуляция. Образование простагландинов может увеличиваться под влиянием нагрузки и воспалительных цитокинов. Окись азота может ингибировать функцию остеокластов, в то время как лейкотриены стимулируют резорбцию кости.
- ТФР-бета и семейство костных морфогенных белков, состоящее, по крайней мере, из десяти белков, которые продуцируются множеством различных клеток, и которые оказывают множественное влияние на рост и развитие. ТФР-бета может регулироваться эстрадиолом и может замедлять резорбцию кости и стимулировать остеогенез. Костные морфогенный белок - 2 и другие члены этого семейства увеличивают дифференциацию остеобластов и остеогенез, когда вводятся подкожно или внутримышечно.
Факторы роста фибробластов - другое семейство белков, вовлеченных в развитие скелета. Мутации рецепторов для этих факторов приводят к патологическим скелетным фенотипам, таким как ахондроплазия. В костной ткани образуются другие факторы роста, такие как эндотелиальный фактор роста, который может играть роль в ремоделировании кости.
Лашутин С.В., 27.05.01 г.
остеокласты - это... Что такое остеокласты?
Остеокласты — и остеобласты на трабекуле нижней челюсти коровьего эмбриона Остеокласты гигантские многоядерные клетки позвоночных животных, появляющиеся в местах рассасывания костных структур.[1] Функция их заключается в удалении продуктов распада кости и… … Википедия
ОСТЕОКЛАСТЫ — (от остео... и греч. klao ломаю, разбиваю), костедробители, обычно многоядерные крупные клетки, разрушающие (резорбирующие) костную ткань и обызвествлённый хрящ с помощью выделяющихся из них гидролитич. ферментов, сконцентрированных в… … Биологический энциклопедический словарь
Остеокласты — (от остео... (См. Ocтeo...) и греч, kláō ломаю, разбиваю) клетки, разрушающие костную ткань при её перестройках у позвоночных животных и человека. Содержат от трёх до нескольких десятков ядер и очень много лизосом (См. Лизосомы),… … Большая советская энциклопедия
Остеокласты — см. Кости … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
остеокласты — остеокл асты, ов, ед. ч. л аст, а … Русский орфографический словарь
остеокласты — мн., Р. остеокла/стов; ед. остеокла/ст (2 м) … Орфографический словарь русского языка
Остеокласт — Остеокласты и остеобласты на трабекуле нижней челюсти коровьего эмбриона Остеокласты гигантские многоядерные клетки позвоночных животных, появляющиеся в местах рассасывания костных структур.[1] Диаметр остеоклас … Википедия
Кость — I Кость (os) орган опорно двигательного аппарата, построенный преимущественно из костной ткани. Совокупность К., связанных (прерывно или непрерывно) соединительной тканью, хрящом или костной тканью, образует Скелет. Общее количество К. скелета… … Медицинская энциклопедия
КОСТЬ — плотная соединительная ткань, свойственная только позвоночным. Кость обеспечивает структурную опору организма, благодаря ей тело сохраняет свою общую форму и размеры. Местоположение некоторых костей таково, что они служат защитой для мягких… … Энциклопедия Кольера
Кость — У этого термина существуют и другие значения, см. Кость (значения). У этого термина существуют и другие значения, см. Кости (значения). Кость, как орган живого организма, сос … Википедия
Остеобласт - это... Что такое Остеобласт?
Остеобласты — молодые остеобразующие клетки кости (Диаметр 15-20 мкм), которые синтезируют межклеточное вещество — матрикс. По мере накопления межклеточного вещества, остеобласты замуровываются в нём и становятся остеоцитами. Остеобласты богаты элементами зернистой эндоплазматической сети, рибосомами, имеют хорошо развитый комплекс Гольджи. Их многочисленные отростки контактируют между собой и с отростками остеоцитов. Вспомогательной функцией остеобластов является участие в процессе отложения солей кальция в межклеточном веществе (кальцификации матрикса) из-за высокого содержания щелочной фосфатазы, что свидетельствует о высокой синтетической активности остеобластов. При этом происходит образование пещер (лакун), в которых они и залегают, превращаясь в остеоциты.
| Опорно-двигательная система, соединительная ткань: костная и хрящевая | |
|---|---|
| Хрящи | |
| Хрящевой рост | надхрящница, костная мозоль, эпифизарная пластинка |
| Клетки | хондробласт, хондроцит |
| Типы хрящевой ткани | гиалиновая, эластическая, волокнистая |
| Кости | |
| Оссификация | эндесмальная, эндохондральная |
| Клетки | остеобласт, остеоцит, остеокласт |
| Типы костной ткани | губчатая, компактная |
| Отделы | субхондральная кость, эпифиз, метафиз, диафиз |
| Структура | остеон, гаверсовы каналы, фолькмановские каналы, эндост, надкостница, костный мозг, пневматизация |
| Форма | длинные, короткие, плоские, сесамовидные, смешанные |