Люминофор что это такое
Люминофор — Википедия
Люминофо́р (от лат. lumen — свет и др.-греч. φορός — несущий) — вещество, способное преобразовывать поглощаемую им энергию в световое излучение (люминесцировать).
 Часы с тритиевым люминофором
Часы с тритиевым люминофором По химической природе люминофоры разделяются на неорганические (фосфо́ры), большинство из которых относится к кристаллофосфо́рам, и органические (органолюминофоры). Свечение неорганических люминофоров (кристаллофосфоров) обусловлено в большинстве случаев присутствием посторонних катионов, содержащихся в малых количествах (от 0,0001 % до 2 %).
Такие примеси (активаторы) обычно являются ионами переходных металлов, например, люминесценция сульфида цинка активируется примесью ионов меди.
Люминесценция — нетепловое свечение вещества, происходящее после поглощения им энергии возбуждения. Впервые люминесценция была описана в XVIII веке.
Один из видов люминесценции, хемилюминесценция (свечение в результате химической реакции), наблюдался впервые в 1669 году Хеннигом Брандом, открывшим фосфор.[1]
До ХХ века теоретические представления о сущности хемилюминесценции, сходились на том, что часть выделяющейся при химической реакции энергии не превращается в теплоту; атомы реагирующих веществ переходят при этом в возбужденное состояние, проявляющееся в свечении.
В ХХ веке Каутский и Цохер в работе над ненасыщенными соединениями кремния обнаружили, что при действии света на них происходит очень яркое явление хеми-, катодо- и фотолюминесценции (фосфоресценции и флюоресценции). Ученые обнаружили, что при охлаждении происходит усиление люминесценции, что навело их на мысль о том, что источником хемилюминесценции могут быть те же объекты, которые вызывают флюоресценцию, то есть атомы вещества, которые не принимают непосредственного участия в химической реакции, а получающие энергию для свечения от прореагировавших частиц.
В 20-х годах ХХ века по инициативе С. И. Вавилова начались исследования, направленные на создание люминесцентных ламп, новых для того времени источников света. В то же время О. В. Лосевым была обнаружена электролюминесценция, впоследствии, использующаяся в производстве светодиодов.
С начала 90-х годов помимо традиционных явлений люминесценции (газового разряда, фотолюминесценции, инжекционной и полевой электролюминесценции, низко- и высоковольтовой катодолюминесценции) началось исследование катодолюминесценции в среднем диапазоне энергий электронного пучка. [2]
В настоящее время явление люминесценции активно используется в создании люминесцентных ламп и светодиодов, в люминофорных экранах для медицинского оборудования, в цветных экранах телевизоров и других электронных приборов, в дизайне, а также в системе безопасности и эвакуации.
С каждым годом технологии производства люминесцирующих веществ совершенствуются, что помогает создавать люминофоры с улучшенными световыми качествами.
Список веществ, способных создавать свечение под тем или иным воздействием достаточно обширен, и поэтому существует несколько видов классификаций данных соединений.[2] Классификация по методу возбуждения является наиболее удобной, поэтому во многих книгах о люминофорах используют именно её.
| Способ возбуждения люминесценции | Вид люминофоров |
|---|---|
| УФ излучением | Фотолюминофор |
| Пучком электронов | Катодолюминофор |
| Электрическим полем | Электролюминофор |
| α-, β- излучением радиоактивных волн | Радиолюминофоры |
| Рентгеновским или γ- излучением | Рентгенолюминофор |
| Вид люминесценции | Вид поглощаемой энергии |
|---|---|
| Фотолюминесценция | Электромагнитное излучение (УФ, видимое) |
| Рентгенолюминесценция | Электромагнитное излучение (рентгеновское) |
| Катодолюминесценция | Кинетическая энергия электронов |
| Электролюминесценция | Энергия электрического поля |
| Радиолюминесценция | Энергия α-, β-, γ- лучей, ионов |
| Хемилюминесценция | Энергия химической реакции |
| Биолюминесценция | Энергия биохимической реакции |
| Триболюминесценция | Механическая энергия трения |
| Термолюминесценция | Тепловая энергия |
| Характер | Люминофор |
|---|---|
| Внутрицентровой | Используется непроводящий люминофор с, или люминофор с дискретными центрами |
| Рекомбинационный | Используется фотопроводящий люминофор |
Важная характеристика люминофоров — спектры поглощения, отражающие зависимость величины поглощаемой энергии от длины волны падающего на люминофор света. Спектр излучения люминофора зависит от химической природы активатора и основы люминофора, их взаимодействия, а в случае люминофоров с несколькими активаторами и от взаимодействия активаторов между собой. Спектры излучения могут зависеть от интенсивности и длины волны возбуждающего света, а также от температуры.[3]
Зависимость спектров излучения от длины волны возбуждающего света может быть хорошо прослежена на характеристических люминофорах (Ca, Mg)3(PO4)2·Sn и (Ca, Zn)3(PO4)2·Sn. Их спектры излучения состоят из широких полос, расположенных в красной и зелёной областях спектра.[3]
Количество веществ, которые можно использовать для синтеза люминофоров достаточно велико, однако на практике используются следующие классы соединений: халькогениды и фосфаты металлов второй группы, силикаты, оксиды, вольфраматы, соединения редкоземельных элементов.
Технология изготовления люминофоров относится к высокотемпературному тонкому неорганическому синтезу. Люминофоры используют в виде поликристаллических порошков, реже в виде монокристаллов и тонких плёнок. Синтез люминофоров производят при 900—1200ºС.
Для получения люминофора с заданными свойствами необходимо строго соблюдать состав шихты и условия прокаливания, не допускать попадания случайных примесей, обеспечить тщательную сушку люминофора. Также необходимо соблюдать чистоту материалов на всех этапах синтеза.[2]
- Халькогениды элементов второй группы
Почти все халькогениды представляют собой фотополупроводниковые соединения с электронным типом проводимости (примесь имеет валентность большую, чем чистый полупроводник, появляются свободные электроны). Для теллурида цинка характерна дырочная проводимость (примесь имеет меньшую валентность, чем чистый полупроводник, появляются разрывы связей — дырки), а для теллурида кадмия дырочная и электронная.[2]
Халькогенидам цинка и кадмия присуща «самоактивированная» люминесценция, обусловленная собственными дефектами, либо ассоциатами с примесью галогенов или трехвалентных катионов. Также для халькогенидов характерна люминесценция, связанная с введением активирующих примесей.[3]
Люминофоры на основе сульфидов щелочноземельных металлов синтезируют прокаливанием смесей соответствующих карбонатов с активатором, серой, плавнями и восстановителем. Основная реакция, которая протекает при синтезе люминофоров может быть представлена уравнением :
- 4MeCO3+4S→3MeS+MeSO4+4CO2{\displaystyle {\mathsf {4MeCO_{3}+4S\rightarrow 3MeS+MeSO_{4}+4CO_{2}}}}
Сульфид цинка можно получить сероводородным методом по реакции:
- ZnSO4+h3S→ZnS+h3SO4{\displaystyle {\mathsf {ZnSO_{4}+H_{2}S\rightarrow ZnS+H_{2}SO_{4}}}}
Также следует упомянуть тиосульфатный метод получения сульфидов, основанный на реакциях, которые могут быть упрощенно записаны как:
- MeSO4+2Na2S2O3→MeS2O3+Na2SO4{\displaystyle {\mathsf {MeSO_{4}+2Na_{2}S_{2}O_{3}\rightarrow MeS_{2}O_{3}+Na_{2}SO_{4}}}}
- MeS2O3+h3O→MeS+h3SO4{\displaystyle {\mathsf {MeS_{2}O_{3}+H_{2}O\rightarrow MeS+H_{2}SO_{4}}}}
При синтезе халькогенидных люминофоров исходные сульфиды получают заранее. Синтез происходит в 3 этапа:
Приготовление шихты
На технических весах взвешивают нужное количество халькогенида (порошок) и добавляют к нему заданное количество растворов плавня (вещество, добавляемое к руде при её плавке для увеличения плавкости имеющихся в ней примесей и образования шлаков) и активатора (вещество, интенсифицирующее физические и химические процессы). Шихта (исходная смесь, использующаяся в пирометаллургических или иных высокотемпературных процессах) тщательно перемешивается.
Сушка
Шихта высушивается при 100—120ºС в сушильном шкафу до пыления в течение времени зависящего от количества шихты (примерно 0,5-1 час).
Прокаливание
Прокаливание проводится в муфельной печи при заданной температуре 900—1200ºС в течение времени, зависящего от количества шихты (около 0,5-1 часа). На стадии прокаливания шихты происходит процесс образования люминофора, то есть кристаллизация основного вещества, диффузия введенных в шихту активирующих примесей, гетерогенные химические и межкристаллические реакции образования в решетке различных дефектов.[2]
Селениды цинка и кадмия получают из сульфидов по реакции, которая в упрощенном виде выглядит так:[3]
- MeS+h3SeO3→MeSe+SO2+h3O{\displaystyle {\mathsf {MeS+H_{2}SeO_{3}\rightarrow MeSe+SO_{2}+H_{2}O}}}
- Фосфаты металлов второй группы
Среди фосфатов наиболее широкое применение в производстве люминофоров находит фосфат кальция, который используется для люминесцентных источников света. Разнообразие люминесцентных свойств фосфатов заключается в наличии у них большого количества полиморфных модификаций, относительной рыхлостью решеток, которые создают благоприятные условия для формирования люминофора. Также для синтеза люминофоров используют фосфат цинка, который является основой для синтеза катодолюминофоров с красным излучением. Двойные фосфаты кальция и магния используют для синтеза люминофоров, которые впоследствии применяют в лампах ультрафиолетового излучения.[2]
Фосфаты в твердой фазе можно синтезировать по-разному. Например, фосфаты кальция и стронция получаются по одному из следующих вариантов:[3]
- Me2P2O7+MeCO3→1000∘CMe(PO4)2+CO2{\displaystyle {\mathsf {Me_{2}P_{2}O_{7}+MeCO_{3}{\xrightarrow {1000^{\circ }C}}Me(PO_{4})_{2}+CO_{2}}}}
- 3MeCO3+2(Nh5)2HPO4→1100∘CMe3(PO4)2+4Nh4+3CO2+2h3O{\displaystyle {\mathsf {3MeCO_{3}+2(NH_{4})_{2}HPO_{4}{\xrightarrow {1100^{\circ }C}}Me_{3}(PO_{4})_{2}+4NH_{3}+3CO_{2}+2H_{2}O}}}
- Силикаты
Самое большое распространение в производстве силикатных люминофоров получил силикат цинка, использующийся как основа для катодолюминофоров с зелёным свечением. Благодаря высокой химической и термической стойкости, стабильности к электронной бомбардировке, силикатные люминофоры используются в электронно-лучевых приборах.[2] Силикат цинка готовят прокаливанием смеси ZnO c SiO2 при 1200º.[3]
Силикат кальция, активированный Pb и Mn может быть получен путем прокаливания смеси карбонатов или окислов соответствующих металлов с SiO2. Для этого требуется температура в 1150º и атмосфера водяного пара, который оказывает минерализующее действие (превращение в твердое состояние).[3]
- Оксидные системы
Многие металлы II, III, IV групп периодической системы обладают люминесценцией при фото-, катодном и рентгеновском возбуждении, но практическое применение имеют немногие. Наиболее широкое применение получил оксид цинка, использующийся в качестве катодолюминофора с очень коротким послесвечением, а также в низковольтных катодолюминофорных индикаторах.
В качестве основы для синтеза катодолюминофоров всё более широкое применение имеют оксиды и оксисульфиды редкоземельных элементов (РЗЭ). Их существенным преимуществом является большая насыщенность цвета и высокая стабильность к электронной бомбардировке.[2]
- Вольфраматы
Вольфраматные люминофоры в основном относятся к самоактиворованным, то есть люминесцируют без введения активатора.[2]
- Соединения редкоземельных элементов
Соединения РЗЭ успешно играют роль, как основного вещества, так и активатора. Такие соединения используются в синтезе катодолюминофоров, работающих при высоких плотностях тока электронного возбуждения.[2]
Использование люминофоров в технике позволяет нам экономить на электроэнергии, так как развитие полупроводниковой техники стимулировало работы по созданию инжекционных электролюминесцентных источников освещения. Возможность смотреть телевизор предоставляется благодаря люминофорам, ведь для экранов приемных телевизионных трубок практикуется использование смесей люминофоров для получения высокой яркости свечения близкого к белому. Применение люминофоров в медицинской отрасли позволяет делать рентген и флюорографию. А также способность люминофоров светиться без электрического источника энергии нашла применение в системах эвакуации и пожарной безопасности.
Неорганические люминофоры применяют в люминесцентных лампах, электронно-лучевых трубках, для изготовления рентгеновских экранов, служат индикаторами радиации и др.
Органические люминофоры (иногда их называют «люмогены») применяют для изготовления ярких флуоресцентных красок для окрашивания текстиля, пластмасс, украшений, в типографских красках, для пигментации полимерной глины, красок для обоев, пигментов для татуировки, косметики, люминесцирующих материалов, используют для выявления трещин в деталях, чувствительном люминесцентном анализе в химии, биологии, медицине и криминалистике.
- ↑ Волков В.А., Вонский Е.В., Кузнецова Г.И. Выдающиеся химики мира. — Москва, 1991.
- ↑ 1 2 3 4 5 6 7 8 9 10 Гурецкая З.И. Технология люминофоров и люминесцентных экранов. — Москва, 2005.
- ↑ 1 2 3 4 5 6 7 Казанкин О.Ф., Марковский Л.Я., Миронов И.А., Пекерман Ф.М., Пето-шина Л.Н. Неорганические люминофоры. — Ленинград, 1975.
- Жиров Н. Ф. Люминофоры. — М.: Гос. изд-во оборонной пром-ти, 1940. — 480 с.
Что такое люминофор и его виды
Мы не будем утомлять Вас, сложными научными и техническими терминами, а постараемся доступно и понятно рассказать Вам,что такое Люминофор! Итак..
Что такое Люминофор?
Люминофор- это светонакопительный пигмент или светящийся в темноте порошок, абсолютно безопасный и нетоксичный аналог фосфора! Производится на основе редкоземельных металлов и способен преобразовать поглощенную световую энергию в эффект послесвечения в темноте без дополнительных источников энергии! Заряжается от любого источника света - солнечного, ультрафиолетового, обычной лампы накаливания и светит до 14 часов! К сожалению, в мире не бывает люминофоров светящих дольше,их еще просто не придумали! И если в интернете Вы видели или Вам предложили купить люминофор светящий 18- 24 ,а то и все 48 часов, то будте уверенны - Вас наглым образом обманывают!)) Да, некоторые недобросовестные фирмы- однодневки,у которых стоит задача продать вам " здесь и сейчас" могут обещать "свечение в течении 24 или 48 часов", но они умалчивают о том, что свечение на 48-м часу можно зафиксировать только специальными приборами. Как факт - свечение есть, но вот ВИДИМОГО ЧЕЛОВЕЧЕСКОМУ ГЛАЗУ - НЕТ!
Какие Люминофоры бывают?
Есть много видов люминофоров, но наиболее распостраненные это на основе алюминатов редкоземельных металлов, (которые мы производим и продаем!),а так же сульфатов и сульфидов цинка! Люминофоры на основе дешевых сульфатов и сульфидов цинка имеют неяркое свечение, хотя бывают такие, что ПЕРВЫЕ 5 МИНУТ! светят достаточно ярко,но светят очень недолго! Начинают разрушаться уже в первые месяцы от воздействия металлов и света солнца. Поэтому люминофоры бывают дешевыми и дорогими, как впрочем и любой товар! Очень жаль, что люди приобретая недорогой и некачественный люминофор, потом разочаровываются в продукте, перестают развивать светящийся бизнес, и переубедить их потом в обратном очень сложно! Вы конечно же, можете подумать, что мы расхваливаем свой товар с целью, чтобы Вы покупали только у нас! Мы торговая организация производящая люминофоры и конечно заинтересованы в том, чтобы продавать, но еще больше нам бы хотелось сберечь ваши деньги и не подорвать доверия к продукту в целом! Обладая всей достоверной информацией, Вы сможете принимать решение о возможном БИЗНЕС- партнерстве на постоянной основе!
Чем отличаются Люминофоры?
1). Длительностью свечения 2). Яркостью первоначального свечения 3). Яркостью свечения после определенного времени (например 1 часа) 4).Составом (редкоземельные металлы, ZnS, алюминаты и т.п.) 5). Водостойкостью 6). Крупностью частиц 7). Однородностью частиц (зависит от качества оборудования и технологии) 8). Цветом свечения.
Вы хотите получить люминофор, подходящий именно для Вашей конкретной задачи? Посмотрите наш "КАТАЛОГ ТОВАРОВ". Учтите, что помимо этих люминофоров, мы производим люминофоры "под заказ" - необходимой Вам крупности, с необходимыми параметрами (если таковые возможны в принципе,) с обработкой для использования в водных средах или без нее! Что Вам могут предложить те, у кого ассортимент люминофоров ограничивается 3-4 видами фотолюминофоров? Возможно, один из этих видов ,подойдет для решения Вашей задачи. Тогда Вам просто повезло! В остальных же случаях, Вам просто будут усиленно продавать то, что ЕСТЬ, а не то, что НАДО!
Фотолюминофоры — Википедия
Фотолюминофо́ры — группа люминофоров, которые люминесцируют под воздействием света. Сохраняют накопленную световую энергию и отдают её как непосредственно в момент возбуждения, так и в виде послесвечения какой-либо продолжительности после прекращения возбуждения в видимом, ультрафиолетовом и/или инфракрасном спектре. К этому классу люминофоров относится очень широкий список соединений. Различают как природные фотолюминофоры, так и искусственно синтезированные.
К природным фотолюминофорам относят категорию минералов, которые во время своего образования могли претерпеть особые изменения, связанные с температурным режимом, наличием определённого состава примесей, давления, минералы, обладающие флуоресценцией (свечением, заметным в темноте), к примеру, такие как вюрцит — ZnS, некоторые смесевые разновидности барита и кальцита. Эта категория минералов является очень редкой и ценной.
К искусственным фотолюминофорам относят синтезированные соединения, обладающие улучшенными характеристиками послесвечения и свойствами, намного превосходящими природные минералы. К ним относятся сульфиды и селениды элементов второй группы таблицы Менделеева, в частности селенид магния MgSe, кальция CaSe, стронция SrSe, бария BaSe, цинка ZnSe. К фотолюминофорам относят также нитриды бора и некоторые окисные соединения металлов второй группы. К искусственным фотолюминофорам так же относят и сравнительно недавно синтезированные составы. Эти соединения являются формульными и структурными аналогами природного минерала шпинели — MgAl2O4.
В подавляющем большинстве, фотолюминофоры — это искусственно синтезированные соединения со значительно улучшенными характеристиками и с оптимальным составом. Представляют собой основу — какое либо соединение, с добавкой активатора какого либо металла и плавнями, хлоридами, сульфатами, боратами, фторидами и фосфатами элементов первой и второй групп таблицы Менделеева. По химическому составу условно выделяются несколько групп:
- Сульфиды. В первую группу входят сульфид цинка, а также смесь сульфидов цинка и кадмия в разной стехиометрии, активированные медью, свинцом, марганцем, висмутом. В группу входят также сульфиды кальция магния, стронция и бария, с активаторами висмута, меди, цинка, сурьмы, свинца, марганца, серебра, олова, и РЗЭ — самария и церия, которые готовятся из сульфидов или карбонатов с добавкой серы, восстановителей и плавней. В большинстве своем обладают длительной и интенсивной флуоресценцией, термолюминесценцией, и некоторые триболюминесценцией.
- Селениды. Сюда относятся селениды цинка, кадмия, кальция, стронция и бария, активированные медью, цинком, сурьмой свинцом, висмутом, серебром. Все готовятся из готовых селенидов или исходных соединений с добавкой плавней. Обладают сравнительно интенсивной флуоресценцией и термолюминесценцией.
- Сульфиды-селениды. Группа включает в себя смеси соединений первой и второй группы.
- Окисные фотолюминофоры. Это окиси магния, кальция, стронция и карбонат бария, прокаленные с плавнями и активаторами из второй группы. Готовятся без добавления серы. Обладают хорошей люминесценцией, также флуоресценцией и сильной термолюминесценцией.
- [Неорганические бораты]. Разной стехиометрии бораты цинка и кадмия с марганцевым активатором. Имеют хорошую флюоресценцию оранжево-красных тонов.
- Прочие кристаллофосфоры, в частности нитриды бора и их смеси.
Все группы фотолюминофоров различаются не только по химическому составу, но и по физическим свойствам, присущим разным составам, а также способами синтеза, обработки и применения таких составов на практике.
При возбуждении люминофора светом энергия может быть поглощена как на уровне активатора, так и на уровне основного вещества.
Поглощение световой энергии на уровне активатора сопровождается переходом электрона с основного уровня активатора на возбужденный, а излучение света происходит при обратном перемещении электрона. Возникает явление флуоресценции. Электроны, вырванные возбуждающим светом, могут перейти в зону проводимости и локализоваться на ловушках. Освободиться из ловушек электроны могут лишь в том случае, если им сообщить необходимое количество энергии. При этом электроны либо переходят в зону активатора и рекомбинируют с центрами свечения, либо будут повторно захвачены ловушками. В этом случае возникает явление фосфоресценции (длительное свечение)[1].
При поглощении света на уровне основного вещества электроны переходят в зону проводимости из валентной зоны. В валентной зоне образуются дырки, которые переходят и могут локализоваться в зоне активатора. Помимо образования электронно-дырочных пар, в решетке могут образоваться экситоны (квазичастицы, представляющие собой электронное возбуждение в кристалле), которые способны ионизировать центры свечения. Возникает явление люминесценции[1].
Эвакуационный знак с люминофорным покрытиемСфера применения фотолюминофоров достаточно обширна. Узкополосные люминофоры, активированные редкоземельными элементами, используются при создании люминесцентных ламп. Перспективность применения этих люминофоров обусловлена возможностью одновременного повышения световой отдачи и индекса цветопередачи люминесцентных ламп. Это помогает добиться существенной экономии расходов на освещение[2].
Фотолюминофоры нашли применение в эвакуационных системах, поскольку в отличие от электрических эвакуационных систем не потребляют энергию, не требуют затрат на эксплуатацию и позволяют реализовать протяжённую разметку в труднодоступных местах.
Для оптимизации поисковых работ предлагается использовать альтернативные источники световой энергии – люминофоры длительного послесвечения (ЛДП). Люминофоры можно наносить на одежду в виде вставок. Также люминофоры можно использовать для маркировки пострадавших.
ЛДП используются в изделиях в двух основных типах:
- Лакокрасочный вариант характеризуется высокой яркостью свечения, экономичным расходом люминофора, высокой долговечностью, устойчивостью к внешним воздействиям. Наносится на изделие поверх отражающего слоя (белый грунт) и покрывается сверху защитным слоем. К недостаткам относится низкая гидролитическая устойчивость, особенно при воздействии солнечного облучения.
- Монолитный вариант представляет собой изделие из материала с малым оптическим поглощением.
Алюминат стронция в виде тонкослойного источника света используется в эвакуационных знаках и знаках пожарной безопасности[3]
- ↑ 1 2 Казанкин О. Ф., Марковский Л. Я., Миронов И. А., Пекерман Ф. М., Петошина Л .Н. Неорганические люминофоры. — Ленинград, 1975.
- ↑ Быстров Ю. А., Литвак И. И., Персианов Г. М. Электронные приборы для отображения информации. — Москва, 1985.
- ↑ Абовян М. Ю., Микаэль Ю., Большухин В. А., Буйновский А. С. Функциональные оксидные материалы на основе редких и редкоземельных металлов. — Томск, 2005.
Как сделать люминофор своими руками — DRIVE2

1
Люминофор — особое вещество, способность которого в преобразовании поглощаемой энергии в обычный свет.
Другими словами, люминофор способен излучать свет под действием ультрафиолета, электромагнитного поля или другого типа излучения.
Так, применяемые в неоновых трубках люминофоры, горят под действием ультрафиолетовых лучей, а также излучения ртутных паров.
В переводе с греческого люминофор — «несущий свет».
Виды люминофора
Сегодня можно выделить несколько видов люминофоров.
По химическим свойствам их можно поделить на два вида.
Неорганические (кристаллофосфоры).
Такой вид люминофоров нашел применение в люминесцентных лапах, ЭЛТ (электрических лучевых трубках), экранах для рентгена и так далее.
Кроме этого, неорганический люминофор является индикатором радиации.
Свечение «неорганики» обусловлено наличием большого числа катионов, которые содержатся в минимальном объеме (до 0,001%). По своей сути неорганические люминофоры — катионы металлов.
Органические люминофоры.
Используются в производстве флуоресцентных красок, люминесцирующих материалов и так далее.
Часто их применяют для проведения люминесцентного анализа в различных отраслях, к примеру, в медицине, биологии, химии, криминалистике, автомобилестроении и так далее.

2
Делим люминофоры по характеристикам
По своим характеристикам люминофоры бывают:
фотолюминфоры;
катодолюминофоры;
рентгенолюминофоры;
электролюминофоры;
радиолюминофоры.
Наибольшей популярностью пользуется фотолюминофор — вид люминофора, который обладает определенными свойствами и может длительно сохранять энергию.
После ее накопления люминофор может длительно отдавать ее в форме излучения — ультрафиолетового, инфракрасного или того, который виден глазу человека.
Именно люминофор типа фотолюминофор можно сделать своими руками.
Сфера применения
Люминофор активно применяется в самых различных сферах — в полиграфических и текстильных изделиях, в декорациях и шоу-технике, для создания спасительных устройств, для наружной рекламы, при изготовлении спецодежды и так далее.
Широкое применение люминофор получил и в аэрографии — художественной росписи автомобиля.

3
Люминофор можно наносить на кузов автомобиля или колпаки. Достаточно небольшого слоя, чтобы в темное время суток автомобиль преображался и излучал яркий свет в местах обработки.
Почти во всех перечисленных случаях применяется фотолюминофор — наиболее безопасный, простой в применении и красивый вид люминофора.
Состав
Стандартный люминофор состоит из двух основных компонентов — борной кислоты и концентрата хвои.

4

5
Обе составляющие найти несложно. К примеру, хвойный концентрат продается во многих аптеках. При этом будьте внимательны. Нужен не экстракт, а именно концентрат. Для приготовления люминофора это очень важно.
Процесс приготовления и меры безопасности
Теперь рассмотрим, как приготовить люминофор самостоятельно. Действуйте в приведенной ниже последовательности.
1. Насыпайте (наливайте) концентрат хвои в заранее подготовленную посуду.

6
2.Добавляйте небольшое количество воды. Итог таких манипуляций — получение раствора тартразина.

7
Сам тартразин представляет собой синтетический краситель, имеющий желтый цвет. Данный элемент относится к категории пищевых добавок (известен под названием Е 102/запрещен в ряде европейских стран).

8
Как правило, тартразин добавляется в йогурты, пюре, мороженое, супы и прочую еду. Минус таких красителей — опасность для астматиков. Чрезмерное попадание Е 102 в организм может привести к зуду, нарушению зрения, мигрени и так далее.
3. Сыпьте немного борной кислоты в ложку.

9
4. Смачивайте полученную смесь с помощью тартразина.

10
5. Перемешивайте состав до тех пор, пока не получится однородная масса.

11
6. Грейте смесь до момента, пока она не превратиться в густой состав зеленоватого оттенка. Чтобы лучше прогреть смесь, возникшие сверху пузырьки необходимо проткнуть.

12
7. После этого охлаждайте смесь и вливайте небольшое количество тартразина. После этого снова прогревайте состав.

13
В итоге вы должны получить желтое однородное вещество.

14
8. Подействуйте на получившийся состав фотовспышкой (яркие световые лучи необходимы для «активации»).
Вот и все. Впоследствии готовый люминофор можно перетереть в порошок, добавить в жидкость (как правило, обычную воду).
Кроме этого, люминофор можно изготовить, смешав родамин и борную кислоту (в последнем случае качество продукта будет много хуже).
При выполнении работ будьте осторожны, работайте в перчатках и по возможности защитите глаза с помощью очков.
Что касается готового люминофора, то он считается совершенно безопасным для здоровья.источник www.avto-pulss.ru
Люминофоры. Немного теории и практики / Habr
 Как и обещал, продолжение темы «светящихся в темноте».
Как и обещал, продолжение темы «светящихся в темноте». Примерно полгода назад мы искали для себя дополнительный бизнес с элементами развлечения. Остановились на светящихся в темноте красках и предметах. Настоящий вау-эффект был, когда мы своими руками покрасили буквы из пенопласта. Писал об этом в июле.
Наша компания на данный момент имеет весьма большой опыт работы с поставщиками и ассортимент того, что мы сами опробовали как качественное.
Для начала нужно сказать, что разновидностей люминофоров весьма достаточно:
- Фотолюминофоры
- Электролюминофоры
- Катодолюминофоры
- Рентгенолюминофоры
- Радиолюминофоры
Я изучаю фотолюминофоры. Даю ссылку на единственного известного мне производителя люминофоров в России, если кому-либо интересно «посмотреть всех».
Немного теории
Сам люминофор представляет собой порошок с размером частиц 15 – 50 мкм. Яркость свечения зависит от размера частиц. Но большого размера частицы не везде можно использовать. Скажем, если речь идет о применении в шелкографии или покраске краскопультом, то размер частиц тут должен укладываться в нужные интервалы, чтобы не забить сетку или сопла покрасочного оборудования.
Самые распространенные цвета свечения – желто-зеленый и бирюзовый. Это люминофоры с длительным послесвечением (до 12 часов).
В его основе – алюминат стронция (SrAl2O4):Eu,Dy,Y. Он имеет отличную устойчивость к воде и различным излучениям, поэтому срок его хранения практически не ограничен. Еще одно его преимущество – он безопасен для здоровья людей и животных. Мне попадались даже составы для нанесения на кожу – гипоаллергенные. Кроме того, тот люминофор, которым мы занимаемся, «заряжается» также и в УФ-лучах, что расширяет области его применения.
При дневном свете цвет порошка близок к белому (чуть зеленоватый). Для изменения цвета используются специальные флуоресцентные пигменты (светятся при УФ-излучении). Добавляются в пропорции 3%-5% от массы люминофора. Цвета, которые видел – синий, белый, желтый, зеленый, красный. Цвет пигментов достаточно «ядовитый». Если с ними переборщить, можно совсем убить эффект послесвечения.
Кстати, по-настоящему ярко светиться окрашенная поверхность будет в течение первых 60-80 минут, после чего свечение будет неравномерно угасать: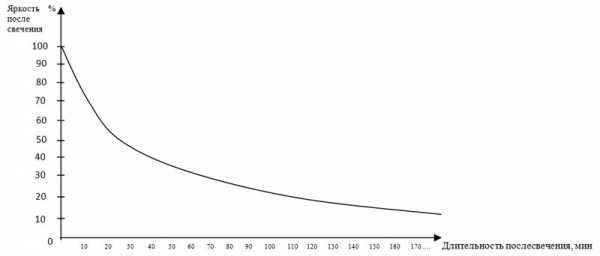
Самые распространенные картинки по технологии нанесения люминофора выглядят примерно так: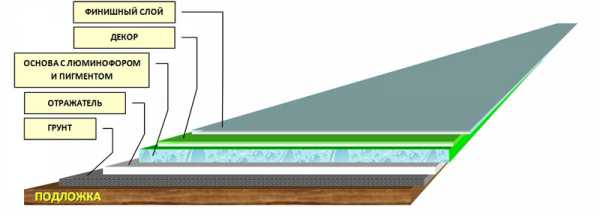
На этой картинке объяснить стоит только значение основы, отражателя, финишного слоя.
- Люминофор не растворяется и его замешивают в лак (основу) в зависимости от типа окрашиваемой поверхности. Важно, чтобы в лаке не было УФ-фильтров, иначе послесвечения не будет.
- В идеале подложка, на которую наносится готовый состав, должна быть белой. Именно белый цвет служит лучшим отражателем, в результате чего эффект послесвечения будет наилучшим.
- После окраски лаком с люминофором поверхность будет «шершавой», т.к. частицы люминофора все-таки крупные. Поэтому для глянца и ровной поверхности нужно будет дополнительное прозрачное покрытие.
Для тех, кто жаждет больше узнать о технологии использования и покраски, выложил найденный мною в публичном доступе архив.
Немного денег
Я получил несколько вопросов в личном кабинете по поводу создания своего небольшого бизнеса на люминофорах.
Позволю себе пару абзацев по этому поводу.
Ситуация неоднозначна. Я списывался примерно с 40 компаниями, которые являются поставщиками или представителями крупных оптовиков. Все очень по-разному в зависимости от выбранной ниши и конкретного города. Один товарищ, к примеру, писал, что у него упали продажи, когда наступили белые ночи.
Все наперебой пишут, что это легкий для подъема бизнеса. Нифига подобного. Люминофор – штука для многих непонятная. Все до сих пор еще вспоминают фосфор, который лет 15 уже как запрещен к свободному использованию и несомненно, вреден для здоровья.
По-настоящему заработать можно либо на услугах, связанных с применением люминофора (дизайн интерьеров, тюнинг авто), либо с продажей крупных партий краски/порошка. На перепродаже готовых изделий заработать сложно. Их хорошо держать в офисе в качестве примеров применений, чтобы можно было «пощупать».
Это связано с тем, что на большинстве сайтов поставщиков фотки такие, что приходилось заказывать все, чтобы посмотреть, как это на самом деле выглядит.
Немного картинок
Вобщем, ищите нишу и задавайте вопросы. Я отвечу всем.
ЛЮМИНОФОРЫ - это... Что такое ЛЮМИНОФОРЫ?
(от лат. lumen, род. падеж luminis - свет и греч. phoros - несущий), синтетич. в-ва, способные преобразовывать разл. виды энергии в световую - люминесцировать. По типу возбуждения подразделяются на фото-, катодо-, электро-, рентгено-, радио-, хемилюминофоры и др. (см. также Люминесценция, Хемилюминесценция).
Неорганические Л. (фосфоры). Их свечение м. б. обусловлено как св-вами в-ва основы, так и наличием примесей - активаторов, к-рые образуют в осн. в-ве центры свечения, соактиватора и сенсибилизатора. Концентрация активатора обычно составляет 10-1-10-3%. Существуют самоактивир. Л., не содержащие активаторов, напр. CaWO4. Л. обозначают ф-лой основы с указанием активатора и сенсибилизатора, часто соактиватора, напр. ZnS : Ag, Ni; в-во после знака ":" - активатор, соактиватор или сенсибилизатор. Большинство неорг. Л. имеет кристаллич. структуру и относятся к кристаллофосфорам. Требования к Л. - яркость и цвет свечения, длительность послесвечения, дисперсность, термостойкость и др. - определяются параметрами устройств, в к-рых их применяют. Л. обычно используют в виде относительно тонких поликристаллич. слоев (1-100 мкм), наносимых на внутр. пов-сть светящихся - экранов электровакуумных приборов. Состав нек-рых фото- и катодолюминофоров и области их применения представлены в таблице. Фотолюминофоры возбуждаются оптич. излучением в диапазоне от вакуумной УФ до ближней ИК области. наиб. широкое применение фотолюминофоры находят в люминесцентных лампах низкого давления. В лампах для общего освещения используют галофосфат Са -3[Са 3 (РО 4)2].Са(Сl, F)2 : Sb, Mn, в лампах высокого давления с исправленной цветопередачей - смеси на основе фосфатов и силикатов, излучающие в синей, зеленой и красной областях спектра. Свечение возбуждается резонансной линией Hg с l =253,7 нм. Световая отдача (отношение светового потока лампы к мощности) ламп с галофосфатным Л.
составляет 85 Лм/Вт, ламп со смесями - от 50 до 60 Лм/Вт. Созданы лампы "нового поколения" с Л. на основе РЗЭ (алюминаты, фосфаты и др.), сочетающие высокую светоотдачу ( ~ 95 Лм/Вт) с высоким качеством цветопередачи. Фотолюминофоры применяют для исправления цветности ламп высокого давления, ламп, излучающих в УФ области, и т. д. (см. табл.). Катодолюминофоры возбуждаются пучком электронов; используются в экранах кинескопов, в электронных микроскопах, электроннолучевых и радиолокац. установках. В кинескопах цветного изображения применяют Л. с синим (l макс 455 нм), зеленым (l макс 525 нм) и красным (l макс 612 и 620 нм) цветом свечения. Их наносят на экран кинескопа в виде точек, расположенных треугольником, или чередующихся полос. Суммарный цвет изображения получается при сложении трех цветов свечения нанесенных Л. и зависит от соотношения их яркостей. Для получения хорошей цветопередачи цвет свечения исходных Л. должен быть по возможности более насыщенным, для чего поверхность "синего" Л. пигментируют СоАl2 О 4, а "красного" - Fe2O3. 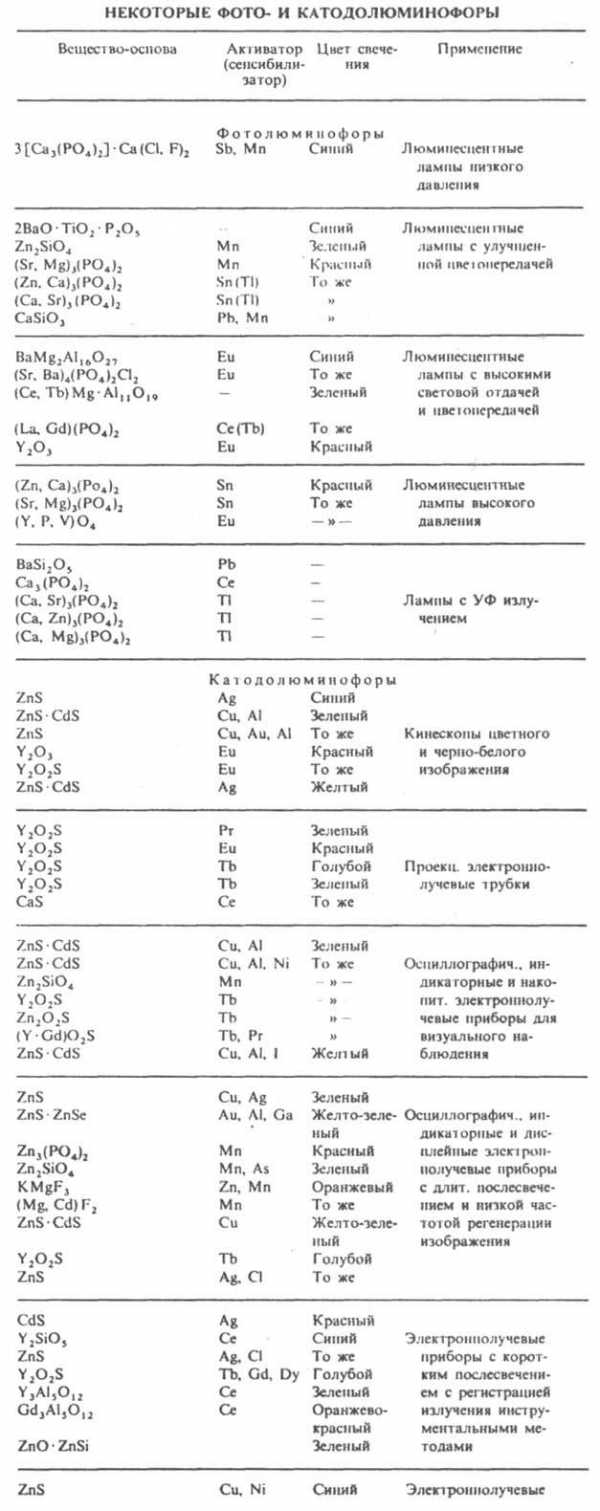
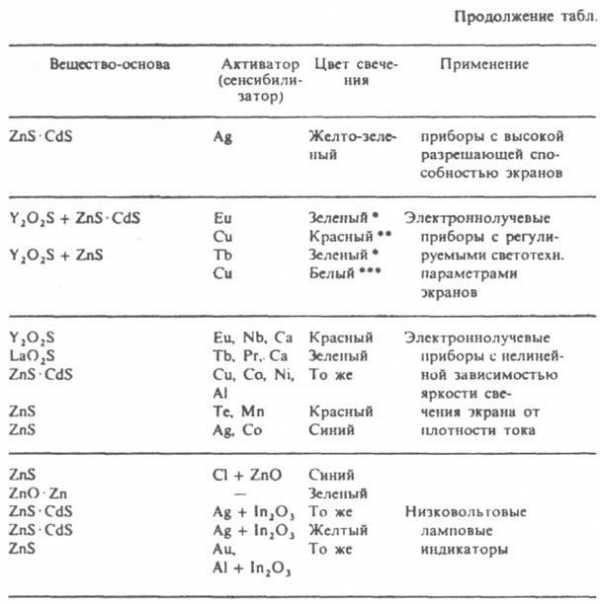
* При напряжении 6 кВ. ** При напряжении 14 кВ. *** При напряжении 12 кВ.
Покрытие кинескопов черно-белого изображения состоит из смеси Л., имеющих синий и желто-зеленый (l макс 560 нм) цвет свечения, обеспечивающих в целом белый свет свечения кинескопа. Для повышения контрастности используют пигментирование "синего" Л. красителем. Электролюминофоры возбуждаются переменным или постоянным электрич. полем. Hаиб. распространенные электролюминофоры - ZnS : Сu и Zn(Cd)S(Se) : Сu. В зависимости от введенного дополнительно к Сu соактиватора (Сl, Аl, Вr, Са или Mn) получают Л., обладающие голубым, зеленым, желтым, оранжевым и красным цветом свечения. Рентгенолюминофоры возбуждаются рентгеновскими лучами; применяются при рентгенологич. обследованиях человека и в пром. дефектоскопии. Л. CaWO4 нашел применение в мед. экранах, пром. рентгенографии с использованием малосeребряных материалов и дефектоскопии при высоких напряжениях. В разл. типах мед. рентгенологич. экранов применяют также BaSO4 : Pb; (Sr,Ba)SO4 : Eu; BaF,Cl : Eu; Ba3(PO4)2 : Eu; LaOBr : Tb,Yb; ZnS : Ag; ZnS.CdS : Ag; CsI : Tl. Радиолюминофоры возбуждаются радиоактивным излучением; применяются для дозиметрии и радиометрии. При дозиметрии обычно используют св-во нек-рых Л. высвечивать при повышении т-ры энергию, запасенную при возбуждении. Для дозиметрии g- и рентгеновского излучения применяют LiF : Mg,Ti и MgB4O7 : Dy, для быстрых нейтронов - CaS : Na, Bi, Zn; для a-радиометрии - ZnS : Ag. Среди неорг. Л. большое практич. применение находят также люминесцирующие стекла. Их получают при варке стекла, добавляя в шихту активаторы, чаще соли РЗЭ или актиноиды. Стекла обладают хорошей оптич. прозрачностью и могут применяться в качестве лазерных материалов, а также визуализаторов изображения.
Органические Л. (люминоры, органолюминофоры). Их свечение обусловлено хим. строением орг. соед. и сохраняется в разл. агрегатных состояниях. По хим. строению различают след. орг. Л.: ароматич. углеводороды или их производные (полифенильные углеводороды, углеводороды с конденсированными ароматич. ядрами или арилэтиленовой и арилацетиленовой группировками), 5- и 6-членные гетероциклы и их производные, соед. с карбонильными группами; к орг. Л. относят также комплексы металлов с орг. лигандами. Орг. фотолюминофоры применяют в качестве флуоресцентных красок, свечение к-рых вызывается УФ и коротковолновым видимым излучением. Пигменты красок представляют собой твердые р-ры орг. Л. или их смесей с красителями в разл. смолах (чаще всего в составе карбамид-и меламиноформальдегилных смол, модифицированных одно- и многоатомными спиртами или арилсульфамидами). Для получения желтого цвета используют обычно 3-метоксибензантрон, голубого - арилэтиленовые замещенные 2,5-диарилоксазолов, оранжевого - смесь 3-метоксибензантрона с родаминами С и 6Ж. Нек-рые орг. Л. применяют для окрашивания пластмасс и синтетич. волокон, оптич. отбеливания тканей, бумаги, натуральных и искусств. волокон и разл. покрытий. Так, для окрашивания сополимеров винилхлорида применяют родамин С (красный цвет), 2,2'-дигидрокси-1,1'-нафтальазин (желтый), смесь 2,2'-дигидрокси-1,1'-нафтальазина с фталоцианином меди (зеленый), производные пиримидинантрона (красно-оранжевый), для окрашивания полистирола в оранжево-красные окраски - нафтоиленбензилимидазолы и его замещенные. При оптич. отбеливании Л., поглощая свет в ближней УФ-области, флуоресцируют в фиолетовой (l макс 415-429 нм), синей (430-440 нм) или зелено-синей (441-466 нм) частях видимой области спектра. Оптич. наложение их флуоресценции и желтых лучей, отраженных отбеливаемым материалом, вызывает ощущение белизны. При оптич. отбеливании используют производные стильбена, кумарина, пиразолина, нафталимида, бензоксазола и др. Орг. Л., способные испускать свет под действием радиоактивных излучений, применяют в качестве сцинтилляторов. Существуют монокристаллич. (антрацен, тетрацен, пирен, карбазол, арилзамещенные этилена и оксазола), жидкие (полифенильные углеводороды, 2,5-диарилзамешенные оксазола) и пластмассовые орг. сцинцилляторы. Последние представляют собой твердые р-ры жидких сцинцилляторов в полимерных основах (полистироле, поливинилксилоле). Многие орг. Л. - активные среды жидкостных лазеров, напр. цианиновые, полиметиленовые и др. красители, люминесцентные индикаторы. Кроме того, орг. Л. применяют в люминесцентной дефектоскопии и аналит. химии (см. Люминесцентный анализ), а также в мол. биологии и медицине (флуоресцеин, акридин и др.) в качестве меток или зондов (см., напр., Липидные зонды). О хеминолюминофорах см. Хемилюминесценция. Лит.: Гугель Б. М., Люминофоры для электровакуумной промышленности, М.. 1967; Неорганические люминофоры, М., 1975; Карнаухов В. Н., Люминесцентный спектральный анализ клетки, М., 1978; Красовицкий Б. М., Болотин Б. М., Органические люминофоры, 2 изд., М., 1984; Тезисы докладов 5-го Всесоюзного совещания "Синтез, свойства, исследования, технология и применение люминофоров", ч. 1-2. Ставрополь. 1985. И. Ф. Голубев.
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
Люминофор - это... Что такое Люминофор?
Люминофо́р (от лат. lumen — свет и др.-греч. φορός — несущий) — вещество, способное преобразовывать поглощаемую им энергию в световое излучение (люминесцировать).
Основные сведения
По химической природе люминофоры разделяются на неорганические, большинство из которых относится к кристаллофосфорам, и органические. Свечение неорганических люминофоров (кристаллофосфоров) обусловлено в большинстве случаев присутствием посторонних катионов, содержащихся в малых количествах (от 2 % до 0,0001 %).
Такие примеси (активаторы) обычно являются ионами металлов; например, свечение сульфида цинка активируется ионом меди. Неорганические люминофоры применяют в люминесцентных лампах, электронно-лучевых трубках, для изготовления рентгеновских экранов, служат индикаторами радиации и др. Органические люминофоры (люмогены) применяют для изготовления ярких флуоресцентных красок, люминесцирующих материалов, используют в чувствительном люминесцентном анализе в химии, биологии, медицине и криминалистике.
Разновидности
Существует несколько разновидностей люминофоров. Из них стоит выделить следующие:
- Фотолюминофоры — разновидность люминофоров, которые обладают свойствами сохранения накопленной энергии при возбуждении, и её отдачи, с обладанием собственного послесвечения какой либо продолжительности после прекращения возбуждения в виде светового излучения в видимой, ультрафиолетовой или инфракрасной зоне.
- Электролюминофоры
- Катодолюминофоры
- Рентгенолюминофоры
- Радиолюминофоры
См. также
Примечания
Ссылки
Литература
- Жиров Н. Ф. Люминофоры. — М.: Гос. изд-во оборонной пром-ти, 1940. — 480 с.
Что такое люминофор
По своей сути, светящийся люминофор – это вещество, которое преобразует поглощаемую энергию в свечение. Однако видов этого вещества несколько, как и сфер применения. Расскажем, какие бывают люминофоры, как долго они могут светиться и в каких областях применяются.

Почему светится люминофор и что это такое?
Эффект свечения на различных минералах или насекомых наблюдался еще с древних времен. Позже это свечение было названо люминесценцией, а вещество, способное его воспроизводить – люминофором (от латинского слова «люмен» – «свет», и греческого «форос» – «несущий»).
Природа возникновения люминесценции стала понятна с появлением атомной физики. Итак, почему светится люминофор? Ученые выяснили, что свечение возникает при переходе атома из возбужденного в спокойное состояние, а само возбуждение вызывают различные реакции – ультрафиолетовое излучение, химические реакции и т.д. Люминофор поглощает эти виды энергии, а затем преобразует их в световую, создавая излучение света в определенном спектре цвета.
Как долго светится люминофор?
Процесс свечения люминофора зависит от многих факторов – типа вещества, размера его частиц, состава, способа применения, а также среды. Поэтому на вопрос – как долго светится люминофор – однозначно ответить нельзя. Если речь идет о веществах, используемых в лакокрасочной или полиграфической продукции, то срок свечения люминофора составит не более суток.
Каким бывает люминофор?
По химическому составу люминофор может быть органическим и неорганическим. С помощью неорганического люминофора изготавливают люминесцентные лампы, электронно-лучевые трубки, индикаторы реакции, рентгеновские аппараты. Органический люминофор используется для производства светящихся типографских красок, различных материалов с эффектом флуоресценции, а также для проведения анализов в криминалистике, медицине и биологии.
Также эти вещества делятся по способу возникновения свечения:
-
Фотолюминофоры, возникающие от УФ-излучения – это люминофор в лампах;
-
Катодолюминофоры, свечение которых вызвано работой электронов;
-
Радиолюминофоры, создающие свечение при помощи радиоактивных волн;
-
Электролюминофоры, начинающие светится от воздействия электронного поля;
-
Рентгенолюминофоры, воспроизводящие свечение от рентгеновского излучения.
Исходный цвет свечения люминофоров – зеленоватый, синий и голубой. Но их часто смешивают с другими компонентами, чтобы добиться определенного оттенка люминесценции. Так, для изготовления индукционных ламп на внутреннюю поверхность колбы наносят многокомпонентный люминофор, позволяющий получить основную триаду цветов – синий, зеленый и красный, чтобы получить свечение в чистом белом спектре.
|
|
ЛЮМИНОФОРЫ (от лат. lumen, род. падеж luminis - свет и греч. phoros - несущий), синтетич. в-ва, способные преобразовывать разл. виды энергии в световую - люминесцировать. По типу возбуждения подразделяются на фото-, катодо-, электро-, рентгено-, радио-, хемилюминофоры и др. (см. также Люминесценция, Хемилюминесценция).
Неорганические люминофоры (фосфоры). Их свечение м.б. обусловлено как св-вами в-ва основы, так и наличием примесей - активаторов, к-рые образуют в осн. в-ве центры свечения, соактиватора и сенсибилизатора. Концентрация активатора обычно составляет 10-1-10-3%. Существуют самоактивир. люминофоры, не содержащие активаторов, напр. CaWO4. Люминофоры обозначают ф-лой основы с указанием активатора и сенсибилизатора, часто соактиватора, напр. ZnS : Ag, Ni; в-во после знака ":" - активатор, соактиватор или сенсибилизатор. Большинство неорг. люминофоров имеет кристаллич. структуру и относятся к кристаллофосфорам. Требования к люминофорам - яркость и цвет свечения, длительность послесвечения, дисперсность, термостойкость и др. - определяются параметрами устройств, в к-рых их применяют. Люминофоры обычно используют в виде относительно тонких поликристаллич. слоев (1-100 мкм), наносимых на внутр. пов-сть светящихся - экранов электровакуумных приборов. Состав нек-рых фото- и катодолюминофоров и области их применения представлены в таблице. Фотолюминофоры возбуждаются оптич. излучением в диапазоне от вакуумной УФ до ближней ИК области. наиб. широкое применение фотолюминофоры находят в люминесцентных лампах низкого давления. В лампах для общего освещения используют галофосфат Са -3[Са3(РО4)2].Са(Сl, F)2 : Sb, Mn, в лампах высокого давления с исправленной цветопередачей - смеси на основе фосфатов и силикатов, излучающие в синей, зеленой и красной областях спектра. Свечение возбуждается резонансной линией Hg с l = 253,7 нм. Световая отдача (отношение светового потока лампы к мощности) ламп с галофосфатным люминофором составляет 85 Лм/Вт, ламп со смесями - от 50 до 60 Лм/Вт. Созданы лампы "нового поколения" с люминофорами на основе РЗЭ (алюминаты, фосфаты и др.), сочетающие высокую светоотдачу ( ~ 95 Лм/Вт) с высоким качеством цветопередачи. Фотолюминофоры применяют для исправления цветности ламп высокого давления, ламп, излучающих в УФ области, и т.д. (см. табл.). Катодолюминофоры возбуждаются пучком электронов; используются в экранах кинескопов, в электронных микроскопах, электроннолучевых и радиолокац. установках. В кинескопах цветного изображения применяют люминофоры с синим (lмакс 455 нм), зеленым (lмакс 525 нм) и красным (lмакс 612 и 620 нм) цветом свечения. Их наносят на экран кинескопа в виде точек, расположенных треугольником, или чередующихся полос. Суммарный цвет изображения получается при сложении трех цветов свечения нанесенных люминофоров и зависит от соотношения их яркостей. Для получения хорошей цветопередачи цвет свечения исходных люминофоров должен быть по возможности более насыщенным, для чего поверхность "синего" люминофора пигментируют СоАl2О4, а "красного" - Fe2O3. * При напряжении 6 кВ. ** При напряжении 14 кВ. *** При напряжении 12 кВ.
Покрытие кинескопов черно-белого изображения состоит из смеси люминофоров, имеющих синий и желто-зеленый (lмакс 560 нм) цвет свечения, обеспечивающих в целом белый свет свечения кинескопа. Для повышения контрастности используют пигментирование "синего" люминофора красителем.
Электролюминофоры возбуждаются переменным или постоянным электрич. полем. Hаиб. распространенные электролюминофоры - ZnS : Сu и Zn(Cd)S(Se) : Сu. В зависимости от введенного дополнительно к Сu соактиватора (Сl, Аl, Вr, Са или Mn) получают люминофоры, обладающие голубым, зеленым, желтым, оранжевым и красным цветом свечения.
Рентгенолюминофоры возбуждаются рентгеновскими лучами; применяются при рентгенологич. обследованиях человека и в пром. дефектоскопии. Люминофоры CaWO4 нашел применение в мед. экранах, пром. рентгенографии с использованием малосeребряных материалов и дефектоскопии при высоких напряжениях. В разл. типах мед. рентгенологич. экранов применяют также BaSO4 : Pb; (Sr,Ba)SO4 : Eu; BaF,Cl : Eu; Ba3(PO4)2 : Eu; LaOBr : Tb,Yb; ZnS : Ag; ZnS.CdS : Ag; CsI : Tl.
Радиолюминофоры возбуждаются радиоактивным излучением; применяются для дозиметрии и радиометрии. При дозиметрии обычно используют св-во нек-рых люминофоров высвечивать при повышении т-ры энергию, запасенную при возбуждении. Для дозиметрии g- и рентгеновского излучения применяют LiF : Mg,Ti и MgB4O7 : Dy, для быстрых нейтронов - CaS : Na, Bi, Zn; для a-радиометрии - ZnS : Ag.
Среди неорг. люминофоров большое практич. применение находят также люминесцирующие стекла. Их получают при варке стекла, добавляя в шихту активаторы, чаще соли РЗЭ или актиноиды. Стекла обладают хорошей оптич. прозрачностью и могут применяться в качестве лазерных материалов, а также визуализаторов изображения.
Страница «ЛЮМИНОФОРЫ» подготовлена по материалам химической энциклопедии. |

|
Люминофор. Обзор материала и вариантов применения
Это давно изученный и в то же время очень интересный материал, способный "впитывать" свет и отдавать его в темноте. Рассмотрим его особен... Просмотров: 41074
Люминофор — это специальное вещество, которое способно преобразовывать поглощаемую энергию в световое излучение. Все люминофоры разделяются на неорганические (большинство из которых относится к кристалл фосфорам) и органические. Люминофоры так же отличаются яркостью свечения, величиной частиц, водостойкостью.Люминофоры способны накапливать на свету, а затем отдавать полученную энергию (в результате свечения) в темноте суток. На длительность свечения влияют только первые 40 минут зарядки, после чего люминофор перестает поглощать энергию.
Люминофор позволяет воплотить в жизнь самые интересные решения в области декоративной подсветки. Купить люминофор можно у нас в интернет магазине.
На данный момент люминофор существует в виде:
порошка, для добавления к различным лакокрасочным материалам, в том числе на водной основе.
Крошки, которая сама по себе может применяться для декоративной подсветки, без смешивания.
флуоресцентной краски, представляющую собой краску с добавления люминофора.
флуоресцентных пигментов, смол, окрашенных флуоресцентными красителями. Тип смолы определяет свойства пигмента: для окраски различных пластмасс, лакокрасочных материалов на основе воды или сильных растворителей.

светящейся пленки, обладающей способностью накапливать свет

Фотобумаги, обладающей флуоресцентными свойствами.

флуоресцентных маркеров, для использования в наружной рекламе в сочетании с Led досками.
Положительной особенностью люминофора является возможность использования его без дополнительного оборудования и дополнительных технологий. Рассмотрим возможные варианты применения люминофора.
Смешать люминофор с лаком
Для начала, нужно придать люминофору нудный нам цвет. Для этого смешиваем его с флуоресцентным пигментом. Важно помнить. Что чем больше пигмента. Тем слабее будет свечение. Рекомендуется использовать соотношение 1/10 по отношению к люминофору
При смешивании люминофора с различными разновидностями лака в пропорции 1 часть лака 0,3 части порошка люминофора, мы получаем лак, обладающий люминесцентными свойствами.
1. Покраска металлической поверхности.
Если мы хотим покрасить металлическую поверхность, то мы берем акриловый лак и вводим в него люминофор в соотношении часть лака 0,3 части порошка люминофора.
Теперь, когда краска готова, ее можно наносить на поверхность. Для нанесения краски на металлическую поверхность можно использовать кисточку или валик, но, так как люминофор не растворяется в лаке, а находиться в взвешанном состоянии, для его равномерного нанесения лучше использовать краскопульт или аэрограф.
Подсветка дисков.
Для начала необходимо демонтировать диски и очистить их от грязи. Сделать это лучше водой и обезжиривателем.

После этого, покрываем диски грунтовкой, после чего можно приступить к покраске. Используя аэрограф наносим изготовленную нами смесь на диски в несколько слоев.
Последний этап – дополнительная лакировка дисков. Слой лака позволит в некоторой степени защитить слой люминофора.

После этого достаточно несколько минут подержать диски рядом с источником света для 8-12 часов свечения
По такой же схеме можно подсветить колпаки.
Подсветка велосипеда.
Технология та же. Используя кисточку, либо аэрограф, наносим смесь на предварительно очищенную поверхность велосипеда в несколько слоев.

Подсветка фар люминофором
Интересным вариантом является частичная покраска отражателя фары. Например по периметру! В этом случае после того как вы приехали домой или остановились около магазина и выключили фары, люминофорный рисунок в фаре будет ярко светиться.
Лестницы, ступеньки и т.д.
Подсветка более обширных металлических поверхностей требует большего количества материала, но технология нанесения покраски идентична.
1. Покраска деревянной поверхности.
Основное отличие покраски деревянной поверхности от металлической в подготовке поверхности к покраске. В первом случае, мы используем грунтовку и шкурку для создания ровной поверхности. Здесь все немного сложнее.
Метод предварительной подготовки поверхности к покраске зависит от состояния самой деревянной поверхности и состояния старого покрытия.
Самый простой вариант предварительной подготовки — это очистка щеткой или промывка водой и щеткой. Если лакокрасочная пленка отслаивается, старое покрытие следует удалить полностью. Процесс осуществляется механически (скобление, шлифовка, обработка щеткой или пескоструйной очисткой), или химически (средства для удаления краски). Если Вы столкнулись со сложным случаем, лучше полностью заменить поверхность. Кроме очистки, перед покраской важно оценить состояние самих конструкций.
Часто обрабатываемые поверхности требуют шлифовки.
Окраска не вызывает затруднений, если старое покрытие находится в хорошем состоянии. При этом достаточно удалить пыль и грязь щеткой до перекраски. Однако, если старое покрытие облезает, необходимо полностью его удалить.
Промывка окрашиваемой деревянной поверхности щелочным раствором поможет очистить окрашиваемую поверхность от жиров, масел и прочих загрязнений.
Старую краску с деревянной поверхности можно снимать, нагревая ее феном.
В качестве лака для смешивания применяются органические, либо алкидные мебельные лаки.
В последующем осуществляем покраску с помощью кисточки, либо краскопульта.
Для крупных поверхностей, возможно применение кисточки, с помощью которой, мы покрываем поверхность лаком в несколько слоев.
Для более сложных поверхностей. Лучше использовать краскопульт.

После окраски, желательно дополнительно покрыть поверхность дерева лаком для лучшей защиты.
2. Покраска бетона и стен
Обрабатываемая поверхность должна быть чистой и сухой. Если покраска проводится со свежими, сверхплотными бетонными поверхностями, то рекомендуется удалить цементное молочко путем травления разбавленной соляной кислотой.
Далее следует нанесения грунта. В большинстве случаев грунт не нужен. Поверхности бетона, или кирпича пронизаны большим количеством пор, благодаря чему, обеспечивается высокая адгезия. Если же поверхность имеет высокую плотность, наличие грунта рекомендуется.
В качестве лака для смешивания можно использовать:
полиуретановый лак для бетонных поверхностей
лак на основе перхлорвинилового сополимера и акриловых смол для бетонных поверхностей
эпоксидный лак для бетона.
На высохший грунт (если использовался), используя кисточку, валик, либо краскопульт, наносим смесь в несколько слоев.
Таким образом, можно красить как любые бетонные или кирпичные конструкции.

Так и любые другие с похожей плотностью

3. Покраска стекла.
Особенность этого вида покраски заключается в том, что дополнительно рекомендуется использовать камеру термической сушки с температурой 70 градусов по Цельсию.
Для начала, необходимо подготовить поверхность. Используя хлопчатобумажную ткань, смоченную в спирте, обезжириваем окрашиваемую поверхность.
После этого прогреваем изделие 5 минут в термокамере.
В качестве лака, для смешивания используем двухкомпонентный лак, на акриловой основе. Глянцевый. Термоустойчивый.
После смешивания лака и нагревания изделия, используя краскопульт, наносим смесь на поверхность изделия в несколько слоев.
После этого вновь помещаем изделие в камеру термической сушки на 5 минут
4. Нанесение краски на кожу.
Для театрализованных представлений, и просто для красоты можно наносить люминофор на поверхность кожи.
Для этого нужно смешать его с кремом для тела.
Смыть можно теплой водой с мылом.
Это совершенно безопасно. Но нужно исключить попадание материала в глаза и желудок.
Использование флуоресцентных маркеров.
Флуоресцентные маркеры производятся на водной основе. Благодаря своей структуре, их можно наносить на стекло, пластик, металл и множество других поверхностей. Они оставляют след, который светится в ультрафиолете.
С их помощью можно делать надписи на информационных и рекламных досках, различные объявления на вывесках, табличках и меню, оформлять декорации, наносить маркировку.
Днем такие надписи имеют яркий насыщенный оттенок. Ночью, взаимодействуя с ультрафиолетовой подсветкой, достигается эффект свечения.
Как правило, для использования маркеров для создания красочных вывесок используются Led доски, которые представляют собой доски со светодиодной подсветкой, на поверхность которых можно наносить информацию с помощью флуоресцентных маркеров.
Возможно также использование маркеров без Led досок, при наличии ультрафиолетового освещения.

Радиолюминесценция — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 30 мая 2018; проверки требуют 13 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 30 мая 2018; проверки требуют 13 правок. Брелок с радиолюминесцентной (в данном случае — тритиевой) подсветкойРадиолюминесценция — люминесценция вещества, вызванная воздействием ионизирующего излучения.
В технике для активации светосоставов постоянного действия (СПД) широко использовались радионуклиды, излучающие гамма-лучи, альфа- или бета-частицы. Например, торий или радий-226. Люминофор СПД изготавливался на базе сульфида цинка. Такие СПД способны излучать свет очень долго — в течение нескольких лет или даже десятилетий.
Первые радиолюминесцентные краски начали применяться с 1910-х годов. Долгое время (приблизительно с 1920-х до 1950-х годов) именно радий-226 (а со второй половины XX века — и прометий-147) применялись в радиолюминесцентных красках для покрытия элементов циферблатов часов, приборов и другого оборудования. В специальных источниках относительно большой яркости часто использовался криптон-85. В настоящее время в радиолюминесцентных источниках света для приборов применяется[1]тритий, радиоактивный изотоп водорода. Он излучает бета-частицы (электроны) очень низкой энергии (в среднем 5.5 кЭв, максимум 18.6[2]), которые полностью поглощаются защитным стеклом источника света или просто воздухом (длина пробега таких частиц в воздухе измеряется миллиметрами, в стекле — микронами[3])
Радиолюминесцентные источники света нашли применение в тех областях техники, где требуется высокая автономность источника света — морские бакены, ампулированные источники для ночного обозначения габаритов несущих винтов вертолетов, источники света для работы во взрывоопасных средах (в шахтах и на рудниках), различного рода аварийные и автономные осветители, указатели, источники света для циферблатов приборов, подсветки оружейных прицелов и так далее.
Существуют международные стандарты ISO 3157 и NIHS 97-10, определяющие минимальное количество люминесцентного вещества, необходимого для того, чтобы различать в темноте нанесённые этим веществом символы, либо выполнять на его основе постоянную подсветку циферблатов часов и других приборов.
Интенсивность свечения, кроме качества состава, также зависит от площади поверхности покрытия и толщины слоя. Со временем радионуклид расходуется, превращаясь в стабильные изотопы. Люминофор также деградирует, источник света теряет яркость. Тем не менее даже потерявшие яркость СПД являются источником повышенной радиобиологической опасности и подлежат специальной утилизации.