Адсорбция что это такое
Адсорбция — Википедия
Адсорбция (лат. ad — на, при, в; sorbeo — поглощаю) — самопроизвольный процесс увеличения концентрации растворённого вещества у поверхности раздела двух фаз (твёрдая фаза — жидкость, конденсированная фаза — газ) вследствие нескомпенсированности сил межмолекулярного взаимодействия на разделе фаз[1]. Адсорбция является частным случаем сорбции, процесс, обратный адсорбции — десорбция[2].
Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтив, поглощённое — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твёрдым веществом (в случае газа и жидкости) или жидкостью (в случае газа) — адсорбентом. При этом, как и в общем случае адсорбции, происходит концентрирование примеси на границе раздела адсорбент-жидкость либо адсорбент-газ. Процесс, обратный адсорбции, то есть перенос вещества с поверхности раздела фаз в объём фазы, называется десорбция. Если скорости адсорбции и десорбции равны, то говорят об установлении адсорбционного равновесия. В состоянии равновесия количество адсорбированных молекул остается постоянным сколько угодно долго, если неизменны внешние условия (давление, температура и состав системы)[3].
На поверхности раздела двух фаз помимо адсорбции, обусловленной в основном физическими взаимодействиями (главным образом это Ван-дер-Ваальсовы силы), может идти химическая реакция. Этот процесс называется хемосорбцией. Чёткое разделение на адсорбцию и хемосорбцию не всегда возможно. Одним из основных параметров, по которым различаются эти явления, является тепловой эффект: так, тепловой эффект физической адсорбции обычно близок к теплоте сжижения адсорбата, тепловой эффект хемосорбции значительно выше. Кроме того, в отличие от адсорбции, хемосорбция обычно является необратимой и локализованной, то есть происходит на определённых местах — активных центрах. Примером промежуточных вариантов, сочетающих черты и адсорбции, и хемосорбции, является взаимодействие кислорода на металлах и водорода на никеле: при низких температурах они адсорбируются по законам физической адсорбции, но при повышении температуры начинает протекать хемосорбция.
В предыдущем разделе говорилось о случае протекания гетерогенной реакции на поверхности — хемосорбции. Однако бывают случаи гетерогенных реакций по всему объёму, а не только на поверхности: это обычная гетерогенная реакция. Поглощение по всему объёму может проходить и под воздействием физических сил. Этот случай называется абсорбцией.
| Виды взаимодействий | Взаимодействия только на поверхности | Взаимодействия по всему объёму |
|---|---|---|
| Физические | Адсорбция | Абсорбция |
| Химические | Хемосорбция | Гетерогенная реакция |
| Модели физической адсорбции | |
| Образование монослоя | Энергетическая диаграмма |
| Рис. 1: a) адсорбент, b) адсорбат, c) адсорбтив (газовая фаза или раствор) | Рис. 2: a) адсорбент, b) адсорбат, c) газовая фаза, d - расстояние, E - энергия, Eb - энергия адсорбции, (1) десорбция, (2) адсорбция |
| Поликонденсация | Избирательная адсорбция |
| Рис. 3: a) адсорбент, b) адсорбат, c) конденсат, d) адсорбтив (газовая фаза или раствор) | Рис. 4: a) адсорбент, b) адсорбат, c) адсорбтивы (газовая фаза или раствор): показана преимущественная адсорбция частиц голубого цвета |
Причиной адсорбции являются неспецифические (то есть не зависящие от природы вещества) Ван-дер-Ваальсовы силы. Адсорбция, осложнённая химическим взаимодействием между адсорбентом и адсорбатом, является особым случаем. Явления такого рода называют хемосорбцией и химической адсорбцией. «Обычную» адсорбцию в случае, когда требуется подчеркнуть природу сил взаимодействия, называют физической адсорбцией.
Физическая адсорбция является обратимым процессом, условие равновесия определяется равными скоростями адсорбции молекул адсорбтива P на вакантных местах поверхности адсорбента S* и десорбции — освобождения адсорбата из связанного состояния S − P:
- S∗+P↔S−P{\displaystyle S^{*}+P\leftrightarrow S-P};
уравнение равновесия в таком случае:
- K=[S−P][S∗][P]{\displaystyle K={\frac {[S-P]}{[S^{*}][P]}}},
где K — константа равновесия, [S − P] и [S*] — доли поверхности адсорбента, занятые и незанятые адсорбатом, а [P] — концентрация адсорбтива.
Количественно процесс физической мономолекулярной адсорбции в случае, когда межмолекулярным взаимодействием адсорбата можно пренебречь, описывается уравнением Ленгмюра:
- θ=α⋅P1+α⋅P{\displaystyle \theta ={\frac {\alpha \cdot P}{1+\alpha \cdot P}}},
где θ{\displaystyle \theta } — доля площади поверхности адсорбента, занятая адсорбатом, α{\displaystyle \alpha } — адсорбционный коэффициент Ленгмюра, а P — концентрация адсорбтива.
Поскольку [S−P]=θ{\displaystyle [S-P]=\theta } и, соответственно, [S∗]=1−θ{\displaystyle [S^{*}]=1-\theta }, уравнение адсорбционного равновесия может быть записано следующим образом:
- K=θ(1−θ)P{\displaystyle K={\frac {\theta }{(1-\theta )P}}}
Уравнение Ленгмюра является одной из форм уравнения изотермы адсорбции. Под уравнением изотермы адсорбции (чаще применяют сокращённый термин — изотерма адсорбции) понимают зависимость равновесной величины адсорбции от концентрации адсорбтива a=f(С) при постоянной температуре (T=const). Концентрация адсорбтива для случая адсорбции из жидкости выражается, как правило, в мольных либо массовых долях. Часто, особенно в случае адсорбции из растворов, пользуются относительной величиной: С/Сs, где С — концентрация, Сs — предельная концентрация (концентрация насыщения) адсорбтива при данной температуре. В случае адсорбции из газовой фазы концентрация может быть выражена в единицах абсолютного давления, либо, что особенно типично для адсорбции паров, в относительных единицах: P/Ps, где P — давление пара, Ps — давление насыщенных паров этого вещества. Саму величину адсорбции можно выразить также в единицах концентрации (отношение числа молекул адсорбата к общему числу молекул на границе раздела фаз). Для адсорбции на твёрдых адсорбентах, особенно при рассмотрении практических задач, используют отношение массы или количества поглощённого вещества к массе адсорбента, например мг/г или ммоль/г.
Адсорбция — всеобщее и повсеместное явление, имеющее место всегда и везде, где есть поверхность раздела между фазами. Наибольшее практическое значение имеет адсорбция поверхностно-активных веществ и адсорбция примесей из газа либо жидкости специальными высокоэффективными адсорбентами. В качестве адсорбентов могут выступать разнообразные материалы с высокой удельной поверхностью: пористый углерод (наиболее распространённая форма — активированный уголь), силикагели, цеолиты, а также некоторые другие группы природных минералов и синтетических веществ.
Адсорбция (особенно хемосорбция) имеет также важное значение в гетерогенном катализе. Пример адсорбционных установок приведён на странице азотные установки.
Установка для проведения адсорбции называется адсорбер.
- Фролов Ю. Г. Курс коллоидной химии. Поверхностные явления и дисперсные системы. - М.: Химия, 1989. - 464 с.
- Кельцев Н. В. Основы адсорбционной техники. - М.: Химия, 1984. - 592 с.
- Грег С., Синг К. Адсорбция, удельная поверхность, пористость. - М.: Мир, 1984. - 310 с.*
- Адамсон А. Физическая химия поверхностей. – М.: Мир. 1979. – 568 с.
- Оура К., Лифшиц В. Г., Саранин А. А. и др. Введение в физику поверхности / Под ред. В. И. Сергиенко. — М.: Наука, 2006. — 490 с.
- Карнаухов А.П. Адсорбция. Текстура дисперсных и пористых материалов. — Новосибирск: Наука. 1999. — 470 с.
- Химическая энциклопедия. Т. 1. — М.: Советская энциклопедия, 1990. — 623 с.
- Полторак О.М. Термодинамика в физической химии. — М.: Высшая школа, 1991. — 319 с.
- Берёзкин В.И. Введение в физическую адсорбцию и технологию углеродных адсорбентов. — СПб.: Виктория плюс, 2013. — 409 с. — ISBN 978-5-91673-128-6
адсорбция - это... Что такое адсорбция?
АДСО́РБЦИЯ -и; ж. [от лат. ad- - к и sorbere - поглощать, всасывать]. Поглощение вещества из газа или раствора поверхностным слоем жидкого или твёрдого адсорбента (используется в химии, технике и т.п. для разделения и очистки веществ).
◁ Адсорбцио́нный, -ая, -ое.
АДСО́РБЦИЯ (от лат. ad — на, при и sorbeo — поглощаю), поглощение какого-либо вещества (адсорбата) из газообразной среды или раствора поверхностным слоем жидкости или твердого тела (адсорбентом). Различают два вида адсорбции: физическую и химическую (хемосорбцию (см. ХЕМОСОРБЦИЯ)). Менее прочная физическая адсорбция не сопровождается существенными изменениями молекул адсорбата. Она обусловлена силами межмолекулярного взаимодействия (см. МЕЖМОЛЕКУЛЯРНОЕ ВЗАИМОДЕЙСТВИЕ), которые связывают молекулы в жидкостях и некоторых кристаллах и проявляются в поведении сильно сжатых газов. Существенное отличие физической адсорбции — ее обратимость. При хемосорбции молекулы адсорбата и адсорбента образуют химические соединения. Часто адсорбция обусловлена и физическими и химическими силами, поэтому не существует четкой границы между физической адсорбцией и хемосорбцией.Явление адсорбции связано с тем, что силы межмолекулярного взаимодействия на грАݐؑƐՠраздела фаз нескомпенсированы, и, следовательно, пограничный слой обладает избытком энергии – свободной поверхностной энергией (см. ПОВЕРХНОСТНАЯ ЭНЕРГИЯ). В результате притяжения поверхностью раздела фаз находящихся вблизи нее молекул адсорбата свободная поверхностная энергия уменьшается, т.е. процессы адсорбции энергетически выгодны. Адсорбция всегда является экзотермическим процессом, т. е. протекает с выделением теплоты адсорбции Hs.
Значения энтальпии (см. ЭНТАЛЬПИЯ) физической адсорбции достаточно велики (порядка 10 ккал/моль) из-за слабых атомных взаимодействий. Физическая адсорбция легко обратима, поэтому, например, в случае адсорбции газа, достаточно легко может осуществиться замена адсорбированного слоя газа другим газом. Это явление называется обменной адсорбцией.
Процесс адсорбции заканчивается установлением адсорбционного равновесия между адсорбентом и адсорбатом. Условием равновесия является равенство химических потенциалов обеих фаз. С ростом температуры или давления адсорбата в объеме увеличивается частота попаданий молекул адсорбата на поверхность адсорбента; пропорционально ей возрастает скорость адсорбции и увеличивается равновесное количество адсорбированных молекул. Кривые зависимости равновесной адсорбции от температуры или давления адсорбата называются, соответственно, изобарой и изотермой адсорбции.
Адсорбированные молекулы могут перемещаться по поверхности, совершая при этом колебательные движения, то приближаясь к поверхности, то удаляясь от нее. Время, в течение которого молекула находится на поверхности, называется временем адсорбции. С ростом температуры время адсорбции уменьшается: чем выше температура, тем интенсивнее колебательное движение, и больше вероятность того, что в процессе таких колебаний связь молекулы с поверхностью будет разорвана и молекула покинет поверхность. Процесс, при котором адсорбированные молекулы покидают поверхность, называется десорбция (см. ДЕСОРБЦИЯ). Скоростью адсорбции (десорбции) называется отношение количества молекул, адсорбирующихся (десорбирующихся) за единицу времени, к единице поверхности или массы адсорбента. Если скорости адсорбции и десорбции равны друг другу, устанавливается адсорбционное равновесие. В состоянии равновесия количество адсорбированных молекул остается постоянным сколь угодно долго, если неизменны внешние условия (давление, температура и др.).
В случае контакта поверхности кристалла и жидкого раствора из жидкости на поверхность твердого тела переходят молекулы, находящиеся в растворе. Между их концентрациями в растворе и на поверхности адсорбента устанавливается равновесие. Вещества, адсорбируемые из раствора, называются поверхностно-активными веществами (см. ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА (ПАВ)) (ПАВ). Высокая адсорбируемость ПАВов связана с сильным снижением поверхностного натяжения (см. ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ) раствора на данной поверхности по сравнению с поверхностным натяжением чистого растворителя на этой же поверхности. Инактивные вещества повышают поверхностное натяжение и ухудшают адсорбцию.
Если теплота адсорбции сравнима с поверхностной энергией адсорбента, то в процессе адсорбции может существенно меняться кристаллическая структура поверхности твердого тела, причем при физической адсорбции перестройке подвергаются в основном поверхности молекулярных кристаллов, а в случае хемосорбции изменения поверхностной структуры наблюдаются даже для металлов и ионных кристаллов. Адсорбированные на поверхности пленки сильно изменяют свойства поверхности, а в ряде случаев затрагивают и более толстые приповерхностные слои.
Адсорбция играет важную роль во многих природных процессах, таких, как обогащение почв и образование вторичных рудных месторождений. Именно благодаря адсорбции осуществляется первая стадия поглощения различных веществ из окружающей среды клетками и тканями биологических систем, функционирование биологических мембран, первые этапы взаимодействия ферментов с субстратом, защитные реакции против токсичных веществ. Многие адсорбенты (активный уголь, каолин (см. КАОЛИН), иониты (см. ИОНИТЫ) и др.) служат противоядиями, поглощая и удаляя из организма вредные вещества. Адсорбенты обычно имеют большую удельную поверхность — до нескольких сотен м2/г. В промышленности адсорбцию осуществляют в специальных аппаратах — адсорберах; применяют для осушки газов, очистки органических жидкостей и воды, улавливания ценных или вредных отходов производства.
АДСОРБЦИЯ • Большая российская энциклопедия
АДСО́РБЦИЯ (от лат. ad – на и sorbeo – поглощать), поглощение вещества из газовой фазы или жидкого раствора поверхностным слоем твёрдого тела или жидкости. Явление А. вызывается наличием адсорбц. cилового поля, создаваемого за счёт нескомпенсированности межмолекулярных cил в поверхностном слое. Вещество, создающее такое поле, называется адсорбентом, вещество, молекулы которого могут адсорбироваться, – адсорбтивом, уже адсорбиров. вещество – адсорбатом. Процесс, обратный А., – десорбция. А. – частный случай сорбции. Применение адсорбц. процессов датируется кон. 18 в., когда независимо и практически одновременно появились три публикации: итал. натуралист Ф. Фонтана и К. Шееле в 1777 описали поглощение газов древесным углем, в 1785 Т. Е. Ловиц обнаружил способность таких углей обесцвечивать растворы винных кислот, поглощая органич. примеси.
Физич. А. вызывается силами молекулярного взаимодействия. Осн. вклад в энергию взаимодействия вносят дисперсионные силы. Их величина приблизительно постоянна для адсорбентов любой химич. природы, поэтому вызываемое этими силами взаимодействие носит неспецифич. характер. Иногда дисперсионное взаимодействие усиливается электростатическим – ориентационным и индукционным. Электростатич. взаимодействие зависит от химич. природы адсорбтива, следовательно, является специфическим. Специфич. взаимодействие может усиливаться за счёт образования водородных связей между адсорбиров. молекулами и полярными группами, находящимися на поверхности адсорбента (напр., водородные связи образуются при А. воды и спиртов на силикагеле, поверхность которого покрыта гидроксильными группами). Теплота физич. А. составляет, как правило, 8–25 кДж/моль. Физич. А. можно обратить, понизив давление газа или концентрацию растворённого вещества. Физич. А. не вызывает изменений индивидуальных свойств молекул адсорбата. Поглощение вещества может быть обусловлено образованием химич. связи между молекулами адсорбата и поверхностным слоем адсорбента. Такое поглощение называется хемосорбцией. Хемосорбция необратима, её теплота св. 80 кДж/моль. При хемосорбции молекулы адсорбата образуют поверхностные химич. соединения с адсорбентом.
Равновесная адсорбция
Если скорости А. и десорбции равны, то это свидетельствует об установлении адсорбц. равновесия. Кривые зависимости равновесной А. от концентрации или давления адсорбтива при постоянной темп-ре называются изотермами А. Наиболее простая изотерма А. представляет собой прямую, выходящую из начала координат, где на оси абсцисс отложено давление адсорбтива $p$ (или концентрация $c$), по оси ординат – величина адсорбции $a$. Эта область А. называется областью Генри: $a=Γp, Γ$ – коэф. Генри.
И. Ленгмюром была предложена (1914–1918) теория мономолекулярной локализов. А. (молекулы адсорбата не передвигаются по поверхности) при следующих допущениях: поверхность однородна, т. е. все адсорбц. центры имеют одинаковое сродство к молекулам адсорбтива; молекулы адсорбата не взаимодействуют друг с другом. Уравнение Ленгмюра имеет вид: $a=a_{макс}bp/(1+bp)$ или $p=a/b(a_{макс}-a)$, где $a$ – количество адсорбиров. вещества, $a_{макс}$ – предельная величина А. в плотном монослое, $p$ – давление адсорбтива, $b$ – адсорбц. коэф. Полимолекулярная, или многослойная, А., при которой молекулы пара, адсорбируясь, образуют плёнку толщиной в неск. монослоёв, описывается уравнением Брунауэра – Эммета – Теллера (уравнение БЭТ, 1938):$$a=\frac{a_{макс}Cp/p_0}{(1-p/p_0)[1+(C-1)p/p_0},$$где $p_0$ – давление насыщенного пара при темп-ре А., $C$ – константа. Уравнение БЭТ применяют для определения удельной поверхности адсорбентов.
В 1914 М. Полани предложена потенциальная теория А., согласно которой вблизи поверхности адсорбента существует потенциальное адсорбц. поле, убывающее с расстоянием от поверхности; давление адсорбтива, равное вдали от поверхности $p$, вблизи неё возрастает и на некотором расстоянии достигает значения $p_0$, при котором адсорбтив конденсируется.
Адсорбенты обычно разделяют на непористые (радиусы кривизны поверхностей которых весьма велики и стремятся к бесконечности) и пористые. Пористые адсорбенты содержат микро-, супермикро-, мезо- и макропоры (см. Пористость). В макропорах А. крайне мала, её обычно не учитывают при оценке адсорбц. свойств адсорбентов. Характерная особенность А. в микро- и супермикропорах – повышение энергии А. по сравнению с поглощением вещества на непористом адсорбенте той же химич. природы. Этот эффект является результатом наложения полей поверхностных сил противоположных стенок пор. В микро- и супермикропорах А. происходит объёмно, в мезопорах – по механизму послойного заполнения, завершаемого капиллярной конденсацией.
Для микропористых адсорбентов М. М. Дубинин разработал теорию объёмного заполнения микропор (ТОЗМ). Введя представление о функции распределения объёмов пор по значениям химич. потенциала адсорбата в них, Дубинин и Л. В. Радушкевич получили (1947) уравнение изотермы А., которое записывается в виде: $W/W_0=exp[–(A/βE_0)^2]$, где $W$ и $W_0$ – текущая и предельная величины А. пара в единице объёма, $A$ – дифференциальная мольная работа адсорбции, $A=RT\ln(p_0/p)$, $R$ – универсальная газовая постоянная, $T$ – абсолютная темп-ра, $E_0$ – характеристич. энергия адсорбции стандартного пара (обычно бензола или азота), $β$ – коэф. подобия, аппроксимируемый отношением парахоров адсорбируемого и стандартного веществ.
Уравнение Дубинина – Радушкевича применимо для описания изотерм А. в интервале относит. равновесных давлений от 5·10–4 до 0,4 на адсорбентах с однородной микропористой структурой, т. е. адсорбентах, в которых отсутствуют супермикропоры. Т. к. в адсорбц. технике микропористые адсорбенты получили наибольшее распространение, ТОЗМ применяется не только в физико-химич. исследованиях, но и в инженерных расчётах.
Кинетика и динамика адсорбции
Элементарный акт А. осуществляется практически мгновенно. Поэтому временны́е зависимости А. лимитируются в осн. механизмом диффузии вещества к месту А. Диффуз. процессы определяются концентрацией адсорбтива, темп-рой, химич. природой и пористой структурой адсорбента, концентрацией др. веществ в объёме и на поверхности. А. в порах протекает значительно медленнее, чем на открытой поверхности. А. из жидких растворов происходит с меньшей скоростью, чем из газовых смесей. Зависимость величины А. от времени называют кинетической кривой А.
Кинетику А. в потоке газа изучают, используя единичные гранулы адсорбента и слой толщиной в одну гранулу. На практике обычно применяют слои адсорбента, толщина которых существенно превышает слой в одно зерно, т. е. изучают А. в динамич. условиях. При изучении динамики А. через слой адсорбента пропускают газовый или жидкостный поток, содержащий адсорбируемые вещества, и измеряют нарастание концентрации адсорбируемого вещества за слоем адсорбента как функцию времени. Появление за слоем поглощаемого вещества называется проскоком, время до проскока – временем защитного действия. Зависимость концентрации данного компонента за слоем от времени – выходная кривая, из анализа которой получают полную информацию об эффективности адсорбц. процесса.
Технологическое оформление адсорбционных процессов
Широко распространены установки с неподвижным слоем адсорбента, осн. узлом которых являются адсорберы – полые колонны, заполненные адсорбентом. Газовый или жидкостный поток, содержащий адсорбируемые компоненты, пропускается через шихту (слой адсорбента) до проскока адсорбтива; затем поток направляется в др. адсорбер. Целевые компоненты, поглощённые шихтой, извлекаются путём регенерации адсорбента (нагреванием адсорбера, вытеснением водяным паром и др.). Высокой производительностью характеризуются адсорбц. установки с псевдоожиженным («кипящим») слоем адсорбента, в которых газовый поток поступает в адсорбер снизу, приводя адсорбент во взвешенное состояние, что сокращает время А. и десорбции. Применяются установки с движущимся слоем адсорбента. В них адсорбент под действием силы тяжести медленно опускается, из нижней части адсорбера потоком воздуха направляется в вертикальную трубу, смонтированную параллельно адсорбц. колонне, и поднимает зёрна адсорбента в верхнюю часть колонны. Газовый поток, содержащий пары адсорбиров. веществ, поступает в ср. часть адсорбера и движется вверх к адсорбенту. В верхней части колонны непрерывно происходит А., в нижней – регенерация адсорбента. Широко используются т. н. короткоцикловые установки: при А. газ подаётся в адсорбер под значит. давлением, десорбция происходит из-за сброса давления, затем вновь давление поднимают.
В качестве адсорбентов применяют вещества с развитой поверхностью: активир. угли, силикагели, оксид алюминия, цеолиты; из непористых адсорбентов – технич. углерод (сажа) и высокодисперсный SiO2 (аэросил). См. также Сорбенты.
Адсорбция в природе и технологии
А. играет важную роль во мн. природных (напр., обогащение почв, образование вторичных рудных месторождений) и биологич. (функционирование клеточных мембран) процессах. Адсорбц. технологии широко применяют для очистки, осушки, разделения газовых и жидких смесей: очистки пром. выбросов и сточных вод, в т. ч. выбросов атомных электростанций, детоксикации загрязнённых почв, кондиционирования питьевой воды, разделения нефтей, извлечения драгоценных металлов из растворов и пульп, получения обогащённого кислородом воздуха, очистки лекарственных препаратов. Адсорбенты используют как наполнители при произ-ве полимеров, носители в катализе, в хроматографии, а также в медицине для извлечения вредных веществ, попавших в желудочно-кишечный тракт организма (энтеросорбция) или для очистки крови (гемосорбция). Явление А. используется при крашении тканей, в полиграфич., пищевой пром-сти, в радиоэлектронной технике и др.
Адсорбция что это? Значение слова Адсорбция
Значение слова Адсорбция по Ефремовой:
Адсорбция — Поглощение, всасывание вещества из раствора или газа поверхностью твердого тела или поверхностным слоем жидкости.
Адсорбция в Энциклопедическом словаре:
Адсорбция — (от лат. ad — на — при и sorbeo — поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) илижидкости. Адсорбенты обычно имеют большую удельную поверхность — донескольких сотен м2/г. Физическая адсорбция — результат действиядисперсионных или электростатических сил. Если адсорбция сопровождаетсяхимической реакцией поглощаемого вещества с адсорбентом, то она называетсяхемосорбцией. В промышленности адсорбцию осуществляют в специальныхаппаратах — адсорберах. применяют для осушки газов, очистки органическихжидкостей и воды, улавливания ценных или вредных отходов производства.
Значение слова Адсорбция по словарю медицинских терминов:
адсорбция (ад- лат. sorbeo поглощать) — поглощение (концентрирование) газов или растворенных веществ на поверхности твердого тела или жидкости.
Значение слова Адсорбция по словарю Брокгауза и Ефрона:
Адсорбция (хим.) — слово, введенное в употребление главным образом В. Оствальдом ("Allgemeine Chemie", 2-е изд., 1-й т., 1084). оно обозначает обыкновенно явление поглощения некоторыми твердыми телами газов, красок, солей и т. п. веществ из растворов. в более широком смысле под А. подразумеваются явления изменения концентрации среды, вызываемые введением в эту среду некоторых твердых тел. Так, напр., если внести толченый древесный уголь в раствор йода или в атмосферу его паров, то на поверхности угля сгущается некоторое количество йода и концентрация его в растворе (или давление пара) падает. если взбалтывать раствор поваренной соли с животным углем, то концентрация раствора возрастает (Лагергрен). Что тут имеется некоторый вид равновесия, явствует из опытов Шаппюи, показавшего, что при постоянной температуре количество углекислого газа, поглощаемого определенным количеством древесного угля, зависит только от давления газа. Механизм процесса до сих пор не ясен. По-видимому, он находится в связи с явлениями изменения концентрации растворов при прохождении через капилляры (Schonbein, "Pogg. Ann.", 1 861). с другой стороны, он может быть связан со способностью твердого тела образовывать на своей поверхности сильно сжатый слой раствора (ср. Nernst, "Theor. Ch.", 1903), благодаря чему возможна и "отрицательная А.", как приведенная выше в случае раствора поваренной соли в присутствии животного угля (давление понижает растворимость NaCl, а след., сжатый раствор, прилегающий к углю, становится беднее NaCl). Практические применения А. многочисленны. достаточно указать, что Ловитц еще в 1791 г. подметил, что древесный уголь (см.) обесцвечивает различные окрашенные жидкости (благодаря А. краски), что с 1810 г., по указанию Фигье, животный уголь (см.) употребляется для обесцвечивания сахарного сиропа (см.). что углем же очищают на холоду водку от сивушного масла (см.) и т. п.. с помощью А. при низких температурах Дьюар (Dewar) достигает больших разрежений и выделения гелия (см.) из газовых смесей, его содержащих. Литературу см. Ostwald, "Allg. Ch.", l. с., и E. Fischer и E. Schimdmer, "Lieb. Ann.", 1892. А. И. Горбов.
Определение слова «Адсорбция» по БСЭ:
Адсорбция (от лат. ad — на, при и sorbeo — поглощаю)
поглощение к.-л. вещества из газообразной среды или раствора поверхностным слоем жидкости или твёрдого тела. Например, если поместить в водный раствор уксусной кислоты кусочек угля, то произойдёт А. — количество кислоты в растворе уменьшится, молекулы кислоты сконцентрируются на поверхности угля. А. и Абсорбция — поглощение в объёме тела, объединяются общим термином Сорбция. Явление А. стало изучаться со 2-й половины 18 в. (Шееле, 1773), хотя несомненно, что в практической деятельности человечества А. использовалась с незапамятных времён. Учение об А. является частью более общей теории многокомпонентных гетерогенных систем, основы которой заложены У. Гиббсом (1876).
Явление А. тесно связано с особыми свойствами вещества в поверхностном слое. например, молекулы, лежащие на поверхности раздела фаз жидкость — пар, втягиваются внутрь жидкости, т. к. испытывают большее притяжение со стороны молекул, находящихся в объёме жидкости, чем со стороны молекул пара, концентрация которых во много раз меньше концентрации жидкости. Это внутреннее притяжение заставляет поверхность сокращаться и количественно характеризуется поверхностным натяжением. По той же причине молекулы какого-либо другого вещества, оказавшиеся вблизи поверхности, притянутся к ней и произойдёт А. После А. внутреннее притяжение частично компенсируется притяжением со стороны адсорбционного слоя и поверхностное натяжение уменьшается. Гиббс вывел формулу, связывающую значение А. с изменением поверхностного натяжения. Те вещества, А. которых сильно уменьшает поверхностное натяжение, принято называть поверхностно-активными.
Вещество, на поверхности которого происходит А., называется адсорбентом, а поглощаемое из объёмной фазы — адсорбатом. В зависимости от характера взаимодействия между молекулой адсорбата и адсорбентом А. принято подразделять на физическую А. и хемосорбцию. Менее прочная физическая А. не сопровождается существенными изменениями молекул адсорбата. Она обусловлена силами межмолекулярного взаимодействия, которые связывают молекулы в жидкостях и некоторых кристаллах и проявляются в поведении сильно сжатых газов. При хемосорбции молекулы адсорбата и адсорбента образуют химические соединения. Часто А. обусловлена и физическими и химическими силами, поэтому не существует чёткой границы между физикой А. и хемосорбцией.
Физически адсорбированные молекулы более или менее свободно перемещаются по поверхности, при этом их свойства часто аналогичны свойствам очень тонкого слоя газа, т. н. двухмерного газа. Они могут собираться группами, образуя слой двухмерной жидкости или двухмерного твёрдого тела. Адсорбированные молекулы рано или поздно покидают поверхность — десорбируются. Время, в течение которого молекула находится на поверхности, называется временем А. Времена А. могут колебаться в очень широких пределах. Скоростью А. (соответственно скоростью десорбции) называется количество молекул, адсорбирующихся (или десорбирующихся) за единицу времени, оба значения величин относят к единице поверхности или массы адсорбента. Скорость хемосорбции, как и скорость любого химического процесса, чаще всего увеличивается с повышением температуры (т. н. активированная А., см. Хемосорбция). Если скорости А. и десорбции равны друг другу, то говорят, что установилось адсорбционное равновесие. В состоянии равновесия количество адсорбированных молекул остаётся постоянным сколь угодно долго, если неизменны внешние условия (давление, температура и др.).
Адсорбированные молекулы не только совершают движение вдоль поверхности адсорбента, но и колеблются, то приближаясь к поверхности, то удаляясь от неё. Чем выше температура, тем интенсивнее колебательное движение, а стало быть, больше вероятность того, что в процессе таких колебаний связь молекулы с поверхностью будет разорвана и молекула десорбируется. Благодаря этому с ростом температуры уменьшается время А. и равновесное количество адсорбированных молекул.
С ростом концентрации или давления адсорбата в объёме увеличивается частота попаданий молекул адсорбата на поверхность адсорбента. пропорционально ей возрастает скорость А. и увеличивается равновесное количество адсорбированных молекул. Кривые зависимости равновесной А. от концентрации или давления адсорбата при постоянной температуре называются изотермами А.
Если адсорбат покрывает поверхность слоем толщиной в одну молекулу, А. называется мономолекулярной. Простейшая изотерма мономолекулярной А. представляет собой прямую линию, выходящую из начала координат, где на оси абсцисс отложено давление адсорбата P, а на оси ординат степень заполнения поверхности
&Theta., т. е. доля поверхности, покрытая адсорбированными молекулами. Это — т. н. изотерма Генри:
&Theta. = kP.
Коэффициент пропорциональности k зависит главным образом от температуры и характера взаимодействия адсорбент — адсорбат.
Уравнение Генри справедливо при очень низких степенях заполнения для однородной поверхности. По мере увеличения степени заполнения всё большую роль начинает играть взаимодействие между адсорбированными молекулами и интенсивность их поверхностной подвижности. Если молекулы адсорбата притягиваются друг к другу, то каждая вновь адсорбирующаяся молекула будет испытывать притяжение и адсорбата и молекул, адсорбированных ранее. Поэтому, по мере заполнения поверхности, силы, удерживающие адсорбированную молекулу, будут увеличиваться и условия для А. будут всё более и более благоприятными. В этом случае с ростом давления изотерма всё круче и круче идёт вверх (см. кривую 1). Однако по мере заполнения поверхности вновь адсорбирующимися молекулами становится всё труднее найти свободное (не занятое др. молекулами адсорбата) место на поверхности. Поэтому с увеличением давления рост А. замедляется и степень покрытия стремится к постоянному значению, равному единице (см. кривую 2, которая характерна при отсутствии взаимного притяжения молекул адсорбата). Если действуют оба эти фактора, то получаются вогнуто-выпуклые изотермы (см. кривую 3).
Выпуклые изотермы (см. кривую 2) часто описывают уравнением Ленгмюра
Здесь а — адсорбционный коэффициент, аналогичный по физическому смыслу константе Генри k. Уравнение Ленгмюра справедливо для мономолекулярной А. на однородной поверхности, если можно пренебречь притяжением молекул адсорбата между собой и их подвижностью вдоль поверхности.
При дальнейшем увеличении давления происходит заполнение второго, третьего и т. д. слоев, т. е. имеет место полимолекулярная А. Если адсорбент имеет узкие поры и смачивается адсорбатом (см. Смачивание), то в порах может произойти конденсация при давлениях более низких, чем давление насыщенного пара адсорбата. Это явление называется капиллярной конденсацией. Поверхность твёрдых адсорбентов чаще всего неоднородна по адсорбционным свойствам: одни участки поверхности адсорбируют лучше, другие — хуже. При малых давлениях преобладает А. на наиболее активных участках поверхности, с увеличением давления заполняются менее активные участки. Однако, строго говоря, А. происходит одновременно на всей поверхности, и получаемая на опыте изотерма представляет собой сумму изотерм, каждая из которых соответствует определённому типу поверхности. Благодаря этому экспериментальные изотермы мономолекулярной А. могут существенно отличаться от кривых, приведённых на рис.
Почти всегда процесс А. сопровождается выделением тепла, называемой теплотой А. Хотя теплота А. не является единственным фактором, характеризующим прочность А., однако чаще всего чем прочнее А., тем больше её теплота. Теплота хемосорбции обычно составляет несколько десятков ккал/моль, теплота физической А. редко превосходит 10 ккал/моль (40 кдж/моль). По мере заполнения неоднородной поверхности теплота А. обычно уменьшается. При переходе в область полимолекулярной А. теплота А. понижается до величины, близкой к теплоте конденсации адсорбата.
А. играет важную роль при теплообмене между газообразными, жидкими и твёрдыми телами. например, молекулы газа, адсорбируясь на горячей поверхности, приобретают энергию, соответствующую температуре поверхности, и после десорбции сообщают эту энергию другим молекулам газа, нагревая его. Это не единственный, но важный механизм теплообмена.
А.- один из решающих факторов в стабилизации коллоидных систем (см. Дисперсные системы, Мицелла, Коагуляция) и одна из важнейших стадий реакций в гетерогенных системах, в частности в гетерогенном катализе (см. Топохимические реакции, Катализ). В биологических системах А. — первая стадия поглощения субмикроскопическими коллоидными структурами, органеллами, клетками и тканями различных веществ из окружающей среды, функционирование биологических мембран, первые этапы взаимодействия ферментов с субстратом, защитные реакции против токсичных веществ, процессы всасывания — всё это связано с А. Многие адсорбенты (активный уголь, каолин, иониты и др.) служат противоядиями, поглощая и удаляя из организма попавшие в желудочно-кишечный тракт вредные вещества.
А. применяется для разделения газовых и жидких смесей, для осушки и очистки газов и жидкостей (например, очистки воздуха в противогазах). Одним из древнейших применений А. является очистка вина. В науке и технике приобрёл большое значение хроматографический метод анализа, основанный на различной способности компонентов анализируемой смеси к А. (см. Хроматография). А. используют также для получения и очистки биологически активных веществ — витаминов, ферментов, гормонов, антибиотиков и др.
При крашении тканей, в полиграфической промышленности имеют дело с А. молекул красителей. При производстве полимеров наполнителями служат адсорбенты. В вакуумной технике А. на стенках откачиваемой аппаратуры замедляет скорость откачки и ухудшает вакуум, однако, с другой стороны, действие различных сорбционных насосов основано на явлении А. В радиоэлектронной промышленности А. используется для стабилизации электрических свойств полупроводниковых приборов. Вообще во всех явлениях и процессах, где существенны поверхностные свойства, А. играет важную роль.
Лит.: Курс физической химии, т. 1, М., 1964. Бур Я.Х., Динамический характер адсорбции, пер. с англ., М., 1962. Трепнел Б., Хемосорбция, пер. с англ., М., 1958. Бладергрен В., Физ. химия в медицине и биологии, пер. с нем., М., 1951.
В.И. Шимулис.
Типичные изотермы мономолекулярной адсорбции на однородной поверхности.

Адсорбция - это... Что такое Адсорбция?
поглощение к.-л. вещества из газообразной среды или раствора поверхностным слоем жидкости или твёрдого тела. Например, если поместить в водный раствор уксусной кислоты кусочек угля, то произойдёт А. — количество кислоты в растворе уменьшится, молекулы кислоты сконцентрируются на поверхности угля. А. и Абсорбция — поглощение в объёме тела, объединяются общим термином Сорбция. Явление А. стало изучаться со 2-й половины 18 в. (Шееле, 1773), хотя несомненно, что в практической деятельности человечества А. использовалась с незапамятных времён. Учение об А. является частью более общей теории многокомпонентных гетерогенных систем, основы которой заложены У. Гиббсом (1876). Явление А. тесно связано с особыми свойствами вещества в поверхностном слое. например, молекулы, лежащие на поверхности раздела фаз жидкость — пар, втягиваются внутрь жидкости, т. к. испытывают большее притяжение со стороны молекул, находящихся в объёме жидкости, чем со стороны молекул пара, концентрация которых во много раз меньше концентрации жидкости. Это внутреннее притяжение заставляет поверхность сокращаться и количественно характеризуется поверхностным натяжением (См. Поверхностное натяжение). По той же причине молекулы какого-либо другого вещества, оказавшиеся вблизи поверхности, притянутся к ней и произойдёт А. После А. внутреннее притяжение частично компенсируется притяжением со стороны адсорбционного слоя и поверхностное натяжение уменьшается. Гиббс вывел формулу, связывающую значение А. с изменением поверхностного натяжения. Те вещества, А. которых сильно уменьшает поверхностное натяжение, принято называть поверхностно-активными.Вещество, на поверхности которого происходит А., называется адсорбентом, а поглощаемое из объёмной фазы — адсорбатом. В зависимости от характера взаимодействия между молекулой адсорбата и адсорбентом А. принято подразделять на физическую А. и хемосорбцию. Менее прочная физическая А. не сопровождается существенными изменениями молекул адсорбата. Она обусловлена силами межмолекулярного взаимодействия, которые связывают молекулы в жидкостях и некоторых кристаллах и проявляются в поведении сильно сжатых газов. При хемосорбции молекулы адсорбата и адсорбента образуют химические соединения. Часто А. обусловлена и физическими и химическими силами, поэтому не существует чёткой границы между физикой А. и хемосорбцией.
Физически адсорбированные молекулы более или менее свободно перемещаются по поверхности, при этом их свойства часто аналогичны свойствам очень тонкого слоя газа, т. н. двухмерного газа. Они могут собираться группами, образуя слой двухмерной жидкости или двухмерного твёрдого тела. Адсорбированные молекулы рано или поздно покидают поверхность — десорбируются. Время, в течение которого молекула находится на поверхности, называется временем А. Времена А. могут колебаться в очень широких пределах. Скоростью А. (соответственно скоростью десорбции) называется количество молекул, адсорбирующихся (или десорбирующихся) за единицу времени, оба значения величин относят к единице поверхности или массы адсорбента. Скорость хемосорбции, как и скорость любого химического процесса, чаще всего увеличивается с повышением температуры (т. н. активированная А., см. Хемосорбция). Если скорости А. и десорбции равны друг другу, то говорят, что установилось адсорбционное равновесие. В состоянии равновесия количество адсорбированных молекул остаётся постоянным сколь угодно долго, если неизменны внешние условия (давление, температура и др.).Адсорбированные молекулы не только совершают движение вдоль поверхности адсорбента, но и колеблются, то приближаясь к поверхности, то удаляясь от неё. Чем выше температура, тем интенсивнее колебательное движение, а стало быть, больше вероятность того, что в процессе таких колебаний связь молекулы с поверхностью будет разорвана и молекула десорбируется. Благодаря этому с ростом температуры уменьшается время А. и равновесное количество адсорбированных молекул.
С ростом концентрации или давления адсорбата в объёме увеличивается частота попаданий молекул адсорбата на поверхность адсорбента; пропорционально ей возрастает скорость А. и увеличивается равновесное количество адсорбированных молекул. Кривые зависимости равновесной А. от концентрации или давления адсорбата при постоянной температуре называются изотермами А.
Если адсорбат покрывает поверхность слоем толщиной в одну молекулу, А. называется мономолекулярной. Простейшая изотерма мономолекулярной А. представляет собой прямую линию, выходящую из начала координат, где на оси абсцисс отложено давление адсорбата Р, а на оси ординат степень заполнения поверхности Θ, т. е. доля поверхности, покрытая адсорбированными молекулами. Это — т. н. изотерма Генри:
Θ = kP.
Коэффициент пропорциональности k зависит главным образом от температуры и характера взаимодействия адсорбент — адсорбат.
Уравнение Генри справедливо при очень низких степенях заполнения для однородной поверхности. По мере увеличения степени заполнения всё большую роль начинает играть взаимодействие между адсорбированными молекулами и интенсивность их поверхностной подвижности. Если молекулы адсорбата притягиваются друг к другу, то каждая вновь адсорбирующаяся молекула будет испытывать притяжение и адсорбата и молекул, адсорбированных ранее. Поэтому, по мере заполнения поверхности, силы, удерживающие адсорбированную молекулу, будут увеличиваться и условия для А. будут всё более и более благоприятными. В этом случае с ростом давления изотерма всё круче и круче идёт вверх (см. кривую 1). Однако по мере заполнения поверхности вновь адсорбирующимися молекулами становится всё труднее найти свободное (не занятое др. молекулами адсорбата) место на поверхности. Поэтому с увеличением давления рост А. замедляется и степень покрытия стремится к постоянному значению, равному единице (см. кривую 2, которая характерна при отсутствии взаимного притяжения молекул адсорбата). Если действуют оба эти фактора, то получаются вогнуто-выпуклые изотермы (см. кривую 3).
Выпуклые изотермы (см. кривую 2) часто описывают уравнением Ленгмюра
Здесь а — адсорбционный коэффициент, аналогичный по физическому смыслу константе Генри k. Уравнение Ленгмюра справедливо для мономолекулярной А. на однородной поверхности, если можно пренебречь притяжением молекул адсорбата между собой и их подвижностью вдоль поверхности.
При дальнейшем увеличении давления происходит заполнение второго, третьего и т. д. слоев, т. е. имеет место полимолекулярная А. Если адсорбент имеет узкие поры и смачивается адсорбатом (см. Смачивание), то в порах может произойти конденсация при давлениях более низких, чем давление насыщенного пара адсорбата. Это явление называется капиллярной конденсацией (См. Капиллярная конденсация). Поверхность твёрдых адсорбентов (См. Адсорбенты) чаще всего неоднородна по адсорбционным свойствам: одни участки поверхности адсорбируют лучше, другие — хуже. При малых давлениях преобладает А. на наиболее активных участках поверхности, с увеличением давления заполняются менее активные участки. Однако, строго говоря, А. происходит одновременно на всей поверхности, и получаемая на опыте изотерма представляет собой сумму изотерм, каждая из которых соответствует определённому типу поверхности. Благодаря этому экспериментальные изотермы мономолекулярной А. могут существенно отличаться от кривых, приведённых на рис.Почти всегда процесс А. сопровождается выделением тепла, называемой теплотой А. Хотя теплота А. не является единственным фактором, характеризующим прочность А., однако чаще всего чем прочнее А., тем больше её теплота. Теплота хемосорбции обычно составляет несколько десятков ккал/моль, теплота физической А. редко превосходит 10 ккал/моль (40 кдж/моль). По мере заполнения неоднородной поверхности теплота А. обычно уменьшается. При переходе в область полимолекулярной А. теплота А. понижается до величины, близкой к теплоте конденсации адсорбата.
А. играет важную роль при теплообмене между газообразными, жидкими и твёрдыми телами. например, молекулы газа, адсорбируясь на горячей поверхности, приобретают энергию, соответствующую температуре поверхности, и после десорбции сообщают эту энергию другим молекулам газа, нагревая его. Это не единственный, но важный механизм теплообмена.
А.— один из решающих факторов в стабилизации коллоидных систем (см. Дисперсные системы, Мицелла, Коагуляция) и одна из важнейших стадий реакций в гетерогенных системах, в частности в гетерогенном катализе (см. Топохимические реакции, Катализ). В биологических системах А. — первая стадия поглощения субмикроскопическими коллоидными структурами, органеллами, клетками и тканями различных веществ из окружающей среды, функционирование биологических мембран, первые этапы взаимодействия ферментов с субстратом, защитные реакции против токсичных веществ, процессы всасывания — всё это связано с А. Многие адсорбенты (активный уголь, каолин, иониты и др.) служат противоядиями, поглощая и удаляя из организма попавшие в желудочно-кишечный тракт вредные вещества. А. применяется для разделения газовых и жидких смесей, для осушки и очистки газов и жидкостей (например, очистки воздуха в противогазах). Одним из древнейших применений А. является очистка вина. В науке и технике приобрёл большое значение хроматографический метод анализа, основанный на различной способности компонентов анализируемой смеси к А. (см. Хроматография). А. используют также для получения и очистки биологически активных веществ — витаминов, ферментов, гормонов, антибиотиков и др.При крашении тканей, в полиграфической промышленности имеют дело с А. молекул красителей. При производстве полимеров наполнителями служат адсорбенты. В вакуумной технике А. на стенках откачиваемой аппаратуры замедляет скорость откачки и ухудшает вакуум, однако, с другой стороны, действие различных сорбционных насосов основано на явлении А. В радиоэлектронной промышленности А. используется для стабилизации электрических свойств полупроводниковых приборов. Вообще во всех явлениях и процессах, где существенны поверхностные свойства, А. играет важную роль.
Лит.: Курс физической химии, т. 1, М., 1964; Бур Я.Х., Динамический характер адсорбции, пер. с англ., М., 1962; Трепнел Б., Хемосорбция, пер. с англ., М., 1958; Бладергрен В., Физ. химия в медицине и биологии, пер. с нем., М., 1951.
В.И. Шимулис.
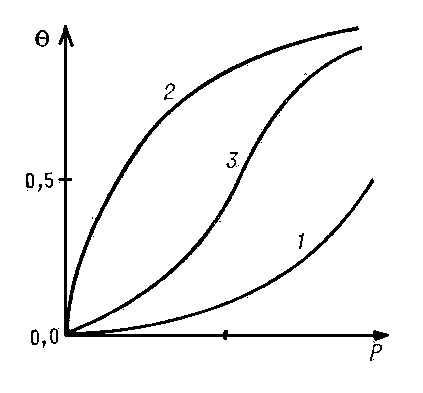
Типичные изотермы мономолекулярной адсорбции на однородной поверхности.
Адсорбция - это... Что такое Адсорбция?
Адсорбция (лат. ad — на, при; sorbeo — поглощаю) — это, в широком смысле, процесс изменения концентрации у поверхности раздела двух фаз, а в более узком и употребительном — это повышение концентрации одного вещества (газ, жидкость) у поверхности другого вещества (жидкость, твердое тело).
Основные понятия
Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтив, поглощённое — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твёрдым веществом (в случае газа и жидкости) или жидкостью (в случае газа) — адсорбентом. При этом, как и в общем случае адсорбции, происходит концентрирование примеси на границе раздела адсорбент-жидкость либо адсорбент-газ. Процесс, обратный адсорбции, то есть перенос вещества с поверхности раздела фаз в объём фазы, называется десорбция. Если скорости адсорбции и десорбции равны, то говорят об установлении адсорбционного равновесия. В состоянии равновесия количество адсорбированных молекул остается постоянным сколь угодно долго, если неизменны внешние условия (давление, температура и состав системы)[1].
Адсорбция и хемосорбция
На поверхности раздела двух фаз помимо адсорбции, обусловленной в основном физическими взаимодействиями (главным образом это Ван-дер-Ваальсовы силы), может идти химическая реакция. Этот процесс называется хемосорбцией. Чёткое разделение на адсорбцию и хемосорбцию не всегда возможно. Одним из основных параметров по которым различаются эти явления является тепловой эффект: так, тепловой эффект физической адсорбции обычно близок к теплоте сжижения адсорбата, тепловой эффект хемосорбции значительно выше. Кроме того в отличие от адсорбции хемосорбция обычно является необратимой и локализованной. Примером промежуточных вариантов, сочетающих черты и адсорбции и хемосорбции является взаимодействие кислорода на металлах и водорода на никеле: при низких температурах они адсорбируются по законам физической адсорбции, но при повышении температуры начинает протекать хемосорбция.
Схожие явления
В предыдущем разделе говорилось о случае протекания гетерогенной реакции на поверхности- хемосорбции. Однако бывают случаи гетерогенных реакций по всему объему, а не только на поверхности- это обычная гетерогенная реакция. Поглощение по всему объёму может проходить и под воздействием физических сил- этот случай называется абсорбцией.
| Виды взаимодействий | Взаимодействия только на поверхности | Взаимодействия по всему объёму |
|---|---|---|
| Физические | Адсорбция | Абсорбция |
| Химические | Хемосорбция | Гетерогенная реакция |
Физическая адсорбция
| Модели физической адсорбции | |
| Образование монослоя | Энергетическая диаграмма |
| Рис. 1: a) адсорбент, b) адсорбат, c) адсорбтив (газовая фаза или раствор) | Рис. 2: a) адсорбент, b) адсорбат, c) газовая фаза, d - расстояние, E - энергия, Eb - энергия адсорбции, (1) десорбция, (2) адсорбция |
| Поликонденсация | Избирательная адсорбция |
| Рис. 3: a) адсорбент, b) адсорбат, c) конденсат, d) адсорбтив (газовая фаза или раствор) | Рис. 4: a) адсорбент, b) адсорбат, c) адсорбтивы (газовая фаза или раствор): показана преимущественная адсорбция частиц голубого цвета |
Причиной адсорбции являются неспецифические (то есть не зависящие от природы вещества) Ван-дер-Ваальсовы силы. Адсорбция, осложнённая химическим взаимодействием между адсорбентом и адсорбатом, является особым случаем. Явления такого рода называют хемосорбцией и химической адсорбцией. «Обычную» адсорбцию в случае, когда требуется подчеркнуть природу сил взаимодействия, называют физической адсорбцией.
Физическая адсорбция является обратимым процессом, условие равновесия определяется равными скоростями адсорбции молекул адсорбтива P на вакантных местах поверхности адсорбента S* и десорбции — освобождения адсорбата из связанного состояния S − P:
- ;
уравнение равновесияя в таком случае:
- ,
где K — константа равновесия, [S − P] и [S*] — доли поверхности адсорбента, занятые и незанятые адсорбатом, а [P] — концентрация адсорбтива.
Количественно процесс физической мономолекулярной адсорбции в случае, когда межмолекулярным взаимодействием адсорбата можно пренебречь, описывается уравнением Ленгмюра:
- ,
где — доля площади поверхности адсорбента, занятая адсорбатом, — адсорбционный коэффициент Ленгмюра, а P — концентрация адсорбтива.
Поскольку и, соответственно, , уравнение адсорбционного равновесия может быть записано следующим образом:
Уравнение Ленгмюра является одной из форм уравнения изотермы адсорбции. Под уравнением изотермы адсорбции (чаще применяют сокращённый термин — изотерма адсорбции) понимают зависимость равновесной величины адсорбции от концентрации адсорбтива a=f(С) при постоянной температуре (T=const). Концентрация адсорбтива для случая адсорбции из жидкости выражается, как правило, в мольных либо массовых долях. Часто, особенно в случае адсорбции из растворов, пользуются относительной величиной: С/Сs, где С — концентрация, Сs — предельная концентрация (концентрация насыщения) адсорбтива при данной температуре. В случае адсорбции из газовой фазы концентрация может быть выражена в единицах абсолютного давления, либо, что особенно типично для адсорбции паров, в относительных единицах: P/Ps, где P — давление пара, Ps — давление насыщенных паров этого вещества. Саму величину адсорбции можно выразить также в единицах концентрации (отношение числа молекул адсорбата к общему числу молекул на границе раздела фаз). Для адсорбции на твёрдых адсорбентах, особенно при рассмотрении практических задач, используют отношение массы или количества поглощённого вещества к массе адсорбента, например мг/г или ммоль/г.
Значение адсорбции
Адсорбция — всеобщее и повсеместное явление, имеющее место всегда и везде, где есть поверхность раздела между фазами. Наибольшее практическое значение имеет адсорбция поверхностно-активных веществ и адсорбция примесей из газа либо жидкости специальными высокоэффективными адсорбентами. В качестве адсорбентов могут выступать разнообразные материалы с высокой удельной поверхностью: пористый углерод (наиболее распространённая форма — активированный уголь), силикагели, цеолиты а также некоторые другие группы природных минералов и синтетических веществ.
Адсорбция (особенно хемосорбция) имеет также важное значение в гетерогенном катализе. Пример адсорбционных установок приведён на странице азотные установки.
Установка для проведения адсорбции называется адсорбером.
См. также
Примечания
Литература
- Фролов Ю. Г. Курс коллоидной химии. Поверхностные явления и дисперсные системы. - М.: Химия, 1989. - 464 с.
- Кельцев Н. В. Основы адсорбционной техники. - М.: Химия, 1984. - 592 с.
- Грег С., Синг К. Адсорбция, удельная поверхность, пористость. - М.: Мир, 1984. - 310 с.*
- Адамсон А. Физическая химия поверхностей. – М.: Мир. 1979. – 568 с.
- Оура К., Лифшиц В. Г., Саранин А. А. и др. Введение в физику поверхности / Под ред. В. И. Сергиенко. — М.: Наука, 2006. — 490 с.
- Карнаухов А.П. Адсорбция. Текстура дисперсных и пористых материалов. — Новосибирск: Наука. 1999. — 470 с.
- Химическая энциклопедия. Т. 1. — М.: Советская энциклопедия, 1990. — 623 с.
- Полторак О.М. Термодинамика в физической химии. — М.: Высшая школа, 1991. — 319 с.
Ссылки
Адсорбция.
Коллоидная химия
Адсорбция.
Сорбция
Сорбцией (от латинского sorbeo – поглощаю, втягиваю) называют любой процесс поглощения одного вещества (сорбтива) другим (сорбентом), независимо от механизма поглощения.
В зависимости от механизма сорбции различают адсорбцию, абсорбцию, хемосорбцию и капилярную конденсацию.
Адсорбция
Адсорбция это процесс, происходящий на границе раздела фаз. Он затрагиваетолько поверхностные слои, взаимодействующих фаз, и не распространяется на глубинные слои этих фаз.
Адсорбцией называют явление накопления одного вещества на поверхности другого. В общем случае, адсорбцией называют изменение концентрации вещества на границе раздела фаз.
Абсорбция
Абсорбция, в отличии от адсорбции, это процесс захватывающий не только поверхность раздела фаз, но распространяющийся на весь объём сорбента.
Примером процесса абсорбции является растворение газов в жидкости.
Хемосорбция
Хемосорбцией называется поглощение одного вещества другим, сопровождающееся их химическим взаимодействием.
Капилярная конденсация
Капиллярная конденсация — сжижение пара в капиллярах, щелях или порах в твердых телах.
Явление конденсации отлично от физической адсорбции.
Таким образом, сорбционные процессы различны по их механизму. Однако, любой сорбционный процесс начинается с адсорбции на границе соприкасающихся фаз, которые могут быть жидкими, газообразными или твёрдыми.
Адсорбция
Напомним, что адсорбцией называют явление накопления одного вещества на поверхности другого. В общем случае, адсорбцией называют изменение концентрации вещества на границе раздела фаз.
Адсорбция происходит на любых межфазовых поверхностях и адсорбироваться могут любые вещества.
Адсорбционное равновесие, т.е. равновесное распределение вещества между пограничным слоем и граничащими фазами является динамическим равновесием и быстро устанавливается.
Адсорбция понижается с понижением температуры.
Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтивом, поглощённое — адсорбатом. Вещество, на поверхности которого происходит адсорбция – адсорбентом.
Адсорбция представляет собой обратимый процесс. Процесс, обратный адсорбции, называется десорбцией.
Удаление адсорбированных веществ с адсорбентов при помощи растворителей называют элюцией.
Различают молекулярную и ионную адсорбцию. Это различение происходит в зависимости от того, что адсорбируется – молекулы или ионы вещества.
Адсорбция на поверхности жидкостей
На поверхности жидкостей могут адсорбироваться частицы веществ, растворённых в жидкостях. Адсорбция сопровождает процесс растворения, влияя на распределение частичек растворённого вещества между поверхностным слоем растворителя и внутренним его объёмом.
В соответствии со вторым началом термодинамики поверхностная энергия жидкостей стремится к минимуму. В чистых растворителях уменьшение этой энергии происходит путём сокращения поверхности.
В растворах поверхностная энергия может понижаться или увеличиваться за счёт изменения концентрации частиц в поверхностном слое жидкости.
Гиббсом было установлено, что распределение растворяемого в жидкости вещества происходит так, чтобы достигалось максимальное уменьшение поверхностного натяжения.
Он же предложил уравнение, определяющее величину адсорбции Г, т.е избытка вещества, накапливающегося в 1 см2 поверхностного слоя, имеющего толщину примерно в одну молекулу, по сравнению с содержанием этого вещества в таком же объёме внутри жидкости.
Где Δσ - изменение поверхностного натяжения, соответствующее изменению концентрации ΔС. Величина Δσ/ΔС называется поверхностной активностью.
Следовательно, адсорбция Г зависит от величины поверхностной активности и концентрации вещества С.
Если при этом поверхностное натяжение уменьшается, то адсорбция Г имеет положительное значение.
Положительная адсорбция. Поверхностно-активные вещества.
Чем сильнее вещество понижает поверхностное натяжение, тем больше оно будет накапливаться в поверхностном слое.
Концентрация растворённого вещества в поверхностном слое станет значительно выше, чем в остальном объёме жидкости. Возникающая разность концентраций неизбежно вызовет диффузию, которая будет направлена из поверхностного слоя внутрь жидкости и явится препятствием для полного перехода всех растворённых частиц в поверхностный слой. Установится подвижное адсорбционное равновесие между растворённым веществом в поверхностном слое и остальном объёме жидкости.
Адсорбцию, сопровождающуюся накоплением вещества в поверхностном слое, называют положительной. Пределом её служит полное насыщение поверхностного слоя адсорбируемым веществом.
Положительно адсорбирующиеся вещества называют также поверхностно-активными веществами (ПАВ). В водных растворах роль ПАВов будут играть вещества с жирной и дифильной природой (жиры, большинство жирных кислот, кетоны, спирты, холестерин и др.).
Отрицательная адсорбция. Поверхностно-инактивные вещества.
Если растворённое вещество увеличивает поверхностное натяжение, то оно будет выталкиваться из поверхностного слоя внутрь адсорбента. Такую адсорбцию называют отрицательной.
Пределом отрицательной адсорбции является полное вытеснение адсорбтива из поверхностного слоя внутрь адсорбента (растворителя).
В результате разности концентраций возникнет диффузия, которая будет направлена в поверхностный слой. Поэтому в поверхностном слое всегда окажется некоторое количество адсорбтива.
Вещества, резко повышающие поверхностное натяжение, почти не содержатся в поверхностном слое разбавленных растворов. Лишь значительное увеличение концентрации подобных растворов приводит к перемещению в поверхностный слой заметных количеств растворённого вещества, что сопровождается увеличением поверхностного натяжения.
Отрицательно адсорбирующиеся вещества называются поверхностно-инактивными.
Адсорбция и поверхносное натяжение биологических жидкостей
Отрицательная и положительная адсорбция различных веществ в крови и протоплазме клеток имеет большое значение для обмена веществ в живых организмах.
Поверхностное натяжение биологических жидкостей значительно ниже, чем воды. Поэтому гидрофобные вещества, например кислоты жирного ряда, стероиды, будут накапливаться у стенок сосудов, клеточных мембран, что облегчает их проникновение сквозь эти мембраны.
Жидкость | Поверхностное натяжение эрг/см2 |
|---|---|
Ртуть | 430,0 |
Вода | 72,7 |
Глицерин | 65,0 |
Сыворотка крови человека (при 38 С) | 46 - 47 |
Этиловый спирт | 22,0 |
Эфир | 16 |
Цитоплазма амёб (на границе с маслом) | 0,5 - 1,5 |
Для адсорбции из водных растворов большое значение имеет наличие у молекул полярных (гидрофильных) и неполярных (гидрофобных) групп.
Так, в молекуле масляной кислоты имеется полярная группа СООН и гидрофобная углеводородная цепь:
Молекулы обладающие одновременно обеими видами групп, называются дифильными.
У дифильной молекулы с короткой гидрофобной цепью преобладают гидрофильные свойства, поэтому такие молекулы хорошо растворяются в воде, адсорбируясь отрицательно.
С удлинением углеводородной цепи усиливаются гидрофобные свойства молекул и понижается их растворимость в воде.
Следовательно, к поверхностно-активным веществам принадлежат вещества дифильной структуры, имеющие меньшее, чем растворитель, поверхностное натяжение, и растворение которых приводит к положительной адсорбции, вызывая понижение поверхностного натяжения.
Поверхностно-инактивные вещества обладают противоположными свойствами.
Одновременно с увеличением гидрофобных свойств молекул повышается их поверхностная активность. Так удлинение цепи в гомологическом ряду жирных кислот, спиртов, аминов и др. на радикал –СН2– увеличивает их способность к положительной адсорбции в разбавленных растворах в 3,2 раза (правило Траубе-Дюкло).
Поверхностные плёнки
Молекулы веществ с преобладанием гидрофобных свойств (жирные кислоты с большим молекулярным весом и др.) располагаются в основном на поверхности воды, образуя поверхностные плёнки.
При небольшом количестве таких молекул поверхностной плёнки не образуется. Если же молекул много, то они располагаются упорядоченно, одна рядом с другой, причём их гидрофобные части выступают над водной поверхностью, образуя так называемый частокол Лэнгмюра.
1 - беспорядочное расположение дифильных молекул; 2 - частокол Лэнгмюра; 3 - избыток молекул; 4 - гидрофильная часть молекул; 5 - гидрофобная часть молекул;
Поверхностная плёнка образуется мономолекулярным слоем молекул, каждая из которых занимает на поверхности воды определённую площадь. Толщину слоя и площадь, занимаемую каждой молекулой, можно расчитать.
Так, молекулы жирных кислот, имеющие по одной полярной группе (масляная, валериановая, каприновая кислоты и т.п.) занимают на поверхности воды площадь 21 · 10-16 см2, независимо от длины углеводородной цепи.
Жирные кислоты с двумя полярными группами (например, олеиновая кислота) занимает площадь, вдвое большую, а молекулы с тремя полярными группами (например, тристеарин) – втрое большую площадь и т.д.
При избытке вещества с преимущественно гидрофобными свойствами его молекулы располагаются над молекулярной плёнкой.
Кессонная болезнь
Образование поверхностных плёнок нередко затрудняет процесс фильтрации.
На границе раздела воздух–вода в пузырьках воздуха, находящихся в растворе, может адсорбироваться поверхностно-активное вещество. Плёнка этого вещества образует как-бы оболочку вокруг пузырька. Такой пузырёк при продавливании через узкие поры в фильтре не способен резко деформироваться и поэтому может закупорить более крупные отверстия в фильтре, чем пузырёк без плёнки.
У водолазов, работающих на больших глубинах, иногда возникает, так называемая, кесонная болезнь. В их скафандры воздух подаётся под давлением и, следовательно, в крови водолазов растворяется повышенное количество газов.
При слишком быстром поднятии на поверхность давление в скафандрах резко понижается, и значительная часть газов крови выделяется в виде пузырьков, на которых образуется поверхностная плёнка из содержащихся в крови поверхностно-активных веществ.
Пузырьки газов закупоривают мелкие сосуды в различных тканях и органах, что приводит к тяжёлому заболеванию или даже гибели человека.
Подобная же паталогия может возникнуть и в результате резкого падения атмосферного давления при разгерметизации скафандров лётчиков и кабин самолётов при высотных полётах.
Для лечения кессонной болезни больного помещают в барокамеру, где создают большое давление. Пузырьки газов вновь растворяются в крови. В течении нескольких суток давление в барокамере медленно снижают. За это время избыточный газ из крови столь же медленно удаляется через лёгкие, не создавая закупорок.
Адсорбция твёрдыми телами
Твёрдыми телами могут адсорбироваться газы и пары, а также молекулы и ионы растворённых веществ.
Природа сил, вызывающих адсорбцию
Адсорбция на твёрдых телах может быть объяснена наличием силовых полей притяжения, возникающих за счёт неуравновешенных связей в кристалической решётке.
На выступающих участках твёрдого адсорбента (на активных центрах) адсорбция идёт особенно сильно. Так выступы на частичке угля в 4,5 раза интенсивнее адсорбируют кислород, чем углубления на его поверхности.
Адсорбционные силы слагаются из валентных сил взаимодействия (химических) и более слабых ван-дер-ваальсовых (физических). Роль тех и других при разных случаях адсорбции различна. Так, в самом начале адсорбции большинства газов, когда их давление мало, наблюдается химическая адсорбция. С увеличением давления она уступает место физической, которая в основном определяет адсорбцию газов.
Адсорбционные силы могут быть достаточно велики. Так, для полного удаления со стекла адсорбированных молекул воды его необходимо сильно нагревать в вакууме.
Адсорбенты, обладающие мощными силовыми полями, оказываются сплошь покрытыми адсорбированными частицами. При незначительных же адсорбционных силах только более активные центры покрываеются адсорбируемыми частицами.
На адсорбцию влияет не только природа адсорбента, но и адсорбтива. Так, на твёрдых адсорбентах сильнее адсорбируются те газы, которые легче сжижаются, т.е. критическая температура которых выше.
Обратимость адсорбции
Адсорбция представляет собой обратимый процесс. Адсорбированные частицы не остаются не остаются неподвижными. Они удерживаются на адсорбенте всего сотые и тысячные доли секунды и, десорбируясь, замещаются на новые частицы. К тому же они не являются строго фиксированными на адсорбенте, а могут перемещаться по его поверхности. В итоге устанавливается динамическое адсорбционное равновесие между свободными и адсорбированными частицами.
Скорость адсорбции
Скорость адсорбции имеет большое значение для практического использования различных адсорбентов.
Например, в противогазе проходящий через коробку воздух должен очень быстро очищаться от примесей отравляющих веществ, что возможно лишь при высоких скоростях адсорбционных процессов.
Необходимо указать, что активированный уголь в противогазе играет роль не только адсорбента ряда отравляющих веществ, но и катализатора реакций разложения некоторых из них.
В частности, активированный уголь катализирует гидролиз фосгена:
COCl2 + h3O = HCl + CO2.
Повышение температуры понижает физическую адсорбцию адсорбцию, так как при этом усиливается движение молекул в адсорбционном слое, нарушается ориентация адсорбированных молекул, т.е. увеличивается десорбция.
С другой стороны увеличение температуры увеличивает энергию адсорбированных частиц, что усиливает химическую адсорбцию.
Следовательно, в одних случаях повышение температуры усиливает десорбцию, в других – увеличивает адсорбцию.
Так, для большинства газов повышение температуры уменьшает адсорбцию. В то же время увеличение температуры от –185 до +20°С в 10 раз увеличивает адсорбцию кислорода платиной, так как при этом возрастает химическая адсорбция.
Повышение давления газов и паров увеличивает адсорбцию.
Капилярная конденсация
При адсорбции паров наблюдают так называемую капилярную конденсацию, протекающую на угле и других пористых адсорбентах.
Сконденсировавшаяся в капилярах жидкость образует вогнутый мениск, над которым пар оказывается насыщенным при более низком давлении, чем над плоской поверхностью. Это повышает конденсацию паров в капилярах адсорбента.
Капилярная конденсация особенно выражена у легко сжижаемых газов.
Хемосорбция
При хемосорбции вещество вступает с адсорбентом в химическую реакцию, например:
O2 + 2Cu = 2CuO.
Если вновь образующиеся при хемосорбции молекулы диффундируют в глубь вещества адсорбента, то достижение сорбционного равновесия наступает медленнее, так как оно зависит от скорости диффузии.
Если же при хемосорбции на поверхности сорбента возникают недиффундирующие молекулы, т.е. образуется плёнка, то она тормозит и со временем останавливает процесс хемосорбции.
Так, пластинка алюминия, сорбируя кислород, покрывается плёнкой из оксида оалюминия, что быстро прекращает процесс хемосорбции:
4Al + 3O2 = 2Al2O3.
Хемосорбция, как и всякая химическая реакция, может быть экзо- или эндотермической. Следовательно повышение температуры усиливает одни хемосорбционные процессы и ослабляет другие.
Полностью разграничить адсорбцию и хемосорбцию нельзя. Обычно эти два процесса протекают совместно.
Адсорбция — Студопедия
Процесс самопроизвольного концентрирования газов или растворенных веществ на поверхности раздела фаз называют адсорбцией. В зависимости от природы контактирующих фаз различают адсорбцию на границах: газ - твердое тело, газ – жидкость, жидкость - твердое тело и жидкость - жидкость.
Еще в 1785 г русский ученый Т.Е. Ловиц открыл способность угля поглощать растворенное вещество. С тех пор изучению явлений адсорбции было посвящено много работ, среди которых первостепенное значение имеют работы русских ученых: академика Н.Д.Зелинского, предложившего уголь в качестве универсального средства защиты от газообразных отравляющих веществ; М.С.Цвета, разработавшего хроматографический метод разделения веществ по их адсорбционной способности; академика К.К. Гедройца, создавшего учение о поглотительной способности почв; академика М.М. Думанского, разработавшего методику получения активных адсорбентов. Очень много для разработки теории и практики адсорбции сделали зарубежные ученые Гиббс, Ленгмюр, Фрейндлих, Поляни, Бранауэр и др.
Адсорбция является следствием снижения ненасыщенности молекулярных, атомных или ионных сил на поверхности раздела фаз и обусловлена накоплением вещества, снижающего свободную поверхностную энергию. Адсорбция – процесс самопроизвольный, т.к. в результате процесса адсорбции происходит уменьшение свободной поверхностной энергии, а по второму закону термодинамики такие процессы являются самопроизвольными.
Вещества, которые адсорбируются, называют адсорбатами (иногда - адсорбтивами), а вещества, которые адсорбируют на своей поверхности - адсорбентами.
В зависимости от характера сил, действующих между частицами (молекулы, атомы, ионы) адсорбата и адсорбента, различают физическую или ван-дер-ваальсову адсорбцию и химическую или хемосорбцию.
Природу адсорбции можно установить, исследовав её кинетику и энергетику. Действительно, физическая адсорбция происходит под влиянием относительно слабых межмолекулярных сил сцепления (сил Ван-дер-Ваальса) и по своей природе аналогична процессам конденсации паров адсорбата, теплота её близка к теплотам конденсации и составляет 10 - 50 кДж/моль. Поэтому при увеличении температуры физическая адсорбция уменьшается.
Хемосорбция связана с перекрыванием электронных орбиталей частиц адсорбата и адсорбента, т.е. вызывается их химическим взаимодействием, не приводящим, однако, к образованию объемной фазы. Теплота хемосорбции соизмерима с теплотами химических реакций и составляет обычно 60 - 600 кДж/моль. Химическая адсорбция с увеличением температуры увеличивается.
Адсорбция представляет собой обратимый процесс. Процесс, обратный адсорбции, называется десорбцией.
Различают молекулярную и ионную хемосорбцию в зависимости от того, что адсорбируется – молекулы или ионы вещества. В свою очередь, ионная адсорбция делится на обменную и адсорбцию потенциалопределяющих ионов.
Обменная адсорбция. Обменная адсорбция протекает на границе твердое тело / раствор электролита и состоит в том, что адсорбент и раствор обмениваются между собой катионами или анионами в эквивалентных количествах, благодаря чему принцип электронейтральности раствора электролита и адсорбента остается ненарушенным.
Основными факторами обменной адсорбции, определяющими ее специфичность, являются: наличие двойного электрического слоя на поверхности твердого адсорбента, валентность, величина радиуса и степень гидратации ионов раствора электролита.
Обменная адсорбция протекает несколько медленнее, чем обычная.
Для уяснения процесса обменной адсорбции можно рассмотреть процесс образования двойного электрического слоя при взаимодействии частицы хлористого серебра с раствором хлорида калия. Ионы хлора, сталкиваясь с частицами [AgCl]n будут соединяться с ионами серебра, образуя прочно удерживаемый слой С1- ионов, тем самым заряжая поверхность частицы. Такие ионы получили название потенциалопределяющих, а т.к. присоединившиеся С1- -ионы увеличивают свою концентрацию, т.е. адсорбируются на поверхности, то такой вид адсорбции называется адсорбцией потенциалопределяющих ионов.
Адсорбированные С1--ионы заряжают частицу отрицательно, и под действием электростатических сил притяжения будет увеличиваться количество К+-ионов, прилегающих к поверхности частицы. Другими словами, будет происходить адсорбция противоионов под действием электростатических сил. Так как К+-ионы могут быть заменены другими ионами такого же знака, взаимодействующими с частицей лишь электростатически, такие ионы называются обменными, адсорбция их - обменной.
Таким образом, обменная адсорбция происходит в процессе обмена ионов двойного электрического слоя адсорбента и ионов раствора. Схематически это можно представить следующими уравнениями:
Адсорбент-½Н+ + Na+ + Cl- à Адсорбент-½Na+ + H+ +Cl-
Адсорбент+ ½OH- + Na+ + Cl- à Адсорбент+½Cl- + Na+ + OH-
Из приведенной схемы видно, что в ходе адсорбции ионов может изменяться рН среды (в раствор переходят H+ или OH- ионы), раствор приобретает кислую или щелочную реакцию, такой вид адсорбции называется гидролитический.
Так как обменная адсорбция является химической, то обмен ионов происходит в строго эквивалентных соотношениях.
Обменные ионы на твердой поверхности обладают определенной величиной и знаком заряда, поэтому, чтобы не нарушался двойной электрический слой (ДЭС), обменными ионами из раствора, могут быть только ионы одного и того же знака. При этом не должна изменяться и величина заряда поверхности. Таким образом, обменная адсорбция может быть только анионообменной или катионообменной.
Явления обменной адсорбции играют важную роль в процессах, происходящих в почвах. Обменным комплексом почв является почвенный поглощающий комплекс (ППК), состоящий из коллоидных частиц, заряженных отрицательно. Обменными ионами почвы являются катионы. Важнейшие свойства почвы: водопроницаемость, влагоемкость, набухаемость, структура, рН почвенного раствора и др. – определяются составом адсорбированных ионов. Например, почвы, содержащие в составе обменных катионов значительное количество ионов натрия, приобретают особые, так называемые, “солонцовые свойства”. Они отличаются высокой дисперсностью, плотным сложением, высокой щелочностью, повышенной набухаемостью и вязкостью, малой водопроницаемостью. Эти почвы трудно обрабатываются и, несмотря на большой запас питательных веществ, мало плодородны. Если же в состав обменных катионов почвы входят преимущественно ионы кальция, то такие почвы обладают хорошей структурой, малой распыленностью, хорошей водо- и воздухопроницаемостью. Эти почвы относятся к наиболее плодородным. Примером почв с большим содержанием обменного кальция и прекрасными физико-химическими свойствами являются черноземные почвы.
Ионообменные процессы в почвах можно представить следующей схемой:
[ППК]-2Na+ + Са2+ + SO42- = [ППК]- Cа2+ + Na2SO4
Б.П. Никольский и Е.Н. Гапон предложили уравнение, описывающее обменную адсорбцию:
Здесь g1 и g2 – количество г-моль (г-экв) адсорбированных и десорбированных ионов единицей массы адсорбента, а1 и а2 – активности обменивающихся ионов в растворе при равновесии; z1 и z2 – заряд ионов, К – константа данного адсорбционного процесса.
Явление адсорбции находит широкое применение в промышленности и сельском хозяйстве. Так, на активированном угле производят адсорбционную очистку (рафинирование) сиропа сахарозы. Именно силы адсорбции удерживают ионы минеральных удобрений (К+, РО4-3и т.п.) и молекулы (мочевины) в почве. Адсорбция мочевины физическая, молекулы её слабо удерживаются почвой. Поэтому мочевину, чтобы её не вынесло весенним паводком, вносят обычно весной. Калийные удобрения можно вносить в почву и осенью, так как адсорбция ионов К+ вызывается химическими силами (ионные связи) и она прочная.
В общем случае адсорбция является функцией давления Р (для газов) или концентрации С (для жидких растворов) и температуры, т.е. изображается плоскостью в координатах Г = f(C,T). Обычно один из параметров поддерживают постоянным и адсорбцию графически изображают в виде кривых.
Количественная зависимость, устанавливаемая между адсорбентом и адсорбтивом при постоянной температуре в виде уравнения или кривой, называется изотермой адсорбции.
Cуществует несколько типов изотерм адсорбции - простейшими уравнениями для описания адсорбции являются уравнение Фрейндлиха и уравнение Ленгмюра.
Изотерма адсорбции по Фрейндлиху. Адсорбция растворенного вещества на твердой поверхности подчиняется определенной закономерности, согласно которой концентрация адсорбированного вещества возрастает не пропорционально его концентрации в растворе, а значительно медленнее, и пропорциональна корню n-ой степени из концентрации раствора. Эта зависимость при постоянной температуре может быть представлена следующем уравнением:
Х/m = К С1/n
где Х – количество (моль) вещества, адсорбированного m г адсорбента: С- равновесная концентрация; К и 1/n – эмпирические константы, характерные для данных адсорбента и адсорбата, значение 1/n колеблется между 0,1 – 0,7. Данное уравнение известно под названием изотермы адсорбции и имеет вид параболы.
Для графического построения изотермы адсорбции по Фрейндлиху на оси абсцисс откладывается равновесная концентрация в ммоль/л, а на оси ординат – величина адсорбции на единицу поверхности Х/m в ммоль/грамм. На рисунке 7 показано графическое изображение уравнения Фрейндлиха.
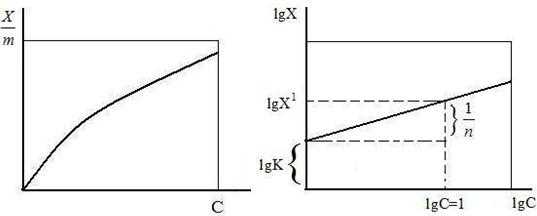 |
Рис. 7. Изотерма адсорбции по Фрейндлиху Рис.8. Графическое определение постоянных адсорбции уравнения Фрейндлиха
Логарифмируя данное уравнение, можно найти значения постоянных К и 1/n:
lg X/m = lg K + 1/n lg C
Если на абсциссе отложить величину lg C, а на ординате – величину lg X/m, то мы получаем прямую, отсекающую на оси ординат отрезок, равный lgК, а тангенс угла наклона этой прямой к абсциссе дает значение 1/n.
Графически значение 1/n находят следующим образом: из точки lgС = 1 восстанавливают перпендикуляр к прямой. Из точки пересечения опускают перпендикуляр на ось ординат – точка lgХ1
1/n будет равна разности (lgХ1 - lgК), где lgХ1 –ординаты точки, абсцисса которой lgС1 = 1 (рис. 8). Уравнение Фрейндлиха находит широкое применение, но имеет и ряд недостатков, т.к. применимо только в области средних концентраций.
Изотерма адсорбции по Ленгмюру. В 1917 году Ленгмюр предложил более удобное уравнение адсорбции, которое выведено им на основании молекулярно-кинетической теории газов.
Изотерма адсорбции по Ленгмюру является уравнением гиперболы и может быть представлена в виде:
Г = Г¥ ×
где Г – величина адсорбции на единицу поверхности; Г¥ - предельное количество вещества, адсорбированного единицей поверхности при полном насыщении поверхности; С – равновесная концентрация. В уравнении Ленгмюра также имеются две константы - Г¥ и К. Графическое изображение изотермы адсорбции Ленгмюра представлено на рисунке 9.
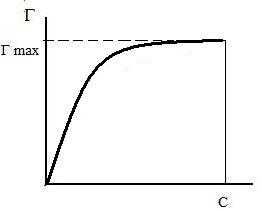 | 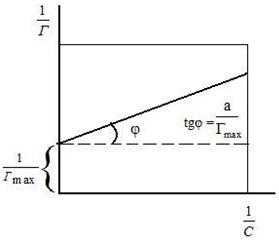 | ||
Рис. 9. Изотерма адсорбции по Ленгмюру Рис.10. Графическое определение постоянных адсорбции уравнения Ленгмюра
Вывод уравнения Ленгмюра основан на предположении о мономолекулярном слое адсорбированного вещества. Молекулы адсорбата поглощаются лишь на отдельных точках поверхности адсорбента. Эти точки – активные центры – обладают остаточными валентностями и способны связывать только одну молекулу адсорбата. Заполнение всех активных центров соответствует насыщению поверхности. Таким образом, насыщенный адсорбционный слой мономолекулярен, т.е. только один слой молекул связан силами молекулярного сцепления с поверхностью. На твердой поверхности при постоянной температуре устанавливается подвижное равновесие между молекулами, адсорбирующимися на поверхности, и молекулами, отрывающимися от поверхности. Концентрация адсорбата на момент установления динамического адсорбционного равновесия называется равновесной. Следовательно, активные центры удерживают адсорбированные молекулы только в течение определенного промежутка времени.
Вывод уравнения Ленгмюра основан на предположении о мономолекулярном слое адсорбированного вещества. Однако адсорбция может быть и многослойной, тогда уравнение изотермы адсорбции Ленгмюра становится неприменимой, более точными являются так называемые S-образные изотермы БЭТ (по фамилиям ученых Браунер, Эммет, Теллер), одна из которых представлена на рисунке 11. Изотерме адсорбции Ленгмюра соответствует только нижняя часть (ОА) кривой. S-образные изотермы и соответствующие им уравнения особенно часто используются для случаев адсорбции паров на твердых поверхностях.
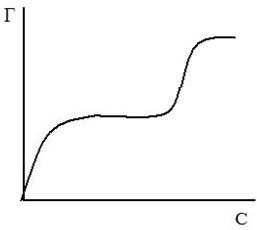 |
Рис.11. S-образная изотерма БЭТ
Практическое значение явлений адсорбции. Явления адсорбции находят широкое применение в промышленности, технике, биологии, медицине, ветеринарии. Так, например, с адсорбционными процессами мы встречаемся в химической и пищевой промышленности при сахароварении, очистке соков и вин, при ректификации спирта, в текстильной промышленности при крашении тканей.
Среди различных адсорбентов одно из первых мест занимает уголь. Древесный, костяной, кровяной и другие сорта углей получили широкое распространение как адсорбенты в самых различных областях.
Адсорбция широко используется в медицине с лечебными целями. Адсорбенты способны связывать многие ядовитые вещества, поэтому многие коллоиды применяют в качестве противоядий. Так, например, коллоидное железо употребляется при мышьяковом отравлении. Для этих же целей употребляются различные мелко растертые порошки, чаще всего животный и древесный уголь.
Явления адсорбции имеют большое биологическое значение. В организме имеется огромное количество поверхностей, на которых идут адсорбционные процессы. Это, во-первых, поверхности раздела между организмом и средой, затем поверхности стенок сосудов, разнообразнейшие мембраны, поверхности клеток, поверхности ядер, поверхности вакуолей и, наконец, поверхности коллоидных частиц протоплазмы. На всех этих поверхностях в процессе обмена веществ могут адсорбироваться различные вещества.
Если для высших организмов поверхность раздела между организмом и средой адсорбционной роли почти не играет, то для организмов, живущих в воде, особенно для низших организмов, эта поверхность имеет весьма существенное значение в процессах питания и проникновения пищевых веществ.
По исследованием Траубе поверхностно-активные вещества легко проникают в клетку, а пищевые вещества, как правило, поверхностно-активны. Поэтому, первым этапом усвоения, является адсорбция питательных веществ, после чего начинается процесс химического превращения.
Процессы обмена веществ в организме осуществляются посредством разнообразных специфических катализаторов-ферментов, являющихся коллоидами. Первые стадии действия фермента сводятся к адсорбции субстрата на поверхности ферментного комплекса, и только после этого фермент проявляет свое специфическое каталитическое действие. Явления адсорбции широко распространены в жидкостях и тканях организма. Такие важные жизненные процессы как, питание, дыхание, выделение и другие процессы жизнедеятельности организма сопровождаются многообразными явлениями адсорбции.
Таким образом, если учесть огромнейшие величины поверхностей раздела у высших организмов и адсорбционные возможности этих поверхностей, то будет понятно все то значение, которое имеет адсорбция в процессах жизнедеятельности.
Что такое адсорбция и абсорбция?
Абсорбция — поглощение газов или паров из газовых или паровых смесей ЖИДКИМИ поглотителями, называемыми абсорбентами. Этот процесс является избирательным и обратимым, что дает возможность применять его не только с целью получения растворов газов в жидкостях, но также и для разделения газовых или паровых смесей. В последнем случае после избирательной абсорбции одного или нескольких компонентов из газовой или паровой смеси проводят десорбцию — выделение этих компонентов из жидкости — и таким образом осуществляют разделение. Регенерированный абсорбент вновь возвращается на абсорбцию (круговой процесс) . Различают физическую абсорбцию и хемосорбцию. При физической абсорбции растворение газа не сопровождается химической реакцией. При хемосорбции абсорбируемый компонент вступает в химическую реакцию в жидкой фазе. Адсорбция — поглощение газов или паров из газовых смесей или растворенных веществ из растворов ТВЕРДЫМИ поглотителями, называемыми адсорбентами. Особенностью процессов адсорбции являются избирательность и обратимость. Благодаря этой особенности процесса возможно поглощение из паро-газовых смесей или растворов одного или нескольких компонентов, а затем в других условиях, десорбирование их, т. е. выделение нужного компонента из твердой фазы в более или менее чистом виде. Адсорбция широко распространена в различных отраслях химической технологии как метод разделения смесей. В качестве конкретных примеров можно указать выделение бензола из паро-газовых смесей, разделение смесей газообразных углеводородов, сушку воздуха, очистку жидких нефтепродуктов от растворенных в них примесей и т. д. Природа сил, вызывающих адсорбцию, может быть различной. При адсорбции происходит концентрация молекул поглощаемого вещества на поверхности адсорбента под действием ван-дер-ваальсовых сил. Этот процесс часто сопровождается конденсацией паров поглощаемого вещества в капиллярных порах адсорбента, присоединением молекул поглощаемого вещества по месту ненасыщенных валентностей элементов, составляющих кристаллическую решетку адсорбента, и другими процессами. Независимо от природы адсорбционных сил на величину адсорбции влияют следующие факторы: природа поглощаемого вещества, температура, давление и примеси в фазе, из которой поглощается вещество.
первый выделяет влагу, другой поглащает
<a rel="nofollow" href="http://slovari.yandex.ru/search.xml?text=адсорбция+" target="_blank">http://slovari.yandex.ru/search.xml?text=адсорбция+</a> Вот тут, в словаре, есть точное определение. Вообще, адсорбция - осаждение на поверхности, а абсорбция - всасывание внутрь.. .приблизительно так....
Это тебе для гемостаза? Если да, то адсорбция - фильтрация, а абсорбция - прилипание или склеивание.
понимаю, что запоздал с ответом, но может другим поможет) <img src="//otvet.imgsmail.ru/download/u_cab59371e9ecc19d6a00e27e3533197a_800.png" alt="" data-lsrc="//otvet.imgsmail.ru/download/u_cab59371e9ecc19d6a00e27e3533197a_120x120.png" data-big="1">
АДСОРБЦИЯ — Большая Медицинская Энциклопедия
АДСОРБЦИЯ (adsorptio; латинский ad — на, при и sorbeo — поглощаю) — поглощение газов, паров или растворенных веществ поверхностью твердого тела или жидкости.Тело, на поверхности которого происходит адсорбция, называют адсорбентом, адсорбируемое вещество — адсорбтивом или адсорбатом. Адсорбция газов твердыми телами (древесным углем) была открыта шведским химиком Шееле (С. W. Scheelе) в 1773 году и независимо от него итальянцем Фонтаной (F. Foiitana) в 1777 году; адсорбция веществ из растворов древесным углем — русским химиком академиком Т. Е. Ловицем в 1785 году. Возможность адсорбции на поверхности жидкости и связь этого явления с поверхностным натяжением впервые теоретически были доказаны американским математиком и физиком Гиббсом (J. W. Gibbs) в 1876 году Впоследствии было показано, что адсорбция относится к чрезвычайно распространенным явлениям и обнаруживается почти всюду, где газы, пары и растворенные вещества находятся в контакте с поверхностью жидкости или твердого тела.
Различают физическую и химическую адсорбцию. В первом случае адсорбированные молекулы сохраняют свою индивидуальность; при химической адсорбции, называемой также хемосорбцией, молекула адсорбируемого вещества вступает в химическую связь с поверхностью адсорбента. Физическая адсорбция, которую обычно называют просто адсорбция, представляет собой обратимый процесс, заканчивающийся установлением адсорбционного равновесия, при котором скорость адсорбции равна скорости обратного процесса — десорбции. Хемосорбция, как правило, необратима.
Адсорбция часто сопровождается абсорбцией (см.), хемосорбцией и конденсацией паров адсорбтива в порах адсорбента. Во всех этих случаях сложный процесс поглощения называют сорбцией (см.).
Величину адсорбции на поверхности жидкости, граничащей с газом или с другой жидкостью, непосредственно не измеряют, а вычисляют с помощью уравнения Гиббса:
где Г — количество адсорбированного вещества в молях на 1 см2 поверхности жидкости, С — молярная концентрация адсорбтива в жидкости, R — газовая постоянная из уравнения Клапейрона—Менделеева, Т — абсолютная температура, Δσ — изменение поверхностного натяжения, соответствующее изменению концентрации адсорбтива на ΔС.
Величину адсорбции газа или растворенного вещества на твердом адсорбенте измеряют непосредственно и выражают в молях адсорбированного вещества на 1 г адсорбента. Количество адсорбированного газа обычно определяют по привесу адсорбента, поглотившего газ; величину адсорбции растворенного вещества — по уменьшению его концентрации в растворе.
Зависимость величины адсорбции при постоянной температуре от равновесной концентрации адсорбтива, выраженную графически или в виде уравнения, называют изотермой адсорбции. На рис. представлена типичная экспериментальная изотерма адсорбции. При очень малых концентрациях величина адсорбции пропорциональна концентрации, что находит свое выражение в прямолинейном ходе изотермы адсорбции в области малых концентраций. С дальнейшим ростом концентрации рост величины адсорбции замедляется. При очень больших концентрациях величина адсорбции достигает предельного значения, что объясняется насыщением поверхности адсорбента молекулами адсорбтива, образующими мономолекулярный адсорбционный слой. В тех случаях, когда адсорбционный слой полимолекулярен или адсорбция осложнена капиллярной конденсацией (см. Сорбция), изотерма поглощения имеет более сложный вид.
На практике для аналитического выражения изотермы адсорбция при средних значениях концентраций обычно пользуются уравнением Фрейндлиха:
a = kcn,
где а — величина адсорбции в молях на 1 г адсорбента, с — концентрация в молях на 1 л, k и n — константы. Константа k численно равна величине адсорбции при концентрации, равной 1; величина ее определяет высоту кривой над осью абсцисс и меняется в широких пределах в зависимости от природы адсорбента и адсорбтива. Константа п определяет кривизну изотермы; ее численная величина мало изменяется с природой адсорбента и адсорбтива и колеблется в пределах от 0,1 до 0,6. Уравнение Фрейндлиха графически представляет собой параболическую кривую (рис.).
Рис. Изотерма адсорбции : a — величина адсорбции; с — равновесная концентрация; аsub∞/sub — предельная величина адсорбции; 0—1 — область малых концентраций; 1—2 — область средних концентраций; 2—3 — область больших концентрацийДля более широкой области концентраций чаще применяют уравнение Лангмюра:
где а и с имеют те же значения, что и в уравнении Фрейндлиха, а∞ и α — константы, численные значения которых зависят от природы адсорбента и адсорбтива. Константа их равна предельной величине адсорбции, соответствующей полному насыщению поверхности поглотителя молекулами адсорбтива. Константа α равна отношению константы скорости десорбции к константе скорости адсорбции.
Помимо концентрации адсорбтива, величина адсорбции зависит от природы адсорбента и адсорбтива; Адсорбция возрастает с увеличением удельной поверхности поглотителя. Для органических веществ одного и того же гомологического ряда величина адсорбции возрастает приблизительно в 3 раза с увеличением углеводородной цепи на одну группу CH2 (правило Дюкло—Траубе). Величина адсорбции, как правило, уменьшается с повышением температуры. Величина адсорбции из растворов зависит от природы растворителя: чем лучше вещество растворяется в данном растворителе, тем хуже оно из него адсорбируется.
Адсорбция из растворов сильных электролитов подразделяют на следующие виды: эквивалентная адсорбция, при которой катионы и анионы электролита адсорбируются в эквивалентных количествах; избирательная адсорбция — в этом случае избирательно адсорбируются или катионы, или анионы электролита; поверхность адсорбента при этом приобретает соответственно положительный или отрицательный электрический заряд. Ионообменная адсорбция представляет собой обмен катионов или анионов между адсорбентом и раствором (см. Иониты).
В насыщенном адсорбционном слое молекулы адсорбтива ориентированы, например, на поверхности водных растворов полярные группы адсорбированных молекул погружены в раствор. Представление об ориентации молекул в насыщенном адсорбционном слое сыграло большую роль при изучении структуры биологических мембран.
Практическое значение адсорбционных явлений очень велико. Адсорбция лежит в основе крашения тканей, дубления кож и так далее. Адсорбция является начальной стадией процесса поглощения любых веществ клетками и тканями. С адсорбцией тесно связаны также процессы взаимодействия ферментов с субстратами, антител с антигенами, поляризации и деполяризации биологических мембран.
Адсорбция играет основную роль при протекании многих каталитических реакций (см. Катализ) и в химии коллоидных растворов.
Ряд адсорбентов (уголь, каолин, гидроокись железа, ионообменные смолы и другие) применяют как противоядия (см.) для связывания ядов и токсинов, попавших в желудочно-кишечный тракт, а также для адсорбции кишечных газов при метеоризме (см.). Активированный древесный уголь используют как адсорбент в военных и промышленных противогазах. В технике адсорбции применяют для очистки веществ, в том числе и лекарственных, регенерации ценных летучих растворителей, для разделения и анализа сложных смесей (см. Хроматография).
См. также Поверхностное натяжение.
Библиография: Адам Н. К. Физика и химия поверхностей, пер. с англ., М.—Л., 1947; Бладергрён В. Физическая химия в медицине и биологии, пер. с нем., М., 1951; Брунауэр С. Адсорбция газов и паров, пер. с англ., т. 1, М., 1948, библиогр.; Мак Бен Д. В. Сорбция газов и паров твердыми телами, пер. с англ., М.—Л., 1934.
В. П. Мишин.
адсорбция - это... Что такое адсорбция?
АДСОРБЦИЯ — (от лат. ad на, при и sorbeo поглощаю), процесс, приводящий к аномально высокой концентрации в ва (а д с о р б а т а) из газообразной или жидкой среды на поверхности её раздела с жидкостью или тв. телом (а д с о р б е н т о м). Частный случай… … Физическая энциклопедия
Адсорбция — [adsorptio всасывание, поглощение] поглощение поверхностью фазово инородного тела (адсорбента) каких либо веществ (адсорбатов) из смежной газовой или жидкой среды, протекающее на границе раздела фаз. А. из газовой фазы или из растворов нашла… … Геологическая энциклопедия
АДСОРБЦИЯ — (от лат. ad на при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. Адсорбенты обычно имеют большую удельную поверхность до нескольких сотен м²/г. Физическая адсорбция… … Большой Энциклопедический словарь
адсорбция — Самопроизвольное изменение концентрации раствора или газовой смеси вблизи поверхности раздела фаз. Примечание Адсорбирующее твердое тело называется адсорбентом, адсорбируемое вещество адсорбатом. [ГОСТ 17567 81] адсорбция Удерживание физическими… … Справочник технического переводчика
Адсорбция — – поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. [Терминологический словарь по бетону и железобетону. ФГУП «НИЦ «Строительство» НИИЖБ и м. А. А. Гвоздева, Москва, 2007 г. 110 стр.]… … Энциклопедия терминов, определений и пояснений строительных материалов
АДСОРБЦИЯ — (от лат. ad на и sorbeo поглощаю) поглощение различных веществ из растворов или воздушной среды поверхностями твердых тел. Может быть физической или химической (с образованием химических соединений), чаще всего сопровождается выделением тепла.… … Экологический словарь
адсорбция — и, ж. adsorption f. <лат. ad при + sorbere поглощать, всасывать. спец. Поглощение, всасывание вещества из раствора или газа поверхностью твердого тела или поверхностным слоем жидкости. Явления адсорбции. Адсорбция газов. Работы по изучению… … Исторический словарь галлицизмов русского языка
адсорбция — – самопроизвольное изменение концентрации растворенного вещества на границе раздела фаз. Общая химия : учебник / А. В. Жолнин [1] Адсорбция – поглощение вещества поверхностью твердого или жидкого сорбента. Словарь по аналитической химии [3] … Химические термины
АДСОРБЦИЯ — (от латинского ad на, при и sorbeo поглощаю), поглощение газов, паров или жидкостей поверхностным слоем твердого тела (адсорбента) или жидкости. В промышленности адсорбцию осуществляют в аппаратах адсорберах. На адсорбции основаны осушка газов,… … Современная энциклопедия
АДСОРБЦИЯ — АДСОРБЦИЯ, притяжение газа или жидкости к поверхности твердого тела или жидкости, в отличие от абсорбции, при которой подразумевается проникновение одного вещества в другое (как, например, губка пропитывается водой). Количество адсорбируемого… … Научно-технический энциклопедический словарь