Блокатор протонной помпы что это такое
Ингибиторы протонной помпы. Секреты эффективности. Отличия. Вопросы безопасности

Здравствуйте, дорогие фарм. труженики!
Вы просили меня разобрать тему ингибиторов протонной помпы, что я сегодня и сделаю.
Мы разберем:
- Что такое протонная помпа? Как она работает?
- Когда нужны ингибиторы протонной помпы (ИПП)? Их механизм действия.
- Общая характеристика группы.
- Когда ИПП могут оказаться неэффективными?
- Самые частые побочные эффекты.
- Чем они отличаются друг от друга? Их особенности.
- Что может быть от длительного применения ИПП?
Как всегда, лезть в фармацевтические дебри я не буду. Объясню маскимально просто и понятно.
Поехали!
Что такое протонная помпа?
В стенке желудка есть клетки, которых вырабатывают соляную кислоту. Они называются париетальными, или обкладочными.
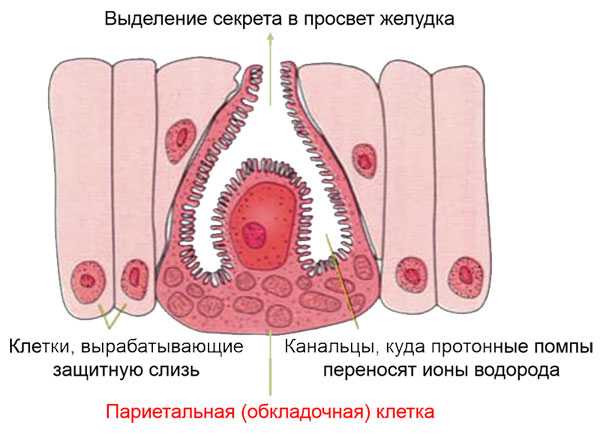
Секреция соляной кислоты была бы невозможна без фермента с длинным и мудрёным названием: «водородно-калиевая аденозинтрифосфатаза, или Н⁺/К⁺-АТФаза». А по-простому, протонная помпа, или протонный насос, или водородная помпа.
Запоминаем: протонная помпа – это фермент, который контролирует образование париетальными (обкладочными) клетками желудка соляной кислоты.
Как работает протонный насос?
Продукцию соляной кислоты запускают 3 вещества: гастрин, гистамин и ацетилхолин.
Гастрин – один из гормонов пищеварительной системы.
Гистамин – это не только провокатор аллергических реакций, но еще и регулятор многих физиологических процессов, включая пищеварение.
Ацетилхолин – представитель парасимпатической нервной системы. Отвечает за интеллектуальные способности, нервно-мышечную передачу, а через свои рецепторы, которые есть во многих органах, и за работу этих органов, в том числе за секрецию соляной кислоты.
Эти вещества начинают выделяться, когда мы думаем о еде, видим пищу, ощущаем ее запах, когда первые порции еды попадают в рот.
— А причём здесь протонная помпа? — спросите вы.
Все протонные помпы находятся внутри париетальных клеток желудка в неактивном состоянии.
Под действием вкуса и запаха пищи выделяются упомянутые выше гистамин, гастрин и ацетилхолин, которые «выталкивают» протонные помпы из клеток на поверхность мембран секреторных канальцев.
И те принимаются за дело. За счет энергии АТФ они переносят ионы водорода из париетальных клеток в канальцы. Ионы водорода встречаются здесь с ионами хлора. В результате образуется соляная кислота. Так выглядит работа протонных помп в самом упрощенном виде.
Роль соляной кислоты в пищеварении
Чтобы понимать, почему ингибиторы протонной помпы нельзя принимать всем подряд, вспомним, что делает соляная кислота:
- Подготавливает белки пищи к их дальнейшей обработке. Изменяется структура их молекул, белки набухают.
- Создает идеальные условия для работы протеолитических ферментов (ферментов, расщепляющих белки).
- При ее участии пепсиноген превращается в пепсин – фермент, необходимый для полноценного переваривания белков.
- «Подготавливает» для работы двенадцатиперстную кишку – раздражает ее рецепторы и как бы передает эстафетную палочку следующему отделу ЖКТ в переваривании пищи.
- Регулирует секрецию желудочных и поджелудочных желез.
- Стимулирует двигательную активность желудка.
- Обеспечивает противомикробную защиту от патогенных бактерий, поступающих с пищей.
А теперь, глядя на этот список, попробуйте представить, что будет, если выработка соляной кислоты затормозится.
Представили?
Нет?
Тогда представим вместе:
- Нарушится переваривание белков.
- Ухудшится переваривание пищи в других отделах пищеварительного тракта.
- Нарушится моторика желудка.
- Увеличится вероятность бактериальных инфекций ЖКТ.
А значит, как минимум, возможны боли в животе, диарея или запоры, метеоризм, отрыжка.
Что такое ингибиторы протонной помпы?
Ингибиторы протонной помпы – это препараты, подавляющие секрецию соляной кислоты.
Помните, какие еще препараты влияют на кислотность в желудке?
Напомню:
- Антациды. Попадая в желудок, они нейтрализуют соляную кислоту и уменьшают симптомы, связанные с ее избытком или забросом в пищевод: изжога, жжение за грудиной, боли, отрыжка кислым и пр. Они действуют быстро, но кратковременно, т.к. на образование соляной кислоты не влияют.
- Блокаторы Н2-гистаминовых рецепторов (Ранитидин, Фамотидин). Связываются с Н2-гистаминовыми рецепторами париетальных клеток слизистой желудка, гистамин к ним не может прицепиться, и благодаря этому продукция соляной кислоты уменьшается. Однако, они не всегда хорошо справляются со своей основной задачей, поскольку «отключают» только гистамин. Но ведь остаются еще гастрин и ацетилхолин, которые тоже запускают секрецию соляной кислоты. К тому же, h3-гистаминоблокаторы вызывают массу побочных, иногда очень серьезных (гепатит, гемолитическую анемию, аритмию, аменорею и пр.).
- М-холинолитики. Блокируют м-холинорецепторы в области окончаний парасимпатических нервов и «выключают» действие ацетилхолина на желудок. Попутно они подавляют его действие и на другие органы, а это далеко не всегда нужно.
Представитель М-холинолитиков – Гастроцепин. Но его действие на желудочную секрецию оставляло желать лучшего, и он ушел в историю.
И, наконец, не так давно на рынке появилась группа ингибиторов протонной помпы.
Как работают ингибиторы протонной помпы?
Они поступают в пищеварительный тракт, всасываются в кровь, с кровью попадают в канальцы париетальных клеток, активируются под действием кислоты, связываются с протонными помпами и за счет этого блокируют перенос ими ионов водорода в просвет канальцев. Иными словами, они «выключают» протонные помпы, и те уже не могут влиять на выработку соляной кислоты.
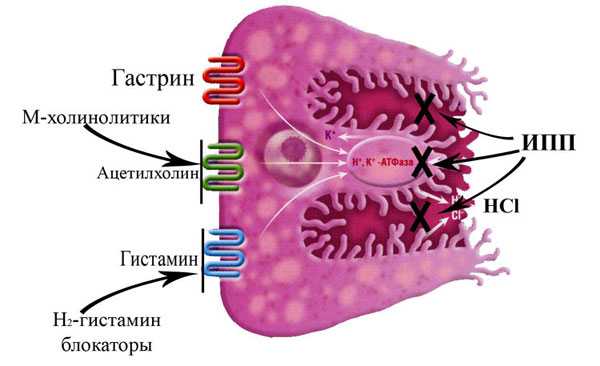
Главное, что нужно из этого запомнить:
1. Чтобы ИПП оказали свой эффект они должны быть активированы.
2. Активация происходит благодаря определенной pH желудка. Причем, одни препараты активируются при pH, равной 1-2, а другие — при более высоких значениях pH.
О чем это говорит?
О том, что если у человека пониженная кислотность желудка, а ему назначили ингибитор протонной помпы, не каждый препарат сработает.
Очень важно!
Часто ингибиторы протонного насоса принимают эпизодически для снятия изжоги. Это в корне неверно!
Разовое и первые применения ингибитора протонной помпы не дадут ожидаемого эффекта. Все ИПП имеют довольно короткий период полувыведения. В первый прием «выключаются» те протонные помпы, которые активны в данный момент.
Во второй прием – те, которые стали активны уже после приема первой дозы. В третий прием – те, которые активировались после второго применения.
И так далее.
Протонный насос – это одноразовый фермент. Если он вышел на поверхность клетки и сделал свою работу, обратно в клетку он не уходит. Он погибает. А времени для синтеза новых протонных насосов требуется до 96 часов.
Поэтому для получения ощутимого эффекта ИПП принимают ежедневно минимум неделю.
Основные ситуации, когда назначаются ИПП
Когда нужно снижать выработку соляной кислоты?
- При язвенной болезни желудка и 12 п.к. – чтобы дать возможность язве зарубцеваться. Кислота этому мешает.
- При гастроэзофагеальной рефлюксной болезни – чтобы уменьшить агрессивность желудочного содержимого, которое забрасывается в пищевод. Иначе можно заработать его ожог, эрозии, язвы.
- Для профилактики образования эрозий и язв на фоне приема нестероидных противовоспалительных препаратов, особенно, неселективных. Напомню, что такие НПВС без разбора блокируют фермент циклооксигеназу 1 и 2 типа (ЦОГ-1 и ЦОГ-2). Но ЦОГ-1 нужна нам для выработки веществ, защищающих слизистую желудка от повреждений соляной кислотой. Если ЦОГ-1 блокируется, защитной слизи вырабатывается меньше, и многократно повышается риск повреждения слизистой желудка соляной кислотой.
Когда еще назначают ИПП?
- В схемах эрадикации Helicobacter pylori, т.к. чем выше pH в желудке, тем более чувствительными к антибиотикам становятся бактерии H.Pylori.
- При назначении антиагрегантов, особенно, в комбинации с антикоагулянтами, т.к. это в разы повышает риск желудочно-кишечных кровотечений.
Очень важно!
Чтобы ингибитор протонной помпы гарантированно оказал свое лечебное действие, в желудке должна быть pH на уровне 1-2.
О нормальной кислотности говорят, когда pH в просвете тела желудка натощак = 1,5-2.
О пониженной, если pH больше 2,5.
Нейтральная кислотность – это pH = 7. Все, что меньше этой цифры – кислая среда, все, что больше – щелочная.
Общая характеристика ингибиторов протонной помпы
- Все ИПП – пролекарства. Активируются в кислой среде париетальных клеток желудка.
- Малоэффективны при первом применении, т.к. протонные помпы блокируются постепенно.
- Кислоточувствительны – в кислой среде желудка разрушаются. Поэтому их выпускают либо в кишечнорастворимых капсулах, либо в таблетках, покрытых кишечнорастворимой оболочкой.
- Если на упаковке не указано, что капсула кишечнорастворимая, это значит, что внутри капсулы находятся гранулы, или пеллеты, каждая из которых покрыта кишечнорастворимой оболочкой.
- ИПП блокируют протонные помпы НЕ при непосредственном контакте с клетками, вырабатывающими соляную кислоту, а попадая в них с током крови.
- Восстановление секреции соляной кислоты происходит после того, как на мембране канальцев париетальных клеток желудка оказались новые протонные помпы, которые еще не успел связать и «выключить» из работы ингибитор протонной помпы.
- Имеют короткий период полувыведения: 0,5-2 часа.
- Принимаются по 1 таблетке или капсуле 1-2 раза в день в зависимости от заболевания. Если назначена одна таблетка или капсула в день, то лучше принимать ее утром, т.к. 70% протонных помп активируется после утреннего приема пищи.
Самые частые побочные эффекты
- Диарея или запор.
- Тошнота.
- Рвота.
- Боли в животе.
- Головная боль.
- Головокружение.
- Нарушения сна.
- Боли в мышцах, суставах.
- Кожная сыпь.
Чем отличаются друг от друга ингибиторы протонной помпы?
- Значением pH, при котором они превращаются из пролекарства в лекарство. При pH = 1-2 все ИПП активируются быстро. При pH = 3 в 2 раза снижается скорость активации пантопразола, при pH = 4 - омепразола, эзомепразола и лансопразола, при pH = 4,9 – рабепразола.
- Периодом полувыведения.
- Скоростью наступления эффекта.
- Дозировками.
- Продолжительностью антисекреторного действия.
- Разнообразием лекарственных форм.
- Лекарственными взаимодействиями.
- Возрастными ограничениями.
- Влиянием пищи на их всасывание.
- Количеством побочных.
Омепразол
Омепразол – «первенец» в группе ИПП.
Представители: Лосек МАПС, Омез, Гастрозол, Ультоп и др.
Лосек – это оригинальный омепразол.
Аббревиатура «МАПС» означает Multiple Unit Pellet System, или многокомпонентная пеллетная система.
Каждая таблетка содержит около 1000 кислотоустойчивых микрокапсул.
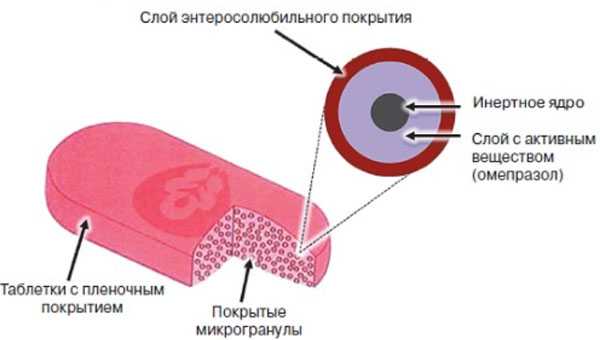
Она быстро распадается в желудке на микрокапсулы. Защищенные от желудочного сока специальным покрытием, пеллеты поступают в кишечник. Здесь под действием щелочной среды микрокапсулы растворяются, Омепразол высвобождается и всасывается в кровь.
Максимальная концентрация в крови достигается через 1-2 часа после приема, но ощутимый эффект будет только спустя 4 дня лечения, поскольку протоновые помпы «выключаются» не все сразу.
Безрецептурный Омепразол в дозировке 10 мг показан при симптомах ГЭРБ — изжоге, отрыжке кислым.
После однократного приема Омепразол начинает действовать уже в течение часа, и действие его длится 24 часа, несмотря на короткий период полувыведения. Это связано с особенностями фармакокинетики.
Период полувыведения составляет 30-90 минут.
Его можно принимать одновременно с антацидами.
Совместный прием ИПП с антацидами логичен: ИПП «выключает» протонные помпы постепенно, и сразу изжогу не снимет, а антацид действует быстро, но кратковременно. Вот вам еще одна возможность повышения среднего чека. Если покупателю от изжоги назначили только ИПП, предложите ему дополнительно антацид и объясните, что ИПП подействует не сразу, а антацид быстро.
Омепразол снижает активность клопидогрела. Это обязательно нужно учитывать, поскольку антиагрегант часто принимают сердечники. Но такая комбинация повышает риск инфарктов и инсультов.
Если необходимо быстро уменьшить кислотность желудочного сока, препарат вводят внутривенно в дозе 40 мг. В вашем ассортименте есть лиофилизаты для приготовления инфузионного раствора.
Омепразол оказывает бактерицидное действие на H.pylori.
Биодоступность после первого приема примерно 30-40%, повышается до 60% к седьмой дозе.
Оптимально его принимать за полчаса до еды, хотя в инструкциях некоторых производителей этот момент игнорируется. Но если вы внимательно читали механизм действия ИПП, то поняли, что протонные помпы активируются гистамином, гастрином и ацетилхолином, которые начинают выделяться перед едой и с первыми порциями пищи. Поэтому в идеале нужно, чтобы к приему пищи протонные помпы уже находились на мембранах париетальных клеток, а ИПП успел всосаться в кишечнике в кровь и «добежать» до этих самых клеток.
Стандартная суточная дозировка для лечения: 20-40 мг. Курс зависит от заболевания: от 2 до 8 недель.
Есть покупатели, которые испытывают трудности с проглатыванием таблеток, капсул.
Им можно предложить Омез Инста.

Это порошок для приготовления суспензии. А поскольку Омепразол в кислой среде желудка разрушается, производитель добавил в препарат соду (натрия гидрокарбонат). Содержимое пакетика разводят водой и принимают за полчаса до еды.
Честно говоря, это не лучшее средство для уменьшения секреции соляной кислоты, т.к. сода – всасывающийся антацид. Действует быстро, но очень кратковременно, и к тому же вызывает феномен кислотного рикошета, когда секреция HCl после окончания действия препарата повышается. Получается замкнутый круг.
Впрочем, в инструкциях к некоторым дженерикам Омепразола есть указание, что при трудностях с проглатыванием капсулы, ее можно вскрыть, смешать содержимое с водой, фруктовым соком, пюре, размешать и выпить. В таких капсулах омепразол заключен в кишечнорастворимые гранулы (пеллеты), поэтому не разрушится в желудке.
Если у больного — ГЭРБ (гастроэзофагеальная рефлюксная болезнь), и монопрепараты ИПП малоэффективны, врач может назначить комбинированное средство, в составе которого Омепразол и Домперидон: Омез Д или Омез ДСР с модифицированным высвобождением действующих веществ.
В такой комбинации Омепразол будет блокировать секрецию соляной кислоты, а Домперидон повысит тонус нижнего пищеводного сфинктера, чтобы уменьшить вероятность заброса желудочного содержимого в пищевод.
Омепразол на сегодняшний день – самый изученный ингибитор протонной помпы, поэтому может применяться даже у детей с 2 лет при рефлюксах, т.е. забросах кислого содержимого в желудок.
Водителям его следует принимать с большой осторожностью, т.к. он снижает концентрацию внимания и скорость реакции. Это касается большинства ИПП.
Дальше коротко об особенностях других ингибиторов протонной помпы.
Лансопразол
Представители: Ланцид, Эпикур.
Характеристики:
- Биодоступность его после первого применения 80-85% (самая высокая в этой группе) и остается постоянной при повторных приемах. Лечебный эффект развивается быстрее, чем при приеме других ИПП.
- Максимальная концентрация в крови достигается позже, чем у омепразола: через 1,5-2,2 часа.
- Максимальный лечебный эффект – тоже через 4 дня лечения.
- Длительность антисекреторного эффекта — больше 24 часов.
- Противопоказан детям до 18 лет.
- С осторожностью пожилым.
- Принимать его нужно до еды, т.к. прием пищи замедляет его всасывание.
- В отличие от Омепразола, пить его одновременно с антацидами нельзя. Нужно развести их во времени в 1-2 часа.
- Из побочных реакций в числе прочих может вызывать кашель, ринит, фарингит, инфекции верхних дыхательных путей, гриппоподобный синдром.
Рабепразол
Представители: Париет, Рабелок, Хайрабезол, Разо.
Характеристики:
- Биодоступность после первого приема чуть выше Омепразола – 52%, но при последующих приемах остается той же.
- Максимальная концентрация в крови – через 2-5 часов.
- Антисекреторное действие после приема первой дозы длится до 48 часов.
- Стабильный эффект развивается через 3 дня (чуть раньше, чем Омепразола).
- Детям разрешен с 12 лет.
- В отличие от Лансопразола, инфекций дыхательных путей не вызывает.
- Пища не влияет на его всасывание.
- Можно принимать его одновременно с антацидами.
- Важная «фишка»: рабепразол отличает низкая pH-селективность. Это означает, что он активируется и при pH 1-2, и при pH = 3-4. Он даже при pH, равном 5 будет работать, хотя и не так эффективно, как при более низких значениях pH.
Какое практическое значение это имеет?
Его можно назначить «вслепую», т.е. даже тогда, когда по каким-то причинам нет возможности определить pH желудка у конкретного пациента.
Но это – палка о двух концах. Как оказалось, протонные помпы есть не только в париетальных клетках желудка, но и в эпителии кишечника, желчного пузыря, почечных канальцах, эпителии роговицы, мышцах, даже клетках иммунной системы (нейтрофилах, макрофагах и пр.) Поэтому рабепразол теоретически может работать и в этих органах, где нет такой высокой кислотности. Следовательно, нарушится работа этих органов, и можно ожидать больше побочных эффектов.
Пантопразол
Представители: Контролок, Санпраз, Панум, Нольпаза.
- Биодоступность – 77%.
- Практически не активируется, если pH желудочного сока больше 3, т.е. по-хорошему должен назначаться только после pH-метрии (исследования, позволяющего определить pH желудка).
- Меньше других ИПП взаимодействует с лекарственными средствами.
- Эффективность не зависит от приема пищи.
- Противопоказан до 18 лет.
- Можно принимать одновременно с антацидами.
- Полностью убирает изжогу через 7 дней приема.
Эзомепразол
Представители: Нексиум, Эманера.
- Биодоступность его выше, чем омепразола.
- Медленнее других ИПП выводится из организма.
- Прием пищи замедляет его всасывание.
- Противопоказан до 12 лет.
Декслансопразол
Представитель: Дексилант.

- Производится по технологии двухфазного высвобождения действующего вещества. В капсуле единственного на сегодняшний день препарата декслансопразола –Дексиланта – 2 типа гранул, которые растворяются в разное время в зависимости от уровня pH. Поэтому его антисекреторное действие самое длительное. Вызывает 2 пика концентрации в крови: через 1-2 часа после приема и через 5-6 часов.
- Его биодоступность 76% и более.
- Противопоказан до 18 лет.
- Совместим с антацидами.
- В ряде случаев вызывает инфекции дыхательных путей, кашель, повышение АД.
Что может быть от длительного и бесконтрольного применения ИПП?
1. Феномен ночного кислотного прорыва. Причины его до конца неясны.
Он случается у 70-80% больных, принимающих ИПП 2 раза в сутки. pH ночью падает ниже 4, и это продолжается больше часа. Феномен ночного кислотного прорыва проявляется кашлем, болью в груди, изжогой.
2. Нарушение всасывания витамина В12 и развитие В12-дефицитной анемии.
3. Нарушение всасывания железа, которое тоже зависит от кислотности желудочного сока.
4. Развитие остеопороза и увеличение риска переломов из-за нарушения всасывания кальция.
5. Гипомагниемия и связанные с ней утомляемость, судороги, головокружение, аритмии.
6. Подавляя продукцию соляной кислоты в желудке, по механизму обратной связи все ИПП способствуют повышению уровня гастрина. А он стимулирует рост некоторых типов клеток, что повышает риск развития рака. Впрочем, пока убедительных доказательств этого нет.
7. Атрофия слизистой оболочки желудка.
8. Повышение риска бактериальных диарей, т.к. соляная кислота, помимо всего прочего, обеспечивает защиту от патогенных бактерий, попадающих в желудок.
9. Повышение риска инфарктов и инсультов при совместном применении ИПП (прежде всего, омепразола) с клопидогрелом, т.к. они блокируют ферменты, которые нужны для превращения клопидогрела в активную форму.
10. ИПП – зависимость. На одном форуме обнаружила шокирующую информацию, опубликованную врачом-гастроэнтерологом, кандидатом мед. наук. Суть вот в чем: как бы ни уверяли производители ингибиторов протонной помпы, что они не вызывают привыкания, вызывают. Причем, очень часто. Как ни парадоксально это звучит, ИПП могут спровоцировать развитие состояния, при котором часто сами назначаются. Речь идет о гастроэзофагеальном рефлюксе.
Это связано с тем, что они расслабляют нижний пищеводный сфинктер (мышечную «заслонку», которая препятствует забросу желудочного содержимого в пищевод), и возникают рефлюксы (забросы).
Человек начинает принимать ИПП, ему становится лучше. Через некоторое время он прекращает прием, и его, как выразился этот доктор, «ошпаривает кипятком изнутри».
Избавиться от ИПП-зависимости бывает непросто.
Резюме
Первое. ИПП имеют вполне определенные показания. Это кислотозависимые заболевания или профилактика повреждений слизистой ЖКТ на фоне приема препаратов, повышающих риск эрозий, язв, желудочных кровотечений.
Второе. Рекомендовать их при любой изжоге я бы тоже не стала. При эпизодической вполне подойдет антацид.
Третье. Сказать, какой ИПП лучше или хуже, сложно. Каждый имеет свои плюсы и минусы.
Четвертое. Идеального ИПП, к сожалению, на сегодняшний день нет.
Пятое. ИПП не так безопасны, как преподносят нам производители.
Это все, что я хотела вам сегодня сказать.
Если появились вопросы, пишите внизу в окошечке комментариев.
До новой встречи на блоге «Аптека для Человека»!
С любовью к вам, Марина Кузнецова
Ингибиторы (блокаторы) протонной помпы, список препаратов нового поколения
Нарушения пищеварительной системы, когда в желудке повышается кислотность, встречается у многих людей. В такие моменты для лечения врач назначает ингибиторы протонной помпы.
Что же такое ингибиторы протонной помпы и чем они могут помочь больному? Это специальный вид лекарственных средств, направленных на лечение кислотозависимых заболеваний желудка и кишечника, так как блокируют протонную помпу в клетках слизистой оболочки желудка и тем самым снижают активную выработку желудочного сока.
Какие вещества относятся к семейству
Ингибиторы протонной помпы, что же это такое?
Что такое ингибиторы – это блокаторы транспортировки ионов калия и водорода из клетки. Благодаря этому происходит снижение кислотности желудочного сока.
Ингибиторы называются так потому, что способны ингибировать (сдерживать) выработку желудочного сока.
Эти лекарственные средства при своём действии снижают уровень кислоты в желудочном соке и востребованы в лечении гастроэнтерологических заболеваний. Благодаря действию этих медикаментов, протонный насос, находящийся в мембране клетки, снижает свою работу, а значит и выработка кислоты замедляется, и больному становится легче.
Лекарства нового поколения облегчают лечение заболеваний пищеварительной системы.
Дополнительная информация! Первым лекарством, которое смогло снизить чрезмерную выработку желудочного сока, считается Омепразол.
Омепразол – распространённый препарат, многие принимают его для снятия симптомов в домашних условиях. Но стоит понимать, что у этого лекарства имеются и свои побочные эффекты, которые не позволяют принимать его долгое время.
Медицинскими работниками уже давно изготовлены и другие медикаменты, имеющие свойства снижения кислотности в желудке человека. В аптечных пунктах можно найти любой подходящий для этого препарат, у которого практически отсутствуют побочные эффекты.
К тому же для лечения некоторых заболеваний нужно использовать комбинированные средства. В их состав входят не только препараты ипп, но и антибактериальные препараты.
Омепразол – этот препарат был выпущен в продажу после того, как прошёл все испытания. Сразу после этого многие люди получили хорошее средство для снятия симптомов заболеваний кишечного тракта в момент, когда активируются клетки, отвечающие за выработку соляной кислоты.
Так как это средство стало хорошим помощником для лечения гастроэнтерологических болезней, было принято решение о создании других подобных препаратов, которые смогут облегчить состояние больного, а также будут обладать минимальными побочными действиями.
На данный момент в аптечных пунктах можно найти пять вариантов генерации ингибиторов протонной помпы:
- Омепразол;
- Лансопразол;
- Пантопразол;
- Рабепразол;
- Эзомепразол.
Дополнительная информация! Важно понимать, что препараты этого вида не могут полностью излечить от заболевания, а только способствуют длительной ремиссии. Чтобы болезнь вылечить, нужно пройти комплексное лечение, одной из частей которого и будут ингибиторы протонного насоса.

Самым действенным препаратом из всей группы считается Пантопразол. Используют его в основном в поликлиниках. Получается так потому, что чем позднее было произведено лекарство, тем более действенным оно является.
Как работают
Ингибиторы протонной помпы пользуются популярностью в лечении гастроэнтерологических болезней. Благодаря этим средствам при лечении язвы и рефлюкса пациентам удаётся достичь состояния длительной ремиссии.
Через три с половиной часа после приёма таблетки все активные элементы из тонкого кишечника попадают в плазму. А дальше попадают в париетальные клетки и начинают своё действие, в результате чего блокируют чрезмерную активность.
Работа ингибиторов протонной помпы хоть и разная, но отличается стабильностью. Действия ингибиторов не зависят от приёма пищи или иных медикаментов.
После второго приёма препарата Омепразол биодоступность начинает падать, при приёме Эзомепразола она, наоборот, увеличивается, при приёме последних лекарственных средств этого вида она остаётся стабильной от первого до последнего дня курса лечения.
Распад всех активных веществ происходит в печени человека, при этом они выводятся обычным способом – при мочеиспускании.

Стоит понимать, что у Омепразола период действия составляет не более 14 часов, в связи с этим больному для постоянного эффекта рекомендуется принимать его не менее двух раз в сутки. Длительное лечение может спровоцировать появление побочных действий.
В отличие от него, Эзомепразол имеет метаболическую устойчивость, что помогает принимать лекарства в течение 24 дней и при этом не беспокоиться о появлении побочных эффектов. Принимать препарат следует один раз в день, отпускается в аптеках без рецепта врача.
Пантопразол чаще всего используют для лечения в больницах в виде уколов. Обычно приём медикамента происходит совместно с антибактериальными препаратами, что помогает усилить эффект действия средства.
Механизм действия:
- всасывается из тонкого кишечника и попадает в кровяные каналы;
- скапливается в париетальных клетках;
- в кислой среде желудка протоны начинают связываться между собой;
- активируется протонная помпа под воздействием кислоты;
- группы SH протонного насоса связываются, и происходит ингибирование (сдерживание).
Препараты принимать стоит регулярно, одноразовое лечение не принесёт никаких результатов.
Важно! В медицинской практике протоновым насосом называется фермент, который находится в мембране клеток стенок желудка. Названия протоновый насос и протоновая помпа имеют одно и то же значение, они отвечают за кислотность желудочного сока.
Когда назначают
Лечащий врач рекомендует принимать ингибиторы протонной помпы после обнаружения болезни, которая вызвана кислотозависимым состоянием пищеварительной системы. Показания к применению ингибиторов протонного насоса:
- Гастрит – при воспалении слизистой оболочки желудка.
- При длительном приёме медицинских препаратов с большим содержанием гормонов.
- Когда человек проходит лечение нестероидными средствами различных воспалений.
- Если происходит заброс еды в пищевод из желудка.
Для лечения иных болезней пищеварительной системы используют ингибитор протонной помпы, эти препараты помогают снизить выработку желудочного сока.

Совместно с антибактериальными препаратами средства этой группы помогают быстрее вылечить заболевания пищеварительной системы, которые были вызваны бактерией Helicobacter pylori.
Лечение назначается только лечащим врачом после правильного диагностирования заболевания, так как для лечения многих болезней требуются сложные комбинации, в список которых входят ингибиторы:
- с метронидозолом;
- тинидазолом;
- аммоксицилином;
- кларитромицином.
Врач перед выбором препаратов проведёт некоторые исследования и измерит кислотность в верхних отделах желудка. Если одно средство не дало должного результата, врачом назначается иной препарат.
Так как у каждого человека организм имеет индивидуальные особенности, реакция на один препарат у людей может отличаться. У некоторых больных может быть замечена устойчивость к ингибиторам протонового насоса, связано это с генетическими способностями организма, а также осложнениями во время болезни.
Поэтому перед тем, как назначить полноценное лечение, врач проведёт анализ внутрижелудочного pH, а уже потом подберёт курс лечения и дозировку.
Классификация ингибиторов происходит в зависимости от того, для лечения какого заболевания они будут использоваться. При этом стоит помнить, что диагностировать болезнь правильно может только врач, поэтому стоит воздержаться от неосознанного приёма лекарственных средств самостоятельно.
Кому прием запрещен
Медикаменты, которые блокируют выработку желудочного сока, имеют ряд противопоказаний. Связано это с тем, что они оказывают влияние на клетки слизистой оболочки желудка, при этом проходят через плацентарный барьер, в результате чего они скапливаются в грудном молоке. Из-за этого в период беременности и кормления грудью женщинам не разрешается использование указанных лекарственных средств.

Сотрудники медицины не рекомендуют принимать эти лекарства и детям, не достигшим 12-летнего возраста. Так как до этого внутренние системы организма проходят становление правильной работы. А блокаторы водородной помпы приводят к серьёзному сбою.
Тем, кто обладает повышенной чувствительностью к элементам, входящим в состав лекарственных средств, приём медикаментов рекомендуется прекратить.
Какие побочные эффекты развиваются при приёме ингибиторов протоновой помпы:
- сонливость;
- постоянные головные боли;
- проблемы со сном;
- аллергия.
Если человека во время приёма лекарств беспокоят подобные явления, нужно рассказать об этом лечащему врачу, который подберёт другое средство, и можно будет продолжить лечение. Запускать болезнь не рекомендуется из-за вероятности развития осложнений.

Таким образом, становится понятно, что появление ингибиторов протонных помп стало действенным средством для лечения большого количества болезней пищеварительной системы. Больным они помогают быстро снять симптомы дискомфорта, вызванного чрезмерной выработкой желудочного сока, и избавить от изжоги. А в дальнейшем и вылечить болезнь полностью, есть принимать препараты в комплексной терапии.
Какие ингибиторы протонной помпы безопаснее при длительном приёме?
В лечении кислотозависимых заболеваний желудочно-кишечного тракта в последние десятилетия наблюдается значительный прогресс. Важнейшая роль в этом принадлежит антисекреторным препаратам, подавляющим продукцию кислоты в желудке. Наиболее эффективными антисекреторными средствами для лечения язвы желудка, двенадцатиперстной кишки, осложнений и симптомов ГЭРБ являются ингибиторы протонной помпы (ИПП). При терапии некоторых заболеваний, например, при эрозивной форме ГЭРБ, прием ИПП должен происходить в течение очень длительного времени и, в этой ситуации, при выборе конкретного ИПП важнейшим критерием является безопасность лечения этим препаратом.Главный учёный секретарь Научного общества гастроэнтерологов России, доктор медицинских наук Дмитрий Станиславович Бордин (слева) в своей новой статье "Безопасность лечения как критерий выбора ингибитора протонной помпы больному гастроэзофагеальной рефлюксной болезнью" анализирует различные классы ИПП и дает рекомендации.
На российском фармацевтическом рынке представлен широкий спектр различных ингибиторов протонной помпы:
- активное вещество омепразол: биопразол, веро-омепразол, гастрозол, демепразол, зероцид, золсер, ломак, лосек, лосек МАПС, омегаст, омез, омекапс, омепар, омепразол, омепразол пеллеты, омепразол-АКОС, омепразол-акри, омепразол-Е.К., омепразол-рихтер, омепразол-ФПО, омепрол, омепрус, омефез, омизак, омипикс, омитокс, оцид, пептикум, плеом-20, промез, рисек, ромесек, сопрал, улзол, ультоп, хелицид, хелол
- активное вещество пантопразол: контролок, нольпаза, панум, пептазол, санпраз
- активное вещество лансопразол: геликол, ланзап, ланзоптол, лансопразол, лансопразол пеллеты, лансофед, ланцид, эпикур
- активное вещество рабепразол: париет
- активное вещество эзомепразол: нексиум.
- омепразол: гасек, лосид, омепразол-астрафарм, омепразол-дарница, омепразол-КМП, омепразол-лугал, церол
- пантопразол: зогаст, золипент, паноцид, пантасан, панатап, проксиум, протонекс, ультера
- лансопразол: ланза, ланзедин, ланпро, лансогексал, лансопрол, ланцерол
- рабепразол: барол-20, геердин (порошок для приготовления раствора для инъекций и таблетки, покрытые кишечно-растворимой оболочкой), рабезол, рабемак, рабимак, рабепразол-здоровье, разо, разол-20.
Доктор Бордин пишет: проблема безопасности имеет два аспекта: безопасность ИПП как класса и безопасность отдельных препаратов. Сам по себе прием ИПП, как кратковременный, так и длительный, даже в случае употребления высоких доз не ведет к увеличению риска развития рака. Ситуация меняется при наличии у больного инфекции Helicobacter pylori. На фоне значительного и длительного подавления кислотопродукции происходит распространение H. pylori из антрального отдела на тело желудка. При этом ускоряется развитие атрофического гастрита и, возможно, рака желудка. Поэтому всем больным ГЭРБ, которым планируется лечение ИПП, необходимо проводить диагностику H. pylori и при выявлении – эрадикацию. Обсуждается, что при длительном приеме ИПП возможно повышение риска развития бактериальных кишечных инфекций, внебольничной пневмонии, остеопороза и риска переломов. Имеющиеся сегодня данные в этом отношении противоречивы. Поэтому рекомендации сводятся к тому, что пациенты должны получать ИПП по показаниям и столь длительно, сколько требует клиническая ситуация. Если необходимость приема ИПП сохраняется и после достижения клинического результата, то доза уменьшается до минимально эффективной.
Ведущим показателем, определяющим скорость развития эффекта ИПП, является биодоступность препарата. Наименьшая биодоступность у омепразола: после первого приема она составляет 30–40% и повышается до 60–65% к 7-й дозе. В отличие от него биодоступность уже начальной дозы лансопразола составляет 80–90%. Это определяет быстрое начало действия лансопразола, выявляемое при рН-мониторинге. Клинически это проявляется быстрым уменьшением и купированием симптомов.
Следующей важной проблемой безопасности лечения является возможность изменения эффектов лекарственных средств при совместном приеме с ИПП. Известно, что метаболизм ИПП осуществляется в печени с участием изоформ цитохрома Р-450. В процессе метаболизма происходит снижение их активности, которое лежит в основе межлекарственных взаимодействий. Наибольшее значение придается воздействию на CYP2С19, поскольку он участвует в метаболизме значительного количества лекарственных препаратов. В частности, в процессе метаболизма омепразол и, частично, лансопразол замедляют метаболизм антипирина, карбамазепина, циклоспорина, диазепама, дигоксина, нифедипина, фенитоина, теофиллина, R-варфарина. Среди ИПП пантопразол имеет самую низкую аффинность к системе цитохрома Р-450, поскольку после инициального метаболизма в этой системе дальнейшая биотрансформация происходит под воздействием сульфатрансферазы цитозоля. Это объясняет меньший потенциал межлекарственных взаимодействий пантопразола, чем у других ИПП. Поэтому пантопразол предпочтителен у больных, получающих несколько лекарственных препаратов.
В 2009 году было выяснено, что одновременное использование клопидогрела и ИПП значительно повышает риск возникновения больших неблагоприятных сердечно-сосудистых событий, к которым относятся инфаркт миокарда, нестабильная стенокардия, необходимость повторных коронарных вмешательств и коронарная смерть. FDA опубликовала сообщение о возможном уменьшении эффекта клопидогрела при приеме ИПП (омепразола) и о нежелательности использования такой комбинации. Выявлено повышение риска повторного обширного инфаркта миокарда на 40% у больных, принимавших клопидогрел и ИПП, за исключением пантопразола. Поэтому сопутствующую терапию клопидогрелом и ИПП, кроме пантопразола, рекомендуется по возможности ограничить.
Резюмируя изложенное, доктор Бордин отмечает, что ИПП наиболее эффективны для лечения рефлюкс-эзофагита и контроля симптомов ГЭРБ. Эффективность всех ИПП при длительном лечении ГЭРБ сходна. На ранних сроках терапии определенные преимущества в скорости наступления эффекта имеет лансопразол, что потенциально повышает приверженность больного лечению. Вместе с тем, поскольку ИПП при ГЭРБ назначаются длительно, большее значение имеет не столько скорость наступления эффекта, сколько безопасность лечения. Наибольшая рН-селективность и наименьший профиль лекарственных взаимодействий пантопразола обеспечивают его безопасность при длительном приеме, особенно при необходимости одновременного лечения сопутствующей патологии другими лекарствами.
Более подробно о выборе ингибиторов протонной помпы см. Бордин Д.С. "Безопасность лечения как критерий выбора ингибитора протонной помпы больному гастроэзофагеальной рефлюксной болезнью" и "Ингибиторы протонной помпы".
Источник: статья Д.С. Бордина "Безопасность лечения как критерий выбора ингибитора протонной помпы больному гастроэзофагеальной рефлюксной болезнью". Фотография Д.С.Бордина (вверху) взята с страницы Dmitry Bordin в Facebook. Спсисок ИПП взят из статьи "Ингибиторы протонной помпы" сайта "Функциональная гастроэнтерология".
Ингибиторы протонной помпы (ИПП) могут быть опасны ! — dolgo-jv.ru
Ингибиторы протонной помпы (ИПП), к которым относятся такие препараты как Омез, Омепразол, Ребепразол, Пантопрозол, Лансопрозол и др. относятся к числу наиболее часто употребляемых лекарств и используются для подавления секреции желудочной соляной кислоты и лечения рефлюксной болезни (изжоги), эзофагита, язвенной болезни и некоторых других заболеваний.
На сегодняшний день накоплены серьезные доказательства, указывающие на связь этих лекарственных препаратов с рядом возможных побочных эффектов, начиная сердечно-сосудистыми рисками и заканчивая повреждениями почек и деменцией.
https://www.ncbi.nlm.nih.gov/pubmed/28092694
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4902745/
Данные исследований свидетельствуют о том, что ИПП могут повысить риск повреждения различных тканей, возникающих от окислительного стресса, а также способствуют укорочению теломер, концевых участков хромосом, ответственных за продолжительность жизни.
Исследователи делают свои выводы на основании национальных данных, полученных из систем здравоохранения с участием более чем 6 миллионов человек, чье состояние здоровья отслеживалось в течение шести лет.
Ингибиторы протонной помпы показали увеличение риска смертности от всех причин на 25% по сравнению с лекарственными средствами аналогичного действия - блокаторами гистаминовых рецепторов.
http://bmjopen.bmj.com/content/7/6/e015735
Имеются данные о негативных событиях в отношении сердечно-сосудистой системы при приёме ингибиторов протонной помпы (ИПП).
ИПП плохо сказываются на функционировании сосудов, тем самым повышая риск инфаркта миокарда.
http://www.medscape.com/viewarticle/846202
Предполагается, что ингибиторы протонной помпы повышают риск сердечно-сосудистых заболеваний по какому-то неизвестному в настоящее время механизму, не связанному с агрегацией тромбоцитов.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4462578/
www.ncbi.nlm.nih.gov/pubmed/26061035
Ингибиторы протонной помпы ускоряют старение эндотелия (слой клеток, выстилающий внутреннюю поверхность кровеносных сосудов), тем самым ускоряя старение сосудов.
www.ncbi.nlm.nih.gov/pubmed/27166251
Основное условие развития такого побочного эффекта - длительный прием этих лекарственных средств.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4902745/
Ингибиторы протонной помпы увеличивают риск инсульта. Наиболее опасными в этом отношении оказались Омепразол, Пантопразол и Лансопразол. При этом, другие группы препаратов, используемых для лечения кислото-зависимых заболеваний, не увеличивали риск инсульта.
Обнаружилась взаимосвязь между дозировкой препарата и риском инсульта. С увеличением дозировки увеличивался и риск. При приеме низких дозировок такого эффекта не возникало.
Хотя данное исследование было обсервационным (наблюдательным, в котором исследователи лишь ведут подсчёт и проводят статистический анализ), и не подходит для выводов о причинно-следственной связи, обнаруженная дозозависимость делает исследование весьма убедительным.
http://www.medscape.com/viewarticle/872483
Исследованиями также установлено, что применение ингибиторов протонной помпы может быть связано с повышенным риском слабоумия (деменции), хронической болезни почек и смерти.
Пациенты, принимающие ИПП, имеют повышенный риск развития деменции, по сравнению с теми, кто не принимают эти препараты.
https://www.ncbi.nlm.nih.gov/pubmed/26882076
https://www.ncbi.nlm.nih.gov/pubmed/27429966
https://www.ncbi.nlm.nih.gov/pubmed/25341874
С учётом того, что ингибиторы протонной помпы связаны с повышенным риском развития хронической болезни почек, пациенты, принимающие эти лекарственные средства, должны быть осведомлены о их потенциальных побочных эффектах.
https://www.ncbi.nlm.nih.gov/pubmed/27487959
https://www.ncbi.nlm.nih.gov/pubmed/28583827
https://www.ncbi.nlm.nih.gov/pubmed/28339835
Результаты исследований позволяют предположить увеличение риска смерти при длительном лечении ингибиторами протонной помпы.
www.ncbi.nlm.nih.gov/pubmed/28676480
С учётом вышеизложенных рисков, имеет смысл ограничить применение ингибиторов протонной помпы, в особенности для продолжительного лечения.
Значительно безопаснее пользоваться препаратами фармакологической группы "h3-антигистаминные средства", которые тормозят выработку соляной кислоты и пепсина. К препаратам этой группы относятся Ранитидин, Фамотидин, Циметидин и др.
https://www.rlsnet.ru/fg_index_id_183.htm
Данная статья носит информационный характер. Для назначения любых лекарственных препаратов необходимо обратиться к лечащему врачу!
Рекомендую также прочесть:
Изжога - причины и лечение
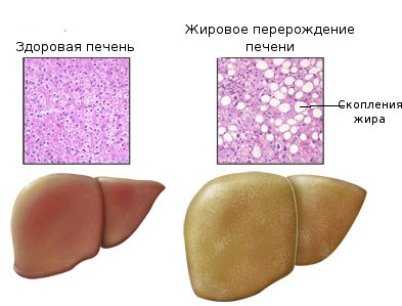
Жировой гепатоз печени (стеатоз). Лечение
Влияние холестерина на здоровье человека
Геморрой. Лечение и профилактика
Гипертония сокращает продолжительность жизни
Дешевые препараты для улучшения эректильной функции
Как избавиться от пигментации кожи?
Контрацепция после незащищенного полового акта
Мало энергии? Возможно в организме не хватает Магния!
Опасность лечения гомеопатическими препаратами
Сенолитики - препараты для уничтожения старых (сенесцентных) клеток
Современные взгляды на безопасность длительной терапии ингибиторами протонной помпы
 Кислотозависимые заболевания (КЗЗ) являются актуальной проблемой для здравоохранения в связи с их широкой распространенностью и тенденцией к неуклонному росту, необходимостью назначения сложной, многоэтапной длительной кислотосупрессивной терапии.
Кислотозависимые заболевания (КЗЗ) являются актуальной проблемой для здравоохранения в связи с их широкой распространенностью и тенденцией к неуклонному росту, необходимостью назначения сложной, многоэтапной длительной кислотосупрессивной терапии.
В настоящее время в структуре обращаемости взрослого населения по поводу болезней органов пищеварения ведущая роль принадлежит КЗЗ. КЗЗ могут проявляться в самом разном возрасте. Такие тяжелые состояния, как гастроэзофагеальная рефлюксная болезнь (ГЭРБ), рефлюкс-эзофагит с эрозиями слизистой оболочки пищевода, встречаются отнюдь не только у взрослых и пожилых больных, но и у детей первого года жизни.
В настоящее время под КЗЗ подразумевают хронические многофакторные патологические процессы, требующие длительной терапии и повышающие вероятность назначения сопутствующего лечения. Для лечения КЗЗ используют средства, препятствующие образованию кислоты в желудке или способствующие ее нейтрализации.
Появление ингибиторов протонной помпы (ИПП) на фармацевтическом рынке создало революционный прорыв в лечении КЗЗ. И действительно, ИПП относятся к наиболее часто назначаемым препаратам. В настоящее время ИПП представлены препаратами: Омепразол, Лансопразол, Рабепразол, Пантопразол, Эзомепразол, Декслансопразол, Дексрабепразол. Последний не имеет разрешения для применения на территории Российской Федерации. Существует ряд ИПП, находящихся на различных стадиях разработки и клинических испытаний. Наиболее известны Тенатопразол и Илапразол, последний уже применяется в Китае и Южной Корее.
При лечении КЗЗ перед врачом стоит задача снизить кислотопродукцию желудка — основное звено патогенеза этих патологических процессов. При лечении ГЭРБ, синдрома Золлингера — Эллисона требуется длительная, а зачастую и пожизненная кислотосупрессия.
Безусловно, положительные эффекты ИПП неоспоримы, препараты этой группы вправе считаться базисным средством в лечении КЗЗ, являются обязательным компонентом эрадикационной терапии, применяются для лечения НПВП- гастропатии (поражений гастродуоденальной зоны, связанных с приемом нестероидных противовоспалительных препаратов). Широта использования и длительность назначения ИПП порождают вопрос об их безопасности. Долгосрочное лечение ИПП может вызывать ряд нежелательных эффектов, анализу которых и посвящена обзорная статья.
Дефицит магния
В настоящее время рассматривается гипотеза о том, что длительное лечение ИПП может провоцировать развитие гипомагниемии. В 2006 г. впервые было описано 2 подобных случая. Состояние гипомагниемии вызывалось применением омепразола 20 мг более одного года. Интересно, что уровень магния в сыворотке и моче быстро нормализовался после отмены приема препарата. После публикации этого наблюдения ряд работ посвятили взаимосвязи ИПП и дефицита магния. Механизм развития гипомагниемии в настоящее время не ясен. Симптомы возникают при снижении уровня магния в моче менее 5 ммоль/л: тетания, аритмии, судороги.
В США было проведено крупномасштабное исследование, посвященное этой теме. Было обследовано 11 490 пациентов, поступивших по разным причинам на лечение в отделение интенсивной терапии. Среди них 3286 больных принимали диуретики совместно с ИПП по различным показаниям. Этот факт значительно увеличивал риск развития гипомагниемии в 1,54 раза. У тех, кто не принимал диуретики, уровень магния соответствовал референсным значениям.
В сентябре 2014 г. были опубликованы результаты другого крупного исследования, включающего 429 пациентов старшей возрастной группы, принимающих ИПП по разным показаниям. Результаты исследования установили отсутствие какой-либо ассоциации между лечением ИПП и гипомагниемией.
Гипергастринемия и риск развития опухолей
Еще одним ожидаемым нежелательным эффектом, ассоциированным с длительным приемом ИПП, является гипергастринемия, возникающая из-за реакции G-клеток слизистой оболочки желудка на повышение pH среды. Характер реакции кроется в механизме обратной связи регуляции кислотообразования. Чем выше значения pH, тем сильнее секретируется гастрин, который в последующем действует на париетальные и энтерохромаффинные клетки. Итак, какие эффекты могут возникнуть из-за гипергастринемии?
Опыты, проведенные на грызунах, показали существенное увеличение уровня гастрина вследствие длительного приема ИПП и возможность развития карциноидных опухолей из ECL- клеток. Причем гиперплазия ECL-клеток зависела от дозы ИПП и пола животного. В 2012 г. были описаны 2 пациента, принимающих ИПП по 12-13 лет для лечения ГЭРБ. При дополнительном исследовании были обнаружены высокодифференцированные нейроэндокринные опухоли, локализованные в желудке. Признаки атрофического гастрита отсутствовали, но наблюдалась гиперплазия энтерохромаффино-подобных клеток, продуцирующих гастрин. После эндоскопического удаления опухолей и отмены ИПП опухоль регрессировала, а показатели гастрина нормализовались в течение 1 нед. после прекращения лечения.
Опубликованные результаты крупного метаанализа, включавшего в общей сложности 785 пациентов, показали, что длительный прием ИПП для поддержания ремиссии у пациентов с ГЭРБ не сопровождается увеличением частоты атрофических изменений в слизистой оболочке желудка, а также гиперплазией энтерохромаффино-подобных клеток по крайней мере в течение 3-х лет непрерывного лечения по результатам рандомизированных клинических исследований. Аналогичные результаты были получены в крупномасштабном 5-летнем исследовании LOTUS, которые показали, что длительная, в течение 5 лет, терапия пациентов с ГЭРБ эзомепразолом не сопровождалась появлением дисплазии и метаплазии слизистой оболочки желудка, несмотря на некоторую гиперплазию энтерохромаффино-подобных клеток.
Гастрин стимулирует рост некоторых типов эпителиальных клеток в желудке, слизистой оболочке толстой кишки, поджелудочной железе. В этой связи для изучения возможности развития рака колоректальной зоны вследствие длительного приема ИПП в 2012 г. был проведен крупный метаанализ, включивший 737 статей и 5 исследований, и было доказано отсутствие связи между длительным лечением препаратами группы ИПП и возникновением рака колоректальной зоны.
Дефицит витамина В12
Исследования по поводу длительного лечения препаратами группы ИПП и развитием дефицита витамина В12 дали еще более противоречивые результаты. Известно, что большая часть поступающего с пищей витамина В12 связана с белками. В желудке под действием кислоты и пепсина он высвобождается и связывается с R-белками слюны — транскобаламинами I и III, а затем с внутренним фактором Касла. Далее этот комплекс достигает терминального отдела подвздошной кишки, где всасывается. При подъеме значений pH среды желудка нарушается превращение пепсиногена в пепсин, что существенно затрудняет всасывание витамина В|2 и может даже приводить к мальабсорбции этого вещества и, как следствие, к анемии.
В 2010 г. было проведено исследование, в котором изучались 34 пациента в возрасте 60-80 лет, длительно применяющих ИПП. Авторы пришли к выводу, что лица, длительно принимающие ИПП, достоверно подвергаются риску развития В12-дефицитного состояния. Такой вывод подтвердило еще одно совсем недавно опубликованное сравнительное ретроспективное исследование 25 956 пациентов с установленной В12-дефицитной анемией. Результаты исследования показали, что терапия ИПП в течение 2-х и более лет достоверно приводит к дефициту В12.
Острый интерстициальный нефрит
Предполагается, что длительный прием ИПП может провоцировать развитие острого интерстициального нефрита (ОИН). Центр мониторинга нежелательных реакций в Новой Зеландии сообщил о 15 случаях за 3 года и назвал ИПП самой частой причиной острого интерстициального нефрита из всех классов лекарственных средств.
Механизм возникновения этой патологии до конца не ясен. Считается, что ОИН обусловлен гуморальной и клеточной реакцией гиперчувствительности, которая приводит к воспалению интерстиция и канальцев почек. В результате анализа морфологического исследования почек у пациентов с ОИН, индуцированным ИПП, авторы пришли к выводу, что ведущую роль в данном воспалении играет воздействие интерлейкина-17 и CD4 клеток на почечные канальцы и связанный с ИПП острый интерстициальный нефрит не так безобиден, как считалось ранее: у 40% пациентов отмечается необратимое повышение сывороточного уровня креатинина, что свидетельствует о серьезном нарушении основных функций почек.
Остеопороз и повышенный риск возникновения переломов
Изначально существовали гипотезы о том, что ИПП самостоятельно влияют на ионные насосы и кислотозависимые ферменты костной ткани, вызывая ремоделирование костей. В конце XX в. было доказано, что ахлоргидрия способствует снижению абсорбции кальция. Этот минерал поступает в организм в виде нерастворимых солей, и для высвобождения ионизированной формы необходима кислая среда. ИПП существенно понижают кислотность в просвете желудка и, соответственно, могут влиять на течение этого процесса. Ряд исследований подтверждают это, однако вопрос нельзя считать до конца решенным.
В 2015 г. было проведено проспективное когортное исследование по поводу возможного риска возникновения остеопороза вследствие применения ИПП у пожилых женщин в Австралии. Было обследовано 4432 женщины, 2328 из которых применяли ИПП по различным показаниям. Анализ результатов возникновения остеопоротических осложнений показал повышенный риск их возникновения на фоне применения Рабепразола в 1,51 раза и Эзомепразола в 1,48 раза соответственно.
Подтверждает более высокий риск переломов бедра у пожилых лиц обоих полов на фоне длительной терапии ИПП и другое исследование, по результатам которого предлагается перед назначением ИПП пожилым пациентам тщательно взвешивать соотношение риска и пользы. В другом исследовании, охватившем 6774 мужчины старше 45 лет, также было показано наличие повышенного риска перелома бедра, который напрямую зависел от длительности терапии ИПП.
В то же время совсем недавно стали известны результаты канадского мультицентрового популяционного исследования, посвященного возможности развития остеопороза на фоне длительной терапии ИПП. Минеральная плотность костной ткани бедренной кости, тазобедренного и поясничного (L1-L4) отделов позвоночника оценивалась в исходном состоянии пациентов, через 5 и через 10 лет на фоне приема ИПП. По результатам исследования сделан вывод, что использование ИПП не привело к прогрессированию изменений костной ткани.
Синдром избыточного бактериального роста в кишечнике
В желудочно-кишечном тракте (ЖКТ) проживает больше полумиллиона видов бактерий, причем в разных отделах ЖКТ проживают различные популяции микроорганизмов. У 30% здоровых людей тощая кишка в норме стерильна, у остальных — имеет низкую плотность заселения, которая увеличивается по мере приближения к ободочной кишке, и только в дистальном отделе подвздошной кишки обнаруживается микрофлора фекального типа: энтеробактерии, стрептококки, анаэробы рода бактероидов и др..
У здоровых людей нормальная микрофлора поддерживается рядом факторов, в т. ч. соляной кислотой. При нарушении ее выработки, в условиях гипо- и ахлоргидрии может формироваться синдром избыточного бактериального роста (СИБР), в основе которого лежит повышенное заселение тонкой кишки фекальной или орофарингеальной микрофлорой, сопровождающееся хронической диареей и мальабсорбцией, в первую очередь жиров и витамина В12.
Заслуживают внимания 2 когортных исследования, проведенных в Новой Англии, в которых участвовали 1166 пациентов. Определялись причинно-следственные связи влияния ИПП на увеличение риска возникновения повторного C. difficile -ассоциированного колита. В первом исследовании применение ИПП во время лечения инфекции С. difficile было связано с более высоким риском рецидива у 42% пациентов. Второе исследование показало, что при увеличении эффекта «доза/реакция» и снижении кислотопродукции желудка у стационарных больных, принимающих ИПП, повышается риск внутрибольничной инфекции С. difficile. Наиболее высокий риск развития инфекции С. difficile наблюдался у пациентов, находящихся в критическом состоянии в реанимационных отделениях, на фоне внутривенного назначения ИПП для профилактики желудочных кровотечений.
Опубликована еще одна работа, в которой описано исследование 450 пациентов. Все они получали лечение препаратами ИПП в среднем 36 мес. При исследовании была обнаружена связь между длительностью приема ИПП и риском развития СИБР: те, кто принимал ИПП 13 мес. и более, в 3 раза чаще приобретали СИБР в отличие от тех, кто принимал ИПП меньше года.
В недавно проведенном исследовании показан высокий риск формирования сальмонеллеза у пациентов, находящихся на лечении ИПП, который уменьшался через 30 дней после отмены препаратов. Одним из объяснений высокого риска микробной контаминации кишечника у пациентов, находящихся на длительной терапии ИПП, может быть снижение двигательной активности тонкой кишки, которая описана у пациентов, принимающих ИПП, особенно в сочетании с индометацином. СИБР, ассоциированный с терапией ИПП, встречается не только у взрослых, но и у детей. В исследовании было выявлено наличие СИБРу 22,5% из 40 детей, получающих лечение ИПП в течение 3 мес. СИБР проявлялся в виде абдоминальных колик и вздутия живота.
Однако не все исследования подтверждают высокий риск развития СИБР у больных, принимающих ИПП. В исследовании с участием госпитализированных пациентов было выявлено, что в целом риск развития инфекции С. difficile минимальный и возможен лишь у лиц негроидной расы, лиц старческого возраста и имеющих тяжелую сопутствующую патологию. Аналогичные результаты относительно безопасности терапии ИПП были получены в недавно проведенном исследовании японских авторов, показавших на основе водородного теста с лактулозой крайне низкую вероятность развития СИБР на фоне терапии ИПП у японских пациентов.
Риск сердечно-сосудистых катастроф
В последние годы обсуждается возможная связь длительной терапии ИПП и повышения риска развития сердечно-сосудистых катастроф. В недавно проведенном исследовании показано, что терапия ИПП является независимым фактором риска инфаркта миокарда: после 120 дней приема ИПП риск увеличивался в 1,58 раза. Аналогичные результаты получены в другом исследовании, в котором риск развития инфаркта миокарда был сопоставим с риском от назначения других препаратов, таких как Н2-гистаминоблокаторы, бензодиазепины.
В проведенном исследовании риска длительной терапии ИПП у лиц, подвергшихся операции стентирования коронарных сосудов и находящихся на двойной анти- тромботической терапии, показаны более частые побочные эффекты в виде повышения сегмента ST на электрокардиограмме, приступов стенокардии у лиц, получавших ИПП дополнительно к антитромботической терапии, по сравнению с лицами, находящимися на лечении только антитромботическими препаратами, — это необходимо учитывать при ведении данной категории пациентов.
Повышенный риск у больных циррозом печени
В последние годы появились публикации относительно возможного риска терапии препаратами ИПП пациентов с циррозом печени: длительная терапия ИПП при циррозе печени является одним из независимых факторов риска смерти пациентов. Однако точную причину такого влияния ИПП выявить не удалось.
В совсем недавнем исследовании большой группы пациентов — 1965 — был показан повышенный риск формирования спонтанного бактериального перитонита у больных с асцитом на фоне цирроза печени, исследование продолжалось с января 2005 г. по декабрь 2009 г.. Аналогичные результаты получены канадскими исследователями в ретроспективном исследовании «случай — контроль», проводившемся с июня 2004 г. по июнь 2010 г..
Еще в одной недавно проведенной работе показано повышение риска бактериального перитонита у пациентов с циррозом печени при одновременном назначении ИПП и бета-блокаторов, что необходимо принимать во внимание при лечении данной категории пациентов.
Заключение
На сегодняшний день ИПП занимают ведущее место среди антисекреторных средств и, несмотря на ряд побочных эффектов, имеют высокий профиль безопасности и достаточную эффективность, что было доказано в крупных исследованиях. Обычно ИПП переносятся достаточно хорошо, и побочные реакции встречаются крайне редко. Проблема всех отдаленных нежелательных эффектов применения ИПП требует дальнейших научных исследований.
В целях снижения риска развития подтвержденных побочных нежелательных эффектов необходимы определенные профилактические мероприятия.
- Для предотвращения дефицита витаминов и минералов необходимо регулярно проводить контроль их концентрации в крови. При дефиците целесообразно назначение витаминов, препаратов магния, железа, кальция.
- В целях канцеропревенции необходимо проводить периодические эндоскопические исследования на выявление признаков новообразований в ЖКТ.
- Для обнаружения и профилактики СИБР целесообразно проводить микробиологические исследования содержимого тонкой кишки, дыхательные тесты.
- При индивидуальной непереносимости ИПП возможно назначение альтернативных лекарств: блокаторов Н2-рецепторов, М-холиномиметиков.
- ИПП следует назначать только при наличии соответствующих клинических показаний, особенно у пациентов с циррозами печени и высоким риском сердечно-сосудистых катастроф.
- С учетом того, что неблагоприятные проявления лечения ИПП могут появиться уже на ранних сроках, лечение должно быть по возможности коротким, с назначением наименьшей эффективной дозы. При хорошем симптоматическом эффекте у пациентов с неосложненной ГЭРБ допускается прием препарата «по требованию».
В.А. Ахмедов, В.А. Ноздряков
2017 г.
Безопасность использования ингибиторов протонной помпы | #07/13
Так называемые кислотозависимые заболевания включают в себя целый комплекс патологических процессов, протекающих на фоне, под воздействием или при нарушении кислотообразования в желудке. К сожалению, распространенность данных заболеваний в последнее время только увеличивается.
Кислотозависимые заболевания могут проявляться в самом разном возрасте. Такие тяжелые состояния, как гастроэзофагеальная рефлюксная болезнь (ГЭРБ), рефлюкс-эзофагит с эрозиями слизистой оболочки пищевода, встречаются отнюдь не только у взрослых и пожилых больных, но даже и у детей первого года жизни. Ошибочное мнение о том, что у детей младшего возраста соляной кислоты в желудке вырабатывается крайне мало, опроверг еще в середине 1980-х гг. А. В. Мазурин, показав, что даже у новорожденного ребенка вырабатывается достаточное количество концентрированной кислоты. Безусловно, объем и концентрацию кислоты в различных возрастах необходимо оценивать относительно объема желудка и качества пищи, съедаемой человеком, в разные периоды жизни (табл.) [1].
Избыточное количество соляной кислоты и агрессивных желудочных ферментов является мощным повреждающим фактором слизистой оболочки пищевода, желудка и двенадцатиперстной кишки, что подтверждает постулат, выдвинутый К. Шварцем еще в 1910 г.: «Нет кислоты — нет язвы». К другим факторам агрессии можно отнести различные лекарственные препараты, Helicobacter pylori, нарушение моторики желудочно-кишечного тракта.
В настоящее время под кислотозависимыми заболеваниями подразумевают хронические многофакторные патологические процессы, требующие длительной терапии и повышающие вероятность назначения сопутствующего лечения [2]. Для нейтрализации избыточно образующейся кислоты и лечения собственно самих кислотозависимых заболеваний используют средства, препятствующие образованию кислоты в желудке или способствующие нейтрализации уже образовавшейся кислоты в просвете желудка.
В настоящее время существует три основных группы препаратов, используемых для лечения кислотозависимых состояний.
К первой из них относятся антациды. Однако использование антацидных препаратов не может радикально решить проблему. Антацидные препараты достаточно быстро нейтрализуют кислоту, находящуюся в просвете желудка. Однако препараты этой группы имеют несколько недостатков. В первую очередь — незначительная продолжительность действия. Даже самые длительно действующие препараты «работают» не более 1,5 часов. По этой причине для достижения необходимого эффекта лечение антацидами требует частого назначения больших доз препаратов. Длительное использование антацидов может привести к развитию побочных и нежелательных эффектов. Побочные эффекты применения антацидов могут проявляться банальным нарушением стула с появление запоров или, наоборот, диареи, в зависимости от того, какие по составу антацидные препараты принимал больной — алюминий- или магнийсодержащие. Кроме того, длительное использование антацидов может привести к нарушению минерального баланса в организме с развитием алкалоза. Терапия антацидами не контролирует выработку соляной кислоты и не может использоваться как основной метод лечения кислотозависимых состояний.
К другой группе средств, используемых для лечения кислотозависимых заболеваний, относятся блокаторы Н2-рецепторов гистамина. Ингибирование Н2-рецепторов гистамина на поверхности париетальной клетки снижает секрецию кислоты. Однако и у этой группы лекарственных средств имеются свои недостатки. Терапевтическая эффективность обеспечивается высоким уровнем препарата в крови, что иногда требует его многократного приема [3]. При использовании блокаторов Н2-гистаминовых рецепторов париетальных клеток слизистой оболочки желудка подавление желудочной секреции достигается воздействием на один тип рецепторов, при этом гиперсекреция соляной кислоты может быть обусловлена стимуляцией других рецепторов, также имеющихся на поверхности клетки, — гастриновых или ацетилхолиновых [4]. Наконец, при использовании этих препаратов может развиться толерантность к ним и появиться синдром «рикошета». Толерантность может развиться уже через два дня после начала лечения [5], поэтому в настоящее время блокаторы Н2-гистаминовых рецепторов практически не используют для лечения.
Третья группа препаратов представляет собой ингибиторы протонной помпы (ИПП). ИПП наиболее эффективны для лечения кислотозависимых заболеваний. Они значительно превосходят блокаторы Н2-рецепторов гистамина, прокинетики, цитопротекторы и плацебо по своей клинической эффективности и возможности контролировать процессы кислотоподавления. Все современные ИПП (омепразол, лансопразол, пантопразол, рабепразол, эзомепразол) являются замещенными бензимидазолами, которые отличаются радикалами в пиридиновом и бензимидазольном кольцах. Это слабые основания, накапливающиеся в секреторных канальцах париетальных клеток, где при низких значениях рН они трансформируются в химически активную форму (тетрациклический сульфенамид) и необратимо связываются с Н+/К+-АТФазой (протонной помпой), блокируя активный перенос ионов водорода из межклеточого пространства в выводные канальцы железы. Ее восстановление происходит после встраивания в мембрану секреторных канальцев новых протонных помп, свободных от связи с активным метаболитом ИПП, поэтому продолжительность антисекреторного эффекта определяется скоростью обновления протонных помп, то есть скоростью обновления эпителиальных клеток желудка.
ИПП, действуя на париетальную клетку, контролирует дневную, стимулированную пищей и ночную секреции, ингибирует продукцию соляной кислоты независимо от стимула, воздействующего на рецепторы париетальных клеток, не вызывает развития синдрома «рикошета» и толерантности, быстро подавляет секрецию кислоты. Именно поэтому ИПП позволяют осуществлять 24-часовой контроль за желудочной секрецией и является основным средством для лечения кислотозависимых заболеваний.
Высокая фармакологическая безопасность ИПП обеспечивается избирательностью их накопления в организме и специфичностью взаимодействия с Н+/К+-зависимой АТФазой — протонным насосом париетальной клетки желез желудка. Чем выше избирательность действия лекарственного средства, тем лучше оно переносится пациентом и тем меньшее число нежелательных реакций вызывает. После приема ИПП и их всасывания в тонкой кишке их активная часть — производное бензимидазола — путем диффузии избирательно накапливается в кислой среде секреторных канальцев париетальной клетки. Там происходит протонирование атома азота пиридинового кольца молекулы ИПП и переход в активную форму — сульфенамид, благодаря чему становится возможным связывание с тиоловыми группами цистеина в составе протонной помпы и блокирование этого фермента. Заряженные (протонированные) формы замещенных бензимидазолов концентрируются там, где рН ниже рК, и происходит их протонирование. В живой клетке есть компартменты с кислой средой — лизосомы, нейросекреторные гранулы и эндосомы, где уровень рН составляет 4,5–5,0. При полной стимуляции париетальной клетки рН секреторного канальца достигает 0,8. Таким образом, для избирательного накопления именно в секреторном канальце рК ИПП должен быть ниже 4,5. Концентрация этих препаратов в секреторных канальцах париетальной клетки в 1000 раз превосходит их концентрацию в крови [6].
При повышении уровня внутрижелудочного рН на фоне приема (особенно длительного и в больших дозах) ИПП развивается гипергастринемия, обусловленная реакцией G-клеток. Кислотная продукция регулируется по механизму отрицательной обратной связи: при сдвиге рН в щелочную сторону происходит активизация гастринпродуцирующих клеток и секреция гастрина, который воздействует и на париетальные клетки непосредственно, и на энтерохромаффиноподобные (ECL) клетки. Гастрин и гистамин, продуцируемый ECL-клетками, служат активирующими стимулами для париетальных клеток — возобновляется кислотная продукция. При назначении ИПП интрагастральный рН находится под лекарственным контролем, а ответная гипергастринемия является ожидаемым эффектом [7].
Опасна ли длительная гипергастринемия на фоне применения ИПП, особенно в плане развития онкологических процессов? На этот вопрос дали ответ результаты экспериментов, проводимых на крысах при долговременном введении ИПП. Так, было показано существенное увеличение уровня гастрина и возможность возникновения карциноидных опухолей, исходящих из ECL-клеток, причем гиперплазия ECL-клеток зависит от дозы ИПП и от пола животного [8, 9]. В дальнейшем были выделены существенные различия между вероятностью развития опухолей из ECL-клеток в эксперименте на крысах и при применении ИПП у человека: различная подверженность повреждению слизистой оболочки желудка гипергастринемии (в эксперименте гипергастринемия развивается лишь при пожизненном приеме ИПП) и видовая генетическая предрасположенность ECL-клеток крыс к гиперплазии [10].
В целом, учитывая многолетний опыт использования ИПП в клинической практике, на основании многих метаанализов не было зафиксировано ни одного случая возникновения не только карциноида, но даже предстадий карциноида. Терапия лансопразолом длительностью до 4 лет, омепразолом — до 7 лет не была связана с каким-либо неопластическим или диспластическим процессом в эндокринных или неэндокринных клетках желудка.
Метаболизм практически всех существующих ингибиторов протонной помпы совершается преимущественно в печени цитохромом Р450. В результате конкурентного взаимодействия ИПП и других лекарственных веществ, метаболизм которых проходит также с участием этого цитохрома, прием ИПП может влиять на печеночный метаболизм некоторых лекарственных средств, изменяя их активность. ИПП могут потенциально изменять растворимость других веществ или нарушать их высвобождение из лекарственных форм с рН-зависимой растворимостью. Чем больше препаратов принимает больной, тем выше вероятность взаимодействий между ними [11]. В клинической практике лекарственное взаимодействие с участием замещенных бензимидазолов редко имеет существенное значение, однако рекомендуется тщательно наблюдать за пациентами, одновременно принимающими омепразол и фенитоин или варфарин. Возможно, что лансопразол влияет на метаболизм теофиллина через CYP1A2 [12].
Данные эпидемиологических исследований и, в частности, исследование МЭГРЕ, проведенное в России, инициированное Центральным научно-исследовательским институтом, свидетельствует, что распространенность ГЭРБ увеличивается с возрастом населения. Если у респондентов до 44 лет количественные признаки ГЭРБ выявляются в 10,8%, то после 60 лет — в 18,8%, при этом у пожилых женщин распространенность ГЭРБ достигает 24%. У больных пожилого возраста, как правило, наблюдается несколько хронических заболеваний. Так, по данным А. А. Машаровой (2008), у 59,3% пожилых больных ГЭРБ выявляется артериальная гипертензия, у 41,1% — ишемическая болезнь сердца (ИБС). А проведенное в Великобритании многоцентровое исследование показало, что из 5453 пациентов с ГЭРБ, наблюдавшихся в 360 лечебных учреждениях, у 20,1% имелась сопутствующая артериальная гипертензия, 16,8% больных страдали артритами, у 13,6% имелась ИБС, у 10% определялись хронические обструктивные заболевания легких, у 8,8% — психические расстройства [13].
Различными исследователями было проведено немало одно- и мультицентровых исследований, показавших, что люди старше 65 лет, как правило, страдают целым рядом хронических заболеваний и вынуждены принимать ежедневно от 3 до 8 различных лекарственных препаратов [14]. Недавно было обнаружено и исследуется лекарственное взаимодействие ИПП и антиагреганта клопидогреля, широко применяемого при лечении больных ИБС. По сравнению с монотерапией ацетилсалициловой кислотой, ее комбинация с клопидогрелем значительно снижает частоту возникновения рецидивов острого инфаркта миокарда (ОИМ). Для уменьшения риска гастроинтестинальных осложнений больным, получающим такую терапию, назначают ИПП. Поскольку клопидогрель является пролекарством, биоактивация которого опосредована изоферментами цитохрома Р450, в основном CYP2C19, прием ИПП, метаболизируемых этим цитохромом, может снизить активацию и антиагрегантный эффект клопидогреля. В мае 2009 г. на 32-й Ежегодной конференции Общества сердечно-сосудистой ангиографии и вмешательств (Society for Cardiovascular Angiography and Interventions, SCAI) были представлены данные, свидетельствующие, что одновременное использование клопидогреля и ИПП значительно повышает риск возникновения больших неблагоприятных сердечно-сосудистых событий, к которым относится инфаркт миокарда, инсульт, нестабильная стенокардия, необходимость повторных коронарных вмешательств и коронарная смерть. Такой вывод был сделан по результатам широкомасштабного исследования, проведенного в США при анализе базы данных Medco, оценившего риск осложнений при одновременном приеме ИПП и клопидогреля у больных, перенесших стентирование. Оказалось, что риск возникновения неблагоприятных сердечно-сосудистых осложнений у больных, принимавших ИПП совместно с клопидогрелем (число пациентов (n) = 9862), составил 25%, в то время как у не принимавших ИПП (n = 6828) риск был ниже — 17,9% [15]. В связи с вышесказанным SCAI выпустило официальное заявление, в котором говорится о необходимости дополнительного изучения данной проблемы. Управление по надзору за качеством пищевых продуктов и лекарственных средств США (Food and Drugs Administration of the United States, FDA) опубликовало сообщение о возможном уменьшении эффекта клопидогреля при приеме ИПП (омепразола) и о нежелательности использовании такой комбинации. В то же время в марте 2009 г. опубликовано популяционное когортное исследование типа «случай–контроль» среди жителей г. Онтарио в возрасте 66 лет и старше, которые начали прием клопидогреля после выписки из больницы после лечения ОИМ (n = 13636). Основную группу составили 734 больных, умерших или повторно госпитализированных с ОИМ в течение 90 дней после выписки из стационара. В группу контроля вошли 2057 больных, которые были соотнесены с основной по возрасту и предсказанной вероятности ранней смерти (в пределах 0,05), определяемой с помощью модели предсказания кардиального риска. Учитывался прием ИПП во время терапии клопидогрелем. В ходе первичного анализа обнаружена существенная связь повторной госпитализации по поводу ОИМ с текущим приемом ИПП (скорректированное отношение шансов (ОШ) 1,27, 95% доверительный интервал (ДИ) 1,03–1,57). Стратифицированный анализ не выявил связи приема пантопразола с повторным ОИМ у больных, получающих клопидогрель (ОШ 1,02, 95% ДИ 0,70–1,47). Напротив, другие ИПП были ассоциированы с повышением риска повторного ОИМ в течение 90 дней после выписки на 40% (ОШ 1,40, 95% ДИ 1,10–1,77). Таким образом, у больных, принимающих клопидогрель после острого инфаркта миокарда, сопутствующий прием ИПП, ингибирующих цитохром Р450 2С19 (омепразол, лансопразол или рабепразол), связан с повышенным риском повторного ОИМ. Этот эффект, не наблюдаемый при терапии пантопразолом, по-видимому, отражает нарушение метаболической биоактивации клопидогреля. До появления дальнейших данных о клиническом значении лекарственных взаимодействий с клопидогрелем сопутствующую терапию клопидогрелем и ИПП, кроме пантопразола, следует по возможности ограничить. Из всех ИПП пантопразол обладает минимальной аффинностью к ферментам CYP2C19 и CYP3A4 [16]. II фаза биотрансформации заключается в конъюгации с сульфатом и протекает в цитозоле. Потенциал участия пантопразола в лекарственных взаимодействиях ограничен по сравнению с другими ИПП [17]. В опубликованном в июле 2009 г. обзоре литературы о взаимодействии ИПП и клопидегреля (PubMed 1980 г. — январь 2009 г., материалы съезда Американской ассоциации кардиологов (American Heart Association, AHA) 2008 г. и научной сессии SCAI 2009 г.) отмечено, что есть достаточно данных, свидетельствующих, что омепразол имеет значимое лекарственное взаимодействие с клопидогрелем. Относительно взаимодействия с ним других ИПП требуются дальнейшие исследования. При необходимости использования ИПП у больных, принимающих клопидогрель, рекомендовано отдавать предпочтение пантопразолу. В проведенных в ЦНИИГ исследованиях у больных, страдающих ИБС, было отмечено, что среди больных, страдающих ГЭРБ, на фоне приема клопидогреля или варфарина в течение 1 года наблюдений повторные инфаркты отмечались только у тех, которые находились на лечении различными производными омепразола, и ни у одного при фоновой терапии ГЭРБ пантопразолом. Следует, однако, отметить, что эти данные пока еще находятся в процессе обработки и говорить о них с полной уверенностью можно будет только после полного анализа полученных данных.
Таким образом, ИПП являются проверенным, безопасным и достаточно мощным инструментом, стоящим на пути кислотозависимых заболеваний. Пожилым больным с ГЭРБ, нуждающимся в одновременном приеме нескольких лекарственных препаратов на фоне приема ИПП с учетом профиля лекарственного взаимодействия, предпочтение следует отдавать пантопразолу, к примеру, препарату Контролок.
Литература
- Мазурин А. В. Болезни органов пищеварения у детей. М.: Медицина, 1984. 685 с.
- Humphries T. J., Merritt G. J. Drug interactions with agents used to treat acid-related diseases // Aliment Pharmacol Ther. 1999; 13 Suppl. 3: 18–26.
- Onasanwo S. A., Singh N., Olaleye S. B., Palit G. Anti-ulcerogenic and proton pump (H+, K+ ATPase) inhibitory activity of Kolaviron from Garcinia kola Heckel in rodents // Indian J Exp Biol. 2011, Jun; 49 (6): 461–468.
- Wilder-Smith C. H., Halter F., Hackiv W., Merki H. S. pH-feedback controlled infusions of ranitidine are no more effective than fixed-dose infusions in reducing gastric acidity and variability in antisecretory responses // Br. J. clin. Pharmac. 1992, 33, 487–493.
- Hogan W. J., Dodds W. J. Gastroesophageal reflux disease (reflux esophagitis). Gastrointestinal disease: Pathophysiology, diagnosis, management, 4 th ed (Sleisenger M. N., Fordtran J. S. eds) W. B. Saunders, Philadelphia, 1989, pp. 594–619.
- Modlin I. M., Sachs G. Acid related diseases. Biology and treatment. Schnetztor-Verlag Gmbh, Konstanz. 1998. P. 126–42.
- Лапина Т. Л. Безопасность ингибиторов протонной помпы // Клинические перспективы гастроэнтерологии, гепатологии. 2009, № 4, с. 22–28.
- Ekman L., Hansson E., Havu N. et al. Toxicological studies on omeprazole // Scand. J. Gastroenterol. 1985. Vol. 20 (Suppl. 108). P. 53–69.
- Havu N. Enterochromaffin-like cell car-cinoids of gastric mucosa in rats after life-long inhibition of gastric secretion // Digestion. 1986. Vol. 35 (Suppl. 1). P. 42–55.
- Freston J. W., Borch K., Brand S. J. et al. Effects of hypochlorhydria and hypergastrine-mia on structure and function of gastrointestinal cells: a review and analysis // Dig. Dis. Sci. 1995. Vol. 40 (Suppl). 50 S–62 S.
- Johnson A. G., Seidemann P., Day R. O. NSAID-related adverse drug interactions with clinical relevance: an update // Int J Clin Pharmacol Ther. 1994; 32: 509–532.
- Белоусов Ю. Б., Леонова М. В. Основы клинической фармакологии и рациональной фармакотерапии. М.: ОАО Изд-во «Бионика». 2002. С. 254–258.
- Grass U. Drug interactions with proton pump inhibitors // Der Kassenarzt. 2000, 43, p. 32–39.
- Johnson et al. // Int J Clin Pharmacol Ther 1994; 32: 509–32. Steward, Cooper. Drugs & Aging 1994; 4: 449–461.
- Ho P. M., Maddox T. M., Wang L. et al. // JAMA. 2009. Vol. 301, № 9. P. 937–44.
- Simon W. A. Pantoprazole: which cytochrome P450 isoenzymes are involved in its biotransformation? [abstract] // Gut. 1995; 37: A1177.
- Radhofer-Welte S. Pharmacokinetics and metabolism of the proton pump inhibitor pantoprazole in man // Drugs Today. 1999; 35: 765–772.
П. Л. Щербаков, доктор медицинских наук, профессор
ГБУЗ ЦНИИГ ДЗМ, Москва
Контактная информация: [email protected]
Купить номер с этой статьей в pdf
смена лидера, стандарта или мировоззрения?
Авторы: С.М. Ткач
Статья в формате PDF
Большинство имеет определенное мировоззрение, которое определено меньшинством.
Станислав Ежи Лец
 Сейчас сложно поверить, что относительно недавно, в начале ХХ столетия, лечение язвенной и гастроэзофагеальной рефлюксной болезни (ГЭРБ) заключалось в назначении щелочных продуктов питания – молока, яиц, пюре. Несколько позже первую скрипку в терапии этих заболеваний стала играть питьевая сода – она облегчала состояние больных, но, к сожалению, не предотвращала развитие осложнений. В середине ХХ столетия появились холиноблокаторы, и на сцену вышел атропин, частично ингибировавший продукцию соляной кислоты посредством блокады мускариновых рецепторов париетальных клеток. Незначительная эффективность, многочисленные побочные эффекты не позволили атропину длительное время удерживать лидирующие позиции в лечении кислотозависимых заболеваний (КЗЗ), и ему на смену пришли блокаторы Н2-рецепторов.
Сейчас сложно поверить, что относительно недавно, в начале ХХ столетия, лечение язвенной и гастроэзофагеальной рефлюксной болезни (ГЭРБ) заключалось в назначении щелочных продуктов питания – молока, яиц, пюре. Несколько позже первую скрипку в терапии этих заболеваний стала играть питьевая сода – она облегчала состояние больных, но, к сожалению, не предотвращала развитие осложнений. В середине ХХ столетия появились холиноблокаторы, и на сцену вышел атропин, частично ингибировавший продукцию соляной кислоты посредством блокады мускариновых рецепторов париетальных клеток. Незначительная эффективность, многочисленные побочные эффекты не позволили атропину длительное время удерживать лидирующие позиции в лечении кислотозависимых заболеваний (КЗЗ), и ему на смену пришли блокаторы Н2-рецепторов.
Настало время ранитидина и фамотидина – они внесли существенные изменения в устоявшиеся принципы лечения КЗЗ: механизм их действия заключался в блокировании гистаминовых рецепторов в париетальных клетках, что сопровождалось достижением непродолжительного контроля над синтезом соляной кислоты.
Несмотря на более высокую эффективность по сравнению с М-холиноблокаторами, применение Н2-блокаторов редко приводило к полному восстановлению и заживлению дефектов слизистой по причине неспособности этих препаратов длительно блокировать секрецию соляной кислоты и долго удерживать целевое рН.
И вот, наконец, на небосклоне появилась новая путеводная звезда – омепразол, представитель ранее неизвестной группы лекарственных средств, а именно: ингибиторов протонной помпы (ИПП). Эффект, произведенный появлением омепразола, часто сравнивают с масштабной терапевтической революцией: высокая афинность к протонной помпе париетальных клеток желудка и более благоприятный по сравнению с предшественниками профиль побочных действий перевернули ранее господствовавшие представления о лечении КЗЗ. .
Годы широкомасштабного клинического применения, множество сравнительных клинических исследований убедительно подтвердили превосходство первого представителя класса ИПП над Н2-блокаторами. Такая убедительная победа омепразола в лечении язвенной болезни и ГЭРБ создали предпосылки для синтеза других ИПП. И вскоре семейство ИПП пополнилось новыми членами – лансопразол, пантопразол, рабепразол, эзомепразол присоединились к своему родоначальнику в борьбе с КЗЗ. Количество назначений ИПП быстро возросло: только в течение 8 лет (с 2000 по 2008 год) частота применения ИПП увеличилась на 200,8%, тогда как число назначений Н2-блокаторов значительно сократилось. Вот так постепенно, с появлением новых препаратов и современных знаний менялись мировоззрение, стандарты и подходы к лечению КЗЗ.
Немного фармакологии
ИПП, попадая в организм в неактивном виде, пролекарства активируются исключительно в суперкислой среде (при рН 1,0-2,0), которая создается исключительно в протоках париетальных клеток желудка. Краткость, необратимость и избирательность действия ИПП позволяют быстро и надежно вывести из строя активированные протонные насосы. Возобновление синтеза соляной кислоты возможно только через определенный промежуток времени, необходимый для синтеза новых белковых молекул, входящих в состав протонной помпы.
ИПП – очень недолго живущие препараты (период полувыведения – 0,5-2 ч) – способны обеспечить чрезвычайно длительный кислотосупрессивный эффект при однократном приеме в течение суток. В настоящее время ИПП продолжают прочно удерживать пальму первенства среди всех существующих классов антисекреторных лекарственных средств: они способны удерживать рН в желудке ≥4,0 на протяжении 18 ч в течение суток. После приема стандартной дозы ИПП синтез соляной кислоты полностью возобновляется только спустя 72-96 ч, а биодоступность препаратов возрастает с приемом каждой последующей дозы.
Короткий период полувыведения ИПП обуславливает низкую токсичность препаратов этой группы, даже у пожилых больных или пациентов с почечной/печеночной недостаточностью. Только в случаях выраженной печеночной недостаточности может понадобиться уменьшение дозы этих препаратов.
В отличие от ИПП, Н2-блокаторы начинают действовать значительно быстрее, однако прием этих препаратов сопровождается развитием тахифилаксии, а выраженность их антисекреторного действия начинает снижаться уже спустя первые 12-24 ч после приема данных лекарственных средств.
В настоящее время Н2-блокаторы используются достаточно редко и назначаются для лечения крайне ограниченного круга заболеваний (легкая неэрозивная ГЭРБ, легкое течение функциональной диспепсии, гиперчувствительность к ИПП), тогда как спектр применения ИПП гораздо шире (табл. 1).
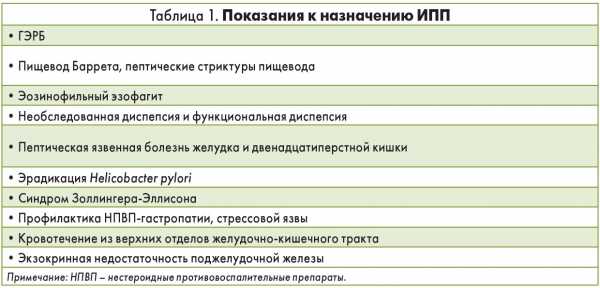
В руководстве Европейского общества кардиологов (European Society of Cardiology, ESC) по лечению острого коронарного синдрома у пациентов без персистирующего повышения сегмента ST, увидевшего свет в 2016 г., приводится еще одно показание для назначения ИПП (табл. 2).
Упорное соревнование, жаркие споры и неожиданный парадокс
Ситуацию равенства и братства в семействе ИПП нарушило желание учеников превзойти учителя: кто-то казался сильнее, кто-то – быстрее, а кто-то – длительнее. Однако выраженность кислотосупрессивного действия оказалась сопоставимой с таковой остальных ИПП, а длительность поддержания внутрижелудочного рН ≈4 омепразола (11,8 ч), хотя и уступала эзомепразолу (14 ч) и рабепразолу (12 ч), но превосходила лансопразол (11,5 ч) и пантопразол (10,1 ч) (Miner et al., 2003). Доказано, что использование омепразола у больных, принимающих ДАТТ с включением низких доз АСК, предотвращает повреждение слизистой оболочки верхних отделов ЖКТ и уменьшает риск кровотечений (Дорофеев А. Э., 2017).
Изучение механизмов действия омепразола позволило установить, что, помимо значительного снижения секреции соляной кислоты, под влиянием омепразола достоверно увеличивается экспрессия гена Bcl‑2 и синтез протеина Ki‑67 у больных с НПВП-ассоциированными язвами, осложненными кровотечением. Именно благодаря этим свойствам ограничивается активность апоптоза и стимулируется пролиферация эпителия желудочно-кишечного тракта, ускоряется репарация эрозивно-язвенных поражений, вызванных приемом НПВП (Rantanen T. et. al., 2014).
Однако самые жаркие споры о превосходстве одного ИПП над другими разгорелись на почве безопасности их применения в отдельной группе больных – у пациентов, получающих ДАТТ ацетилсалициловой кислотой и ингибитором P2Y12 (клопидогрель). В ходе наблюдательных исследований, изучавших возможные взаимодействия при одновременном приеме ИПП и клопидогреля, были получены неоднозначные результаты: некоторые свидетельствовали об ухудшении сердечно-сосудистых исходов, другие не подтверждали наличие подобной связи. Тщательный анализ вероятных неблагоприятных последствий сочетанного применения ИПП и ингибитора P2Y12 показал, что возможная причина их возникновения кроется в особенностях метаболизма указанных медикаментов.
Оказалось, что метаболизм этих препаратов происходит в печени с участием преимущественно трех изоферементов системы цитохрома Р450: CYP2С19, CYP2С9, CYP3А4. Высказано предположение, что ИПП, вступая во взаимодействие с перечисленными ферментами, тем самым ингибируют превращение клопидогреля в его активный метаболит, снижая эффективность последнего и косвенно усиливая агрегацию тромбоцитов.
На первый взгляд все оказалось достаточно просто: клопидогрель метаболизируется посредством CYP2С19, следовательно, при необходимости одновременного приема клопидогреля и ИПП необходимо использовать такой кислотосупрессивный препарат, который бы не воздействовал на указанный изофермент.
Управление по контролю за качеством продуктов питания и лекарственных средств США (FDA, 2009) поспешило опубликовать предостережение о нежелательности применения клопидогреля и ИПП, особенно омепразола и эзомепразола (наиболее изученных представителей этого класса лекарственных средств в то время), и рекомендовало к применению менее изученный препарат – пантопразол, который, предположительно, не влиял на CYP2С19.
Последовавшее за этой публикацией активное клиническое применение пантопразола, а также тщательное изучение свойств других ИПП заставило экспертов усомниться в правильности сделанных умозаключений. Оказалось, что метаболизм клопидогреля осуществляется не только за счет CYP2С19, но и при помощи CYP2С9, CYP3А4, а разные представители группы ИПП оказывают различное воздействие на метаболизм системы цитохрома Р450. Поэтому влияние ИПП на метаболизм клопидогреля и последующие сердечно-сосудистые исходы могут существенно отличаться.
Три сокрушительных удара по устоявшемуся стереотипу
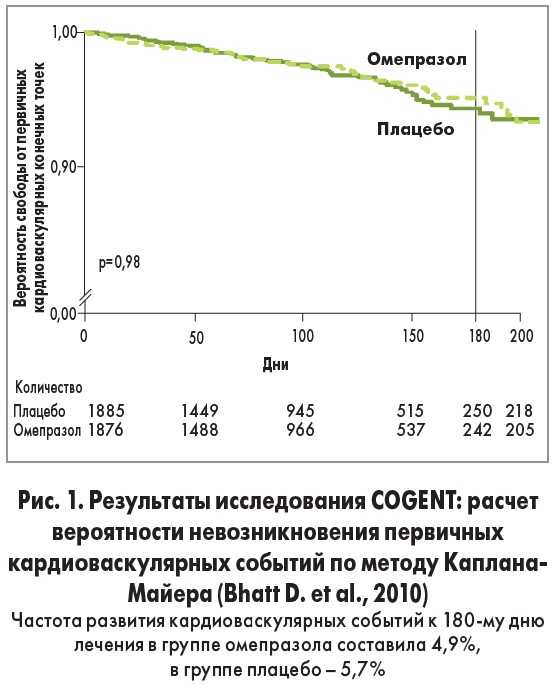 Вскоре появились результаты клинических исследований и метаанализов. Первый сокрушительный удар, поколебавший устоявшийся стереотип в отношении способности омепразола увеличивать сердечно-сосудистый риск у больных, получающих ДАТТ, нанесло исследование COGENT (Clopidogrel and the Optimization of Gastrointestinal Events Trial, 2010).
Вскоре появились результаты клинических исследований и метаанализов. Первый сокрушительный удар, поколебавший устоявшийся стереотип в отношении способности омепразола увеличивать сердечно-сосудистый риск у больных, получающих ДАТТ, нанесло исследование COGENT (Clopidogrel and the Optimization of Gastrointestinal Events Trial, 2010).
Это международное рандомизированное двойное слепое контролируемое с помощью двух плацебо параллельное групповое исследование (n=3873) эффективности и безопасности фиксированной комбинации клопидогреля (75 мг) и омепразола (20 мг) по сравнению с монотерапией клопидогрелем предоставило неожиданные результаты (все пациенты в этом исследовании дополнительно принимали ацетилсалициловую кислоту).
На протяжении всего периода наблюдения, длительность которого составляла 180 дней, поражение желудочно-кишечного тракта (явное / скрытое кровотечение, симптоматические гастродуоденальные язвы / эрозии, обструкция, перфорация) зафиксировано у 51 пациента, при этом они достоверно реже возникали у больных, получавших омепразол (1,1%), по сравнению с участниками, принимавшими плацебо (2,9%; отношение рисков для омепразола 0,3; 95% ДИ 0,03-0,56; р=0,001).
При этом частота возникновения нефатального инфаркта миокарда, инсульта, реваскуляризации, летального исхода по кардиоваскулярным причинам достоверно не отличалась в группах омепразола (4,9%) и плацебо (5,7%; ОР 0,99; 95% ДИ 0,68-1,44; р=0,96). Опубликовав полученные данные (табл. 3, рис. 1), авторы исследования резюмировали, что не зафиксировано значимых кардиоваскулярных взаимодействий между клопидогрелем и омепразолом, но эти результаты не позволяют в полной мере исключить клинически значимые различия в кардиоваскулярных событиях, обусловленных применением ИПП (табл. 3).
Сформулированные выводы были восприняты медицинской общественностью с большой настороженностью – всего лишь год перед этим FDA настоятельно рекомендовало применение пантопразола. Еще одним объяснением данному факту может стать досрочное завершение исследования: в соответствии с планами авторов проекта в этом трайле должны были принять 5 тыс. больных, но медленный набор пациентов и небольшое число кардиоваскулярных событий явились поводом для прекращения финансирования и закрытия исследования COGENT. Однако спустя 6 лет результаты исследования COGENT были проанализированы и перепроверены другой группой ученых, не принимавших непосредственного участия в его проведении.
М. Vaduganathan и соавт. (2016) полностью подтвердили выводы, сформулированные D. Bhatt и соавт.: у пациентов, перенесших чрескожное коронарное вмешательство (n=2676), омепразол значительно уменьшал вероятность развития гастроинтестинальных событий без значимого повышения риска кардиоваскулярных событий по сравнению с плацебо (5,4 vs 6,3%, соответственно; ОР 1,0; 95% ДИ 0,67-1,50; р=1,00). Аналогично в когорте больных острым коронарным синдромом (n=1573) омепразол предупреждал появление значимых гастроинтестинальных событий, не провоцируя возрастание вероятности появления кардиоваскулярных событий по сравнению с плацебо (5,6 vs 4,5% соответственно; ОР 1,4; 95% ДИ 0,77-2,53; р=0,27).
Вторым, не менее серьезным ударом по кардиологическому образу пантопразола стала публикация в авторитетном журнале Американской кардиологической ассоциации систематического обзора, подготовленная под руководством М. Sherwood (2015).
Метаанализ 6 отобранных исследований выявил повышение риска возникновения нежелательных кардиоваскулярных событий у пациентов, принимавших пантопразол (ОР 1,38; 95% ДИ 1,12-1,70), лансопразол (ОР 1,29; 95% ДИ 1,09-1,52) или эзомепразол (ОР 1,27; 95% ДИ 1,02-1,58) по сравнению с больными, не получающими ИПП. Ученые особо подчеркнули тот факт, что упомянутая связь не была значимой для омепразола (ОР 1,16; 95% ДИ 0,93-1,44), т. е. омепразол может использоваться при проведении ДАТТ, т. к. не оказывает негативного влияния на cердечно-сосудистый риск (рис. 2).
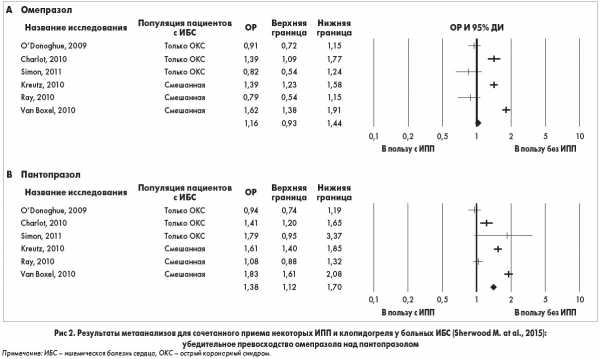
Комментируя полученные данные, М. Sherwood и соавт. высказали предположение, что анализ показателей относительно безопасности приема ИПП при проведении ДАТТ следует проводить для каждого представителя этой группы в отдельности, не обобщая все данные в одну группу и не рассматривая вопрос с позиции «польза / вред всех ИПП».
Чрезвычайно интересны результаты обсервационного исследования, выполненного под руководством А. Guérin (2016). Исследователи постарались установить, как повлияла рекомендация FDA по предпочтительному назначению пантопразола при проведении ДАТТ.
Ученые констатировали два важных факта: публикация рекомендации FDA привела к уменьшению общего количества пациентов, которым была назначена комбинация клопидогреля – ИПП; однако, несмотря на снижение доли больных, получавших комбинацию клопидогрела и ИПП, омепразол оставался наиболее часто используемым препаратом, назначаемым совместно с клопидогрелем.
Третий удар нанесли Т. Shamliyan и соавт. (2017), авторы широкомасштабной работы, в основу которой легли результаты 17 систематических обзоров и метаанализов, 16 рандомизированных контролированных исследований и 16 обсервационных исследований.
Команда ученых анализировала особенности сочетанного приема ИПП с 10 различными классами лекарственных средств. Изучив полученные данные, Т. Shamliyan и соавт. резюмировали: «В отношении конкретных ИПП одновременный прием пантопразола или эзомепразола, но не омепразола и лансопразола, ассоциирован с повышением риска общей летальности, нефатального инфаркта миокарда и инсульта».
Цирроз печени и ИПП – все совсем не просто
Еще одним камнем преткновения в проблеме безопасного применения ИПП стал цирроз печени. Больным циррозом печени, вне зависимости от этиологической причины заболевания, свойственен высокий риск развития портальной гипертензивной гастропатии, появления вариксов в пищеводе и желудке, а также возникновения кровотечения из варикозно-расширенных вен. Для лечения и профилактики указанных осложнений используются ИПП.
Однако оказалось, что эта простая на первый взгляд рекомендация влечет за собой ряд серьезных проблем: применение ИПП у больных циррозом печени ассоциируется с резким возрастанием риска возникновения инфекционных осложнений и печеночной энцефалопатии. Незамедлительно последовала реакция медицинской общественности: одни ученые рекомендовали значительно ограничить показания к назначению ИПП в данной категории больных, другие высказали более радикальное мнение: считать цирроз печени противопоказанием к назначению этих лекарственных средств.
Сгустившиеся тучи над ИПП развеяла статья R. Weersink и соавт., опубликованная в апреле 2018 г. в авторитетном журнале British Journal of Clinical Pharmacology. Эта группа ученых последовала рекомендациям М. Sherwood и проанализировала безопасность применения ИПП, не объединяя все препараты в одну группу. Основываясь на результатах анализа 69 исследований, авторы метаанализа доказали, что применение только трех ИПП не ассоциировано с появлением «дополнительных известных рисков».
В данную категорию вошли омепразол, эзомепразол и рабепразол. R. Weersink и соавт. установили, что безопасность приема перечисленных ИПП зависит от степени тяжести цирроза, определенной по шкале Чайлд-Пью: больным циррозом печени, состояние которых соответствует классу А и В, можно назначать омепразол и рабепразол, но желательно уменьшить максимальную суточную дозу перечисленных лекарственных средств.
Пациентам, находящимся в крайне тяжелом состоянии (класс С), следует рекомендовать только эзомепразол в максимальной суточной дозе 20 мг. Пантопразол и лансопразол признаны «небезопасными препаратами», т. к. их прием ассоциирован с 4-8-кратным увеличением риска различных осложнений.
Заключение, или Продолжение следует?
В настоящее время вопрос безопасности одновременного применения ИПП и клопидогреля в составе ДАТТ продолжает оставаться открытым. По мнению ряда ведущих международных экспертов, следует ожидать обновления рекомендаций различных кардиологических обществ по выбору ИПП при проведении ДАТТ.
Ремарка. Омез®
Среди множества генерических омепразолов, представленных на отечественном рынке, наибольшей известностью пользуется препарат Омез®, представляемый фирмой «Dr. Reddy’s Laboratories Limited». За спиной у Омеза – клинический опыт его активного применения во многих странах мира, равный нескольким десятилетиям. За это время Омез® успел доказать свою терапевтическую эквивалентность оригинальному омепразолу.
Небрендированный омепразол производства «Др. Реддис Лабораторис» занял достойное место в известной Orange Book, публикуемой FDA. Применение Омеза обсуждалось международной экспертной группой Gastrosphere 1.0 и 2.0 для профилактики и лечения НПВП-индуцированных поражений верхних отделов желудочно-кишечного тракта. Омез® в дозе 10-20 мг может использоваться для проведения безопасной кислотосупрессивной терапии у больных циррозом печени класса А-В по шкале Чайлд-Пью.
Выводы
На основании вышеизложенного можно утверждать, что в настоящее время омепразол является одним из наиболее изученных препаратов в своем классе. Важно также отметить, что омепразол является одним из наиболее часто назначаемых ИПП и как ИПП входит в стандарты лечения КЗЗ в США и странах Европы. На украинском фармацевтическом рынке среди генерических омепразолов наибольшую популярность получил препарат Омез®.
Литература
1. Miner PJr, Katz PO, Chen Y, et al. Gastric acid control with esomeprazole, lansoprazole, omeprazole, pantoprazole, and rabeprazole: A five-way crossover study. Am J Gastroenterol 2003;98:2616-20. DOI: 10.1111/j.1572-0241.2003.08783.x.
2. Food and Drug Administration. Follow-Up to the January 26, 2009, Early Communication about an Ongoing Safety Review of Clopidogrel Bisulfate (marketed as Plavix) and Omeprazole (marketed as Prilosec and Prilosec OTC) [Internet]. U. S. Food and Drug Administration; 2009 [cited 1 Jan 2015]. Available: http://www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsand
Providers/DrugSafetyInformationforHeathcareProfessionals/ucm190784.htm.
3. Holmes DR, Dehmer GJ, Kaul S, Leifer D, O’Gara PT, Stein CM. ACCF/AHA clopidogrel clinical alert: approaches to the FDA “boxed warning”: a report of the American College of Cardiology Foundation Task Force on clinical expert consensus documents and the American Heart Association endorsed by the Society for Cardiova. J Am Coll Cardiol. 2010; 56: 321-41. doi: 10.1016/j.jacc.2010.05.013 PMID:20633831.
4. Bhatt DL, Cryer BL, Contant CF, Cohen M, Lanas A, Schnitzer TJ, et al. Clopidogrel with or without omeprazole in coronary artery disease. N Engl J Med. 2010; 363: 1909-17. doi: 10.1056/NEJMoa1007964 PMID: 20925534.
5. Vaduganathan M. Efficacy and Safety of Proton-Pump Inhibitors in High-Risk Cardiovascular Subsets of the COGENT Trial. Am J Med. 2016 Sep;129(9):1002-5. doi: 10.1016/j.amjmed.2016.03.042. Epub 2016 Apr 30.
6. Roffi М. 2015 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Task Force for the Management of Acute Coronary Syndromes in Patients Presenting without Persistent ST-Segment Elevation of the European Society of Cardiology (ESC). European Heart Journal (2016) 37, 267-315. doi:10.1093/eurheartj/ehv320.
7. Guérin A, Mody R, Carter V, Ayas C, Patel H, Lasch K, et al. (2016) Changes in Practice Patterns of Clopidogrel in Combination with Proton Pump Inhibitors after an FDA Safety Communication. PLoS ONE11(1): e0145504. doi:10.1371/journal. pone.0145504.
8. Shamliyan TA. Patient-centered Outcomes with Concomitant Use of Proton Pump Inhibitors and Other Drugs. Clin Ther. 2017 Feb;39(2):404-427.e36. doi: 10.1016/j.clinthera.2017.01.011. Epub 2017 Feb 9.
9. Российские стандарты по лечению инфаркта миокарда (2015).
10. Matthew W. Sherwood. Individual Proton Pump Inhibitors and Outcomes in Patients With Coronary Artery Disease on Dual Antiplatelet Therapy: A Systematic Review. J Am Heart Assoc. 2015;
4: e002245 doi: 10.1161/JAHA.115.002245.
11. Weersink RA. Safe use of proton pump inhibitors in patients with cirrhosis. Br J Clin Pharmacol. 2018 Apr 24. doi: 10.1111/bcp.13615.
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (434-435), липень 2018 р.
СТАТТІ ЗА ТЕМОЮ Терапія та сімейна медицина
05.03.2020 Нефрологія Педіатрія Терапія та сімейна медицина Урологія та андрологія Гематурия у детей: что нужно знать педиатру и семейному врачу?Гематурия является одним из проявлений мочевого синдрома. По данным различных популяционных скринингов, частота гематурии у детей колеблется от 1-4 до 12-18% случаев [2, 11, 19]. Уровень распространенности среди детей школьного возраста составляет 4,1-5,13% на основании только одного анализа мочи [19, 26] и 0,5-2% при исследовании двух и более анализов мочи [11, 19, 26]. Связь гематурии с расой, социально-экономическим статусом, полом и возрастом пациента не установлена [11, 19]....
05.03.2020 Терапія та сімейна медицина Діагностика та лікування респіраторних захворювань у дітей та дорослихГострі інфекції дихальних шляхів (ГІДШ) – найчастіша причина призначення антибіотиків (АБ) у дорослих (41% усіх призначень) (Harris, 2016). Нідерландське обсерваційне дослідження встановило, що надмірне використання АБ було найпоширенішим у віковій групі 18-65 років та серед осіб, які скаржилися на біль у горлі (Dekker, 2015)....
05.03.2020 Алергія та імунологія Терапія та сімейна медицина Алергічний риніт у практиці сімейного лікаряНаприкінці минулого року в Києві відбулася науково-практична конференція з міжнародною участю «Компетенції сімейного лікаря в питаннях реабілітації пацієнтів». У рамках заходу особливу увагу було приділено питанням, із якими найчастіше стикаються спеціалісти первинної ланки охорони здоров’я....
05.03.2020 Терапія та сімейна медицина Медичні кадри України: аналіз за 2018 рік (продовження)В Україні підтримано проголошені резолюцією Генеральної Асамблеї Організації Об’єднаних Націй від 25 вересня 2015 року № 70/1 Глобальні цілі сталого розвитку до 2030 року. Плани щодо реалізації цілей і адаптації завдань та індикаторів з огляду на вітчизняну специфіку викладено в національній доповіді «Цілі сталого розвитку: Україна». Впровадження ініціатив Організації Об’єднаних Націй, міжнародних зобов’язань у рамках євроінтеграційних процесів суттєво змінює систему охорони здоров’я в Україні. ...
Подводные камни длительной кислотосупрессии ингибиторами протонной помпы | #08/14
Кислотозависимые заболевания представляют большую группу страданий, требующих зачастую пожизненной кислотосупрессивной терапии. С позиции патогенеза, прогнозируемой эффективности и безопасности, рациональным выбором для длительной терапии гастроэзофагеальной рефлюксной болезни, эпигастрального болевого синдрома, профилактики НПВП-гастропатии, лечения синдрома Золлингера–Эллисона является класс препаратов, названных «ингибиторы протонного насоса или помпы» (ИПП). В Анатомо-терапевтическо-химической международной системе классификации лекарственных средств (АТХ) эта группа препаратов имеет код A02BC и входит в раздел A02B «Противоязвенные препараты и препараты для лечения гастроэзофагеального рефлюкса» [1]. В Российской Федерации зарегистрировано 5 лекарственных средств: омепразол, лансопразол, пантопразол, рабепразол и эзомепразол [2].
ИПП относятся к наиболее часто назначаемым препаратам. Так, в 2009 г. около 21 млн человек в США принимали ИПП. Большинство пациентов лечились ИПП более 180 дней [3]. Результаты клинических исследований подтвердили их хорошую переносимость. В рамках экспериментов доказан широкий терапевтический диапазон ИПП. Так, разовые пероральные дозы омепразола до 400 мг не вызывали каких-либо тяжелых симптомов. При приеме взрослыми 560 мг омепразола отмечалась умеренная интоксикация. Однократное применение эзомепразола внутрь в дозе 80 мг не вызвало каких-либо симптомов. Повышение дозы до 280 мг сопровождалось общей слабостью и симптомами со стороны желудочно-кишечного тракта. Максимальная суточная доза рабепразола, принятая преднамеренно, составила 160 мг с минимальными нежелательными явлениями, не потребовавшими лечения [2].
Как и другие лекарственные препараты, ИПП не лишены побочных эффектов. Побочным эффектом считается любая реакция организма, возникшая в связи с применением лекарственного препарата в дозах, рекомендуемых инструкцией по его применению [4]. В ходе клинических исследований были зафиксированы неспецифические неблагоприятные нежелательные эффекты, слабо или умеренно выраженные, преходящего характера. Наиболее часто (отметили от ≥ 1/100 до < 1/10 пациентов, принимавших ИПП) возникали жалобы на головную боль, боль в животе, запор, диарею, метеоризм и тошноту. Имеется ограниченное число наблюдений о возможности эффективной замены одного ИПП другим в случаях возникновения неблагоприятных лекарственных реакций или индивидуальной непереносимости какого-либо из препаратов этой группы [2].
Препарат-специфические побочные эффекты: P-гликопротеин, цитохром CYP450
Полипрагмазия является зачастую вынужденным решением при лечении полиморбидных пациентов. При этом возникает необходимость оценить потенциальный риск взаимодействия препаратов. ИПП отличаются по профилю и выраженности межлекарственных взаимодействий из-за различий в степени подавления переносчиков (транспортеров) лекарств и особенностей метаболизма.
Аденозин-трифосфатзависимый эффлюксный транспортный Р-гликопротеин
Одним из препарат-специфических побочных эффектов является взаимодействие ИПП с аденозин-трифосфатзависимым эффлюксным транспортным Р-гликопротеином — продуктом АВСВ1 (MDR1) гена. Р-гликопротеин обладает способностью уменьшать внутриклеточное накопление и цитотоксичность структурно и функционально различных лекарств. Его функцией являются энергозависимый транспорт (эффлюкс) за пределы клетки и уменьшение внутриклеточной концентрации большого числа ксенобиотиков, в том числе лекарственных препаратов. Субстратами, влияющими на активность Р-гликопротеиновой транспортной системы, являются дигоксин, циметидин, такролимус, нифедипин, кетоконазол и амитриптилин. ИПП в разной степени подавляют эту транспортную систему, повышая концентрацию препаратов в крови. В эксперименте было показано, что 50% ингибирование Р-гликопротеин-опосредованного эффлюкса дигоксина достигается при различных концентрациях ИПП (17,7 мкмоль/л для омепразола, 17,9 мкмоль/л для пантопразола и 62,8 мкмоль/л для лансопразола) [5]. Это исследование продемонстрировало большую безопасность лансопразола по сравнению с омепразолом и пантопразолом при сочетании дигоксином. Рабепразол (оригинальный препарат Париет) обладает минимальной тропностью к Р-гликопротеину [6]. Прямое сравнительное наблюдательное исследование лансопразола и рабепразола по степени взаимодействия с цитостатиками после трансплантации органов выявило меньшее влияние на Р-гликопротеин рабепразола, что обеспечило большую безопасность [7].
Цитохром Р450
Все ИПП в различной степени подвергаются биотрансформации в печени, что повышает их гидрофильность и тем самым способствует выведению из организма. Окислительный метаболизм ИПП проходит с участием субстрат-специфичных изоферментов 2 и 3 семейства цитохрома Р450. В ходе метаболизма с участием изоформы CYP2C19 образуются гидрокси- и деметилированные метаболиты, а через окисление CYP3A4 — сульфон. Максимальной аффинностью к CYP2C19 обладают омепразол (тестовый субстрат) и эзомепразол, что объясняет их высокий потенциал взаимодействия. При одновременном применении омепразола и эзомепразола с препаратами, в метаболизме которых участвует изофермент CYP2C19, такими как диазепам, циталопрам, имипрамин, кломипрамин, фенитоин, может увеличиться концентрация этих препаратов в плазме крови и, соответственно, потребоваться уменьшение их дозы [2].
Два ИПП — пантопразол и рабепразол (Париет) обладают особенностями метаболизма, обеспечивающими наименьший риск взаимодействия с другими ксенобиотиками на уровне системы CYP450 [8–10]. Пантопразол, после прохождения I окислительной фазы метаболизма в системе цитохрома, завершает процесс гидрофилизации с участием сульфотрансферазы цитозоля через конъюгацию с сульфатом (II фаза биотрансформации). Конъюгированный сульфат — основной метаболит в плазме. Рабепразол (Париет) имеет преимущественно неэнзиматический нецитохромовый метаболизм. Основным метаболитом рабепразола является тиоэфир. Сульфон — основной метаболит других ИПП (омепразола, эзомепразола и лансопразола), практически не определяется в крови. Около 90% рабепразола выводится с мочой главным образом в виде двух метаболитов: конъюгата меркаптуровой кислоты и карбоновой кислоты. Оставшаяся часть принятого рабепразола натрия выводится с калом. Суммарное выведение составляет 99,8% [2, 8].
Для оценки ингибирующего влияния ИПП на активность ферментов цитохрома Р450 проведен целый ряд экспериментов с микросомами печени человека и рекомбинантными изоформами. Оценивалось значение константы ингибирования (Ki) — минимальной концентрации ИПП для блокирования активности фермента. Выявлены различия в Ki для всех ИПП (лансопразол — 0,4–1,5 мкм, омепразол — 2–6 мкм, эзомепразол — ∼8 мкм, пантопразол — 14–69 мкм и рабепразол — 17–21 мкм) [9]. Высокие значения Ki для пантопразола и рабепразола свидетельствуют о более низком потенциале взаимодействия, что подтверждается и другими источниками официальной информации (табл. 1).
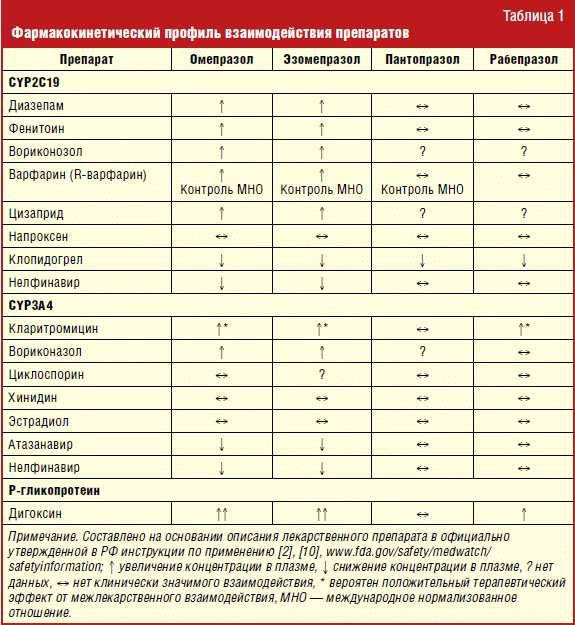
Декслансопразол (одобрен к применению с США) и лансопразол, напротив, могут ускорять элиминацию препаратов, метаболизирующихся при участии изофермента CYP1А2, в частности теофиллина [11].
Клопидогрел
Клинической иллюстрацией значения межлекарственного взаимодействия может служить дискуссия о ИПП и клопидогреле.
На ежегодной научной сессии американского общества сердечно-сосудистой ангиографии и интервенции (SCAI) 6 мая 2009 г. были доложены результаты исследования The Clopidogrel Medco Outcomes Study, в котором оценивалась клиническая эффективность двойной антитромбоцитарной терапии (ДАТ) (Аспирин + клопидогрел) и ДАТ в комбинации с ИПП у больных после ангиопластики коронарных артерий со стентированием. В исследование было включено 16 690 пациентов. Больные принимали ИПП (пантопразол, эзомепразол, омепразол или ланзопразол) в среднем в течение 9 месяцев. Основные клинические исходы включали госпитализации по поводу сердечных приступов, нестабильной стенокардии, инсульта и повторной реваскуляризации миокарда. Комбинация ИПП с клопидогрелом (Плавиксом) увеличивала риск повторных коронарных событий на 50%. До 70% всех событий приходилось на приступы стенокардии и нестабильную стенокардию, 48% — на инсульт и транзиторные ишемические атаки, а в 35% случаев потребовались повторные коронарные процедуры [12]. Анализируя данные исследования The Clopidogrel Medco Outcomes Study и другие работы, Управление по надзору за качеством пищевых продуктов и лекарственных средств США (Food and Drugs Administration of the United States, FDA) в 2010 г. предупредило о риске снижения эффективности клопидогрела (Плавикс) при одновременном применении с любым ИПП независимо от временных рамок, разделяющих прием препаратов в течение суток.
На сегодняшний день получены противоречивые данные о влиянии ИПП на эффективность клопидогрела [13]. Вероятно, сложность трактовки данных объясняется особенностями фармакокинетики самого клопидогрела (Плавикс). Препарат является пролекарством с фармакогенетическими различиями метаболизма. Однако, несмотря на неоднозначную трактовку клинической значимости взаимодействия с клопидогрелом, фирмами-производителями лекарств и FDA пересмотрены инструкции по применению клопидогрела, омепразола и эзомепразола. Новая маркировка предписывает не сочетать перечисленные выше препараты из-за большего, по сравнению с другими ИПП, влияния омепразола и эзомепразола на CYP2C19-опосредованный метаболизм клопидогреля. По результатам исследований отмечено фармакокинетическое и фармакодинамическое взаимодействие между клопидогрелом (нагрузочная доза 300 мг и поддерживающая доза 75 мг/сут) и омепразолом (80 мг/сут внутрь), которое приводит к снижению экспозиции активного метаболита клопидогрела в среднем на 46% и снижению максимального ингибирования АДФ-индуцированной агрегации тромбоцитов в среднем на 16% [2]. При необходимости гастропротекции на фоне приема клопидогрела рекомендуется назначать пантопразол, рабепразол, лансопразол или декслансопразол [14].
Класс-специфические побочные эффекты: биодоступность препаратов с рН-зависимой абсорбцией
Класс-специфические эффекты не зависят от конкретного препарата. Их возникновение связано с фармакологическим действием ИПП. Так как применение этих препаратов прогнозируемо приводит к выраженному и длительному подавлению выработки соляной кислоты, повышение рН содержимого желудка снижает биодоступность препаратов с рН-зависимой абсорбцией. К такому типу взаимодействия можно отнести взаимодействие ИПП с кетоконазолом и итраконазолом. Концентрация этих противогрибковых препаратов в плазме крови при одновременном применении будет снижаться, что может потребовать коррекции дозы [2].
К класс-специфическим эффектам, обусловленным снижением кислотности желудочного сока, относят и выявленное влияние на абсорбцию цианокобаламина (витамина В12), железа, кальция и магния.
Дефицит витамина В12
В организме человека витамин В12 практически не вырабатывается. В желудке витамин В12, содержащийся в пище животного происхождения, под влиянием пепсина связывается с R-белками — транскобаламинами I и III. Эта фаза трансформации необходима для осуществления связи витамина В12 с внутренним фактором Касла в двенадцатиперстной кишке и последующим всасыванием в подвздошной кишке. При ахлоргидрии нарушается переход пепсиногена в пепсин, что приводит к нарушению всасывания и развитию В12-дефицитного состояния и анемии [15].
Короткие курсы ИПП практически не влияют на метаболизм витамина В12 в организме. Еще несколько лет назад результаты клинических наблюдений и метаанализов свидетельствовали о повышении риска анемии только при неблагоприятном преморбидном фоне: у пожилых пациентов с атрофическим гастритом, сочетанным с Helicobacter pylori-ассоциированным и аутоиммунным гастритом, после резекции желудка, при лечении высокими дозами ИПП больных с синдромом Золлингера–Эллисона [16, 17]. Однако результаты последнего опубликованного крупного сравнительного ретроспективного исследования 25 956 пациентов с верифицированной В12-дефицитной анемией позволили сделать вывод о том, что применение антисекреторной терапии в течение двух и более лет достоверно дозозависимо ассоциировалось с повышением риска В12-дефицита (ИПП — ОШ = 1,65 [95% ДИ 1,58–1,73] и блокаторов Н2-рецепторов гистамина — ОШ = 1,25 [95% ДИ 1,17–1,34]) [18].
Дефицит железа
Абсорбция железа также является рН-зависимой. Железо в пище содержится в основном в форме нерастворимого плохо всасывающегося трехвалентного железа Fe (III). Железо всасывается в тонкой кишке только после солюбилизации соляной кислотой и окисления до двухвалентной формы Fе (II) [19]. Кратковременная гипохлоргидрия и ахлоргидрия при нормальном рационе не приводит ни к латентному, ни к явному дефициту железа в организме. Однако длительная кислотосупрессивная терапия ИПП повышает риск развития железодефицитных состояний вследствие мальабсорбции железа [20].
Остеопороз
Первые сведения о том, что ИПП могут снижать минеральную плотность костей, появились в публикациях в 1995 г. Сперва доминировала точка зрения о непосредственном влиянии ИПП на ионные насосы или кислотозависимые ферменты костной ткани, вызывая процессы структурного ремоделирования с развитием остеопении и остеопороза [21]. В настоящее время обсуждается теория мальабсорбции кальция: на фоне медикаментозной ахлоргидрии нарушается переход солей кальция в растворимую форму, ухудшая абсорбцию кальция. Сообщение о новом класс-специфическом побочном действии — повышении риска перелома бедра, запястья, позвоночника у пациентов старше 50 лет при приеме высоких доз ИПП более 1 года было опубликовано 25.05.10 г. на сайте FDA [22]. Недавно стали известны результаты канадского мультицентрового популяционного исследования, посвященному оценке остеопороза. Минеральная плотность костной ткани бедренной кости, тазобедренного и поясничного отдела позвоночника (L1-L4) оценивалась в исходном состоянии пациентов, через 5 и 10 лет на фоне приема ИПП. Сделан вывод о том, что использование ИПП не привело к прогрессированию изменений костной ткани [23].
Гипомагниемия
В 2006 г. впервые была описана гипомагниемия на фоне длительного приема ИПП [24]. В 2011 г., несмотря на единичные случаи, FDA опубликовало сообщение о новом непредвиденном нежелательном явлении — гипомагниемии. Механизм развития гипомагниемии в настоящее время неясен. Симптомы возникают при снижении уровня магния < 0,5 ммоль/л. Указанному снижению часто сопутствует гипокалиемия. Серьезными побочными явлениями были тетания, аритмия и судороги. Пероральный прием препаратов магния уменьшает выраженность клинической симптоматики, но не повышает сывороточную концентрацию магния. В то же время отмена ИПП приводит к восстановлению минерального баланса [25]. У пациентов, длительно принимающих ИПП в сочетании с дигоксином или препаратами, которые могут вызвать гипомагниемию (например, диуретики), необходимо контролировать уровень магния до начала лечения ИПП и в период лечения. Данные по взаимодействию суммированы в табл. 2.
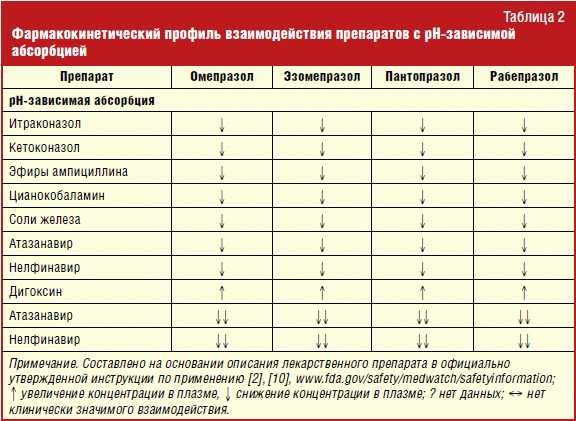
Учитывая влияние на метаболизм минералов и витаминов, необходимо взвешенно подходить к подбору дозы и длительности назначения ИПП пациентам, особенно старших возрастных групп, с учетом индивидуальных особенностей метаболизма и коморбидных состояний.
Класс-специфические побочные эффекты: гипергастринемия, онкогенный потенциал
Подавляя кислотопродукцию в желудке по механизму обратной связи, все ИПП способствуют повышению уровня сывороточного гастрина. Гастрин стимулирует рост некоторых типов эпителиальных клеток (желудка, слизистой оболочки толстой кишки, поджелудочной железы) [26]. Основой опасений в отношении повышения риска развития рака у людей были эксперименты, выполненные на трансгенных мышах с мутантной формой АРС (APCMin-/+). Автору удалось показать влияние индуцированной омепразолом гипергастринемии на скорость пролиферации клеток аденомы и сокращение продолжительности жизни мышей. Гипергастринемия у людей, длительно (от 5 до 15 лет) непрерывно принимающих ИПП, действительно сопровождалась гиперплазией энтерохромаффинноподобных клеток желудка, увеличением массы обкладочных клеток, увеличением уровня хромогранина А (CgA). Концентрация гастрина возвращалась к исходному уровню обычно в течение 1–2 недель после прекращения лечения. Однако ни в одном случае эти изменения не привели к развитию дисплазии, рака или нейроэндокринных опухолей. Кроме того, при отсутствии H. pylori, атрофия слизистой оболочки желудка не прогрессировала ни в антральном, ни в фундальном отделах [27–30].
В доступной литературе имеются противоречивые данные относительно риска развития полипов желудка на фоне длительной терапии ИПП. Однако многолетние наблюдения позволяют сделать вывод о том, что риск малигнизации этих полипов крайне низок при условии эрадикации H. pylori [31].
Эпидемиологических исследований, направленных на изучение связи между длительным лечением ИПП и риском рака поджелудочной железы, не проводилось.
При приеме ИПП обычно увеличивается выработка биологически активного амида гастрина, трофическое воздействие которого на эпителий может быть относительно слабым и обратимым. Частота развития полипов в желудке не коррелирует с уровнем гастрина. У препаратов группы ИПП не подтвержден онкогенный потенциал у людей.
Класс-специфические побочные эффекты: инфекционные осложнения
Гипо- и ахлоргидрия на фоне приема ИПП способствует колонизации желудочно-кишечного тракта патогенной и условно-патогенной микрофлорой, вызывая дисбиотические изменения различных локусов организма.
C. difficile-инфекция
Растет число сообщений о риске развития клостридиальной инфекции во внебольничных условиях при отсутствии других факторов риска Clostridium difficile [32]. Нозокомиальная клостридиальная инфекция на фоне длительного применения ИПП чаще развивается после курса антибактериальной терапии у пожилых и пациентов с иммуносупрессией. У больных в критических состояниях, получающих антисекреторные препараты для профилактики кровотечений, ИПП являются независимым фактором риска клостридиальной диареи [33]. Вероятность развития C. difficile-ассоциированной диареи по показателю number needed to harm (NNH) — число больных, которым в результате лечения причинен вред, = индекс потенциального вреда — составляет 1 случай на 3925 человек, принимавших ИПП в течение года [34]. Не получила подтверждения гипотеза о повышении риска рецидивирующего течения клостридиальной инфекции на фоне ИПП [35].
Пневмония
В основу обсуждаемой проблемы о повышении риска пневмонии на фоне ИПП легли теоретические выкладки о возможной бактериальной аспирационной транслокации вследствие колонизации пищевода и желудка при подавлении кислотного барьера желудка. Результаты трех метаанализов, включивших 8 обсервационных исследований, убедительно показывали связь между приемом ИПП и развитием пневмонии: на 27% повышался риск нозокомиальной или внебольничной пневмонии (ОШ = 1,27, 95% ДИ 1,11–1,46). Вызывает удивление факт обратной зависимости между силой связи и длительностью приема ИПП [36]. Риск развития легочной инфекции значительно выше в первые 48 ч после начала приема ИПП. Продолжительность приема ИПП менее 7 дней ассоциировалась с трехкратным повышением риска внебольничной пневмонии (ОШ = 3,95, 95% ДИ 2,86–5,45). Возможно, речь идет о методической ошибке при оценке взаимосвязи симптомов кашель–изжога–инфекция. Вероятно, начальные симптомы пневмонии трактовались как гастроэзофагеальная рефлюксная болезнь, вследствие чего инициировался прием ИПП, что и послужило причиной протопатической ошибки. Такая точка зрения подкрепляется данными последующего метаанализа. С учетом вероятности протопатической ошибки, не было обнаружено ассоциации между приемом ИПП и внебольничной пневмонией [37].
Профилактическое назначение антисекреторных препаратов (ИПП, блокаторов Н2-рецепторов гистамина) для предупреждения аспирации в рамках предоперационной подготовки или у пациентов, находящихся на искусственной вентиляции легких, сопровождалось увеличением риска нозокомиальной пневмонии и, возможно, обусловлено увеличением риска колонизации желудка больничными патогенами [36].
В целом обсервационные данные в отношении риска пневмонии при применении ИПП крайне противоречивы и требуют уточнения.
Спонтанный бактериальный перитонит
Профилактическое назначение ИПП пациентам с циррозом достоверно повышает риск развития спонтанного бактериального перитонита. Некоторыми авторами обсуждается возможное влияние ИПП на функцию нейтрофилов. Однако общепризнанной является точка зрения о снижении деконтаминирующей функции желудочного сока вследствие гипохлоргидрии на ИПП и развитии синдрома избыточного бактериального роста в тонкой кишке с последующей транслокацией микробов и контаминацией асцитической жидкости [38].
Фармакокинетика в особых ситуациях: почечная, печеночная недостаточность, пожилые люди
Во избежание ошибок дозирования необходимо строго следовать инструкции по применению препарата с учетом торгового названия, так как даже при одинаковом международном непатентованном наименовании препараты могут отличаться по целому ряду описаний. В табл. 3 кратко суммированы наиболее важные для безопасности больного положения о режимах дозирования.
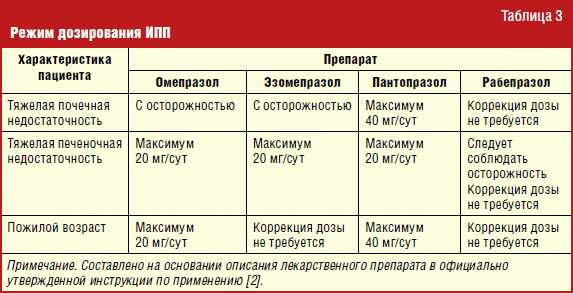
У пациентов с циррозом печени существенно меняется метаболизм ИПП, за счет увеличения площади под фармакокинетической кривой для препаратов. У таких больных (особенно с медленным типом метаболизма по изоферменту CYP2C19) повышается вероятность нежелательных явлений. Максимальную зависимость концентрации от генетического полиморфизма по CYP2C19 демонстрирует омепразол. Влияние типа метаболизма на концентрацию ИПП прогрессивно снижается в ряду: лансопразол, эзомепразол, пантопразол, с наименьшей зависимостью у рабепразола (Париет) [39].
Заключение
ИПП являются наиболее эффективными антисекреторными препаратами для лечения кислотозависимых заболеваний. Многолетнее широкое применение в клинической практике способствовало накоплению информации не только об эффективности, но и о нежелательных явлениях на фоне их использования. Короткие курсы лечения кислотосупрессивными препаратами практически не сопровождаются клинически значимыми нежелательными эффектами. Однако при целом ряде распространенных гастроэнтерологических заболеваний возникает оправданная необходимость не только в постоянном назначении ИПП, но и в сочетании с другими препаратами. Использование нескольких лекарственных средств повышает вероятность их взаимодействия. Знание наиболее часто встречающихся и прогнозируемых нежелательных явлений позволит не только прогнозировать их возникновение, но и предупредить развитие мониторингом показателей. Из имеющихся на российском фармацевтическом рынке ИПП рабепразол (Париет) обладает преимуществом в области безопасности, т. к. имеет наименьший риск межлекарственных взаимодействий в силу особенностей метаболизма. Тем не менее, минимизация дозы и длительности приема ИПП в соответствии с клинической ситуацией, внимательная оценка показателей жизненно важных функций организма, определение электролитного состава крови и исследование минеральной плотности костей в группах риска остеопороза позволят избежать нежелательных явлений.
Литература
- http://www.who.int/classifications.
- grls.rosminzdrav.ru (Нексиум рег. №: П N013775/01 от 31.05.07, Эманера рег. №: ЛП-002047 от 11.04.13, Лосе МАПС рег. №: П N013848/01 от 29.09.11, Ортанол рег. №: ЛСР-007825/08 от 06.10.08, Нольпаза рег. №: ЛСР-009049/08 от 19.11.08, Контролок рег. №: П N011341/01 от 28.04.08, Париет рег. №: П N011880/01 от 15.09.11).
- http://www.fda.gov/drugs: SDI, Vector One®: Total Patient Tracker (TPT). 2002–2009. Data extracted 3–24–10.
- Федеральный закон Российской Федерации от 12 апреля 2010 г. № 61-ФЗ «Об обращении лекарственных средств».
- Pauli-Magnus C., Rekersbrink S., Klotz U. et al. Interaction of omeprazole, lansoprazole and pantoprazole with P-glycoprotein // Naunyn Schniedebergs Arch Pharmacol. 2001; 364: 551–557.
- Itagaki F., Homma M., Takara K. et al. Effect of rabeprazole on MDR1-mediated transport of Rhodamine 123 in Caco-2 and Hvr100–6 cells // Biol Pharm Bull. 2004, Oct; 27 (10): 1694–1696.
- Miura M., Satoh S., Inoue K. et al. Influence of lansoprazole and rabeprazole on mycophenolic acid pharmacokinetics one year after renal transplantation // Ther Drug Monit. 2008, Feb; 30 (1): 46–51.
- Setoyama T., Drijfhout W. J., van de Merbel N. C. et al. Mass balance study of [14 C] rabeprazole following oral administration in healthy subjects // Int J Clin Pharmacol Ther. 2006, Nov; 44 (11): 557–565.
- Andersson T. B., Ahlström M. et al. Comparison of inhibitory effects of the proton pump-inhibiting drugs omeprazole, esomeprazole, lansoprazole, pantoprazole, and rabeprazole on human cytochrome P450 activities // Drug Metab Dispos. 2004, Aug; 32 (8): 821–827.
- Wedemeyer R. S., Blume H. Pharmacokinetic drug interaction profiles of proton pump inhibitors: an update // Drug Saf. 2014, Apr; 37 (4): 201–211.
- Pearce R. E., Rodrigues A. D., Goldstein J. A. et al. Identification of the human P450 enzymes involved in lansoprazole metabolism // J Pharmacol Exp Ther. 1996; 277: 805–816.
- Kreutz R., Stanek E., Aubert R. et al. Impact of proton pump inhibitors on the effectiveness of clopidogrel after coronary stent placement: the clopidogrel medco outcomes study // Pharmacotherapy. 2010; 30 (8): 787–796.
- Gerson L. et al. Lack of significant interactions between clopidogrel and proton pump inhibitor therapy: meta-analysis of existing literature // Dig. Dis. Sci. 2012; 57 (5): 1304–1313.
- Johnson D. A. I., Chilton R., Liker H. R. Proton-pump inhibitors in patients requiring antiplatelet therapy: new FDA labeling // Postgrad Med. 2014, May; 126 (3): 239–245.
- Kapadia C. Cobalamin (Vitamin B12) deficiency: is it a problem for our aging population and is the problem compounded by drugs that inhibit gastric acid secretion? // J Clin Gastroenterol. 2000; 30: 4–6.
- Den Elzen W. P., Groeneveld Y., de Ruijter W., Souverijn J. H., le Cessie S., Assendelft W. J., Gussekloo J. Long-term use of proton pump inhibitors and vitamin B12 status in elderly individuals // Aliment Pharmacol Ther. 2008; 27: 491–497.
- Thomson A. B., Sauve M. D., Kassam N., Kamitakahara H. Safety of the long-term use of proton pump inhibitors // World J Gastroenterol. 2010, May 21; 16 (19): 2323–2330.
- Lam J. R., Schneider J. L., Zhao W., Corley D. A. Proton pump inhibitor and histamine 2 receptor antagonist use and vitamin B12 deficiency // JAMA. 2013, Dec 11; 310 (22): 2435–2442.
- Tempel M., Chawla A., Messina C., Celiker M. Y. Effects of omeprazole on iron absorption: preliminary study // Turk J Haematol. 2013, Sep; 30 (3): 307–310.
- Sarzynski E. I., Puttarajappa C., Xie Y., Grover M., Laird-Fick H. Association between proton pump inhibitor use and anemia: a retrospective cohort study // Dig Dis Sci. 2011, Aug; 56 (8): 2349–2353.
- Tuukkanen J., Väänänen H. K. Omeprazole, a specific inhibitor of H+-K+-ATPase, inhibits bone resorption in vitro // Calcif Tissue Int. 1986, Feb; 38 (2): 123–125.
- Lewis J. R., Barre D., Zhu K., Ivey K. L., Lim E. M., Hughes J., Prince R. L. Long-Term Proton Pump Inhibitor Therapy and Falls and Fractures in Elderly Women: A Prospective Cohort Study // J Bone Miner Res. 2014, May.
- Madanick R. D. Cohort study: Proton pump inhibitors do not induce change in bone mineral density in a long-term observational study // Evid Based Med. 2013; 18: 5, 192–193.
- Epstein M., McGrath S., Law F. Proton-pump inhibitors and hypomagnesemic hypoparathyroidism // N. Engl. J. Med. 2006; 355 (17): 1834–1836.
- Tamura T. et al. Omeprazole- and Esomeprazole-associated Hypomagnesaemia: Data Mining of the Public Version of the FDA Adverse Event Reporting System // Int. J. Med. Sci. 2012; 9 (5): 322–326.
- McWilliams D. F., Watson S. A., Crosbee D. M. et al. Coexpression of gastrin and gastrin receptors (CCK-B and delta CCK-B) in gastrointestinal tumour cell lines // Gut. 1998, 42: 795–798.
- Fiocca R. Gastric exocrine and endocrine cell morphology under prolonged acid inhibition therapy: results of a 5-year follow-up in the LOTUS trial // Aliment Pharmacol Ther. 2012, Nov; 36 (10): 959–971.
- Caos A., Breiter J., Perdomo C., Barth J. Long-term prevention of erosive or ulcerative gastro-oesophageal reflux disease relapse with rabeprazole 10 or 20 mg vs. placebo: results of a 5-year study in the United States // Aliment Pharmacol Ther. 2005, Aug 1; 22 (3).
- Hirschowitz B. I., Simmons J., Mohnen J. Long-term lansoprazole control of gastric acid and pepsin secretion in ZE and non-ZE hypersecretors: a prospective 10-year study // Aliment Pharmacol Ther. 2010, Nov; 15 (11): 1795–1806.
- Brunner G., Athmann C., Schneider A. Long-term, open-label trial: safety and efficacy of continuous maintenance treatment with pantoprazole for up to 15 years in severe acid-peptic disease // Aliment Pharmacol Ther. 2012, Jul; 36 (1): 37–47.
- Fossmark R. I., Jianu C. S., Martinsen T. C., Qvigstad G., Syversen U., Waldum H. L. Serum gastrin and chromogranin A levels in patients with fundic gland polyps caused by long-term proton-pump inhibition // Scand J Gastroenterol. 2008, Jan; 43 (1): 20–24.
- Barletta J. F. I., El-Ibiary S. Y., Davis L. E. et al. Proton Pump Inhibitors and the Risk for Hospital-Acquired Clostridium difficile Infection // Mayo Clin Proc. 2013, Oct; 88 (10): 1085–1090.
- Buendgens L., Bruensing J., Matthes M. et al. Administration of proton pump inhibitors in critically ill medical patients is associated with increased risk of developing Clostridium difficile-associated diarrhea // J Crit Care. 2014, Aug; 29 (4): 696.e11–5.
- Tleyjeh I. M. at al. Association between proton pump inhibitor therapy and clostridium difficile infection: a contemporary systematic review and meta-analysis // PLoS One. 2012; 7 (12).
- Freedberg D. E., Salmasian H., Friedman C., Abrams J. A. Proton pump inhibitors and risk for recurrent Clostridium difficile infection among inpatients // Am J Gastroenterol. 2013, Nov; 108 (11): 1794–1801.
- Eom C. S., Jeon C. Y., Lim J. W. et al. Use of acid-suppressive drugs and risk of pneumonia: a systematic review and meta-analysis // CMAJ. 2011; 183: 310–319.
- Filion K., Chateau D., Targownik L. Proton pump inhibitors and the risk of hospitalisation for community-acquired pneumonia: replicated cohort studies with meta-analysis // Gut. 2014, Apr; 63 (4): 552–558.
- Miura K. I., Tanaka A., Yamamoto T., Adachi M. et al. Proton pump inhibitor use is associated with spontaneous bacterial peritonitis in patients with liver cirrhosis // Intern Med. 2014; 53 (10): 1037–1042.
- Lodato F., Azzaroli F., Di Girolamo M. et al. Proton pump inhibitors in cirrhosis: Tradition or evidence based practice? // World J Gastroenterol. 2008, May 21; 14 (19): 2980–2985.
Н. В. Захарова, доктор медицинских наук, профессор
ГБОУ ВПО СЗГМУ им. И. И. Мечникова МЗ РФ, Санкт-Петербург
Контактная информация: [email protected]
Купить номер с этой статьей в pdf
A02BC. Ингибиторы протонного насоса
Частная терапевтическая фармакология 89
Ингибиторы протонного насоса (или ингибиторы протонной помпы; часто применяется аббревиатура ИПП, реже – ИПН) – класс антисекреторных лекарственных препаратов, снижающих продукцию соляной кислоты путем блокирования в париетальных клетках слизистой оболочки желудка протонного насоса, – водородно-ка- лиевой аденозинтрифосфатазы (Н+/ К+-АТФ-азы).
Историческая справка
Первый опытный образец ИПП был синтезирован в 1974 г., а в 1975 г. появился первый промышленный образец – тимопразол. Первый препарат для клинического применения из группы ИПП – омепразол, был синтезирован в 1979 г. в Швеции и в 1988 г. представлен в Риме на Всемирном конгрессе гастроэнтерологов. Этот конгресс признал ИПП основной группой лекарственных препаратов в лечении кислотозависимых заболеваний. За омепразолом последовали лансопразол (1991 г., Франция), пантопразол (1994 г., Германия) и рабепразол (1996 г., Великобритания).
В 2001 г. в Швеции был создан левовращающий изомер (S-изомер) омепразола – эзомепразол.
АТС классификация
A: ПРЕПАРАТЫ, ВЛИЯЮЩИЕ НА ПИЩЕВАРИТЕЛЬНЫЙ ТРАКТ И ОБМЕН ВЕЩЕСТВ
A02 Препараты для лечения кислотозависимых заболеваний
A02B Средства для лечения пептической язвы и гастроэзофагеальной рефлюксной болезни
A02BC Ингибиторы протонного насоса
A02BC01 Омепразол A02BC02 Пантопразол A02BC03 Лансопразол A02BC04 Рабепразол A02BC05 Эзомепразол
Фармакокинетика
После приема внутрь ИПП быстро абсорбируются из тонкой кишки и поступают в системный кровоток – максимальная концентрация в плазме достигается через 1– 3 часа. Далее транспортируются к париетальным клеткам слизистой оболочки желудка, где выборочно накапливаются в кислой среде секреторных канальцев (концентрация в 1000 раз выше, чем в крови). После всасывания из кишечнике ИПП подвергаются метаболизму (метаболизм «первого прохождения»). Образуются неактивные ме-

90 Н. И. Яблучанский, В. Н. Савченко
таболиты, которые выводятся почками и желудочно-кишечным трактом (ЖКТ) (табл. 1). Метаболизм осуществляется двумя изомерами цитохрома Р450 – CYP2C19 и CYP3A4. Существует вероятность мутации гена, кодирующего CYP2C19, что обуславливает наличие групп людей с различным типом метаболизма ИПП: с интенсивным метаболизмом («быстрые метаболизаторы»), с промежуточным вариантом («промежуточные метаболизаторы») и с низкой скоростью метаболизма («медленные метаболизаторы»). Так, период полувыведения ИПП в группе «быстрых метаболизаторов» составляет около 1 часа, а у «медленных метаболизаторов» – от 2 до 10 часов. Среди других ИПП менее от метаболизма, обусловленного CYP2C19, зависят рабепразол и эзомепразол. Основной путь преобразований рабепразола – неферментативный (90 % выводится почками). Эзомепразол – это оптический S-изомер омепразола, который также полностью метаболизируется цитохромом Р450. Отличие его состоит в том, что R-изомер на 98 % метаболизируется CYP2C19 и лишь на 2 % СYP3А4, а эзомепразол метаболизируется CYP2C19 в значительно меньшей степени (73 %). При этом 27 % S-изомера метаболизируется через CYP3A4. Вследствие чего, у эзомепразола клиренс в 3 раза ниже по сравнению с R-изомером, который определяет его высокую биодоступность.
Основные фармакокинетические показатели ИПП приведены в табл. 1.
|
|
|
|
|
| Таблица 1 | |
|
| Показатели фармакокинетики ИПП |
|
| |||
|
|
|
|
|
|
| |
|
|
| Период | Период | Выведение, (%) | ||
| Путь | Биодоступ- | достиже- | ||||
Препараты | полувыве- |
|
| ||||
введения | ность (%) | ния макс. |
| через | |||
| дения, (ч) | почками | |||||
|
|
| конц., (ч) | ЖКТ | |||
|
|
|
|
| |||
Омепразол | Внутрь, | 30–65 | 0,5–1 | 0,5–3,5 | 77 | 18–23 | |
в/в | |||||||
|
|
|
|
|
| ||
Пантопразол | Внутрь, | 77 | 1,0–1,9 | 1,1–3,1 | 71–80 | 18 | |
в/в | |||||||
|
|
|
|
|
| ||
Лансопразол | Внутрь, | 80–85 | 1,3–1,7 | 1,7 | 14–23 | 75 | |
в/в | |||||||
|
|
|
|
|
| ||
Рабепразол | Внутрь, | 52 | 1,0–2,0 | 2,0–5,0 | 90 | 10 | |
в/в | |||||||
|
|
|
|
|
| ||
Эзомепразол | Внутрь, | 64–89 | 1,2 | 1–2 | 80 | 20 | |
в/в | |||||||
|
|
|
|
|
| ||
Фармакодинамика
Секреция соляной кислоты париетальными клетками слизистой оболочки желудка осуществляется посредством Н+/К+-АТФ-азы, активные молекулы которой встраиваются в апикальную мембрану париетальных клеток и выполняют роль протонного насоса, что обеспечивает перенос против электрохимического градиента ионов водорода (Н+) из клетки в просвет железы в обмен на ионы калия (К+) из внеклеточного пространства. В обратном направлении К+ транспортируются уже по
Частная терапевтическая фармакология 91
электрохимическому градиенту, перенося с собой ионы хлора (Cl-), вследствие чего в просвете секреторных канальцев париетальных клеток появляется соляная кислота.
Все ИПП относятся к производным бензимедазола и, будучи слабыми щелочами, накапливаются в кислой среде секреторных канальцев париетальных клеток в непосредственной близости от молекулы Н+/К+-АТФ-азы. Под влиянием соляной кислоты бензимедазол превращается в тетрациклический сульфенамид, который образует ковалентные дисульфидные связи с SH-группами цистеина Н+/К+-АТФ-азы и ингибирует данный фермент. Такие связи являются необратимыми, поэтому для восстановления секреции соляной кислоты париетальной клеткой, необходимы вновь синтезированные протонные насосы, свободные от связи с ИПП. Продолжительность антисекреторного эффекта обусловлена скоростью обновления молекул фермента (половина молекул обновляется в течении 30-48 часов). При однократном приеме ИПП наблюдается дозозависимое угнетение желудочной секреции, без достижения максимального антисекреторного эффекта (поскольку блокируются не все молекулы Н+/К+-АТФ-азы, а только те, которые находятся на секреторной мембране). Полностью данный эффект реализуется при повторном приеме ИПП в течение четырех дней, стабилизируясь к пятому дню. При этом существенное повышение интрагастральной pH > 6 поддерживается в течение 18 часов, что способствует рубцеванию язвенных дефектов в короткие сроки.
Показания и принципы использования ИПП в терапевтической клинике
–Гастроэзофагеальная рефлюксная болезнь (ГЭРБ).
–Функциональная диспепсия.
–Язвенная болезнь (ЯБ) желудка и двенадцатиперстной кишки, входят в схемы антихеликобактерной терапии.
–Гастропатии, обусловленные приемом нестероидных противовоспалительных средств (НПВС-гастропатии).
–Кровотечения из верхних отделов ЖКТ.
–Синдром Золлингера-Эллисона.
Наиболее эффективными средствами в лечении кислотозависимых заболеваний на сегодняшний день являются ИПП, которые позволяют достигать и поддерживать оптимальный уровень рН желудка в течение длительного времени. Так, для успешного лечения рефлюкс-эзофагита необходима поддержание рН > 4 на протяжении 18 часов в сутки, для заживления язв двенадцатиперстной кишки – рН>3, для эрадикации Helicobacter pylori (Нр) – рН > 5. Результаты многочисленных исследований подтвердили, что применение ИПП при кислотозависимых заболеваниях значительно эффективнее по сравнению с Н2-блокаторами. Препараты данной группы позволяют на протяжении 8–12 недель лечения достичь полного заживления эрозий слизистой оболочки пищевода у 80–90 % больных. У 70 % больных с язвами двенадцатиперст-

92 Н. И. Яблучанский, В. Н. Савченко
ной кишки и у 65 % больных с язвами желудка клиническая ремиссия достигается в течение 2-х недельной терапии ИПП. В эти же сроки почти у 70 % пациентов происходит рубцевание язвенного дефекта двенадцатиперстной кишки. Через 4 недели лечения заживление дуоденальных язв происходит уже у 90–100 % пациентов. Частота рубцевания желудочных язв через 4 и 8 недель лечения составляет 75 % и 90 %, соответственно. Специальным показанием к применению ИПП является наличие язв желудка и двенадцатиперстной кишки, резистентныех к терапии Н2-блокаторами (встречаются у 5–15 % пациентов).
ИПП при неэрозивной форме ГЭРБ (НЭРБ) назначают в поддерживающей дозе (табл. 2). При эрозивной форме ГЭРБ ИПП назначаются в стандартной дозе. При возникновении изжоги возможно применение «по требованию», наиболее быстрое исчезновение симптомов характерно для рабепразола и эзомепразола. В качестве противорецидивной терапии ИПП следует принимать в поддерживающей дозе. Основной курс лечения ГЭРБ – 4–8 недель, курс противорецидивного лечения – 6–12 месяцев.
|
|
|
| Таблица 2 | |
| Суточные дозы и кратность приема ИПП | ||||
|
|
|
|
| |
| Препарат | Средняя доза |
| Кратность приѐма | |
| (мг/сутки) |
| |||
|
|
|
| ||
|
|
| По 20 мг 2 раза в сутки (за | ||
| Стандартная доза | 40 | 30 минут до еды) или 40 мг | ||
Омепразол |
|
| однократно (утром до еды) | ||
Поддерживающая доза | 20 | 1 | раз в сутки (утром) | ||
| |||||
| Парентеральное | 40–80 | В/в капельно | ||
| введение | ||||
|
|
|
| ||
| Стандартная доза | 40 | 1 | раз сутки (утром до еды) | |
Пантопразол | Парентеральное | 40–80 | В/в капельно | ||
| введение | ||||
|
|
|
| ||
Лансопразол | Стандартная доза | 30–60 | 1-2 раза в сутки | ||
Рабепразол | Стандартная доза | 20 | 1 | раз в сутки (утром до еды) | |
Поддерживающая доза | 10–20 | 1 | раз в сутки (утром до еды) | ||
| |||||
Эзомепразол | Стандартная доза | 40 | 1 | раз в сутки (утром до еды) | |
Поддерживающая доза | 20 | 1 | раз в сутки (утром до еды) | ||
| |||||
Функциональная диспепсия (особенно язвенноподобная форма) является показанием к назначению антисекреторных препаратов. Хороший эффект достигается при комбинировании ИПП (в стандартной дозе) с невсасывающимися антацидами.
ИПП в терапии ЯБ в основном рассматриваются как компонент антихеликобактерной схемы (согласно Маастрихтским соглашениям 1996, 2000 и 2005 гг.) – в стандартной дозировке 2 раза в сутки в течение 7–14 дней. Но, в Маастрихтских протоколах лечения не делается различия между Нр-ассоциированной и Нр-негативной ЯБ, при которой нет необходимости в эрадикации Нр. В случаях Нр-негативной ЯБ ИПП назначаются в виде монотерапии в стандартной дозировке 1–2 раза в сутки в течение 2–4 недель. Поддерживающая терапия – в стандартной дозировке 1 раз утром (до 8 недель при язве желудка и до 6 недель при язве двенадцатиперстной кишки).
Частная терапевтическая фармакология 93
Для лечения и профилактики НПВП-гастропатий ИПП назначают в стандартной дозировке 1 раз в сутки (чаще утром) в течение 2–4 недель.
ИПП при парентеральном введение высокоэффективны в терапии кровотечений из верхних отделов ЖКТ. Известно, что при рН желудочного сока ≥ 5 не происходит лизиса тромба, образовавшегося на дне язвы, поэтому при кровотечениях из верхних отделов ЖКТ целесообразно назначение антисекреторных препаратов. Предпочтение отдают ИПП, которые более эффективны чем блокатары Н2-рецепторов, в связи со способностью ИПП устойчиво поддерживать рН желудка > 6 на протяжении длительного время.
При лечении синдрома Золлингера-Эллисона доза ИПП подбирается индивидуально («титруется») до уровня фиксации базальной кислотной продукции ниже 10 мэкв/ч. Начальная доза омепразола составляет 60 мг 1 раз в сутки.
У пациентов с тяжелыми формами заболевания при неэффективности другой терапии дозу увеличивают до 80–120 мг/сут (в два приема).
Побочное действие
ИПП хорошо переносятся при кратковременной и длительной терапии. Побочные эффекты развиваются редко и в большинстве случаев носят легкий и обратимый характер. Возможные минимальные побочные эффекты: боль в животе, тошнота, метеоризм и понос. При длительном (около 40 месяцев) непрерывном приеме ИПП в высоких дозах (40 мг омепразола, 80 мг пантопразола, 60 мг лансопразол) может возникнуть гипергастринемия, прогрессирование явлений атрофического гастрита, иногда – узелковая гиперплазия энтерохромаффинных клеток слизистой желудка. При внутривенном введении омепразола описаны единичные случаи нарушения зрения и слуха.
Побочные эффекты, требующие внимания, если они беспокоят пациента или продолжаются в течение длительного времени:
Кожа:
сыпь;
зуд.
Желудочно-кишечный тракт (ЖКТ):
сухость во рту;
отрыжка;
тошнота;
рвота;
боль в животе;
метеоризм;
запор;
94 Н. И. Яблучанский, В. Н. Савченко
диарея.
Центральная нервная система (ЦНС):
головная боль;
головокружение;
сонливость.
Другие:
миалгия;
артралгия;
слабость.
Редкие побочные эффекты, требующие внимания:
Кожа:
крапивница;
токсический эпидермальный некролиз;
синдром Стивенса-Джонсона;
многоформная эритема;
ангионевротический отек.
ЖКТ:
синдром избыточного роста бактерий.
Кровь:
анемия;
гемолитическая анемия;
нейтропения;
лейкоцитоз;
агранулоцитоз;
тромбоцитопения;
панцитопения.
ЦНС:
депрессия.
Мочеполовая система:
гематурия;
протеинурия;
инфекции мочевыводящих путей.
Печень:
повышение уровня аминотрансфераз;
лекарственное гепатит, печеночная недостаточность, печеночная энцефалопатия (крайне редко).
Другие:
Частная терапевтическая фармакология 95
боль в груди;
бронхоспазм;
нарушения зрения;
периферические отеки.
Противопоказания и предостережения к применению ИПП
Гиперчувствительность к ИПП.
Беременность.
Кормление грудью.
Возраст до 14 лет.
ИПП маскируют симптоматику рака желудка, затрудняют его диагностику, поэтому до начала терапии необходимо исключить злокачественное новообразование.
Упожилых пациентов увеличивается период полувыведения и биодоступность ИПП, однако значение максимальной концентрации достоверно не различается и изменения дозы препарата, как правило, не требуется.
Убольных с печеночной недостаточностью период полувыведения увеличивается в 5–7 раз, что требует соответствующей коррекции дозы.
При выраженной хронической почечной недостаточности значение максимальной концентрации несколько отличается от такового у здоровых лиц, поэтому коррекция дозы ИПП может быть незначительной или оставаться без изменений.
Взаимодействие ИПП с другими лекарственными средствами
ИПП подвергаются метаболизму в печени с участием цитохрома P450, поэтому могут конкурировать с другими лекарственными средствами. Эти взаимодействия, как правило, существенного клинического значения не имеют. Но, рекомендуется тщательное наблюдение при одновременном применении ИПП с фенитоином или пероральными антикоагулянтами. Рабепразол метаболизируется неферментативным путем, поэтому практически не взаимодействует с другими препаратами, которые метаболизируются через систему цитохрома P450.
ИПП могут влиять на абсорбцию препаратов, биодоступность которых зависит от рН желудочного сока: ускорять всасывание (дигоксина, антибиотиков группы макролидов) и замедлять всасывание (ампициллина, атазанавира, кетоконазола, солей железа).