Гиперплазия плаценты что это такое
MEDISON.RU - Мезенхимальная дисплазия плаценты - пренатальная диагностика (клинические наблюдения)
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Мезенхимальная дисплазия плаценты (МДП), или плацентарная мезенхимальная гиперплазия, - редкая аномалия стволовых ворсинок плаценты, характеризуется плацентомегалией, кистозной дилатацией и образованием везикул, сосудистыми аномалиями.
Впервые МДП описана как гиперплазия стволовых ворсин плаценты у беременных с высоким уровнем α-фетопротеина в сочетании с крупной плацентой и эхографическими признаками частичного пузырного заноса. При гистологическом исследовании отсутствовали признаки пролиферации трофобласта, что исключало диагноз частичного пузырного заноса [1]. M. Arizawa и соавт. определили частоту встречаемости данной патологии - 0,02% (7 случаев среди 30 758 плацент более чем за 21 год) [3]. Кроме того, считается, что частота встречаемости МДП занижена и причина гиподиагностики в том, что морфологическая картина до сих пор остается незнакома многим патологоанатомам.
В настоящее время рассматривается несколько теорий возникновения МДП. По одной из них - это врожденный порок развития мезодермы. Эта теория основана на наблюдениях мезенхимальных стволовых гиперплазий ворсинок параллельно с пролиферативными нарушениями плаценты, такими как хорионангиома, дилатация хорионических сосудов, а также гемангиомами плода [3].
Другая, андрогенетическая, теория говорит о том, что МДП - результат эндоредупликации гаплоидного отцовского генома. В этом случае этиология МДП близка к механизму развития полного пузырного заноса. Около 75% случаев полного пузырного заноса возникают от оплодотворения безъядерной яйцеклетки гаплоидным сперматозоидом, которая впоследствии подвергается эндоредупликации, в остальных случаях происходит оплодотворение двумя сперматозоидами. При имплантации таких эмбрионов формируются кистозный отек ворсины хориона, трофобластическая гиперплазия и анэмбриония [4].
Некоторые случаи МДП обусловлены триплоидией, хотя в большинстве зарегистрированных случаев плоды имели нормальный женский кариотип 46,ХХ. На сегодняшний день из описанных в литературе случаев соотношение женского и мужского кариотипа плодов составляет 3,6: 1 [2].
Также в качестве патогенетического механизма формирования МДП рассматриваются гипоксия и гипоперфузии различной этиологии. Считается, что во время гипоксии происходит стимуляция фибробластов, что ведет к увеличению массы соединительной ткани с последующим увеличением производства сосудистого эндотелиального фактора роста (VEGFs), ведущего к ангиогенезу.
По данным ряда авторов, данная патология плаценты часто сочетается с пороками развития плода и имеет неблагоприятный исход. Клиническими проявлениями МДП могут быть задержка внутриутробного роста плода, антенатальная гибель, некоторые хромосомные аномалии, синдром Беквита-Видемана, транзиторный неонатальный сахарный диабет, отцовская однородительская дисомия 6, трисомия 13 и синдром Клайнфелтера [5-7].
В 23% случаев МДП сочетается с синдромом Беквита-Видемана. В большинстве случаев данный синдром возникает спорадически и имеет аутосомно-доминантный тип наследования. Предполагается, что данное заболевание может возникать вследствие перестроек, вовлекающих участок короткого плеча хромосомы 11 р15. Выявление макросомии, омфалоцеле и макроглоссии в сочетании с нормальным кариотипом позволяет диагностировать синдром Беквита-Видемана. С различной частотой обнаруживаются нефромегалия, гепатомегалия, многоводие, складки мочек уха, диафрагмальная грыжа и пороки сердца [5, 6]. Гиперплазия клеток поджелудочной железы встречается в 30-50% случаев, вызывает повышение уровня инсулина и неонатальную гипогликемию, манифестирующую на 2-й или 3-й день жизни [7].
МДП не имеет специфических клинических проявлений. В большинстве случаев в начале беременности диагностируется при ультразвуковом исследовании (УЗИ) в скрининговые сроки и первично обозначается как частичный пузырный занос, в отличие от которого большинство плодов имеют нормальный кариотип, уровень β-ХГЧ на протяжении всей беременности несколько повышен или остается в пределах нормы, уровень α-фетопротеина повышен [8].
Многие случаи протекают бессимптомно и диагностируются после родов на основании морфологического исследования гиперплазированной плаценты. Макроскопически плацента с МДП представляет собой увеличенную по объему и массе плаценту с чередованием кистозных структур и нормальной паренхимы. Кистозные структуры представляют собой кистозные расширения вен стволовых ворсин. Иногда возникают тромбозы и аневризмы, расширение стволовых сосудов ворсин. Сосуды на плодовой части плаценты извиты и расширены. Гистологически для МДП характерны увеличенные отечные стволовые ворсины с расширенными сосудами и отсутствием трофобластической пролиферации. Сосуды толстостенные, с фибромускулярной гиперплазией. Терминальные ворсины, как правило, нормальные. В отличие от пузырного заноса ворсины обычно хорошо васкуляризированы и не имеют признаков пролиферации трофобласта [4, 7].
По литературным данным, ультразвуковая картина МДП похожа на частичный пузырный занос - утолщенная плацента с гипоэхогенными включениями. В других случаях описано несколько маленьких анэхогенных включений в ткани плаценты, не имеющих клинического значения. Бесспорно, что диффузный процесс требует тщательного мониторинга беременности. Выявление при УЗИ гиперплазированной кистозной плаценты вместе с фенотипически неизмененным плодом крайне маловероятно при пузырном заносе и заставляет предположить МДП. Дифференциальную диагностику необходимо проводить также с хорионангиомой и субхорионической гематомой [9,10].
Приводим 4 законченных наблюдения беременности при МДП.
Клиническое наблюдение 1
Пациентка Ш., 32 лет. Беременность повторная, в анамнезе срочные самопроизвольные роды без осложнений. Направлена в поликлинику МОНИИАГ с подозрением на частичный пузырный занос. При УЗИ в 15 нед выявлено утолщение плаценты до 32 мм, примерно 1/3 площади плаценты с измененной структурой - множественными мелкими гипо- и анэхогенными включениями размером до 3 мм (рис. 1). Маркеров хромосомных аномалий и пороков развития плода не выявлено. Уровень ХГЧ в пределах нормы. Заключение УЗИ: беременность 15 нед, частичный пузырный занос. Учитывая отсутствие аномалий развития плода, принято решение о пролонгировании беременности. Течение беременности осложнилось задержкой внутриутробного роста плода. Проводилась стандартная терапия вазоактивными препаратами. Родоразрешена при беременности 37 нед, произошли самопроизвольные роды, родилась девочка с массой тела 2800 г, ростом 46 см, что соответствует гипотрофии плода I степени, с оценкой по шкале Апгар 8-9 баллов. Кровопотеря в родах 350 мл. Послеродовый период протекал без осложнений.
Рис. 1. Пациентка Ш. Структурные изменения плаценты.
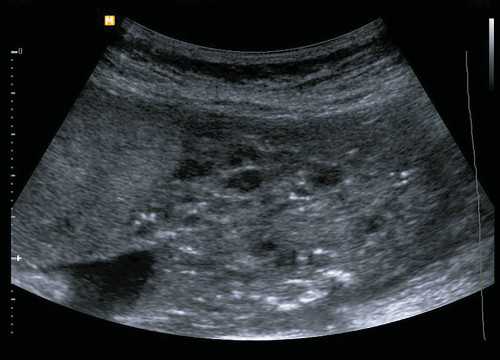
а) 15 недель беременности.
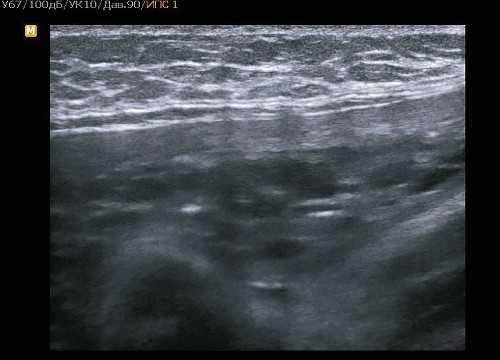
б) 37 недель беременности.
Диагностика МДП проведена при гистологическом исследовании плаценты.
Клиническое наблюдение 2
Пациентка И., 29 лет. Данная беременность вторая. В I триместре скрининговое УЗИ не проводилось. Со слов пациентки при УЗИ, проведенном в 18 нед беременности, возникли подозрения на пузырный занос, в связи с чем консультирована в Российском онкологическом научном центре им. Н.Н. Блохина. Наличие трофобластической болезни не подтверждено. Уровень β-ХГЧ в пределах нормы: 23 335 МЕ/л (10 000-35 000 МЕ/л).
В МОНИИАГ находилась под наблюдением с 20 нед гестации. Данные УЗИ: размеры плода соответствуют 20 нед беременности. Пороки развития и признаки гипотрофии плода не обнаружены. Плацента расположена по передней стенке матки, размерами 145-147 мм, толщиной до 50 мм. Структура плаценты изменена, имеется множество округлых жидкостных включений различного диаметра - от 4 до 12 мм с четкими ровными границами. В структуре плацентарной ткани множественные локусы кровотока. Архитектоника сосудов плаценты не изменена. Кровоток в миометрии сохранен, архитектоника сосудов не изменена. Плодовоплацентарный кровоток не нарушен. Заключение: ультразвуковая картина соответствует МДП (рис. 2-4).
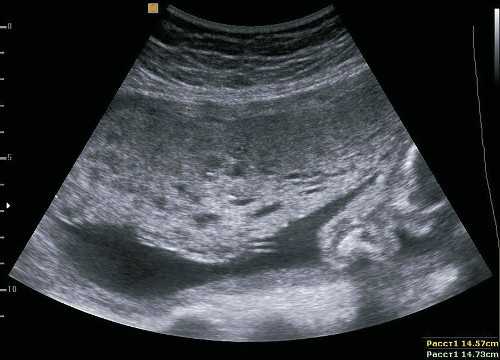
Рис. 2. Пациентка И. МДП. Диффузное утолщение и множественные кистозные включения в плаценте.
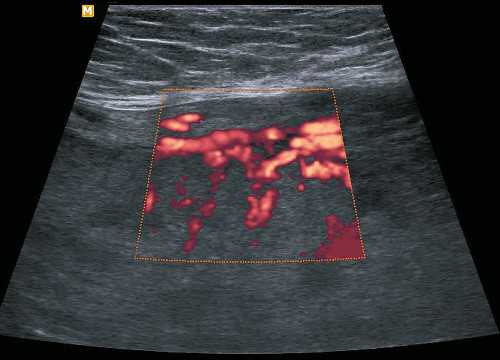
Рис. 3. Сосудистое дерево при МДП. Архитектоника базальных и спиральных артерий не нарушена.
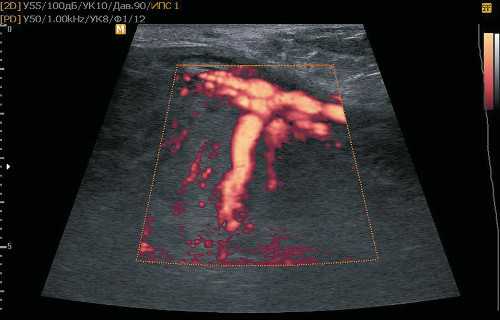
Рис. 4. Сосудистое дерево при МДП. Расширенные сосуды стволовых ворсин.
В течение II триместра выявлена сочетанная тромбофилия по гену MTGFR и фактору Leiden. Уровень гомоцистеина в пределах нормы. Маркеров АФС не выявлено.
УЗИ при сроке гестации 36-37 нед: размеры плода соответствуют 36,6 нед беременности. Признаки гипотрофии и пороки развития плода не обнаружены. Плодовоплацентарный кровоток не нарушен. Количество околоплодных вод в пределах нормы. Плацента расположена по передней стенке матки, толщиной до 78 мм, II степени зрелости. Структура плаценты гиперэхогенная, множественные жидкостные включения до 1 см в диаметре, сосуды плаценты расширены. Гормоны фетоплацентарного комплекса в пределах нормы. Уровень ХГЧ - 8 533 МЕ/л (норма 8 880-29 000 МЕ/л).
Самопроизвольные роды произошли в сроке 38 нед. Родилась живая доношенная девочка с массой тела 2710 г, ростом 47 см, что соответствует гипотрофии I степени, без видимых пороков развития, с оценкой состояния по шкале Апгар 8 и 9 баллов. Кровопотеря в родах 300 мл. Послеродовый период протекал без осложнений.
Масса плаценты 1498 г (медиана 445 г), размерами 28 х 27 см, с краевым прикреплением пуповины. Диск толщиной до 7 см, хориальная пластинка с извитыми, резко полнокровными сосудами, крупными очагами субхориального фибриноида. Материнская поверхность с нарушенной целостностью, в краевых отделах кисты с прозрачным содержимым диаметром до 1,5 см. В крае плаценты обширный очаг инфаркта (18 х 9 см), толщина плаценты в этой области не превышает 1 см. На разрезе ткань с многочисленными широкими белесоватыми прослойками, единичными кистами (рис. 5).
Рис. 5. МДП, макроскопическая картина.
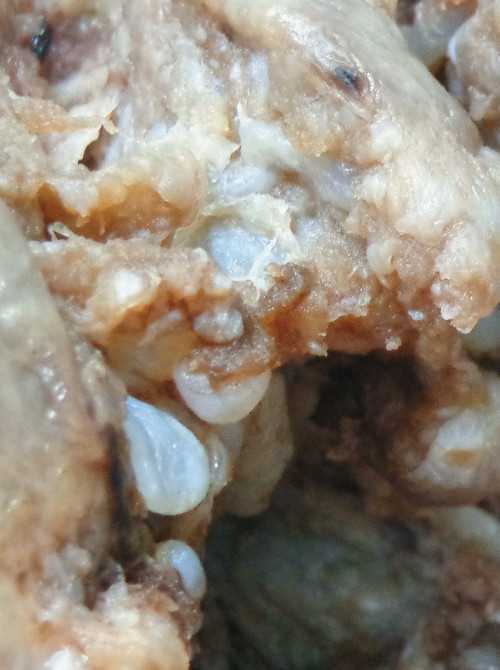
а) Фрагмент ткани плаценты с пузырьковидными ворсинами.
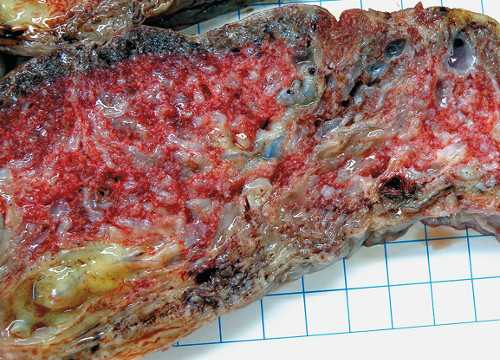
б) Крупные извитые сосуды, окруженные желеобразным материалом, кистозные полости, обилие фибриноида.
При микроскопическом исследовании плаценты определяются крупные стволовые ворсины с отечной, рыхлой стромой, местами с образованием полостей (рис. 6). Сосуды в пораженных ворсинах разного диаметра, нередко причудливо извитые. Наблюдаются разнообразные поражения сосудов: облитерационная ангиопатия, тромбоз, нередко с организацией, геморрагический эндоваскулит. Встречаются группы фиброзированных бессосудистых ворсин. Васкуляризация промежуточных и терминальных ворсин неравномерная, местами определяется ангиоматоз. Трофобластическая выстилка без признаков пролиферации. Гистологическое заключение: МДП.
Рис. 6. МДП, микроскопическая картина.
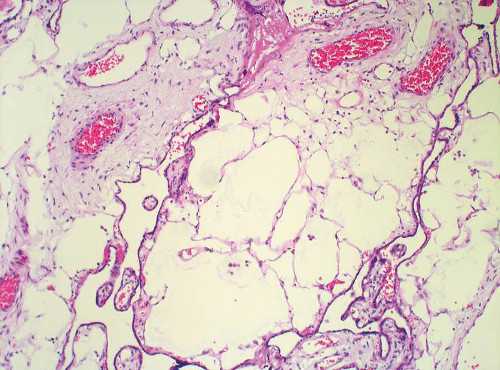
а) Резкий отек стволовых ворсин с образованием полостей. х200. Окраска гематоксилином и эозином.
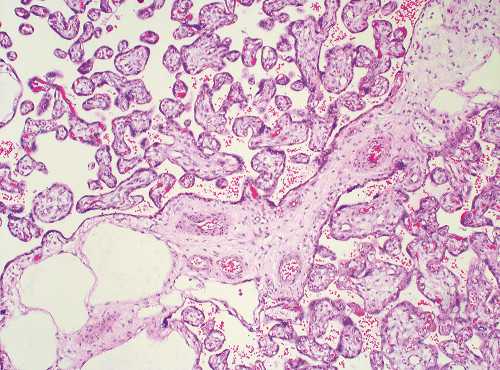
б) Промежуточные и терминальные ворсины обычного вида рядом с отечной стволовой ворсиной. х100. Окраска гематоксилином и эозином.
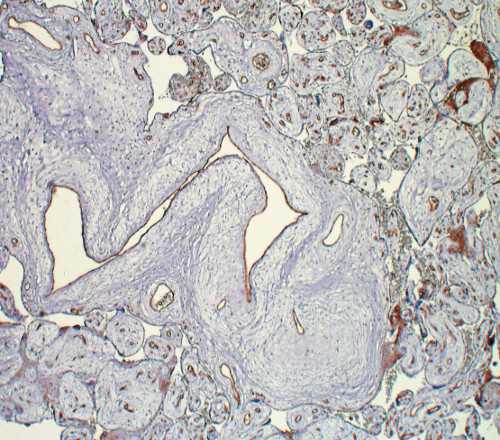
в) Извитой, расширенный сосуд стволовой ворсины. х200. Иммуногистохимическая реакция с антителами к CD31.
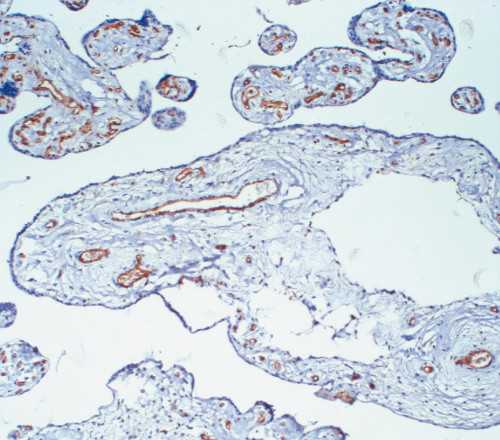
г) Отечная стволовая ворсина с формированием полостей, в сохранной строме видны многочисленные сосуды разного диаметра. х100. Иммуногистохимическая реакция с антителами к CD31.
Клиническое наблюдение 3
Пациентка Ф., 26 лет. Данная беременность первая. В 12 нед при проведении генетического скрининга заподозрены патология хориона?, пузырный занос? Консультирована в медико-генетическом отделении МОНИИАГ: беременность 12 нед 4 дня, аномалия хориона?, частичный пузырный занос?, МДП? При УЗИ в 21 нед гестации: плацента перекрывает внутренний зев с множественными кистозными образованиями. Проводилось обследование на наличие генетических маркеров тромбофилии, выявлена сочетанная тромбофилия по гену MTGFR и PAI - I. Уровень ХГЧ составил 52 624 МЕ/л, α-фетопротеина - 194,0 МЕ/л.
С 25-26 нед гестации выявлена задержка внутриутробного роста плода I степени, асимметричного типа. Плодово-пла центарный кровоток не нарушен. Плацента "0" степени зрелости, толщиной 33 мм (больше нормы), с множественными кистозными образованиями, перекрывает внутренний зев. При исследовании уровня гормонов фетоплацентарного комплекса в 30 нед гестации плацентарный лактоген, прогестерон, кортизол и α-фетопротеин находились в пределах нормативных значений.
При УЗИ в 31 нед значение бипариетального размера соответствует 10-му перцентилю, ДГ ДЖ - 3-му перцентилю, масса плода - 10-му перцентилю, что характерно для задержки внутриутробного роста плода I степени. Плацента по передней стенке матки толщиной до 47-63 мм, III степени зрелости. Особенности строения плаценты: примерно 1/3 плаценты по левому краю со структурными изменениями: множественные жидкостные включения размером до 4-5 мм, кровоток определяется, архитектоника сосудистого дерева не изменена. Прикрепление пуповины к неизмененной части плаценты. Заключение: беременность 31 нед. Головное предлежание. Синдром задержки роста плода I степени. МДП. Умеренное многоводие (рис. 7).
Рис. 7. Пациентка Ф. МДП. Кистозные включения в структуре утолщенной плаценты.
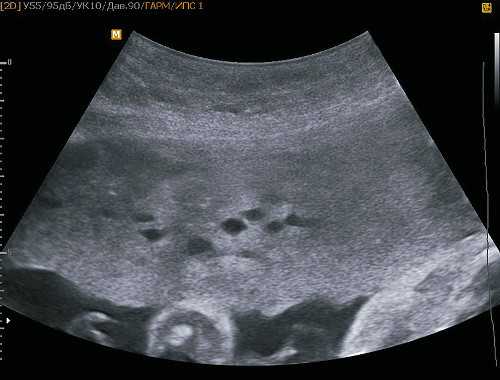
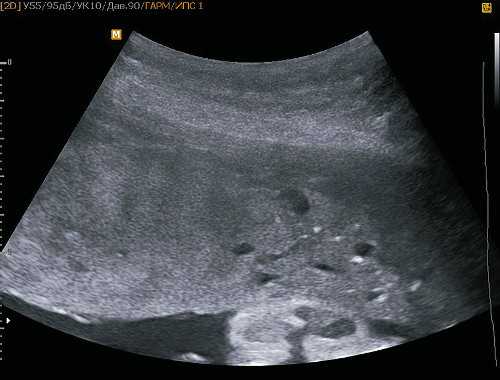
Течение беременности осложнилось присоединением умеренной преэклампсии. Несмотря на проводимую терапию, отмечено нарастание симптомов преэклампсии, появились нарушения плодовой гемодинамики. При сроке гестации 36 нед пациентка родоразрешена путем кесарева сечения. Извлечена живая недоношенная девочка с массой тела 1950 г, ростом 44 см, что соответствовало задержке внутриутробного роста II степени, гипотрофии II степени. Оценка состояния по шкале Апгар 7 и 8 баллов. Операция протекала без технических сложностей. Кровопотеря составила 800 мл.
Масса плаценты нормальная (409 г при медиане 408 г). Диск толщиной 5-7 см, хориальная пластинка с извитыми, резко полнокровными сосудами, крупными очагами субхориального фибриноида. Материнская поверхность с ненарушенной целостностью, в краевых отделах кисты с прозрачным содержимым диаметром до 1,5 см с изменениями ворсинчатого дерева и выраженными гемореологическими изменениями - некрозом больших групп ворсин и облитерацией фибрином не менее 1/3 объема плацентарного диска. Гистологическое заключение: МДП.
Клиническое наблюдение 4
Пациентка О., 28 лет. Направлена в поликлинику МОНИИАГ с подозрением на частичный пузырный занос. При исследовании в МОНИИАГ размеры плода соответствуют 14-15 нед беременности, маркеров хромосомных аномалий и пороков развития плода не выявлено. Плацента расположена по передней стенке матки толщиной 28 мм.
Выявлены массивные структурные изменения плаценты: множественные жидкостные включения различного диаметра - от 4 до 12 мм, округлые, анэхогенные, с ровными четкими контурами. Кровоток в миометрии выраженный, в структуре плацентарной ткани множественные локусы кровотока, сосуды крупного диаметра, сосудистое дерево, архитектоника сосудов сохранены. Плодовая гемодинамика не нарушена.
Заключение: беременность 13-14 нед. Структурные изменения плаценты - нельзя исключить МДП. Дифференциальная диагностика с пузырным заносом после получения анализа крови на β-ХГЧ (рис. 8, 9).
Рис. 8. Пациентка О. Структурные изменения плаценты при МДП.


Рис. 9. Пациентка О. Сосудистая архитектоника при МДП.
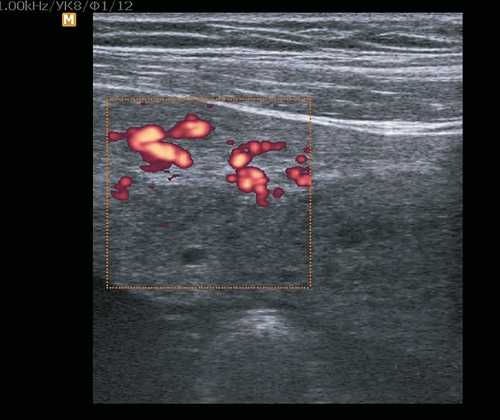
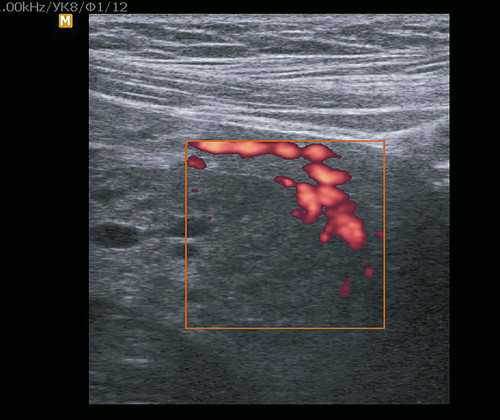
Повышение уровня β-ХГЧ послужило основанием для направления пациентки для консультации в центр трофобластической болезни, где она наблюдалась до 33 нед, проводилась дифференциальная диагностика между множественными хорионангиомами плаценты и дистрофическими изменениями в плаценте. Четких данных о наличии трофобластической болезни не было выявлено, несмотря на значительное повышение уровня β-ХГЧ (103 000 ед. при норме до 78 100 ед.).
УЗИ, проведенное в МОНИИАГ в 33 нед: размеры плода соответствуют 31,2 нед беременности. Предполагаемая масса 1800-1900 г. Аномалий развития не выявлено. Размеры и масса плода соответствуют 25-50-му перцентилю для данного срока, задержки внутриутробного роста не выявлено. Плацента по передней стенке матки толщиной от 40 до 52 мм, III степени зрелости. Особенности строения плаценты: в правой части плацента более эхогенная, в структуре единичные анэхогенные участки неправильной формы, кровоток обычный, сосудистая архитектоника не изменена, кровоток в спиральных артериях прослеживается, индекс резистентности (ИР) 0,36, систолодиастолическое отношение (С/Д) 1,57. Ультразвуковая картина данной части плаценты не типична для пузырного заноса, не типична для III степени зрелости, не имеет признаков хорионангиомы. На остальном протяжении плацента утолщена, структура более характерна для III степени зрелости - определяются граница котиледонов, в центре котиледона - анэхогенная зона с гиперэхогенным кольцевидным участком по периферии. Сосудистая архитектоника не изменена, кровоток в спиральных артериях прослеживается, ИР 0,31, С/Д 1,45. Заключение: беременность 33 нед. Головное предлежание. Диффузное утолщение плаценты. Структурные изменения плаценты не типичны для хорионангиомы, не позволяют дифференцировать частичный пузырный занос и мезенхимальную дисплазию.
Родоразрешена при беременности 37 нед, произошли самопроизвольные роды, протекали без осложнений. Родился живой доношенный мальчик с массой тела 2850 г, ростом 47 см, что соответствует гипотрофии плода I степени, оценка по шкале Апгар 8-9 баллов. Течение послеродового периода без осложнений.
Масса плаценты составила 714 г (более 97-го перцентиля, медиана 430 г). Макроско пическое и микроскопическое исследование подтвердило МДП.
Выводы
На основании немногочисленных наблюдений МДП можно сформулировать некоторые положения, касающиеся диагностики и течения беременности при этой редкой патологии.
- Наиболее значимым методом диагностики МДП в настоящее время можно считать лучевые методы, в частности УЗИ. Ультразвуковая картина мезенхимальной дисплазии плаценты достаточно характерна и заключается в диффузном утолщении плаценты, множественных кистозных полостях, занимающих часть плаценты или всю площадь плаценты. Кистозные полости при МДП имеют существенные отличия от частичного пузырного заноса: размеры кист позволяют дифференцировать их в виде отдельных округлых анэхогенных структур с ровными четкими контурами, гладкой внутренней поверхностью. Морфологическая основа кистозных включений в плацентарной ткани - резкий отек стволовых ворсин с образованием полостей. Архитектоника сосудистой сети не нарушена, топография плацентарных сосудов соответствует строению нормальной сосудистой сети плаценты. Извитые, расширенные сосуды стволовых ворсин могут четко определяться при ЦДК.
- При подозрении на частичный пузырный занос и отсутствии аномалий развития плода можно предполагать МДП, возможно пролонгирование беременности. При МДП уровень β-ХГЧ не всегда соответствует норме для данного срока гестации, а уровень α-фетопротеина не всегда имеет высокие значения, следовательно, ни уровень β-ХГЧ, ни уровень α-фетопротеина не играют решающей роли в постановке диагноза.
- Для течения беременности при МДП характерно формирование плацентарной недостаточности, задержки внутриутробного роста плода. Но не только наличие структурных изменений в плаценте определяет формирование осложнений беременности. Ведение беременности, определение сроков и методов родоразрешения должны проводиться по акушерским показаниям с учетом сопутствующей экстрагенитальной и акушерской патологии.
- При удовлетворительном состоянии плода и отсутствии противопоказаний со стороны матери возможно ведение родов через естественные родовые пути. Ни в одном наблюдаемом случае структурные изменения плаценты не привели к нарушению сократительной деятельности матки в родах или послеродовом периоде, кровопотеря не превысила физиологическую.
Литература
- Moscoso G., Jauniaux E., Hustin J. Placental vascular anomaly with diffuse mesenchymal stem villous hyperplasia: a new clinico-pathological entity? // Pathol Res Pract. 1991; 187 (2-3): 324-328.
- Arigita M., Illa M., Nadal A., Badenas C., Soler A., Alsina N., Borrell A. Chorionic villus sampling in the prenatal diagnosis of placental mesenchymal dysplasia // Ultrasound Obstet Gynecol. 2010; 36: 644-646.
- Arizawa M., Nakayama M. Suspected involvement of the X chromosome in placental mesenchymal dysplasia // Congenit Anom (Kyoto). 2002; 42: 309-317.
- Kaiser-Rogers К.A., McFadden D.E., Livasy C.A., Dansereau J., Jiang R., Knops J.F. Androgenetic/ biparental mosaicism causes placental mesenchymal dysplasia // J Med Genet. 2006; 43: 187-192.
- H'mida D., Gribaa M., Yacoubi T. et al. Placental mesenchymal dysplasia with Beck-Wiedemann syndrome fetus in the context of biparental and androgenic cell lines // Placenta. 2008; 29 (5): 454-460.
- Armes J., McGown I., Williams M. et al. The placenta in Beckwith-Wiedemann syndrome: genotype-phenotype associations, excessive extravillous trophoblast and placental mesenchymal dysplasia // Roy Coll Pathol Aust. 2012; 44 (6): 1-9. 7. Aviram R., Kidron D., Silverstein S. Placental mesenchymal dysplasias associated with transient neonatal diabetes mellitus and paternal UPD6 // Placenta. 2008; 29 (7): 646-649.
- Nayeri U.A., West A.B., Grossetta Nardini H.K., Copel J.A., Sfakianaki A.K. Systematic review of sonographic findings of placental mesenchymal dysplasia and subsequent pregnancy outcome // Ultrasound Obstet Gynecol. 2013; 41 (Issue 4): 366-374.
- Hui Li, Lei Li, Xiao Tang, Fan Yang, Kai-Xuan Yang. Placental mesenchymal dysplasia: a case of a normal-appearing fetus with intrauterine growth restriction. Case Report // Int J Clin Exp Pathol. 2014; 7 (8): 5302-5307.
- Павлов К.А., Дубова Е.А., Щеголев А.И. Мезенхимальная дисплазия плаценты // Акушерство и гинекология. 2010. 5: 15-20.
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
» Все об утолщении плаценты и что с этим делать
Плацента – это временный, но крайне важный орган, который появляется только во время беременности и обеспечивает все потребности растущего в утробе малыша. Различные неблагоприятные факторы могут повлиять на состояние плаценты и ухудшить ее функции. В этих случаях говорят о плацентарной недостаточности, разновидностью которой является утолщение плаценты.
Что это такое гиперплазия плаценты
Гиперплазия или утолщение плаценты — это структурная патология органа, которая сопровождается увеличением толщины внезародышевого слоя. При этом состоянии ее толщина выше установленных физиологических норм, которые определяют на определенных сроках беременности (начиная примерно с 21-22 недели).
Гиперплазия плаценты мешает ей полноценно выполнять свои функции, связанные с обеспечением плода кислородом и необходимыми питательными веществами. В связи с этим замедляется его развитие, что может привести к необратимым последствиям.
Что может стать причиной
Окончательно сформировавшись к 16-ой неделе беременности детское место продолжает расти вместе с плодом. Его толщина постепенно увеличивается и к 36-37 неделе составляет от 2 до 4 см.
В таблице ниже приведены ориентировочные нормы толщины детского места на разных сроках беременности.
Причины этого состояния связывают со следующей патологией:
- Несовместимость матери и плода по иммунологическим показателям крови (гемолитическая болезнь). Возникает при несовпадении групп крови или резус-фактора.
- Тяжелая анемия с уровнем гемоглобина ниже 70 г/л.
- Сахарный диабет, в частности и тот, который развивается только при беременности.
- Наличие инфекционной патологии у беременной, так называемые TORCH-инфекции: цитомегаловирус, герпес, краснуха и другие.
- Тяжелые гестозы при беременности (эклампсия, артериальная гипертензия).
- Инфекции мочеполовой системы (хламидии, уреаплазмы, гонококки, сифилис).
- Генетические проблемы.
- Инфекционные болезни во время беременности (грипп, энтеровирусная инфекция и др.).
Важно! Чаще всего при увеличении толщины плаценты, специалисты подозревают гемолитическую болезнь. Если диагноз не подтверждается, то начинают искать другие причины.
Как проявляется эта патология
Беременная женщина первое время не ощущает никаких признаков того, что происходит гиперплазия плаценты. Выявить это состояние помогает ультразвуковое исследование, которое проводят на определенных сроках.
Позднее женщина может заметить изменение двигательной активности плода. Малыш начинает реже двигаться. При осмотре доктор отмечает уменьшение частоты сердечных сокращений и глухость сердечных тонов. Эти симптомы являются следствием кислородного голодания плода и могут стать косвенным признаком увеличения толщины плаценты.
Гиперплазия плаценты впоследствии приводит к гипоксии (кислородному голоданию) плода и задержке внутриутробного развития. Если вовремя не принять необходимые меры, то последствия могут быть необратимыми.
Важно! Плацентарная недостаточность может начаться в любом триместре беременности, но ее осложнения для плода проявляются в основном в третьем триместре, когда идет интенсивный рост и созревание всех систем и органов малыша.
Как происходит диагностика
Диагностика этой проблемы проводится с помощью УЗИ. Этот метод позволяет установить параметры плаценты и выявить ее утолщение.
Кроме этого, проводят допплерографию. Это исследование сосудов, которое позволяет уточнить состояние кровотока в системе мать-плод.
КТГ (кардиотокография) помогает выявить частоту сердечных сокращений плода и его активность. Снижение этих показателей может быть косвенным признаком того, что произошло плацентарное утолщение.
Дополнительно, при постановке этого диагноза, беременную женщину направляют на сдачу общеклинических анализов крови и мочи, а также проверяют на наличие инфекционной патологии (гистология, цитология мазков, анализы крови и др.).
Понятие о хорионангиоме
Хорионангиома – это доброкачественная сосудистая опухоль плаценты. Она развивается из мелких капилляров, расположенных в ворсинах хориона.
В большинстве случаев это одиночное новообразование, но может быть представлена несколькими узлами. Локализуется на внутренней поверхности плаценты, реже — на других участках.
Гистология определяет эту опухоль, как гамартому, новообразование из клеток сосудистого эпителия. Течение ее доброкачественное, метастазы в другие органы и ткани она не дает.
Потенциальный риск для плода может быть связан с развитием плацентарной недостаточности. Это образование может забирать на себя часть крови, тем самым вызывая синдром обкрадывания плода. В таких случаях наблюдается гипоксия и задержка внутриутробного развития.
Симптомы и состояние беременной зависят от размеров и локализации опухоли. Единичные небольшие хорионангиомы ничем не проявляют себя и беременность протекает без осложнений. Диагностируют на основании данных УЗИ и допплерографии.
Что применяют для лечения гиперплазии плаценты
Терапия этого патологического состояния проводится в нескольких направлениях. Специалисты занимаются лечением основного заболевания и сопутствующих осложнений беременности.
Параллельно терапия направлена на улучшение маточно-плацентарного кровообращения. Это достигается с помощью применения комплекса сосудорасширяющих средств, а также препаратов, улучшающих свойства крови и расслабляющих мускулатуру матки.
При иммунологических причинах специалисты могут порекомендовать женщине прервать беременность или назначить курс интаперитонеальной гемотрансфузии — переливание очищенных эритроцитов с отрицательным резус-фактором внутриутробно.
При выраженной анемии назначают специальную диету, а также препараты железа в комплексе с витамином С. Широко применяют средства, влияющие на тонус сосудов и улучшающие реологические свойства крови (Курантил, Актовегин, Трентал). Все они имеют ряд побочных эффектов, поэтому могут быть назначены только лечащим доктором.
Утолщение плаценты и ее прогноз зависят от многих факторов. Если вовремя предпринять все необходимые меры, то беременность и развитие малыша будут протекать без особенностей. В запущенных и тяжелых ситуациях может понадобиться экстренное родоразрешение путем кесарева сечения. Необходимо помнить, что выявить и вылечить это состояние самостоятельно невозможно, поэтому лучшей профилактикой будет своевременное посещение женской консультации и выполнение всех необходимых плановых обследований.
Похожие статьи
Аномалии плаценты - причины, симптомы, диагностика и лечение
Аномалии плаценты – это нарушения нормальной локализации, прикрепления или формы последа. Могут протекать бессимптомно, характеризоваться признаками фетоплацентарной недостаточности со второго триместра беременности, проявляться угрозой преждевременных родов или кровотечением. Диагностика проводится по данным УЗИ, фетометрии и кардиотокографии плода. Специфическое лечение не разработано. Терапия направлена на поддержание кровотока, устранение признаков гипоксии и пролонгирование беременности. По показаниям после родов проводится ручное отделение плаценты, гистерэктомия.
Общие сведения
Аномалии плаценты встречаются с различной частотой. Низкая плацентация, предлежание плаценты в третьем триместре наблюдается у 3% беременных. Плотное прикрепление последа, приращение к миометрию чаще встречается у беременных с рубцами на матке, перенесших большое количество абортов и выскабливаний, с высоким паритетом родов. За последние десятилетия отмечается увеличение количества приращений последа в 50 раз, что связывают с ростом показаний для кесарева сечения. Аномалии плаценты ведут к повышению частоты кровотечений в последовом и послеродовом периоде, осложнениям со стороны плода.
Аномалии плаценты
Причины
Аномалии плаценты возникают как результат компенсаторно-приспособительных реакций при патологических состояниях эндометрия и миометрия. Врастание, низкая плацентация и изменение формы происходят по одним и тем же причинам. Чаще всего развитие аномалии наблюдается при наличии следующих предрасполагающих факторов:
- Патология эндометрия. Воспалительные заболевания в анамнезе, частые аборты потенцируют дистрофические изменения слизистой оболочки, нарушение рецептивных свойств эндометрия. Бластоциста в поиске оптимального места имплантации может спуститься из дна матки в нижний сегмент, а плацента – плотно прикрепиться.
- Дистрофические изменения в матке. При миоме отмечаются нарушения кровотока, провоцирующие глубокое проникновение ворсин хориона. У женщин после кесарева сечения в месте рубца образуется неполноценный базальный слой слизистой, что приводит к глубокому врастанию плаценты. Если из-за недостатка питания происходит гибель части ворсин хориона, формируется двудолевой послед.
- Чрезмерная активность хориона. Глубокое врастание ворсин связывают с выделением зародышем большого количества хорионического гонадотропина. Повышение уровня гормона в первом триместре может быть связано с хромосомными аномалиями плода, в норме наблюдается при беременности двойней.
- Гормональные нарушения. Рост ворсин хориона сдерживается эстрогенами. При гормональной недостаточности происходит их врастание в мышечный слой матки и формирование приращения плаценты.
- Kiss1-ген. Открыт в 1999 году, выявляется во многих злокачественных опухолях, а также клетках синцитиотрофобласта. Ген стимулирует глубокую инвазию клеток синцитио- и цитотрофобласта в миометрий. Активность гена возрастает при использовании прогестагенов для сохранения беременности на ранних сроках.
Патогенез
Аномалии плаценты являются результатам патологий матки, возникших до наступления беременности. Воспалительные процессы и дистрофические изменения приводят к недостаточной васкуляризации отдельных участков децидуальной оболочки. Это вызывает гибель некоторых ворсин хориона на раннем сроке вынашивания. Формируются участки истончения плаценты и различные дефекты. При полной гибели ворсинчатого хориона образуются очаги без плацентарной ткани (окончатая плацента). При наличии уходящих в сторону сосудов выявляется добавочная долька, которая располагается на отдалении от края детского места.
В маточном дне кровоток усилен за счет ветвей яичниковой артерии. Но в случаях, когда бластоциста имплантируется в нижнем сегменте, она испытывает дефицит кровоснабжения, что потенцирует глубокую инвазию ворсин хориона в миометрий, поэтому низкая плацентация может сопровождаться врастанием плаценты. Иногда предлежание связано с чрезмерным увеличением размеров последа при многоплодной беременности. При гистологическом исследовании отмечаются преждевременные инволюционно-атрофические изменения, вызванные недостаточным кровотоком и перерастяжением нижнего сегмента.
Классификация
Единая классификация аномалий последа не разработана. Патологию условно разделяют на три типа, которые связаны между собой патогенетически. Из-за общего механизма развития различные аномалии могут сочетаться, что ухудшает прогноз и течение беременности. Специалисты в сфере акушерства выделяют следующие варианты аномалий плаценты:
- Нарушения локализации. Включают низкую плацентацию и предлежание плаценты. Полное предлежание диагностируется в 12 недель, практически не устраняется самостоятельно. Низкая плацентация к 3 триместру может сменяться нормальным прикреплением из-за увеличения объема матки и миграции плаценты.
- Аномалии прикрепления. Различают плотное прикрепление и приращение плаценты. Редко наблюдается сквозное прорастание с инвазией хориона в соседние органы. Также оно может быть диффузным (от стенки матки не отделяется все плодное место) или очаговым (врастание происходит на определенном участке).
- Аномалии формы. Плацента, состоящая из двух частей, называется двудолевой. При избыточном истончении диагностируется пленчатый тип. Поясной вид характеризуется образованием по краю плодного места вала, который является участком круговой отслойки или воспаления с отложением гиалина.
Симптомы аномалии плаценты
Данное состояние не всегда сопровождается клиническими симптомами. При двудолевой и окончатой разновидности плодного места, а также добавочной дольке признаки патологии во время беременности отсутствуют, сложности возникают в родах. Добавочная долька может отрываться и сохраняться в полости матки. Определяется гипотония, осложняющаяся кровотечением в раннем послеродовом периоде. Кровотечение в третьем периоде родов развивается при плотном прикреплении плаценты. Признаки отделения последа отсутствуют, а приемы, ускоряющие этот процесс, оказываются неэффективными.
Низкая плацентация сопровождается симптомами угрозы прерывания. Женщина периодически ощущает тянущие боли внизу живота, повышается тонус матки. При полном предлежании со 2 триместра наблюдаются периодические мажущие, иногда умеренные кровянистые выделения из влагалища. Опасность представляет массивное кровотечение, которое быстро приводит к острой гипоксии плода и геморрагическому шоку у беременной.
Осложнения
Патологии последа иногда провоцируют развитие плацентарной недостаточности и хроническую гипоксию плода. Ребенок отстает в росте, рождается с низким весом, хуже переносит период адаптации. Кровотечение при предлежании плаценты может начаться на любом сроке беременности. При несвоевременной помощи оно становится причиной внутриутробной гибели плода, а у матери возникает геморрагический шок и ДВС-синдром. Иногда аномалии прикрепления становятся показанием для экстирпации матки.
Диагностика
Скрининговое УЗИ-обследование проводится в 11 недель беременности, методика позволяет выявить первые признаки аномалии. Результаты повторного обязательного исследования в 21 и 32-34 недели указывают на прогрессирование патологии или уменьшение ее проявлений. Диагностика состояния проводится акушером-гинекологом и базируется на данных следующих методов:
- Физикальный осмотр. При фетоплацентарной дисфункции может определяться несоответствие размера живота сроку гестации. На предлежание плаценты указывает мягкая губчатая ткань над цервиксом. При осмотре в зеркалах могут обнаруживаться сгустки крови или жидкие выделения, которые являются признаком кровотечения.
- УЗИ матки. Патологическое расположение диагностируется уже в конце 1 триместра, но подтверждается только при последнем исследовании в 3 триместре. На полное предлежание указывает расположение последа сразу над внутренним зевом шейки. Нарушения прикрепления определяются по аномальному лакунарному кровотоку в толще миометрия.
- Фетометрия плода. Исследуется размер частей тела плода при помощи УЗИ. Недостаточность фетоплацентарного комплекса проявляется в отставании длины бедренной кости, плеча, копчико-теменного размера и головы. Может уменьшаться окружность живота. Параметры могут уменьшаться равномерно (симметричный тип задержки развития) или неравномерно (асимметричный тип).
- Кардиотокография. Оценивается сердечный ритм плода, его изменения при шевелении, маточных сокращениях. При хронической гипоксии снижается базальный ритм, количество акцелераций, увеличивается число децелераций, становится низкой вариабельность. Тяжесть гипоксии оценивается по балльной системе.
Лечение аномалии плаценты
Повлиять на аномалии локализации, формы или прикрепления медикаментозными или другими способами невозможно, поэтому лечение направлено на пролонгирование беременности, выбор оптимального срока и метода родоразрешения. Необходимо обеспечить улучшение питания плода и минимизировать последствия гипоксии. Аномалии прикрепления требуют экстренной хирургической помощи.
Консервативная терапия
При патологической локализации, выявленной на первом скрининговом УЗИ, применяются медикаментозные средства, улучшающие плацентарный кровоток. При повышении тонуса матки проводится токолитическая терапия раствором магнезии, назначается курс витамина В6 в сочетании с магнием. Мажущие выделения из половых путей при предлежании детского места являются показанием для экстренной госпитализации в отделение патологии беременных.
Консервативная терапия после родов может применяться при приращении последа, которое не удалось устранить ручным способом. Обязательным условием для медикаментозного лечения является отсутствие кровотечения. Используют цитостатики из группы антиметаболитов и ингибиторов фолиевой кислоты. Лекарственные средства вызывают самостоятельную резорбцию последа и позволяют сохранить матку, но не влияют на показатели гемостаза.
Хирургическое лечение
Хирургическая помощь необходима при таких аномалиях, как кровотечение, вызванное предлежанием плаценты, плотное прикрепление или истинное приращение, гипотоническое кровотечение при добавочной дольке. Предлежание, сопровождающееся кровотечением, является показанием для экстренного кесарева сечения вне зависимости от срока гестации. В остальных случаях применяются следующие методы:
- Ручное отделение последа. Используется при отсутствии признаков самостоятельного отделения, а также при гипотонии матки и кровотечении в последнем периоде родов. Манипуляция проводится под общей анестезией в родовом зале в присутствии анестезиолога-реаниматолога.
- Оперативное удаление плаценты. После предварительного лигирования сосудов матки, эмболизации маточных артерий или наложения компрессионных швов на матку плацента отделяется от стенки. Деваскуляризация матки позволяет избежать массивного кровотечения.
- Гистерэктомия. При неудачных попытках отделения последа с аномалиями прикрепления и продолжающемся кровотечении решается вопрос об удалении матки с сохранением придатков. Вмешательство проводится под эндотрахеальным наркозом.
Прогноз и профилактика
Аномалии формы детского места редко ухудшают прогноз течения беременности, иногда диагностируются случайно после родов. При аномалии прикрепления необходимо врачебное наблюдение для предупреждения осложнений. Профилактика заключается в отказе от абортов или использовании медикаментозных способов прерывания беременности. Женщинам рекомендуется применять барьерные методы контрацепции для защиты от инфекций, своевременно лечить воспаление половых органов. Кесарево сечение следует проводить строго по показаниям.
Приращение плаценты - причины, симптомы, диагностика и лечение
Приращение плаценты — это аномалия врастания хориальных ворсин с инвазией трофобласта в базальную отпадающую оболочку, миометрий, периметрий, окружающие органы. Проявляется отсутствием признаков отделения плаценты, профузным маточным кровотечением в последовом периоде, симптомами вовлечения смежных органов (тазовыми болями, примесью крови в кале и моче, запорами и др.). Для диагностики применяют УЗИ тазовых органов, ЦДК, МРТ-пельвиометрию, определение уровня АФП. Лечение предполагает проведение ручного отделения плаценты, надвлагалищной ампутации матки, гистерэктомии, метропластики, донного варианта кесарева сечения.
Общие сведения
Приращение плаценты было впервые описано в 1836 году английским гинекологом Джеймсом Симпсоном, морфологическую основу расстройства в 1889 году определил немецкий патолог Фредерик Харт. За последние 50 лет отмечается более чем десятикратное увеличение частоты патологии – с 1: 30 000 беременных в 1950-60-х годах до 1:2 500 в 2007 году, что напрямую связано со стремительным ростом числа кесаревых сечений. Зачастую патологическая глубокая инвазия хориона сочетается с предлежанием плаценты. По данным исследований, после первого оперативного родоразрешения риск приращения плацентарной ткани при ее предлежании повышается на 10%, а после 4-5-го — на 60% и более.
Приращение плаценты
Причины
Патологическому врастанию ворсин хориона в маточные оболочки способствуют как локальные дистрофические изменения эндометрия, так и нарушения бластогенеза. Риск развития расстройства повышается по мере увеличения возраста женщины и количества выношенных ею беременностей. По мнению большинства специалистов в сфере акушерства, основными причинами приращения тканей плаценты являются:
- Рубцовые изменения маточной стенки. Предпосылками к возникновению локальной дистрофии эндометрия становятся рубцы после перенесенных оперативных вмешательств, инвазивных манипуляций — кесарева сечения, миомэктомии, аборта, диагностического выскабливания. Дистрофические изменения провоцируются нарушениями процессов кровообращения и рубцовым перерождением эпителия.
- Заболевания матки. Нормальная архитектоника эпителиальной оболочки может нарушаться при неспецифическом и специфическом эндометрите, вызванном возбудителями хламидиоза, гонореи, туберкулеза, других инфекционных заболеваний половых органов. Приращение часто наблюдается при синдроме Ашермана, деформации маточной полости одной крупной или множественными подслизистыми миомами.
- Высокая протеолитическая активность хориона. В части случаев аномалии бластогенеза проявляются не нарушениями гаметогенеза и формированием пороков развития плода, а повышенной инвазивной способностью хориона. Более глубокая имплантация наблюдается при нарушении ферментативного равновесия в системе гиалуронидаза – гиалуроновая кислота между бластоцистой и децидуальной оболочкой.
Дополнительными факторами риска, способствующими аномальному врастанию хориальных ворсин, являются низкое расположение или предлежание плаценты, многоплодие, переношенная беременность, аномалии развития (двурогая матка, наличие внутриматочной перегородки). Патологию чаще выявляют у пациенток, страдающих хроническим гломерулонефритом, тяжелыми формами гестозов, при которых отмечаются микроциркуляторные нарушения в различных органах, в том числе в эндометрии и миометрии.
Патогенез
Механизм приращения плаценты основан на несоответствии проникающей способности трофобласта толщине и строению децидуальной оболочки. Недостаточная толщина эндометрия может быть обусловлена физиологической гипотрофией (функциональный слой слизистой обычно более тонкий в нижнем маточном сегменте) и патологическими процессами. Ситуация усугубляется при повышении протеолитической активности ферментов, способствующих внедрению бластоцисты в стенку матки. При наличии посттравматических, воспалительных, дистрофических изменений наблюдается рубцовое перерождение губчатого слоя отпадающей оболочки плаценты, по которому происходит ее отторжение в третьем периоде родов. При врастании в уплотненную ткань плацентарных ворсин становится невозможным их самопроизвольное отделение от стенки матки.
Значительное истончение эпителия сопровождается частичным или полным отсутствием губчатого слоя. В результате хориальные ворсины отделены от миометрия скоплениями фибриноида, а в более тяжелых случаях непосредственно контактируют с мышечными волокнами и даже прорастают в них на различную глубину. Плацентарные септы частично формируются из миоцитов, происходит обильная васкуляризация миометрия, подлежащего под плацентарной площадкой. После родов кавернозно измененная мышечная ткань не может сокращаться под влиянием окситоцина, что приводит к развитию массивного маточного кровотечения.
Классификация
Критериями для систематизации основных вариантов приращения плаценты служат площадь аномального прикрепления плацентарной ткани, глубина ее врастания в матку. Такой подход обеспечивает более точное прогнозирование осложнений и выбор оптимальной врачебной тактики. Приращение бывает полным с вовлечением в процесс всей плаценты и частичным с наличием участков нормальной и патологической плацентации. В зависимости от глубины проникновения в оболочки матки выделяют следующие виды расстройства:
- Ложное приращение (placenta adhaerens). Имеет более благоприятный прогноз в плане сохранения матки. Встречается значительно чаще, чем истинное. Возникает при рубцовом перерождении губчатого слоя. Хориальные ворсины плотно врастают в децидуальную оболочку и достигают базальной мембраны, однако не проникают до миометрия. Плацента самостоятельно не отделяется, использование специальных приемов ручного разделения плацентарной ткани и матки позволяет обойтись без полостной операции.
- Истинное приращение. Развивается на фоне атрофии губчатого слоя, проявляется проникновением ворсин хориона до мышечных волокон (приращенная плацента), в миометрий (вросшая плацента) и за пределы матки (проросшая плацента). Ручное отделение плаценты невозможно. Зачастую единственным методом, позволяющим сохранить жизнь родильницы, становится хирургическое удаление матки. Частота приращенной плаценты составляет около 78% всех случаев истинного приращения, вросшей — 15%, проросшей — 7%.
Симптомы приращения плаценты
Клинические признаки расстройства во время беременности отсутствуют. Патология проявляется в родах отсутствием внешних признаков отделения детского места в течение получаса после изгнания ребенка: маточное дно не поднимается выше пупка, не наблюдается выпячивание плаценты над симфизом, оставшийся конец пуповины не удлиняется, втягивается после натуживания женщины и укорачивается при надавливании на живот. При полном ложном и истинном приращении послеродовое кровотечение не возникает, при частичном приращении и попытке отделить приросший послед вручную начинается профузное маточное кровотечение. О прорастании плаценты в брюшину и другие органы свидетельствуют тазовые боли различной интенсивности, затруднения дефекации, примесь крови в моче или кале.
Осложнения
Диагностика
Для своевременного выявления патологии скрининговое обследование проводится всем беременным из группы риска — многократно рожавшим, женщинам с аномалиями матки, низко расположенной или предлежащей плацентой, пациенткам, ранее перенесшим кесарево сечение, миомэктомию, повторные аборты. Наиболее информативными являются методы ультразвуковой диагностики приращения плаценты:
- Эхография. Признаками возможного аномального крепления плацентарной ткани по данным УЗИ матки и плода считаются уменьшение расстояния между ретроплацентарными сосудами и периметрием до 10 мм и менее, наличие в толще плаценты кист, гиперэхогенных включений. Вероятность приращения повышается при обнаружении гипо- и анэхогенных участков с кровотоком лакунарного типа в мышечной стенке матки.
- Цветовое допплеровское картирование (ЦДК). Метод считается золотым стандартом в пренатальной диагностике приращения. В ходе исследования точно определяется локализация аномальных сосудистых зон. Патогномоничным признаком расстройства является расширение субплацентарного венозного комплекса. ЦДК также обеспечивает точную оценку глубины проникновения хориальных ворсин в миометрий.
В последние годы с диагностической целью акушеры-гинекологи все чаще назначают МРТ-пельвиометрию, позволяющую в сомнительных случаях достоверно визуализировать неровности маточной стенки, патологическую неоднородность структуры миометрия и плацентарной ткани. Косвенным лабораторным признаком расстройства служит повышение уровня альфа-фетопротеина.
При выявлении патологии в родах важно быстро выполнить дифференциальную диагностику между ложным и истинным приращением при помощи ручного отделения последа. При плотном прикреплении плацентарную ткань удается отделить полностью и, таким образом, купировать профузное кровотечение. Об истинном приращении свидетельствует невозможность отделения плаценты единым массивом, разрывы тканей, отсутствие отдельных долек, оставшихся в матке. Заболевание дифференцируют с другими расстройствами, сопровождающимися массивными маточными кровотечениями: маточной гипотонией, ДВС-синдромом, коагулопатиями, беременностью с нормально прикрепленной плацентой в трубном углу удвоенной или двурогой матки и др. По показаниям пациентку консультирует уролог, проктолог, хирург, анестезиолог-реаниматолог.
Лечение приращения плаценты
Выявление патологии служит показанием для проведения хирургического вмешательства. При антенатальной диагностике приращения естественные роды противопоказаны, операция выполняется в плановом порядке на 37-39 неделях гестационного срока одновременно с кесаревым сечением, при обнаружении в родах — экстренно по жизненным показаниям. Рекомендованный объем вмешательства определяется типом приращения плаценты:
- Ручное отделение с выделением последа. Акушерское пособие для извлечения неотделившейся плаценты с плодными оболочками проводят под внутривенной анестезией при ложном приращении. В ходе вмешательства акушер отделяет и удаляет плотно прикрепленную плацентарную ткань вручную.
- Удаление матки. При проникновении ворсин хориона к миометрию или их врастании в гладкомышечные волокна традиционно осуществляется надвлагалищная ампутация или гистерэктомия. Несмотря на травматичность, до недавнего времени такие операции были единственным способом остановить кровотечение.
- Органосохраняющие вмешательства. Антенатальная диагностика с последующим проведением донного кесарева сечения или метропластики позволяет сохранить матку даже при истинном приращении. Подобные операции в России пока производят редко, однако накоплен положительный опыт их выполнения за рубежом.
При прорастании маточной стенки рекомендованы комбинированные урогинекологические и проктогинекологические вмешательства, направленные на полное удаление плацентарной ткани. Часто щадящие хирургические методы дополняют эндоваскулярными для профилактики или остановки маточного кровотечения (эмболизацией маточных артерий, временной баллонной окклюзией). При экстренной операции родильнице показано восстановление объема циркулирующей крови с проведением инфузионной терапии (переливания цельной крови, ее компонентов, коллоидных и кристаллоидных растворов). Симптоматическое лечение включает назначение утеротоников (при сохранении матки), гемостатиков, препаратов для поддержания давления и сердечной деятельности.
Прогноз и профилактика
Благоприятный исход приращения плаценты возможен только при своевременной диагностике и выборе оптимального способа лечения. Для улучшения прогноза используют антенатальный скрининг и плановое хирургическое родоразрешение с выполнением операции рекомендованного объема. Первичная профилактика предполагает отказ от необоснованных диагностических и лечебных внутриматочных вмешательств, планирование беременности, лечение воспалительных заболеваний матки, проведение кесарева сечения строго при наличии акушерских или экстрагенитальных показаний.