Эфир в химии что это такое
Простые эфиры | Химия онлайн
Простыми эфирами называют органические вещества, в которых два углеводородных радикала связаны атомом кислорода: R'–O–R", где R' и R" — различные или одинаковые радикалы.
Простые эфиры могут быть предельными, непредельными, циклическими, ароматическими.
предельные
непредельные
ароматические
циклические
Простые эфиры рассматриваются как производные спиртов. Названия этих соединений строятся из названий радикалов (в порядке возрастания молекулярной массы) и слова «эфир». Например, CH3-O-CH3 - диметиловый эфир; C2H5-O-CH3 - метилэтиловый эфир.
Физические свойства
Два первых простейших представителя – диметиловый и метилэтиловый эфиры – при обычных условиях газы, все остальные – жидкости.
Диэтиловый эфир (C2H5-O-C2H5)– бесцветная легкокипящая прозрачная жидкость (t кип. 35,5 °С), малорастворимая в воде. С этиловым спиртом смешивается в любых отношениях. Температура воспламенения – 9,4°С, образует с воздухом взрывоопасную смесь. Вызывает набухание резин. Широко применяется в качестве растворителя, в медицине (ингаляционный наркоз), вызывает привыкание человека, ядовит.
Диоксан (т. кип. 101°С) — хороший растворитель, смешивается как с водой, так и с углеводородами. За эти качества его назвали «органической водой». Достаточно токсичен. Значительно более опасны галогенсодержащие дибензопроизводные диоксана: диоксин (2,3,7,8-тетрахлордибензо-п-диоксин).
Простые эфиры имеют более низкие температуры кипения и плавления, чем изомерные им спирты. Эфиры практически не смешиваются с водой. Это объясняется тем, что простые эфиры не образуют водородных связей, т.к. в их молекулах отсутствуют полярные связи О-Н.
Простые эфиры хорошо растворяют многие органические вещества и поэтому часто используются как растворители.
Эфиры имеют приятный запах.
Химические свойства
Простые эфиры — малоактивные соединения, они значительно менее реакционноспособны, чем спирты.
1.Расщепление простых эфиров HJ и HBr
Простые эфиры разлагаются под действием концентрированных иодоводородной или бромоводородной кислот:
2. Образование комплексных соединений
Образование нестойких солей оксония (подобных солям аммония) в результате взаимодействия с сильными кислотами:
3. Окисление эфиров, образование перекисей
Несмотря на относительную химическую инертность, эфиры легко образуют при хранении на воздухе перекиси:
Перекиси являются причиной взрывов в конце перегонки эфиров, поэтому эфиры тщательно очищают от перекисей перед перегонкой и применением.
Получение
1. Межмолекулярная дегидратация спиртов
Симметричные простые эфиры R–O–R получают при межмолекулярной дегидратации спиртов:
При этом в одной молекуле спирта разрывается связь О-Н, а в другой — связь С-О. Реакцию можно рассматривать как нуклеофильное замещение группы HО– (в одной молекуле спирта) на группу RO– (от другой молекулы):
2. Взаимодействие галогенпроизводных с алкоголятами (реакция Вильямсона)
Эфиры несимметричного строения R–O–R' образуются при взаимодействии алкоголята и галогенуглеводорода. Например, метилэтиловый эфир можно получить из этилата натрия и хлорметана:
В этой реакции происходит нуклеофильное замещение галогена (Cl–) на алкоксигруппу (CH3O–):
3. Дегидратация спиртов в присутствии ионов водорода как катализаторов
4. Получение гетероцикических кислородсодержащих соединений (циклические простые эфиры) этиленоксид (эпоксид) диоксан
Применение
Вследствие относительной химической инертности, эфиры часто применяются в качестве органических растворителей (диэтиловый эфир, тетрагидрофуран, диоксан).
Эфиры с разветвленными алкильными радикалами (например, метил-трет-бутиловый эфир) используются в последнее время в качестве антидетонационных добавок в моторные топлива (бензины), заменяя чрезвычайно вредный тетраэтилсвинец (ТЭС) — Pb (CH3CH2)4 .
Простые эфиры фенолов и нафтолов имеют своеобразные запахи и применяются в парфюмерии.
Химические свойства фенолов
Эфир (вещество) - это... Что такое Эфир (вещество)?
- Эфиопии
- Эфир (Оккультизм)
Смотреть что такое "Эфир (вещество)" в других словарях:
Эфир диэтиловый — См. также: Диэтиловый эфир (вещество)|Диэтиловый эфир|Диэтиловый эфир (вещество) … Википедия
Эфир медицинский — См. также: Диэтиловый эфир (вещество) Эфир диэтиловый (A … Википедия
Эфир для наркоза — См. также: Диэтиловый эфир (вещество) Эфир диэтиловый (A … Википедия
ЭФИР — (от греч. aither воздух). 1) упругое, незначительной плотности вещество, наполняющее вселенную, колебаниями которого физики объясняют явления света, теплоты, электричества и т. п. 2) в химии: летучая жидкость, получаемая от соединения какой… … Словарь иностранных слов русского языка
ЭФИР — (греч. ?? ?? верхние слои воздуха) 1) термин др. греч. философии, один из элементов, т. н. пятая субстанция (после земли, воды, воздуха и огня). см. Квинтэссенция. 2) Э. миpовой, световой Э., гипотетич. всепроникающая… … Философская энциклопедия
Эфир мировой — Эфир (Светоносный эфир) термин, обозначавший в истории физики гипотетическую всепроникающую среду, колебания которой обнаруживают себя как свет или электромагнитные волны. Содержание 1 История 2 Модели эфира 3 Эфир в современной физике … Википедия
ЭФИР — муж., греч. вообще, самое жидкое, тонкое, легкое и проницательное, что еле доступно чувствам, или даже от них укрывается; предполагаемое во всем пространстве вселенной вещество, по тонкости своей недоступное чувствам, служащее средою для передачи … Толковый словарь Даля
эфир — эфира, мн. нет, м. [греч. aither]. 1. Первонач., в учении греческих философов тончайшая материя, наполняющая мировое пространство, т. наз. “пятая стихия” (квинтэссенция), в противоп. четырем основным (огню, воздуху, воде и земле). 2. перен.… … Толковый словарь Ушакова
ЭФИР — ЭФИР, в физике гипотетическое вещество, которое, заполняет все пространство и не оказывает никакого сопротивления движению. Считалось, что именно эфир способствует передаче электромагнитных излучений (отсюда известное выражение «выйти в эфир» о… … Научно-технический энциклопедический словарь
эфир — ЭФИР (греч. ai8r)p) в исходном значении понятие связывалось с верхними, небесными слоями воздуха. Гомер называет Э. «чертогом Зевса», местом обитания бессмертных олимпийских богов. У Гесиода он один из прародителей мира, сын Эреба и Ночи … Энциклопедия эпистемологии и философии науки
Книги
- Строение материи (как устроен наш мир). Маргулис М. А., Маргулис Милья Аркадьевич. Исследование эфира является одной из фундаментальных проблем естествознания и нашего представления о природе, о пространстве, времени, материи. Автор разработал новую модель электрона и… Подробнее Купить за 498 грн (только Украина)
- Строение материи (как устроен наш мир), Маргулис Милья Аркадьевич. Исследование эфира является одной из фундаментальных проблем естествознания и нашего представления о природе, о пространстве, времени, материи. Автор разработал новую модель электрона и… Подробнее Купить за 389 руб
- Модель эфира и электрона, Маргулис М.. Исследование эфира является одной из фундаментальных проблем естествознания и нашего представления о природе, о пространстве, времени, материи. Автор разработал новую модель электрона в виде… Подробнее Купить за 162 руб
Эфиры (понятия, свойства, применение)

Общие сведения
Эфиры (от греческого слова Aethеr - эфир, небо, воздух) (простые эфиры) - это производные спиртов, энола и фенолов (общая формула R-O-R '). Если радикалы одинаковы, то эфиры - симметричные, если разные - несимметричные или смешанные. В зависимости от природы радикалов различают диалкил, диарилови, дициклоалкилови, арилалкил, алкилвинилови и др. К эфиры относятся также Глим, карбитолы, целлозоли и некоторые гетероциклические соединения (1,4-диоксан, оксиран, оксолан, тетрагидрофуран и т.п.).
Названия эфиров образуют от названий углеводородных радикалов путем добавления суффикса -ный и слова «эфир», например, СН3-О-СН3 - диметиловый эфир, СН3-О-С2Н5 - метилетиловий эфир.
Эфиры рассматривают как алкокси-, циклоалкокси-, арилоксипроизводные углеводородов, в этом случае сложнее радикал считается родоначальной структурой: Ch4-О-СН 2 СН 3 - метоксиетан, С2Н5О-С3Н7 - этоксипропан, С6Н5-ОСН3 - метоксибензол.
Некоторые эфиры имеют тривиальные названия: С6Н5-ОСН3 - анизол, С6Н5-С2Н5 - фенетол, 2-СН3ОС6Н4ОН - гваякол. Диметиловый и метилэтиловый эфиры при обычных условиях являются газами. Все остальные эфиры - это бесцветные жидкости или кристаллические вещества с приятным или характерным «эфирным» запахом, плохорастворимые в воде, хорошо - в органических растворителях (таблица).
Физические, химические и фармакологические свойства
Таблица. Свойства эфиров
| Формула | Название | Ткип, оС | Тпл, оС |
| СН3ОСН3 | Диметиловый эфир (метоксиметан) | -23.7 | -138,5 |
| СН3ОС2Н5 | Метилетиловый эфир (метоксиетан) | 8 | - |
| С2Н5ОС2Н5 | Диэтиловый эфир (этоксиэтан) | 34,6 | -116,3 |
| С2Н5ОСН = СН2 | метилвиниловый эфир (этоксиэтилен) | 36 | - |
| С3Н7ОС3Н7 | Дипропиловый эфир (пропоксипропан) | 91 | -122 |
| С6Н5ОСН3 | Метоксибензол (анизол) | 155 | -37 |
| С6Н5ОС2Н5 | Этоксибензол (фенетол) | 172 | -33 |
| С6Н5ОС6Н5 | Дифениловый эфир (феноксибензол) | 259 | 27,5 |
Эфиры достаточно инертными веществами. Разведенные минеральные кислоты, водные растворы щелочей и щелочные металлы с ними не взаимодействуют. Реакционная способность виниловых и арилових эфиров обусловлена углеводородными радикалами. Через неразделенные пары электронов на атоме кислорода эфиры проявляют слабые основные свойства и с концентрированными минеральными кислотами образуют неустойчивые соли оксония.
[RR'-OH] + Cl-,
а с кислотами Льюиса - эфираты (RR'OBF3). Диалкиловые и алкилариловые эфиры разлагаются под действием НЕ к галогеналканами и соответствующего спирта или фенола:
СН3ОСН3 + НЕТ → СН3ОН + СН3И.
Диариловые эфиры устойчивы к действию концентрированной йодоводистой кислоты. Расщепление метил и этилалкиловых эфиров используют для количественного определения метокси- и этоксигруп (метод Цейзеля). Концентрированная h3SO4 превращает эфиры сложные субстанции серной кислоты, а виниловые эфиры в кислой среде гидролизуются до альдегидов или кетонов и спиртов:
Виниловые эфиры способны полимеризоваться, что используется в синтезе ВМС. При действии алкилнатрия или алкиллития на эфиры происходит β-элиминирования с образованием алкенов:
Ch4Ch3OCh3Ch4 + RNa 1arrow.eps Ch3 = Ch3 + C2H5ONa + RH.
Арилалкил эфиры под действием h3SO4, AlCl3 изомеризируются в орто и пара-алкилзамещенные фенолы, а алилфенилови эфиры - в орто и пара-алилфенолы. При длительном стоянии эфиры окисляются кислородом воздуха с образованием взрывоопасных гидропероксидов R-O-OH и пероксидов R-O-O-R. Поэтому перед использованием простых эфиров необходимо делать пробу с раствором KI. Наличие пероксидов подтверждает буро-коричневый цвет раствора. Для разрушения эфирных пероксидов обрабатывают NaOH или восстановителями Na2SO3, FeSO4 и др. Для получения симметричных эфиров используют реакцию межмолекулярной дегидратации спиртов в присутствии концентрированной h3SO4 или других водозабирающих веществ. Важным методом синтеза симметричных и несимметричных эфиров реакция алкоголятов и фенолятов с алкилгалогенидами (реакция Вильямсона). Для синтеза арилалкиловых эфиров вместо арилгалогенидов можно применять диалкилсульфаты:
C6H5ONa + (Ch4) SO4 C6H5OCh4 + Ch4OSO3Na.
эфиры также образуются по реакции присоединения спиртов или фенолов к олефинов. При нагревании спиртов с ацетиленом получают алкилвиниловые эфиры
HC = -CH + HOCh3Ch4 1arrow.eps Ch3 = CH-O-C2H5.
Взаимодействие ацетилена с диазометаном приводит к образованию алкил- и арилметиловых эфиров.
Применение в медицине и фармации
Диэтиловый эфир применяют для изготовления настоев, экстрактов некоторых лекарственных форм для наружного применения, ограниченно - в хирургической практике для наркоза. Его смесь с этанолом в пропорции 1: 3 под названием капель Гофмана используют при головокружении. Бутилвиниловый эфир является исходным продуктом синтеза поливинилбутилового эфира, который применяют при фурункулах, трофических язвах, ожогах, обморожениях (бальзам М.Ф. Шостаковского или винилин). К арилалкиловым эфирам можно отнести и димедрол, который применяют как антигистаминный препарат. Эфиры - растворители жиров, лаков и других органических соединений. Используются в производстве ароматических веществ, красителей.
Литература
- Химическая энциклопедия. В 5 т. - М., 1990. - Т. 5.
- Черных В.П., Зименковский Б.С., Гриценко И.С. Органическая химия / Под общ. ред. В.П. Черных. - второй изд. - Х., 2007.
Диэтиловый эфир — Википедия
Материал из Википедии — свободной энциклопедии
| Диэтиловый эфир | |||
|---|---|---|---|
| |||
| Систематическое наименование | Этоксиэтан | ||
| Хим. формула | C4H10O | ||
| Состояние | жидкость | ||
| Молярная масса | 74,12 г/моль | ||
| Плотность | 0,714 г/см³ | ||
| Энергия ионизации | 9,53 ± 0,01 эВ[1] | ||
| Температура | |||
| • плавления | -116,3 °C | ||
| • кипения | 34,65 °C | ||
| • разложения | 193,4 °C | ||
| • вспышки | −49 ± 1 °F[1] | ||
| Пределы взрываемости | 1,9 ± 0,1 об.%[1] | ||
| Давление пара | 440 ± 1 мм рт.ст.[1] | ||
| Растворимость | |||
| • в воде | (для 20 °С) 6,5 г/100 мл | ||
| Рег. номер CAS | 60-29-7 | ||
| PubChem | 3283 | ||
| Рег. номер EINECS | 200-467-2 | ||
| SMILES | |||
| InChI | |||
| RTECS | KI5775000 | ||
| ChEBI | 35702 | ||
| Номер ООН | 1155 | ||
| ChemSpider | 3168 | ||
| Пиктограммы ECB | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
| Медиафайлы на Викискладе | |||
Диэтиловый эфир (этиловый эфир, серный эфир, этоксиэтан). По химическим свойствам — типичный алифатический простой эфир. Широко используется в качестве растворителя. Впервые получен в Средние века.
Возможно, что впервые диэтиловый эфир был получен в IX веке алхимиком Джабир ибн Хайяном[2] либо алхимиком Раймундом Луллием в 1275 году[2][3]. Достоверно известно, что он был синтезирован в 1540 году Валерием Кордусом, который назвал его «сладким купоросным маслом» (лат. oleum dulce vitrioli), поскольку получил его перегонкой смеси этилового спирта и серной кислоты, которая тогда называлась «купоросным маслом»[2]. Кордус также отметил его анестезирующие свойства. В 1680 году Роберт Бойль вторично синтезировал эфир. Затем в 1704 году Исаак Ньютон открыл эфир в третий раз, в поисках синтеза искусственного золота.[4]
Название «эфир» было дано этому веществу в 1729 году Фробениусом[en][5].
В 1794 году эфир был испытан для вдыханий с целью уменьшения болей, а в 1795 году Томас Беддоус создал Медицинский пневматический институт для лечения различных легочных заболеваний газами. Такие газы тогда называли "искусственным воздухом".[4]
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например, перегонкой смеси этилового спирта и серной кислоты при температуре порядка 140—150 °C. Также получается как побочный продукт в производстве этилового спирта гидратацией этилена в присутствии фосфорной кислоты или 96—98 % серной кислоты при 65—75 °С и давлении 2,5 МПа. Основная часть диэтилового эфира образуется на стадии гидролиза этилсульфатов (95—100 °C, 0,2 МПа).
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается с этанолом, бензолом, эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути.
- Образующиеся пероксиды нестойки и взрывоопасны, они могут быть причиной самовоспламенения диэтилового эфира при хранении и взрыве при его перегонке «досуха»
По химическим свойствам диэтиловый эфир обладает всеми свойствами, характерными для простых эфиров, например, образует нестойкие оксониевые соли с сильными кислотами:
- (C2H5)2O+HBr→[(C2H5)2OH]+Br−{\displaystyle {\mathsf {(C_{2}H_{5})_{2}O+HBr\rightarrow [(C_{2}H_{5})_{2}OH]^{+}Br^{-}}}}
Образует сравнительно стабильные комплексные соединения с кислотами Льюиса: (C2H5)2O·BF3
Фармакология[править | править код]
В медицине используется в качестве лекарственного средства общеанестезирующего действия, так как его влияние на нейронные мембраны и свойство «обездвиживать» ЦНС очень специфично и полностью обратимо. Применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
В связи с медленным разложением диэтилового эфира, должны строго выдерживаться установленные сроки хранения. Для наркоза можно применять эфир только из склянок, открытых непосредственно перед операцией. По истечении каждых 6 месяцев хранения эфир для наркоза проверяют на соответствие требованиям. Использование технического эфира в этих целях не допускается.
Выдающийся отечественный хирург Н.И. Пирогов первым в истории медицины начал оперировать раненых с эфирным обезболиванием в полевых условиях и всего провел около десяти тысяч операций под эфирным наркозом.
Техника[править | править код]
Диэтиловый эфир — аэрозоль для быстрого запуска.Инструкция утверждает, что возможен запуск при температуре −55 °F (−48,3 °C)
В СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре. Для армии выпускался эфир в алюминиевой запечатанной гильзе, перед использованием гильза протыкалась штык-ножом или отвёрткой. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне. Состав: диэтиловый эфир, индустриальное масло, пропеллент.
Механизм запуска ДВС в этом случае по большей мере компрессионный: смесь эфира с воздухом воспламеняется от сжатия уже при степени сжатия порядка 5-6. Потерявшие компрессию по разным причинам двигатели могут делать несколько оборотов на эфире, но на бензине, тем не менее, не работают.
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0277.html
- ↑ 1 2 3 Toski, A; Bacon, DR; Calverley, RK. The history of Anesthesiology // Clinical Anesthesia / Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K.. — 4th ed. — Lippincott Williams & Wilkins, 2001. — P. 3. — ISBN 978-0-7817-2268-1.
- ↑ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. McGraw-Hill's PCAT. — McGraw-Hill. — P. 39. — ISBN 978-0-07-160045-3.
- ↑ 1 2 П.Ю.Столяренко История обезболивания в стоматологии (часть 1) Архивная копия от 15 июня 2018 на Wayback Machine
- ↑ Dr. Frobenius (1729) "An account of a spiritus vini æthereus, together with several experiments tried therewith, " (недоступная ссылка) Philosophical Transactions of the Royal Society (London), 36 : 283—289.
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР, 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.: Химия, 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чём не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М.: Химия, 1979, с. 332-40;
- Грефе Ю., Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.
ЭФИР - это... Что такое ЭФИР?
ЭФИР — (греч. ?? ?? верхние слои воздуха) 1) термин др. греч. философии, один из элементов, т. н. пятая субстанция (после земли, воды, воздуха и огня). см. Квинтэссенция. 2) Э. миpовой, световой Э., гипотетич. всепроникающая… … Философская энциклопедия
ЭФИР — ЭФИР (греч. αίθήρ), в античной философии один из космических элементов, составляющий субстанцию неба и звезд. В древнегреческой эпической поэзии и у трагиков эфир ясное небо, верхний чистый слой воздуха, противоположный нижнему слою аэру… … Античная философия
ЭФИР — муж., греч. вообще, самое жидкое, тонкое, легкое и проницательное, что еле доступно чувствам, или даже от них укрывается; предполагаемое во всем пространстве вселенной вещество, по тонкости своей недоступное чувствам, служащее средою для передачи … Толковый словарь Даля
эфир — эфира, мн. нет, м. [греч. aither]. 1. Первонач., в учении греческих философов тончайшая материя, наполняющая мировое пространство, т. наз. “пятая стихия” (квинтэссенция), в противоп. четырем основным (огню, воздуху, воде и земле). 2. перен.… … Толковый словарь Ушакова
ЭФИР — (греч. aither) мировой, световой эфир, гипотетич. всепроникающая среда, к рой наука прошлых столетий приписывала роль переносчика света и вообще эл. магн. вз ствий. Первоначально Э. понимали как механич. среду, подобную упругому телу. Соотв.… … Физическая энциклопедия
ЭФИР — ЭФИР, в физике гипотетическое вещество, которое, заполняет все пространство и не оказывает никакого сопротивления движению. Считалось, что именно эфир способствует передаче электромагнитных излучений (отсюда известное выражение «выйти в эфир» о… … Научно-технический энциклопедический словарь
эфир — воздушное пространство, вышина, среда, высь, поднебесье, воздух, высота (поднебесная), небесная высь, пространство; глицерид, лактон, антодин, формиат, метакрилат, гваякол, уретан, эстер, пальмитин, наркотик Словарь русских синонимов. эфир см.… … Словарь синонимов
ЭФИР — ЭФИР, то же, что этиловый эфир … Современная энциклопедия
ЭФИР — электронный финансовый рынок техн., фин. ЭФиР «Экономика, финансы и рынки» информационно аналитическая система «Интерфакса» http://efir.kiev.ua/ фин … Словарь сокращений и аббревиатур
Эфир — ЭФИР, то же, что этиловый эфир. … Иллюстрированный энциклопедический словарь
Простые и сложные эфиры – HIMI4KA

Простыми эфирами называют класс химических соединений, в которых два углеводородных радикала связаны между собой атомом кислорода (кислородным мостиком). В общем виде формула простых эфиров R—O—R1, где R и R1 — углеводородные радикалы. Для этого класса соединений характерны структурная изомерия, а также межклассовая изомерия со спиртами.
Простые эфиры образуются при межмолекулярной дегидратации спиртов, а также при взаимодействии алкоголятов с галоидными алкилами, например:
Простые эфиры химически инертны. Их характерные реакции на примере диэтилового эфира:
Пары диэтилового эфира пожаро- и взрывоопасны.
Сложными эфирами называют класс химических соединений, который отвечает общей формуле R—C(O)O—R1, где R и R1 — углеводородные радикалы. Таким образом, сложные эфиры можно рассматривать как производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен на углеводородный радикал, или производные спиртов, в которых атом водорода гидроксильной группы замещен на кислотный остаток карбоновой кислоты.
Сложные эфиры образуются в результате реакции этерификации (урок 25). При этом следует отметить, что при одной и той же кислоте скорость этерификации первичных спиртов в два раза выше, чем у вторичных и во много раз превосходит третичные.
Кроме того, сложные эфиры можно получить в результате взаимодействия солей карбоновых кислот с галоидными алкилами:
Для сложных эфиров характерны изомерия углеводородных радикалов кислот и спиртов, составляющих сложный эфир, а также межклассовая изомерия с карбоновыми кислотами. Ниже приведены реакции, иллюстрирующие характерные химические свойства сложных эфиров.
1. Кислый или щелочной гидролиз:
2. Реакция переэтерификации (идет в том случае, если брать избыток спирта и отгонять образующийся более легкокипящий спирт):
3. Восстановление:
ЭФИР (в химии) - это... Что такое ЭФИР (в химии)?
ЭФИР — (от греч. aither воздух). 1) упругое, незначительной плотности вещество, наполняющее вселенную, колебаниями которого физики объясняют явления света, теплоты, электричества и т. п. 2) в химии: летучая жидкость, получаемая от соединения какой… … Словарь иностранных слов русского языка
Эфир (физика) — У этого термина существуют и другие значения, см. Эфир. Эфир (светоносный эфир, от др. греч. αἰθήρ, верхний слой воздуха; лат. aether) гипотетическая всепроникающая среда[1], колебания которой проявляют себя как электромагнитные волны… … Википедия
Эфир — Вадревнегреческой мифологии самый верхний, чистый и прозрачный слой воздуха, местопребывание богов. У Гесиода Эфир сын Эреба и Ночи,. У Гомера и Софокла он отождествлялся с оплодотворяющим землю Ураном. Вапредставлении орфиков Эфир мировая душа,… … Религиозные термины
ЭФИР — (Греч.) У древних божественная святоносная субстанция, наполняющая всю вселенную, одеяние Высшего Божества, Зевса, или Юпитера. У современных писателей Эфир (Ether), о значении которого в физике и химии смотреть Словарь Вебстера или любой другой … Теософский словарь
Радикал в химии — (химич. radical, radicale) слово, впервые введенное в научную химическую литературу, по видимому, Гитоном де Морво. В докладе французской Академии наук [ M émoire sur le Développement des Principes de la Nomenclature Mé thodique (18 апр. 1787).… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Радикал, в химии — (химич. radical, radicale) слово, впервые введенное в научную химическую литературу, по видимому, Гитоном де Морво. В докладе французской Академии наук [ Mémoire sur le Développement des Principes de la Nomenclature Méthodique (18 апр. 1787).… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Ацетоуксусный эфир — Ацетоуксусный эфир … Википедия
Метамерия (в химии) — Метамерия в химии, частный случай изомерии, связанный с положением гетероатома в цепи алифатических соединений. Метамерны, например, метилпропиловый эфир Ch4OCh3Ch3Ch4 и диэтиловый эфир Ch4Ch3OCh3Ch4. Термин «М.» предложен И. Берцелиусом в 1830 и … Большая советская энциклопедия
Крахмал в химии* — (Amidon, amidam фр., Starch англ., St ä rke, Satzmehl нем., Amylum лат.) nС 6h20O5 или вернее nС 6h20O5+h3 O (см. соотв. статью). Величина n не установлена окончательно; она несомненно значительна. По Брауну и Моррису, воспользовавшимися методом… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Эритрин в химии — орселиново эритритовый эфир (см. Эритрит) … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Эфир - это... Что такое Эфир?
ЭФИР — (греч. ?? ?? верхние слои воздуха) 1) термин др. греч. философии, один из элементов, т. н. пятая субстанция (после земли, воды, воздуха и огня). см. Квинтэссенция. 2) Э. миpовой, световой Э., гипотетич. всепроникающая… … Философская энциклопедия
ЭФИР — ЭФИР (греч. αίθήρ), в античной философии один из космических элементов, составляющий субстанцию неба и звезд. В древнегреческой эпической поэзии и у трагиков эфир ясное небо, верхний чистый слой воздуха, противоположный нижнему слою аэру… … Античная философия
ЭФИР — (от греч. aither воздух). 1) упругое, незначительной плотности вещество, наполняющее вселенную, колебаниями которого физики объясняют явления света, теплоты, электричества и т. п. 2) в химии: летучая жидкость, получаемая от соединения какой… … Словарь иностранных слов русского языка
ЭФИР — муж., греч. вообще, самое жидкое, тонкое, легкое и проницательное, что еле доступно чувствам, или даже от них укрывается; предполагаемое во всем пространстве вселенной вещество, по тонкости своей недоступное чувствам, служащее средою для передачи … Толковый словарь Даля
эфир — эфира, мн. нет, м. [греч. aither]. 1. Первонач., в учении греческих философов тончайшая материя, наполняющая мировое пространство, т. наз. “пятая стихия” (квинтэссенция), в противоп. четырем основным (огню, воздуху, воде и земле). 2. перен.… … Толковый словарь Ушакова
ЭФИР — (греч. aither) мировой, световой эфир, гипотетич. всепроникающая среда, к рой наука прошлых столетий приписывала роль переносчика света и вообще эл. магн. вз ствий. Первоначально Э. понимали как механич. среду, подобную упругому телу. Соотв.… … Физическая энциклопедия
ЭФИР — ЭФИР, в физике гипотетическое вещество, которое, заполняет все пространство и не оказывает никакого сопротивления движению. Считалось, что именно эфир способствует передаче электромагнитных излучений (отсюда известное выражение «выйти в эфир» о… … Научно-технический энциклопедический словарь
эфир — воздушное пространство, вышина, среда, высь, поднебесье, воздух, высота (поднебесная), небесная высь, пространство; глицерид, лактон, антодин, формиат, метакрилат, гваякол, уретан, эстер, пальмитин, наркотик Словарь русских синонимов. эфир см.… … Словарь синонимов
ЭФИР — ЭФИР, то же, что этиловый эфир … Современная энциклопедия
ЭФИР — электронный финансовый рынок техн., фин. ЭФиР «Экономика, финансы и рынки» информационно аналитическая система «Интерфакса» http://efir.kiev.ua/ фин … Словарь сокращений и аббревиатур
Эфир — ЭФИР, то же, что этиловый эфир. … Иллюстрированный энциклопедический словарь
Ньютоний — Википедия

Ньютоний (лат. Newtonium в честь Исаака Ньютона) — легчайший гипотетический химический элемент, существованием которого Д. И. Менделеев пытался объяснить химическую природу мирового эфира.
Концепция мирового эфира получила развитие в середине XIX века в рамках волновой оптики и электромагнитной теории Максвелла. Мировой эфир стал рассматриваться как гипотетическая всепроникающая сущность, заполняющая мировое пространство и передающая свет, тепло и гравитацию[1].
Очевидно, что открытым оставался вопрос о химической природе эфира: он должен был состоять из легчайших, абсолютно инертных элементов, атомы которых не удерживались бы гравитационными силами. Ни легчайший известный элемент, водород, ни гипотетический короний категорически не годились на эту роль. Таким образом, концепция мирового эфира оказалась тесно связанной с решением проблемы нижней границы периодической системы химических элементов.
Обложка брошюры «Попытка химического понимания мирового эфира» и периодическая таблица элементов из неё (Политехнический музей, Москва)Задачу тяготения и задачи всей энергетики нельзя представить реально решёнными без реального понимания эфира, как мировой среды, передающей энергию на расстояния. Реального же понимания эфира нельзя достичь, игнорируя его химизм и не считая его элементарным веществом.
Д. И. Менделеев, открыв Периодический закон, понимал, что явление периодичности не имеет физического обоснования, и не видел прямых путей, ведущих к его отысканию. Ещё в ранних работах по периодичности Менделеев предполагал, что эфир мог быть специфическим состоянием газов при большом разрежении или особым газом с очень малым весом. Открытие в конце XIX века инертных газов актуализировало вопрос о сущности химических элементов. По предложению Уильяма Рамзая Менделеев формирует нулевую группу периодической таблицы, но также оставляет место для более лёгких, чем водород, элементов. По мнению Менделеева, группа инертных газов могла быть дополнена коронием и ещё более лёгким, пока неизвестным элементом. Свои соображения Менделеев высказал в статье «Попытка химического понимания мирового эфира» (1902, опубл. в 1905) и 8-м издании учебника «Основы химии» (1906).
Если же аналоги аргона вовсе не дают соединений, то очевидно, что нельзя включать ни одну из групп ранее известных элементов, и для них должно открыть особую группу нулевую… Это положение аргоновых аналогов в нулевой группе составляет строго логическое следствие понимания периодического закона… Теперь же, когда стало не подлежать ни малейшему сомнению, что перед той I группой, в которой должно помещать водород, существует нулевая группа, представители которой имеют веса атомов меньше, чем у элементов I группы, мне кажется невозможным отрицать существование элементов более лёгких, чем водород.
… я прибавляю в последнем видоизменении распределения элементов по группам и рядам не только нулевую группу, но и нулевой ряд, и на место в нулевой группе и в нулевом ряде помещён элемент x (мне бы хотелось предварительно назвать его «ньютонием» — в честь бессмертного Ньютона), который и решаюсь считать, во-первых, наилегчайшим из всех элементов, как по плотности, так и по атомному весу, во-вторых, наибыстрее движущимся газом, в-третьих, наименее способным к образованию с какими-либо другими атомами или частицами определенных сколько-либо прочных соединений, и, в-четвертых, — элементом, всюду распространённым и всё проникающим, как мировой эфир.
Менделеев привёл свои расчёты массы атома ньютония, исходя из «возможности движущимся частицам вырываться из сферы притяжения земли, солнца и звёзд». Она, по расчетам ученого, может колебаться в пределах 9.6·10−7 до 5.3·10−11 от массы атома водорода: «…для понимания множества явлений совершенно достаточно признать пока, что частицы и атомы легчайшего элемента х, могущего свободно двигаться всюду, имеют вес, близкий к одной миллионной доле веса водородного атома, и движутся со средней скоростью, недалекою от 2250 километров в секунду».
Следует отметить, что ни в цитируемой выше статье, ни в 7-м и 8-м издании «Основ химии» Менделеев не включил ньютоний и короний в прилагаемые периодические таблицы, признавая очевидное отсутствие экспериментальных доказательств их реальности. При всей умозрительной направленности исходных предпосылок основным и наиболее важным результатом в области физики, полученным благодаря им Д. И. Менделеевым, явился вывод уравнения идеального газа.
Гипотеза о существовании ньютония потеряла актуальность вместе с представлениями о мировом эфире после появления специальной теории относительности и создания квантово-механической модели атома. К 1930-м годам проблема «эфира» уже не существовала в науке, равно как и вопрос об элементах легче водорода. Неоднократные попытки отдельных учёных возродить концепцию эфира в той или иной форме (например, связать эфир с физическим вакуумом) успеха не имели. Следует считать спекулятивными и не имеющими никаких оснований публикации о том, что менделеевская гипотеза о ньютонии — не что иное, как гениальное предвидение не то открытия нейтрино, не то фотона.
Сложные эфиры — понятие, свойства, применение
В прошлой статье мы рассказывали о простых эфирах, а сейчас поговорим о сложных. Сложные эфиры широко распространены в природе. Сказать, что сложные эфиры играют большую роль в жизни человека — ничего не сказать. Мы сталкиваемся с ними, когда нюхаем цветок, обязанный ароматом простейшим сложным эфирам. Подсолнечное или оливковое масло — это тоже сложный эфир, но уже высокомолекулярный — также, как и животные жиры. Мы моемся, моем и стираем средствами, которые получают химической реакцией переработки жиров, то есть сложных эфиров. Еще они используются в самых разных областях производства: с их помощью делают лекарства, краски и лаки, духи, смазки, полимеры, синтетические волокна и многое, многое другое.
Сложные эфиры — органические соединения на основе кислородосодержащих органических карбоновых или неорганических кислот. Структуру вещества можно представить как молекулу кислоты, в которой атом Н в гидроксиле ОН— замещен углеводородным радикалом.
Получают сложные эфиры в результате реакции кислоты и спирта (реакция этерификации).
Классификация
— Фруктовые эфиры — жидкости с фруктовым запахом, молекула содержит не более восьми атомов углерода. Получают из одноатомных спиртов и карбоновых кислот. Эфиры с цветочным запахом получают с помощью ароматических спиртов.
— Воски — твердые вещества, содержат в молекуле от 15 до 45 атомов С.
— Жиры — содержат в молекуле 9-19 атомов углерода. Получают из глицерина (трехатомного спирта) и высших карбоновых кислот. Жиры могут быть жидкими (растительные жиры, называемые маслами) и твердыми (животные жиры).
— Сложные эфиры минеральных кислот по своим физическим свойствам тоже могут быть как маслянистыми жидкостями (до 8 атомов углерода), так и твердыми веществами (от девяти атомов C).
Свойства
В нормальных условиях сложные эфиры могут быть жидкими без цвета, с фруктовым или цветочным запахом, или твердыми, пластичными; как правило, без запаха. Чем длиннее цепочка углеводородного радикала, тем тверже вещество. Почти неводорастворимы. Хорошо растворяются в органических растворителях. Горючи.
Вступают в реакции с аммиаком с образованием амидов; с водородом (именно эта реакция превращает жидкие растительные масла в твердые маргарины).
В результате реакции гидролиза разлагаются на спирт и кислоту. Гидролиз жиров в щелочной среде приводит к образованию не кислоты, а ее соли — мыла.
Сложные эфиры органических кислот малотоксичны, оказывают на человека наркотическое воздействие, в основном относятся ко 2-му и 3-му классу опасности. Некоторые реактивы на производстве требуют использования специальных средств защиты для глаз и дыхания. Чем больше длина молекулы эфира, теми он токсичнее. Эфиры неорганических фосфорных кислот ядовиты.
В организм вещества могут попадать через органы дыхания и кожу. Симптомами острого отравления служат возбуждение и нарушенная координация движений с последующим угнетением ЦНС. Регулярное воздействие может привести к болезням печени, почек, сердечно-сосудистой системы, нарушениям формулы крови.
Применение
— В органическом синтезе.
— Для производства инсектицидов, гербицидов, смазок, пропиток для кожи и бумаги, моющих средств, глицерина, нитроглицерина, олиф, масляных красок, синтетических волокон и смол, полимеров, оргстекла, пластификаторов, реагентов для обогащения руд.
— Как добавка к моторным маслам.
— В синтезе парфюмерных отдушек, пищевых фруктовых эссенций и косметических ароматизаторов; лекарственных средств, например, витаминов А, Е, В1, валидола, мазей.
— Как растворители красок, лаков, смол, жиров, масел, целлюлозы, полимеров.
В ассортименте магазина «ПраймКемикалсГрупп» вы можете купить востребованные сложные эфиры, в том числе бутилацетат и Твин-80.
Бутилацетат
Применяется как растворитель; в парфюмерной промышленности для изготовления отдушек; для дубления кож; в фармацевтике — в процессе изготовления некоторых лекарств.
Твин-80
Он же полисорбат-80, полиоксиэтилен сорбитан моноолеат (основан на сорбите оливкового масла). Эмульгатор, растворитель, техническая смазка, модификатор вязкости, стабилизатор эфирных масел, неионогенный ПАВ, увлажнитель. Входит в состав растворителей и смазочно-охлаждающих жидкостей. Используется для производства продукции косметического, пищевого, бытового, сельскохозяйственного, технического назначения. Обладает уникальным свойством превращать смесь воды и масла в эмульсию.
Формула эфира в химии
Определение и формула эфира
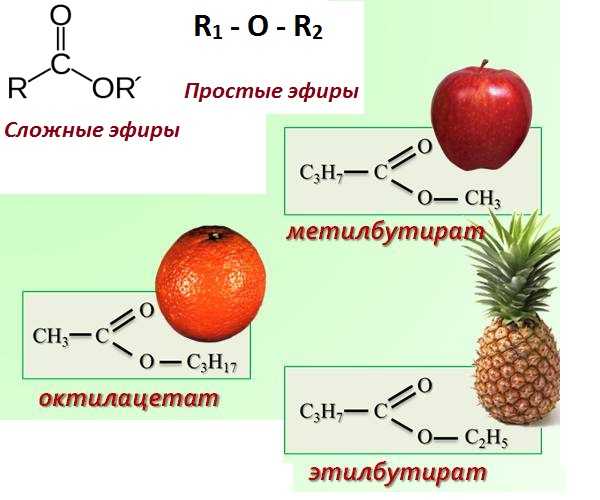
Химическая формула: простой эфир – , где – это углеводородный радикал.
Химическая формула: сложный эфир – , где – это углеводородный радикал.
Физические свойства простого эфира – и являются газами, остальные подвижные легкокипящие жидкости. Эфиры плохо растворимы в воде, легче воды, имеют приятный запах.
Физические свойства сложного эфира – сложные эфиры низших карбоновых кислот и простейших одноатомных спиртов — летучие бесцветные жидкости с характерным, зачастую фруктовым запахом. Сложные эфиры высших карбоновых кислот — бесцветные твердые вещества.
Химические свойства эфира
- Сложные эфиры подвергаются гидролизу:
- Они вступают в реакцию переэтерификации:
- Подвергаются восстановлению:
Применение
Эфиры широко распространены в природе и широко используются в промышленности. Природные жиры — это триэфиры, полученные из глицерина и жирных кислот. Эфиры ответственны за аромат многих фруктов, в том числе яблок, груш, бананов, ананасов, клубники. Несколько миллиардов килограммов полиэфиров производятся промышленностью ежегодно, важные продукты — полиэтилентерефталаты, акрилатные сложные эфиры, и ацетат целлюлозы.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||