Пружинка в сердце что это такое
Пружина для сердца | Лечим Сердце
Основной причиной самого серьезного проявления ишемической болезни сердца, инфаркта миокарда, является нарушение питания мышцы за счет атеросклеротического поражения сосудов.
Атеросклероз поражает стенку артерии. Из-за потери эластичности теряется возможность к достаточному расширению. Отложение атеросклеротических бляшек изнутри вызывает сужение диаметра сосуда, затрудняет доставку питательных веществ. Критическим уменьшением считается 50% диаметра. При этом начинают проявляться клинические симптомы гипоксии (недостатка кислорода) сердца. Это выражается в приступах стенокардии.
Полная закупорка коронарной артерии ведет к развитию участка омертвения (некроза) при инфаркте миокарда. Во всем мире эта патология до сих пор считается одной из главных причин смертности взрослых людей.
Своевременное стентирование сосудов сердца позволяет предотвратить развитие тяжелых осложнений атеросклероза.
Что такое «стентирование»?
Термином «стентирование» называется операция по установке стента внутри артерии, в результате которой проводится механическое расширение суженной части и восстановление нормального кровотока к органу. Операция относится к эндоваскулярным (внутрисосудистым) хирургическим вмешательствам. Проводится в отделениях сосудистого профиля. Требует не только высокой квалификации хирургов, но и технической оснащенности.
В хирургии налажены методики не только коронарного стентирования (сосудов сердца), но и установка стентов в сонной артерии для устранения признаков ишемии мозга, в бедренной — для лечения атеросклеротических изменений ног, в брюшной аорте и подвздошной — при наличии выраженных признаков атеросклеротического поражения.
Что такое «стент», разновидности
Стент — это легкая сетчатая трубка, достаточно прочная, чтобы обеспечивать каркас артерии длительное время. Стенты изготавливаются из сплавов металла (чаще кобальта) в соответствии с высокими технологиями. Существует множество видов. Они отличаются по размерам, структуре сетки, характеру покрытия.
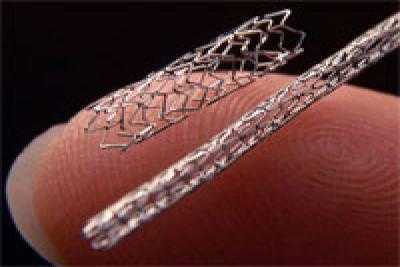
Стенты отличаются по размерам, структуре сетки, характеру покрытия
Можно выделить две группы стентов:
без покрытия — используются при операциях на артериях среднего размера;покрытые специальной оболочкой из полимера, выделяющей в течение года лекарственное вещество, препятствующее повторному стенозу артерии. Стоимость таких стентов значительно дороже. Они рекомендованы для установки в коронарных сосудах, требуют постоянного приема лекарств, снижающих образование тромбов.
Как проходит операция?
Для стентирования сосудов сердца в бедренную артерию вводится катетер, на конце которого располагается крошечный баллончик с надетым на него стентом. Под контролем рентгеновского аппарата катетер вводят в устье коронарных артерий и перемещают к необходимому участку сужения. Затем баллончик раздувается до необходимого диаметра. При этом атеросклеротические отложения вдавливаются в стенку. Стент, как пружина расширяется и оставляется на месте после сдувания баллона и удаления катетера. В результате — кровоток восстановлен.
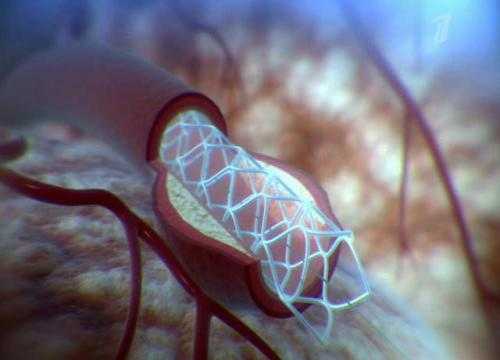
Схема расположения стента внутри сосуда
Операция обычно проводится под местной анестезией. Длится от одного до трех часов. Перед операцией пациенту вводятся препараты, разжижающие кровь для профилактики тромбоза. При необходимости устанавливают несколько стентов.
После хирургического вмешательства больной проводит в стационаре до семи дней под наблюдением вра
сколько живут после операции, инвалидность, видео
Под стентированием сердцем подразумевается расширение ссуженной или забитой артерии (коронарной). Во время операции используется специальный стент и баллон, прикрепляющихся к катетеру. Метод широко применяется для лечения пациентов, имеющих в своем анамнезе стенокардию, ишемическую болезнь сердца, инфаркт миокарда.
Очень часто пациенты задаются вопросом: сколько живут после стентирования сердца? Процедура является малоинвазивной. При соблюдении всех рекомендаций доктора процент выживаемости составляет 95%.
Показания к проведению стентирования
Для стентирования сосудов сердца в бедренную артерию вводится катетер, на конце которого располагается крошечный баллончик с надетым на него стентом. Под контролем рентгеновского аппарата катетер вводят в устье коронарных артерий и перемещают к необходимому участку сужения. Затем баллончик раздувается до необходимого диаметра.
При этом атеросклеротические отложения вдавливаются в стенку. Стент, как пружина расширяется и оставляется на месте после сдувания баллона и удаления катетера. В результате — кровоток восстановлен.
Стентирование артерий сердца, на сегодняшний день является альтернативным методом лечения операции аортокоронарного шунтирования.
Кроме того, если во время баллонной ангиопластики происходит спазм коронарных артерий, что может привести к развитию инфаркта миокарда, стентирование в данной ситуации помогает избежать этих осложнений. Обязательным условием перед операцией является проведение ЭКГ. Ознакомиться с нормами ЭКГ можно здесь «Расшифровка норм показателей эхокардиографии сердца «.
Кроме того через десять лет, после операции аортокоронарного шунтирования, примерно у 50% больных происходит стенозирование шунта. Стентирование шунта, так же является альтернативой, повторной операции аортокоронарного шунтирования.
Показания для операции:
- тяжелые частые приступы стенокардии, определяемые кардиологом как предынфарктное состояние;
- поддержка аортокоронарного шунта (шунтирование — это установка искусственного кровотока в обход перекрытого сосуда), который имеет тенденцию к сужению в течение десяти лет;
- по жизненным показаниям при тяжелом трансмуральном инфаркте.
Противопоказания
Противопоказанием для установки стента является диффузное стенозирование коронарного русла, то есть, нет объекта для установки стента, коим является, локальный стеноз. Кроме того малый диаметр стенозированной артерии, это порядка менее 2,8-3,0 мм, также является техническим препятствием, для установки стента.
Невозможность введения стента определяется во время обследования. При наличии следующих патологий операция тоже противопоказана:
- Распространенное поражение всех коронарных артерий, из-за которого отсутствует конкретное место для стентирования.
- Диаметр суженной артерии меньше трех мм.
- Сниженная свертываемость крови.
- Нарушение функции почек, печени, дыхательная недостаточность.
- Аллергическая реакция пациента на йодистые препараты.
Важно! Для профилактики тромбоза стентирование проводят на фоне антикоагулянтной терапии. Антикоагулянты это вещества, которые препятствуют тромбообразованию.
Эффективность операции, последствия
Преимущество стентирования перед другими операциями:
- малая травматичность методики — нет необходимости вскрывать грудную клетку;
- короткий период нахождения пациента в стационаре;
- сравнительно низкая стоимость;
- быстрое восстановление, возвращение к трудовой деятельности, отсутствие длительной инвалидизации больного.
Важно! Более 90% операций по стентированию сосудов сердца приводят к облегчению проявлений стенокардии.
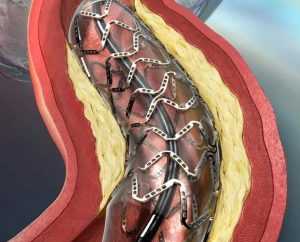
Однако ангиопластика показана не всем пациентам страдающим стенокардией, перед требуется профессиональная кардиодиагностика: операция не рекомендуется пациентам, перенесшим инсульт менее месяца назад, а также страдающим нарушениями свертываемости крови, тяжелой почечной недостаточностью и другими тяжелыми сопутствующими болезнями.
После стентирования стент в кровеносном сосуде постепенно обрастает новой тканью. Формируется такая ткань из эндотелия – слизистой оболочки стенок артерии. Дополнительные ткани выравнивают стенки стента, позволяя установить плавный кровоток в стентированной области.
Возможное усложнение после стентирования сосудов – рестеноз. Под здоровой оболочкой стента нарастание рубцовой ткани продолжается до повторного затруднения кровотока. Формируется такое осложнение в 25% случаев после стентирования, обычно в течение 3-6 месяцев.
Новое поколение стентов с лекарственным полимерным покрытием, препятствующим росту рубцовых тканей в артериях, существенно снижает риск рестеноза.
В целях профилактики после стентирования сосудов назначается постоянный прием антитромботических препаратов, таких как аспирин. При аллергии на ацетилсалициловую кислоту необходимо использовать альтернативные лекарственные средства.
Реабилитация
Перенесенное стентирование сосудов сердца позволяет намного улучшить самочувствие пациента, но это не останавливает атеросклеротический процесс, не изменяет нарушенный жировой обмен. Поэтому больному придется выполнять назначения врача, следить за уровнем холестерина и сахара крови.
В течение первой недели реабилитация связана с ограничением физической активности, противопоказаны ванны (только гигиенический душ). Два месяца врачи не рекомендуют управлять автомобилем. Дальнейшие советы сводятся к противохолестериновой диете, дозированной физкультуре, постоянному приему лекарств.
Лучше, если реабилитация после стентирования будет проводиться в санаторно-курортных условиях, под наблюдением медиков. Ведь некоторое время после операции сохраняется риск повышения артериального давления. О правилах первой помощи при гипертонии описывается в статье «Первая помощь при гипертоническом кризе«.
Операция стентирования проводится уже около сорока лет. Методика и техническое сопровождение постоянно усовершенствуются. Расширяются показания, нет возрастных ограничений. Рекомендуется всем пациентам с ишемической болезнью сердца не бояться консультации хирурга, это возможность продлить активную жизнь.
Правила, рекомендации после операции, диета
Придется исключить из питания животные жиры и ограничить углеводы. Не рекомендуется употреблять в пищу:
- жирную свинину, говядину, баранину;
- сливочное масло, сало;
- майонез и острые приправы;
- колбасные изделия;
- сыр;
- икру;
- макароны из нетвердых сортов пшеницы;
- шоколад, сладости и выпечку;
- белый хлеб;
- кофе, крепкий чай, алкоголь и пиво, газированные сладкие напитки.
Диета требует обязательно ввести в рацион овощи и фрукты в салатах или свежих соках, отварное мясо птицы, рыбу, каши, макаронные изделия из твердых сортов, творог, кисломолочные продукты, зеленый чай. Необходимо наладить 5 – 6 разовое питание, следить за весом.
Стоит знать! При необходимости следует проводить разгрузочные дни.
Итак, основные принципы диетического питания следующие:
- Потребляемые продукты должны содержать минимальное количество жиров. Пищу, в составе которой присутствуют животные жиры, необходимо исключить из рациона полностью.
- Следует значительно сократить количество соли, которая используется для приготовления блюд — не более 5 г в сутки.
- Рацион должен быть обогащен фруктами, овощами, ягодами.
- Полезно питаться несколько раз в день дробным способом, потребляя еду небольшими порциями.
- Готовить блюда желательно на пару или в духовке, от жареного необходимо отказаться.
- В меню должны преобладать продукты, богатые полиненасыщенными кислотами.
- Есть перед сном не рекомендуется, ужин необходимо употреблять за 3 часа до отдыха.
Важно! Оптимальное количество калорий в сутки — не более 2300 Кал.
Ежедневная утренняя гимнастика повышает обмен веществ, улучшает настроение. Нельзя сразу браться за тяжелые упражнения. Рекомендована ходьба, сначала на небольшие расстояния, затем с увеличением дистанции. Популярна медленная ходьба по лестнице. Можно заниматься на тренажерах.
Обязательно пациентам следует научиться считать у себя пульс. Не допускать значительной перегрузки с учащением сердечных сокращений. Из видов спорта рекомендовано катание на велосипеде и посещение бассейна.
Лекарственная терапия сводится к средствам, понижающим артериальное давление (у гипертоников), статинам для нормализации уровня холестерина и препаратам, снижающим тромбообразование.
Стоит знать! Больным с сахарным диабетом следует продолжить специфическое лечение по назначению эндокринолога.
Прогноз после операции
В 90% случаев стентирование сосудов сердца приводит к полной нормализации кровотока к сердцу и стойкому улучшению состояния больных.
У 10% пациентов, которым была проведена операция, возникают различные осложнения, такие как кровотечение, образование гематомы и отека в области прокола бедренной артерии, прободение стенки артерии, закупорка стента, нарушения работы почек.
Такие последствия хирургического лечения устраняются при условии своевременного обращения пациентов к врачу . В единичных ситуациях требуется повторное проведение стентирования сосудов сердца.
Возможные осложнения после операции
После манипуляции больной остается в стационаре до недели, но при отсутствии осложнений и хорошем общем состоянии может быть выписан намного раньше. Сроки варьируются в зависимости от личных особенностей каждого пациента.
Также больной должен внимательно следить за любыми отклонениями в своем состоянии, к которым может относиться:
- появление красноты, отека в том месте, где произошло введение катетера;
- открытие кровотечения из места введения катетера;
- гнойные выделения из места введения катетера;
- развитие синдрома общей интоксикации, к которому относят жар, головную боль, слабость, ломоту в костях и другие признаки инфицирования;
- избыточное выделение пота; потеря чувствительности или неполный объем движений в той конечности, через которую вводили катетер;
- рвота и тошнота, беспокоящие несколько дней подряд;
- сильный кашлевой рефлекс, появление болей в области сердца, отдышка;
- появление кровянистых выделений в моче – гематурия;
- боли при опорожнении мочевого пузыря или слишком частые позывы к опорожнению.
Важно! Если пациента начал беспокоить один из этих симптомов или несколько сразу, ему рекомендуется не медлить и обращаться к врачу, чтобы предотвратить риск развития более серьезных осложнений.
Осложнения
Стентирование, как и любое вмешательство, может приводить к развитию ряда осложнений. Самыми частыми являются:
- сильные кровотечения из бедренной артерии;
- появление аритмий;
- аллергии на контраст или покрытие стента;
- развитие инсульта;
- развитие повторного стеноза или рестеноза.
Что касается инсульта, его начало может протекать незаметно для больного. Это касается и состояния, которое называется микроинсульт. Переносить на ногах такое осложнение категорически нельзя. Ведь даже микроинсульт может привести к летальному исходу. Более подробно об осложнении можно узнать из статьи «Чем опасен перенесенный на ногах микроинсульт?«
Вазоспазмы – это обратимый процесс сужения артерий из-за сокращения клеток. Появляться такие спазмы могут или во время ангиопластики, или в течение нескольких часов после стентирования. Для профилактики вазоспазмов используют специальные препараты во время операции, при возникновении обычно бывает достаточно извлечь из артерий все медицинские инструменты.
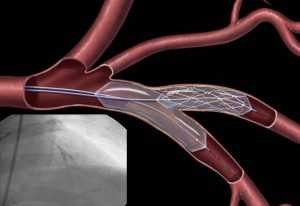 Рестеноз – это естественное осложнение, от которого не застрахован ни один прошедший коронарную ангиопластику пациент (диагностируют у 15-20% людей). Повторное появление бляшек, в том числе на самих имплантах, можно предотвратить только благодаря постоянным наблюдениям у специалиста.
Рестеноз – это естественное осложнение, от которого не застрахован ни один прошедший коронарную ангиопластику пациент (диагностируют у 15-20% людей). Повторное появление бляшек, в том числе на самих имплантах, можно предотвратить только благодаря постоянным наблюдениям у специалиста.
В случае рецидива врач сможет распознать рестеноз на ранней стадии и снова рекомендовать операцию.
Одно из самых опасных и серьезных последствий после коронарной ангиопластики – это тромбоз. Возникнуть он может в любое время и при отсутствии контроля врачей и лечения способен спровоцировать инфаркт.
Важно! Самый высокий риск осложнений после коронарного стентирования – у диабетиков, лиц с нарушенной работой почек и свертываемостью крови. Таким пациентам необходимы более тщательное обследование перед процедурой, более строгий контроль во время и после операции.
Прогнозы
Прогноз ожидаемой длительности жизни после стентирования зависит не столько от самой операции, сколько от заболевания, по поводу которого она проводилась, и от степени поражения сердечной мышцы (то есть от сократительной функции левого желудочка).
Но проведенные научные исследования обнаружили, что после стентирования в течение одного года живыми остаются 95% пациентов, трех лет – 91%, пяти лет – 86%.
Тридцатидневная смертность при инфаркте миокарда зависит от метода лечения:
- консервативная терапия – смертность 13%;
- фибринолитическая терапия – смертность 6–7%;
- стентирование – смертность 3–5%.
Прогноз у каждого конкретного пациента зависит от его возраста, наличия других заболеваний (сахарный диабет), степени поражения миокарда. Для его определения существуют различные шкалы, из которых наиболее широко распространена шкала TIMI.
Общепризнанным является факт, что раннее проведение стентирования улучшает прогноз при инфаркте миокарда.
Отзывы
Большинство отзывов о результатах стентирования позитивные, вероятность неблагоприятных последствий после проведения минимальна и само хирургическое вмешательство считается безопасным. В определенных ситуациях есть вероятность возникновения аллергии организма на вещество, вводимое при операции для рентгеновского наблюдения.
Пациенты, которые подверглись хирургическому вмешательству, характеризуют ее схожесть с достаточно простой медицинской процедурой, а не операцией. Так как нет надобности в продолжительном восстановительном периоде, больные считают, что совсем поправились.
Наталья:
Мне сделали коронографию и стентирование, пью таблетки Плагрил и ещё кучу, вроде бы лучше стало, но по вечерам сердце даёт о себе знать.
Константин:
Мне поставили один стент. Чувствую себя хорошо прошло 10 дней выполняю все, что рекомендовали.
Наташа:
Во время инфаркта сделали стентирование передней нисходящей артерии через запястие правой руки теперь очень сильно ломит руку прошло два месяца после операции.
Важно! Не следует забывать, что при идеальной методике кардиохирургии не отменяется необходимость надлежащим образом заботиться о своем здоровье.
| Здравствуйте,Эдуард Романович!Моему мужу делали стентирование сердца (4 стента) прощло неделя у него температура 37.7 поднялась и изредко кашель,раз в час или 2часа.Что это может быть что вы советуете. Попробуйте заменить БРИЛИНТОЙ. Работать начали не рано. Средство для “чистки сосудов” никуда не годится. И зачем Вам алкоголь. Я исхожу из того, что алкоголь – это яд и ни в каких количествах он полезным быть не может. Дурную привычку к алкоголю понять могу, но делать вид, что это полезно – это фарисейство. И НЕБИВАЛ, и АМПРИЛ понижают давление. Может быть стоит уменьшить дозы? Разумеется, что все лечение надо проводить пол контролем своего лечащего врача. КЛОПИДОГРЕЛ пока принимать надо. В сочетании с КАРДИОМАГНИЛОМ он дает некоторую защиту от ишемического инсульта (для этого и принимают антикоагулянты при мерцательной аритмии). Но эта защита слабее, чем при приеме антикоагулянтов. Если ПРАДАКСА вызывает такие симптомы, то наверное есть смысл от неё отказаться. Любой из перечисленных Вами препаратов её вполне заменит. Дозировки лучше согласовывать с лечащим врачом. Здравствуйте, уважаемый Эдуард Романович. Помогите, пожалуйста! Мне 24 года, резко началась необоснованная ничем гипертония, после КТ с контрастом показало сужение правой почечной артерии на 80%. Хотя до этого было УЗИ почечных артерий и стеноз не показало! Предлагают ставить стент, либо делать шунтирование. Говорят что артерия уходит в бок, и при постановке стента могут возникнуть проблемы. Обещают вариант 50 на 50, или поставим, или нет. Но если нет, потеряете деньги. А операция стоит денег не малых.. Я просто в шоке! Как дальше жить со стентом? Я ещё не рожавшая. Мы с мужем очень хотим ребеночка. Сможет ли стент сместится при беременности или родах? Или при любой физ.нагрузке? Неужели без операции мой молодой организм не справится? Возможно попробовать действительно гирудотерапию, либо игловкалывание? Очень боюсь операции и каких-либо осложнений, возраст всётаки молодой.. верю в то, что организм сам справится? Или я это зря, уважаемый доктор? К сожалению давление держится 150 на 100, мрт уже показало первичную энцефалапотию и очень высокое глазное давление, как следствие давления.. Очень надеюсь получить Ваш ответ, который возможно, поможет мне решится на что-то в ближайшем будущем. Добрый день, уважаемая Ксения! Это очень серьезно. Мне надо подумать и посоветоваться. Отвечу завтра. В Вашем возрасте чаще всего приходится думать о фибро-мускулярнной дисплазии, при которой наступает сужение почечной артерии, обычно в среднем её отделе. Вазоренальная гипертензия при стенозе почечных артерий развивается поэтапно. В стадии компенсации наблюдается умеренная степень артериальной гипертонии, коррегируемая медикаментами; функция почек остается не нарушенной. Обычные гипотензивные лекарства могут надежно контролировать давление у многих больных с рено-васкулярной гипертонией. Нет клинических признаков, по которым можно надежно прогнозировать, будет толк от стентирования или нет. В случае успеха, однако, стент может помочь настолько , что потребность в лекарствах вообще исчезнет. Опасности в отношении предстоящей беременности стент не представляет, почечные артерии проходят забрюшинно и увеличение матки на положении стента не скажется. Уважаемый Эдуард Романович, добрый день! Спасибо Вам большое за Ваш ответ и помощь! Врачи мне предлагают выбирать самой между стентированием и шунтированием пораженной артерии. Как Вы думаете, возможно лучше сразу сделать шунтирование? Клинически доказан успех в данном виде операции? Хирург у которого я была на консультации сказал мне так: «Стентирование это 50 на 50, шунтирование это 90% успеха. Думайте, определяйтесь..» Возможно мне нужно ещё обратиться к оперирующему урологу? Стентирование сердца: основные понятия, методика операции, прогноз и образ жизниИнфаркт миокарда – настоящая пандемия 21 века. Если раньше от инфаркта погибали преимущественно лица пожилого возраста, то сейчас имеется тенденция к «омоложению» данной патологии сердца. Основная причина инфарктов – атеросклеротическое поражение сосудов сердца, питающих сердечную мышцу. Такое повсеместное распространение заболевания привело к тому, что учёные и врачи всего мира ищут всё новые и новые способы борьбы с патологией. Один из методов, позволяющих снизить смертность от инфаркта миокарда и улучшить прогноз жизни, является операция стентирования сосудов сердца. Что такое стентирование сердцаАтеросклеротическая бляшка растёт из мышечной стенки кровеносного сосуда внутрь его просвета. Этот долгий процесс длится на протяжении нескольких лет, поэтому по началу нарушения кровотока не наблюдается. Состояние гипоксии (недостатка кислорода) поначалу компенсируется, и человек даже не подозревает, что болен. Срыв компенсаторных возможностей происходит после того, как бляшка перекрыла более 50% просвета сосудов, а кровоток в органе снизился более чем в 2 раза. С этого момента в органе начинают развиваться необратимые органические изменения. Острая гипоксия приводит к некрозу (гибели) того участка органа, который снабжал кровью поражённый сосуд. Если данный процесс развивался в сердечной мышце, то буквально через пару часов наступает инфаркт миокарда. Операция стентирования – это разновидность хирургического вмешательства, в ходе которого в сосуд, поражённый атеросклерозом, вводится специальный стент. При этом атеросклеротическая бляшка, которая закрывала просвет сосуда и мешала нормальному току крови, «прижимается» к стенкам сосуда, а сам сосуд расправляется, что в конечном итоге приводит к расширению его просвета. Нормализация кровотока предотвращает острую гипоксию, а значит, инфаркт мышечной ткани далее не развивается. Таким образом, операция стентирования улучшает прогноз заболевания, снижает летальность от заболеваний сердца.
Стентирование – сложная для выполнения операция, требующая от хирургов высокого профессионализма. Её проводят в специальной операционной сосудистого профиля, которая оснащена рентгеновской техникой. Стенты устанавливают не только в коронарные артерии сердца. Разработаны методики операции по стентированию артерий головного мозга, бедра, малого таза, подколенных артерий, брюшной аорты. Что такое стентУстановка стента – ключевой момент в стентировании. Стент – это специальная металлическая сетчатая конструкция трубчатого вида. Производятся эти конструкции из инертных металлов, способных поддерживать сосуд в расправленном виде долгое время. Инертные материалы – наиболее безвредные для человеческого организма. Кроме того, они меньше всего вызывают антигенную активность иммунной системы. Чтобы иммунная система человека распознала сетки, как «свои» ткани, они покрываются специальными растворами и материалами. Существует множество разновидностей стентов. Они отличаются по составу материала, из которого изготавливается сама сетка, по диаметру, по строению сетчатой структуры. Поэтому сетка подбирается врачом индивидуально для каждого пациента в отдельности. Как правило, стент перед операцией пациент покупает самостоятельно. Диаметр и материал нужного изделия посоветует вам врач, а вот структуру вы можете выбрать самостоятельно. Как правило, выбор встаёт между двумя видами:
Техника проведения операции стентированияПеред операцией стентирования больному дают препараты разжижающие кровь, после чего делают местную анестезию. В специальной операционной под контролем рентгенэндоваскулярной техники в бедренную артерию вводится катетер. На конце катетера имеется баллончик, на который нанизан установочный стент. После того, как хирург убедился, что катетер находится внутри бедренной артерии, его начинают продвигать вверх по направлению к коронарным артериям. Как только катетер достиг поражённого участка коронарного сосуда, под контролем техники баллончик раздувают так, чтобы атеросклеротическая бляшка вместе со стентом вдавилась и «прижалась» к стенкам артерии. После того, как просвет сосуда расширили, и кровоток восстановился, баллончик сдувают, при этом сетка остаётся «вжатой» в кровеносную стенку, поддерживая каркас артерии. Если поражены сразу несколько коронарных сосудов, устанавливают несколько сеток. Под контролем врача после операции больной находится ещё не менее 7 дней. Больному назначается антикоагулянтная и тромболитическая терапия, первые часы для улучшения прогноза рекомендуется постельный режим. Показания к стентированию сердцаОперацию проводят в плановом и экстренном порядке. В плановом порядке отбор нуждающихся пациентов проводит врач-кардиолог (при отсутствии терапевт) в поликлинике по месту жительства. Показаниями к стентированию являются: Прогрессирующая стенокардия напряжения с тяжёлыми приступами загрудинных болей, с ишемическими изменениями на электрокардиограмме. Попросту говоря, если состояние пациента расценивается как прединфарктное. Пациенты с аортокоронарным шунтированием в анамнезе для поддержания состояния шунтированного кровотока или при повторном тромбозе шунта. Если стентирование проводится в плановом порядке, больной перед операцией должен пройти ряд исследований:
В экстренном порядке операцию стентирования сердца проводят пациентам с тяжёлым инфарктом миокарда и пациентам с острым коронарным синдромом в целях улучшения прогноза для жизни. Противопоказания к операцииНе всем пациентам показано стентирование. Среди противопоказаний следующие состояния:
Прогноз жизни для пациентовОперация стентирования сосудов сердца улучшает прогноз дальнейшей жизни пациентов в десятки раз. Расширение артерий приводит к нормализации и восстановлению кровотока в ишемизированном участке миокарда, что снижает развитие инфаркта в дальнейшем. Новый инфаркт развивается только в случае поражения другой артерии. Стентирование — одна из наиболее безопасных операций на сердце, которая спасла жизни тысячам пациентов. Осложнения встречаются в исключительных случаях, среди них:
Прогноз и послеоперационное восстановлениеОперация – это лишь симптоматическое лечение, помогающее локально решить проблему. Она не останавливает дальнейшее прогрессирование и развитие атеросклеротических бляшек в организме. Прогноз для жизни полностью зависит от самого пациента. Все рекомендации врача сводятся к формированию здорового образа жизни, нормализации питания и восстановлению нормального обмена веществ. Первая неделя после операцииПервые 2-3 дня пациенту рекомендован постельный режим, который затем сменяется полу постельным. Однако это не значит, что больной должен быть полностью прикован к постели. Лёжа в кровати необходимо проводить лечебную физкультуру, направленную на поддержание мышечного тонуса мелких мышечных единиц. Регулярно делайте сжимание и разжимание кисти, сгибание и разгибание локтей, коленей, приведение и отведение бедра в сторону. Первый месяц после операцииПосле выписки для улучшения прогноза рекомендуется ограничение тяжёлых физических нагрузок и изнуряющего труда. В этот период проводите лёгкие физические зарядки по утрам на субмаксимальных нагрузках на сердце (пульс до 120-130 уд. в мин.). Первый месяц откажитесь от походов в баню, сауны, бассейн. Автомобильные поездки за рулём замените прогулками на свежем воздухе неспешным шагом. Принимайте выписанные врачом лекарственные препараты и скорректируйте рацион питания.
Важное видео: Самые современные способы стентирования сосудов сердцаСтентирование сосудов сердца: сколько живут после операции, отзывы
Процесс точечного малоинвазивного воздействия, во время которого хирургом проводится расширение суженных и закупоренных участков сосудов с установкой сосудистого стента, получил название стентирование. Операция носит эндоваскулярный или внутрисосудистый характер. Обработке подлежат сосуды и артерии, отвечающие за снабжение сердца кровью. Вмешательство проводится хирургом узкой специализации – сосудистый или эндоваскулярный. Описание проводимой операцииОснованием для назначения малоинвазивного вмешательства станет атеросклероз. Его симптом – формирование холестериновых бляшек, сужающих просвет сосудов. Оперативное врачебное вмешательство снижает вероятность появления ишемической болезни сердца и инфаркта. Суть стентирования – установка расширителей в тех местах, где коронарная артерия патологически сужена. В случае успешного завершения операционного вмешательства, удается восстановить нормальный уровень кровоснабжения. Ошибочно думать, что стентирование устраняет проблему. На самом деле, речь идет лишь о временном облегчении. Впоследствии пациент нуждается в комплексном лечении. Перед началом операции доктор расскажет обо всех ее особенностях:
Во время операции пациенту вводят специальное вещество – рентгеновский контраст. Он наполняет сосуды, облегчая хирургу работу. Особенности послеоперационного периодаСпустя 72 часа после успешного завершения малоинвазивного вмешательства пациент соблюдает постельный режим. Если побочных эффектов не зафиксировано, то через 5 суток максимум гражданина выписывают. Пациент получает список обязательных рекомендаций, соблюдение которых ускоряет восстановительный процесс. Соблюдение диетыИз меню сразу исключается все жирное, соленое и пряное. Не стоит даже брать в руки продукты, содержащие легкоусвояемые углеводы. Еда с повышенным уровнем холестерина должна быть исключена из рациона. Упор делается на перечисленные ниже продукты:
Последний пункт имеет большое значение. Упомянутое вещество в несколько раз замедляет распространение атеросклероза. Нормированные физические нагрузкиВ течение первых 7 суток после операции любая физическая активность запрещена. Разрешаются лишь непродолжительные прогулки по ровной дорожке. После стентированияОбеспечение здорового образа жизниВрач сразу скажет о необходимости сформировать четкий режим дня. Сон, прием пищи, занятия спортом – все происходит с точностью до минуты изо дня в день. Стабильность и постоянство – 2 фактора, обеспечивающих быстрое восстановление. Резких изменений быть не должно, иначе многократно повышается вероятность развития стрессовой ситуации. После согласования с медиком, целесообразно выполнять регулярные анаэробные упражнения:
Стабилизация состояния здоровья при помощи медикаментовПодбором препаратов, и определением дозировки занимается только врач. Внимание уделяется бета-блокаторам и нитратам. Принимаются они только при наличии учащенного сердцебиения или ярко выраженных болей в области груди. Пожизненно пациент принимает перечисленные ниже вещества:
В обязательном порядке пациент сдает анализ на свертываемость крови, ЭКГ, тест на определение липидного спектра крови и коронарографию. Периодичность определяется медиком. При соблюдении всех рекомендаций медика продолжительность жизни составляет не менее 10-15 лет. Важно постоянно следить за состоянием здоровья и отказаться от вредных привычек. Перечисленные факторы способствуют увеличению продолжительности жизни. Порядок оформления инвалидностиВопрос регулируется Федеральным законодательством. После сдачи анализов и прохождения обследования, заполняется медицинская карта. Если указанные в ней данные отвечают критериям той или иной группы инвалидности, то таковая присваивается. Пациенту достаточно оформить соответствующее заявление, приложив к нему результаты проведенного обследования. В лечебном учреждении расскажут гражданину, что через определенное время придется пройти переосвидетельствование. Суть процедуры – оценить эффективность назначенного реабилитационного курса. Отзывы пациентов после операцииНа фоне наследственной предрасположенности, прошла детальное обследование. Результаты подтвердили необходимость операции. При местном наркозе все сделали за 2 часа. Теперь придерживаюсь диеты. Минимальные психические и физические нагрузки. Несмотря на необходимость изменить образ жизни, достигнутый результат того стоил. Перенес инфаркт. Врачи сказали что нужно провести стентирование. После завершения операции пришлось сменить работу. Необходимо было избавиться даже от малейшей вероятности возникновения стрессовой ситуации. Прошло уже 8 лет. Никаких проблем не возникает. Главное – регулярно принимать назначенные медикаменты. Стентирование сосудов сердца – малоинвазивная процедура, во время которой происходит локальное расширение закупоренного сосуда. Практически сразу достигается выраженный терапевтический временный эффект. Проблема лишь на время теряется из виду, поэтому нужно продолжить терапевтический курс. После завершения операционного вмешательства человек меняет привычный образ жизни и рацион. Обязательно принимаются лекарства, назначенные для стабилизации состояния здоровья. Что такое стентирование сосудов и какая реабилитация необходима после операцииСтентирование сосудов сердца — распространённая операция, которая проводится при многих патологиях. Нередко такое лечение является единственным вариантом, который может спасти человеку жизнь. После операции требуется особая реабилитация, которая позволяет закрепить результат, избавить пациента от осложнений и сократить время, необходимое для выздоровления. Особенности хирургического вмешательстваСтентирование сосудов сердца позволяет расширить коронарные артерии, которые не могут нормально функционировать из-за наличия тромба, и привести в норму нарушенный кровоток. Суть операции заключается во введении в артерию стента, который является особым протезом для стенки поражённого сосуда. По сути, это трубочка со стенками в виде мелкой сетки. Стент располагается в месте сужения артерии. Изначально он имеет сложенный вид. На месте поражения артерии стент раздувается и фиксируется, поддерживая таким образом сосуд в нормальном состоянии. Хоть подобная операция и является малоинвазивным вмешательством, но всё же стенки сосуда находятся в воспалённом состоянии. Для ускорения заживления сосуда, улучшения результатов операции и их закрепления необходимо проходить особую реабилитационную программу. Мы об этом обязательно поговорим, но для начала разберёмся ещё с некоторыми важными вопросами касательно коронарного стентирования. Виды стентовВ мире выделяют около сотни разновидностей стентов. Только опытный кардиохирург может из этого ассортимента выбрать единственный экземпляр, который будет точно подходить под конкретный случай. В любом случае, он должен быть очень качественным и надёжным, ведь стент устанавливается на длительное время и выполняет важную функцию. Современные стенты обладают рядом характеристик и отличительных свойств:
Показания к проведению операции стентированияУстановка стента на артерии сердца имеет ряд показаний. В каждом отдельном случае врач оценивает необходимость проведения такой операции и назначает только тогда, когда другие методы лечения без оперативного вмешательства оказываются безрезультатными. Основные показания к проведению стентирования изложены ниже:
Противопоказания для операцииДалеко не во всех случаях может проводиться стентирование сосудов сердца. Имеется ряд противопоказаний, которые делают проведение этой операции невозможной:
Некоторые противопоказания носят временный характер, могут быть устранены на время или навсегда. Также есть относительные противопоказания, которые могут не учитываться, если человек сам настаивает на операции и при этом риски осложнений невелики. Аллергия на йодосодержащие препараты сюда не относится. Как проходит оперативное вмешательствоСтентирование коронарных сосудов не является особо сложной и длительной операцией. Но всё равно она требует проведения особой подготовки и выполняется по чёткому плану. Предоперационная подготовкаХоть коронарное стентирование и не требует проведения сложной подготовки, но всё же некоторые процедуры придётся сделать. В этом случае предоперационная подготовка сводится в следующему:
Если ситуация не критическая, а операция плановая, то человек проходит комплексное обследование. Оперативное вмешательство часто проводится при экстренных случаях, когда дорога каждая минута. Например, в случае с инфарктом, после начала которого прошло более 5 часов, операцию начинают без результатов анализов. Бригада врачей постоянно следит за тем, как себя ведёт больной, и вносит изменения по ходу проведения стентирования сосудов сердца. Процедура операцииОперация стентирования сосудов сердца выполняется в операционных, в условиях абсолютной стерильности. Также в распоряжении хирургов должно быть точное современное оборудование, которое обеспечит постоянный контроль состояния больного и позволит мониторить ход операции. Операция выполняется по следующему плану, который может меняться в зависимости от конкретной ситуации:
Возможные осложненияВероятность развития ранних осложнений после операции, а также во время её проведения составляет не более 5%. К таким ситуациям относятся следующие состояния:
Жизнь после стентирования сосудов сердцаПосле стентирования сосудов сердца обязателен реабилитационный период. Важно придерживаться всех правил. В этом случае можно снизить вероятность развития осложнений, которые могут возникать после стентирования сосудов сердца. Первые сутки после операции соблюдается постельный режим. При хорошем состоянии больного и отсутствии осложнений на 3 день уже может быть оформлена выписка домой. Сколько живут после операции стентирования, сказать сложно. Очень многое зависит от соблюдения человеком принципов реабилитации. Захочет ли он менять свою жизнь, беречь сердце и сосуды, правильно питаться, не нервничать и нормировать нагрузки. Именно об этом мы и будем сейчас говорить. Строгая диетаКаждый человек обязательно должен придерживаться особого питания после стентирования сосудов сердца. Таким образом можно снизить вероятность образования тромбов и прочих осложнений. Суть диеты заключается в следующем:
Щадящий режим нагрузокФизические нагрузки после стентирования сосудов сердца противопоказаны на протяжении первой недели после операции. Допустима только ходьба по ровной местности. Дальше физические нагрузки добавляются постепенно. Необходимо выработать такой график добавления нагрузки, чтобы максимум через 6 недель вернуться к привычному образу жизни. Желательно заниматься лечебной физкультурой и выполнять комплекс специальных упражнений. Каждый человек должен не только знать, как вести себя после стентирования сосудов сердца, но и чётко придерживаться этих правил. При этом ночная работа и тяжёлый труд, а также сильные нервные потрясения противопоказаны на всё время жизни. Обязательный приём медикаментов и обследованияНекоторое время после операции за состоянием организма нужно наблюдать. Для этого назначаются определённые методы диагностики.
Если врач назначил все эти исследования или одно из них, необходимо без промедления проходить диагностику. Это позволит выявить развитие осложнений ещё на этапе их зарождения и оперативно устранить. Также в период после стентирования требуется приём лекарств, которые будут выписаны специалистом. Нужно помнить, что хоть работа артерии и была восстановлена, но причина, которая привела к таким последствиям, осталась. В некоторых случаях приём медикаментов может продолжаться на протяжении года, хотя никто не исключает пожизненного лечения. Обычно назначаются следующие препараты: Стентирование сосудов сердца — необходимая операция, которая позволяет вернуть сосудам их работоспособность и восстановить кровоток. В некоторых случаях проведение такого оперативного вмешательства является единственным вариантом сохранить человеку жизнь. Но дальнейшее самочувствие и состояние здоровья зависит исключительно от самого человека. Можно вернуться к нормальному образу жизни, а можно свести на нет все усилия врачей. Оценка статьи: Загрузка... Сохранить себе в: Сколько живут после стентирования сосудов сердца Ссылка на основную публикацию wpDiscuzAdblockdetector |
Осложнения после стентирования сосудов сердца
Осложнения после стентирования коронарных артерий
РИСК ОСЛОЖНЕНИЙ ПРИ ОПЕРАЦИИ СТЕНТИРОВАНИЯ
Сосудистые заболевания — ЛЕЧЕНИЕ за ГРАНИЦЕЙ – TreatmentAbroad.ru – 2007
Процесс установки стента контролируется с помощью рентгеновского монитора. Для уверенности закрепления стента на сосудистой стенке баллончик раздувается несколько раз.
Обычно, операция стентирования проводится под местной анестезией, хотя может проводиться и под общим наркозом. Стент устанавливают через бедренную артерию. Для этого в области паховой складки проводится небольшой разрез и отыскивается артерия. Далее, под контролем рентгена стент, закрепленный на конце особого баллонного катетера, вводится в артерию и подводится к месту сужения. После чего баллончик раздувается, расширяя просвет артерии, и стент вдавливается в ее стенку.
Возможные осложнения при стентировании
Чаще всего к ним относится образование тромба в области стентирования. Поэтому всем больным после операции стентирования назначаются препараты, которые препятствуют тромбообразованию.
Реже встречаются другие осложнения, например, кровотечение, что приводит к образованию гематомы в паховой области. Это связано, в основном, с применением во время стентирования препаратов, снижающих свертываемость крови. Иногда может быть инфицирование места введения катетера. Также наблюдается такое осложнение, как аллергическая реакция на рентгеноконтрастное вещество (то есть вещество, используемое для рентгеновского контроля во время операции).
Осложнения после стентирования сосудов сердца и коронарных артерий
Операции с установкой стентов считаются наиболее предпочтительным способом интервенционного хирургического лечения патологического сужения сосудов во многих случаях. Этот метод позволяет эффективно бороться с ишемической болезнью сердца и её последствиями, не прибегая к аортокоронарному шунтированию. Но и при выборе стентирования осложнения всё же возможны.
Какие осложнения могут быть после стентирования коронарных артерий и сосудов сердца
Осложнения после стентирования могут возникать как сразу после операции, так и в отдалённом периоде. Непосредственно после имплантации эндопротеза возможно развитие аллергических реакций на лекарственные препараты, используемые во время вмешательства или в течение дальнейших нескольких дней. Некоторые стенты имеют специальные покрытия, включающие в свой состав вещества, действие которых направлено на предотвращение повторного сужения сосуда. У предрасположенных к аллергиям пациентов возможна реакция на их выделение в кровь.
При проведении стентирования сосудов сердца осложнениями могут являться и повторное сужение просвета сосудов, и образование тромбов. Это наиболее часто встречающиеся осложнения, на борьбу и предупреждение которых направлено в настоящее время внимание учёных-медиков. Не исключаются и такие осложнения после стентирования как возникновение перфорации стенок сосуда, развития кровотечения и образования гематом на месте введения катетера или других участках пути прохождения баллона со стентом.
Как избежать осложнений после стентирования сосудов сердца и коронарных артерий
Наиболее склонны к возникновению осложнений после стентирования коронарных артерий пациенты, имеющие различные серьёзные хронические заболевания – патологии почек, сахарный диабет, различные нарушения кроветворительной и свёртывающей функций. К факторам, повышающим риск, можно отнести и пожилой возраст, неудовлетворительное общее состояние организма пациента на момент операции.
Чтобы предупредить развитие при стентировании коронарных артерий осложнений, связанных с вышеперечисленными причинами, ещё на этапе подготовки к операции проводится тщательное обследование состояния здоровья кандидата на проведение ангиопластики. Сюда входит не только оценка состояния сосудов, но и комплексное обследование с внимательным отношением ко всем жалобам пациента, учёт всех принимаемых им лекарственных средств и их возможных реакций с медикаментами, вводимыми во время и после операции.
Как выявить осложнения после стентирования сосудов на ранней стадии и что делать в случае их появления
На возникновение осложнений после стентирования коронарных артерий может указывать ухудшение общего состояния больного или длительное отсутствие какого-либо эффекта после проведённого вмешательства. При плохой переносимости медикаментов появляются симптомы интоксикации – тошнота, рвота, слабость, повышение температуры – всё в зависимости от интенсивности реакции. Данное состояние может быть скорректировано изменением тактики ведения больного, назначением других доз или замены действующих препаратов.
При развитии тромбоза, рестенозе с повторным сужением сосуда в месте установки стента или на других участках артерий может потребоваться повторное хирургическое вмешательство. Срочность проведения операции будет зависеть от текущего состояния больного.
Каждый пациент, страдающий ишемической болезнью сердца, испытывающий приступы стенокардии, должен проходить регулярное медицинское обследование. После проведения операции ангиопластики со стентированием заболевание, приведшее к осложнениям, не исчезает, и нуждается в дальнейшем наблюдении и лечении.
Стентирование сосудов сердца
Стентирование коронарных артерий это метод лечения форм ишемической болезни сердца (стенокардия, инфаркт миокарда), связанных с сужением или окклюзией (полным закрытием) артерий сердца.
Стент – специальная конструкция, устанавливаемая в просвет сосуда, в месте его стеноза (сужения), после его (стеноза) расширения специальным баллоном. Установка стента препятствует дальнейшему повторному возникновению стеноза.
Встречаются следующие виды стентов:
- Обычный металлический стент
- Стент с лекарственным покрытием
- Рассасывающиеся стенты
Вмешательство, при котором после раздувания баллона стент не устанавливается, называется ангиопластикой.
Коронарное стентирование. Показания.
Как и любое другое оперативное вмешательство, даже малоинвазивное, стентирование сосудов сердца имеет достаточно серьезные риски, поэтому показания к проведению данной процедуры должны сулить пользу, существенно превышающую риски. Это возможно в следующих ситуациях:
- Прогрессирующая стенокардия. Ситуация, когда пациент вынужден регулярно вызывать скорую помощь из-за частых и непрогнозируемых приступов стенокардии.
- Острый коронарный синдром или инфаркт миокарда в ранние сроки развития
- Ранняя постинфарктная стенокардия, ситуация, в которой приступы стенокардии повторяются на фоне лечения инфаркта миокарда.
- Стабильная стенокардия напряжения с низким качеством жизни на фоне адекватной медикаментозной терапии.
- Высокий риск сердечнососудистых катастроф и/или смерти, выявленный в результате неинвазивных методов обследования.
Безусловно, стентирование может быть проведено только при подтверждении технической возможности вмешательства на основании ранее проведенной коронарографии.
Стентирование и стабильная стенокардия напряжения
Как и было указано в показаниях к стентированию коронарных артерий, только при сохранении приступов стенокардии на фоне оптимальной медикаментозной терапии оно является поводом к вмешательству. К сожалению, как показывает практика, доля пациентов, получающих действительно оптимальную терапию, не так высок, как хотелось бы. Поэтому в такой ситуации перед принятием решения следует получить второе мнение о необходимости вмешательства.
Как проводится стентирование сосудов сердца.
Перед проведением стентирования пациент обследуется на предмет показаний к процедуре и оценке рисков. Объем обследований индивидуален и зависит от сопутствующих заболеваний и иных внешних и внутренних факторов. Безусловным и обязательным исследованием перед стентированием является коронарография. Вмешательство проводится натощак, т.е. следует исключить прием пищи за 8 часов до операции. Если пациент принимает варфарин или иные антикоагулянты, то следует обсудить с врачом, необходима ли отмена этих препаратов. Прием антиагрегантов (аспирин, плавикс) обычно не прекращают. Операция проводится в рентгеноперационной. Наркоза не требуется – обычно используются седативные (успокаивающе) средства. Под местной анестезией пунктируется бедренная (в паховой области) или лучевая (предплечье) артерия. В просвет артерии вводится проводник, похожий на тонкую проволоку, по которому проводится интродьюссер (специальное устройство, облегчающее работу врача при проведении в просвет сосуда необходимых инструментов) катетера с системой стент-баллон.
Стент устанавливается в месте стеноза, где после расширения специальным баллоном и устанавливается. Вся процедура проводится под рентгенологическим контролем. Процедура не сопровождается значительными болевыми ощущениями, возможен дискомфорт, как в месте пункции, так и в груди.
Осложнения стентирования артерий сердца
К сожалению, при проведении стентирования, как и любого другого оперативного вмешательства, возможны осложнения. Принято следующее условное деление этих осложнений: Интраоперационные осложнения, т.е. возникающие во время проведения операции:
- Нарушения ритма сердца
- Инфаркт миокарда
- Диссекция сосуда, т.е. отслойка внутренней оболочки артерии
- Приступ стенокардии
- В редких случаях возможен летальный исход.
Редко, но возможно такое развитие ситуации, когда от стентирования возможен переход к аорто-коронарному шунтированию.
- Нарушения ритма сердца
- Тромбоз стента, с возможным развитием инфаркта миокарда
- Гематома в месте пункции
- Истинная или ложная аневризма пунктированной артерии
Поздние послеоперационные осложнения
Медикаментозная терапия после стентирования сосудов сердца
После проведенного вмешательства в обязательном порядке назначаются препараты, снижающие риск тромбозов стента. Наиболее известный препарат этой группы – плавикс. Длительность приема препарата оговаривается отдельно и зависит от установленного стента:
- После перенесенного острого коронарного синдрома не менее 1 года
- При установке стента с лекарственным покрытием не менее 1 года
- При установке стента без лекарственного покрытия не менее 1 месяца
Следует учитывать, что практически все препараты, которые пациент принимал до вмешательства, так же обязательны к употреблению, возможна коррекция их дозировок. Особое внимание следует уделить уровню холестерина и приему статинов. Целевой уровень ЛПНП 1,8 ммоль и ниже.
- После операции не нужно пить лекарства, потому что наступает излечение. Крайне опасное заблуждение. После стентирования коронарных артерий, важность медикаментозной терапии возрастает многократно. Излечение не наступает, существенно улучшается качество жизни, возможно снижение рисков сердечнососудистых катастроф и сердечнососудистой смерти, если операция проведена по показаниям.
- После операции стоимость медикаментозного лечения снизится. Это не так. Стентирование является показанием к использованию плавикса, стоимость этого препарата на сегодняшний день достаточно существенна, поэтому снижения стоимости лечения не произойдет. Но, безусловно, улучшится трудоспособность пациента.
- После операции не будет никаких ограничений. Это не так, следует так же тщательно контролировать уровень артериального давления и лечить артериальную гипертензию (если она была ранее или появилась впервые), столь же тщательно необходимо следить за уровнем сахара и гликированного гемоглобина у пациентов с диабетом, все так же нельзя курить и необходимо следить за весом.
- Плавикс очень дорог, можно ли его заменить на зилт. Формально, зилт является дженериком плавикса, но следует знать, что исследований доказавших такую же как у плавикса эффективность зилта нет, поэтому замена возможна только на свой страх и риск. Мы не можем дать такую рекомендацию.
Осложнения после стентирования
В этом материале рассказывается о процедуре стентирования, о том, как проводится такое вмешательство и в каких случаях, а также о возможных последствиях и осложнениях.
Из статьи читатель узнает о том, что такое стентирование, какова продолжительность оперативного вмешательства, почему после него у пациентов может болеть сердце. Информация подана доступным языком и будет понятна широкому кругу читателей. Основной акцент сделан на том, какие могут быть осложнения после стентирования.
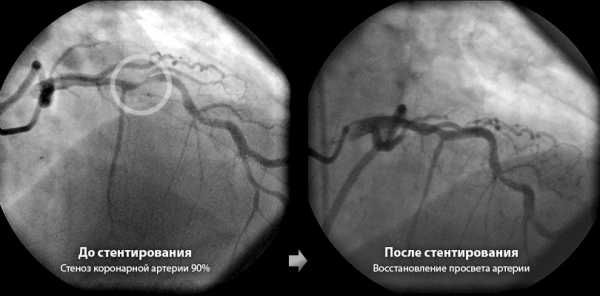
Стентированием называют врачебное оперативное вмешательство с целью установки стента, — прочной металлической сетчатой трубочки, выполняющей роль каркаса для коронарного кровеносного сосуда на достаточно долгий срок. Это приспособление может быть установлено в любых патологически суженных участках сосудов сердца, с целью их расширения и восстановления уровня кровообращения до нормальных показателей.
Данная процедура, по сути, является оперативным эндоваскулярным вмешательством. Стенты, устанавливаемые при этом, могут отличаться между собой по различным конструкционным особенностям: размеру, покрытию, структуре сетки.
Ход оперативного вмешательства
Когда диагноз установлен и определена тактика лечения пациента с применением стентирования, начинается подготовка к оперативному вмешательству, выполняемая в несколько этапов:
1. За сутки перед манипуляцией больной может поужинать, придерживаясь диеты, с требованиями которой его ознакомит врач.
2. На утро дня, когда назначена операция, завтракать не следует.
3. Непосредственно перед стентированием, пациенту делают инъекции медикаментозных препаратов, вызывающих разжижение крови (Гепарин либо Варфарин).
Как только подготовительный этап остается позади, кардиохирурги начинают установку стента по следующей технологии:
– Обезболивают при помощи анестетиков местного воздействия в месте установки катетера.
– Надрезают стенку одной из бедренных артерий и устанавливают специальную трубку.
– Вводят контрастное вещество, которое поможет контролировать ход хирургического вмешательства при помощи рентгеновского аппарата.
– Стент с баллоном лучше вводить, визуализируя происходящее внутри сосуда по технологии компьютерного сканирования.
– Как только зонд окажется в нужном месте, раздувают специальный баллон, раскрывающий стент и вдавливающий бляшку из холестерина в интиму сосуда.
– Раздувают баллоном установленную конструкцию еще раз с целью лучшей ее фиксации.
– Извлекают все оборудование из операционного поля.
– На место прокола накладывают заранее подготовленную стерильную марлевую повязку.
По окончанию операции пациент будет на протяжении первых суток находится реанимационной палате. Потом, при отсутствии осложнений, его помещают в общую палату на 7 дней. Отвечая на вопрос о том, сколько длится операция стентирование, можно указать только примерное время, — 3 часа, но этот срок зависит от многих особенностей организма человека.
Осложнения после оперативного вмешательства
Статистика утверждает, что после подобной операции 9/10 пациентов отмечают, что их общее самочувствие и циркуляция крови улучшилось. Остальная 1/10, перенесших стентирование, предъявляет жалобы на неприятные ощущения за грудиной, вплоть до выраженного болевого синдрома. Как правило, такие изменения самочувствия не угрожают жизни и здоровью человека. Пройдет совсем немного времени и больной выздоровеет, у него стабилизируются показатели кровообращения, улучшится самочувствие.
О возможных осложнениях перед хирург должен уведомить пациента до операции. Стентирование может стать причиной следующих патологических явлений:
– отслойки интимы сосудов;
– повреждения стенок артерий;
– разрывов коронарных артерий;
– аневризма стентированного сосуда;
– гематом в области операционного разреза;
– инфицирования места проникновения катетера;
– образования или переноса тромбов в сосуды легких или конечностей
– тромбозов стента, требующего повторного хирургического вмешательства;
– необходимости перехода на другой вид оперативного вмешательства, — шунтирование;
– расстройства работы почек, вплоть до острой или хронической почечной недостаточности;
– аллергических реакций на медикаментозные препараты, в том числе и рентгенконтрастное вещество, вплоть до анафилактического шока.
В редких случаях оперативное вмешательство может окончится летальным исходом.
Болевые ощущения после стентирования. В чем их причина?
Хирургическое вмешательство позади, но почувствует ли пациент облегчение состояния сразу же по окончании операции? Почему болит сердце после стентирования у некоторых людей?
Улучшение состояния может прийти не сразу, а по окончании реабилитационного периода. Что касается болей за грудиной, то их причина в естественном процессе приспособления сердца к новым реалиям:
– Перераспределении гемодинамики, причем не только в сосудах сердца, но и по всему организму. Адаптационный период при этом у каждого пациента имеет свою продолжительность.
– Сопротивлении со стороны иммунной системы инородному телу, которое теперь находится внутри коронарного сосуда.
– Нахождении свертывающей системы крови в состоянии повышенной готовности. Она способна в любой момент начать откладывать фибрин на стенте.
Кроме того, на чужеродном теле высока вероятность начала образования атеросклеротических бляшек в случае нарушения диеты, неправильном образе жизни или отказе пациента от назначенных ему медикаментозных препаратов.

Шанс на новую жизнь, полученный в ходе операции, нужно закрепить при помощи комплекса лечебной физкультуры, медикаментозного лечения, а также соблюдения рекомендованного рациона питания и нормализации режима труда и отдыха.
Что такое стентирование сосудов и какая реабилитация необходима после операции
Стентирование сосудов сердца — распространённая операция, которая проводится при многих патологиях. Нередко такое лечение является единственным вариантом, который может спасти человеку жизнь. После операции требуется особая реабилитация, которая позволяет закрепить результат, избавить пациента от осложнений и сократить время, необходимое для выздоровления.
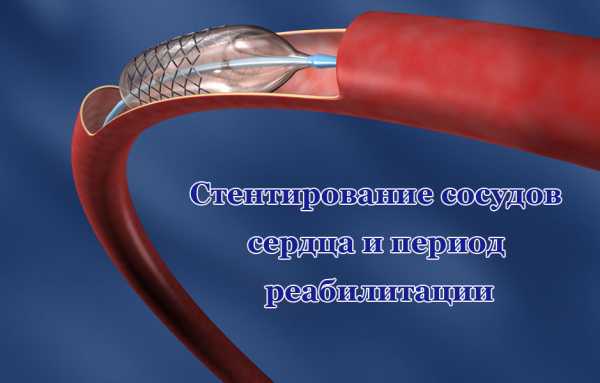
Особенности хирургического вмешательства
Стентирование сосудов сердца позволяет расширить коронарные артерии, которые не могут нормально функционировать из-за наличия тромба, и привести в норму нарушенный кровоток. Суть операции заключается во введении в артерию стента, который является особым протезом для стенки поражённого сосуда. По сути, это трубочка со стенками в виде мелкой сетки. Стент располагается в месте сужения артерии. Изначально он имеет сложенный вид. На месте поражения артерии стент раздувается и фиксируется, поддерживая таким образом сосуд в нормальном состоянии.
Хоть подобная операция и является малоинвазивным вмешательством, но всё же стенки сосуда находятся в воспалённом состоянии. Для ускорения заживления сосуда, улучшения результатов операции и их закрепления необходимо проходить особую реабилитационную программу. Мы об этом обязательно поговорим, но для начала разберёмся ещё с некоторыми важными вопросами касательно коронарного стентирования.
Виды стентов
В мире выделяют около сотни разновидностей стентов. Только опытный кардиохирург может из этого ассортимента выбрать единственный экземпляр, который будет точно подходить под конкретный случай. В любом случае, он должен быть очень качественным и надёжным, ведь стент устанавливается на длительное время и выполняет важную функцию. Современные стенты обладают рядом характеристик и отличительных свойств:
- Для внешнего покрытия используется особое вещество, которое не позволяет крови сворачиваться. Таким образом, осуществляется профилактика образования тромбов.
- Стенты выпускаются в различных конструкциях. Это может быть кольцевой элемент, вариант в виде трубки или сетки. Вариантов существует много, и для хирурга несложно будет подобрать необходимый стент.
- Также стенты различаются по диаметру. Это показатель варьируется в пределах 2 – 6 мм. Длина обычно составляет один сантиметр.
- Стенты могут отличаться по составу. В любом случае, все производители используют особые сплавы, а в основе производства лежат высокие технологии. Чаще всего применяется сплав из кобальта и хрома, но возможны и другие варианты.
- Новые модели стентов имеют покрытие из лекарственных препаратов, действие которых направлено на снижение вероятности развития повторного стеноза и предупреждение инфаркта миокарда. Подобные конструкции в первую очередь необходимы людям с проблемами в работе почек и сахарным диабетом.
Показания к проведению операции стентирования
Установка стента на артерии сердца имеет ряд показаний. В каждом отдельном случае врач оценивает необходимость проведения такой операции и назначает только тогда, когда другие методы лечения без оперативного вмешательства оказываются безрезультатными. Основные показания к проведению стентирования изложены ниже:
- ишемическое заболевание в хронической форме, которое сопровождается развитием атеросклеротических бляшек, перекрывающих артериальный просвет более чем на половину;
- приступы стенокардии, которые возникают при небольших нагрузках;
- вероятность развития инфаркта миокарда в совокупности с коронарным синдромом;
- инфаркт миокарда (обширный или небольшой) в первые 6 часов при стабильном состоянии организма;
- повторное перекрытие артериального просвета после перенесения баллонной ангиопластики, шунтирования и стентирования.
Противопоказания для операции
Далеко не во всех случаях может проводиться стентирование сосудов сердца. Имеется ряд противопоказаний, которые делают проведение этой операции невозможной:
- нестабильное состояние, которое сопровождается нарушениями сознания, скачками давления, шоком и выраженной недостаточностью любого из внутренних органов;
- аллергическая реакция на препараты с содержанием йода;
- выраженная свёртываемость крови;
- протяжённые и множественные сужения в артериях, которые могут быть сосредоточены в одном/нескольких сосудах;
- поражение сосудов с диаметром менее 3 мм.;
- неизлечимые злокачественные опухоли.
Некоторые противопоказания носят временный характер, могут быть устранены на время или навсегда. Также есть относительные противопоказания, которые могут не учитываться, если человек сам настаивает на операции и при этом риски осложнений невелики. Аллергия на йодосодержащие препараты сюда не относится.
Как проходит оперативное вмешательство
Стентирование коронарных сосудов не является особо сложной и длительной операцией. Но всё равно она требует проведения особой подготовки и выполняется по чёткому плану.
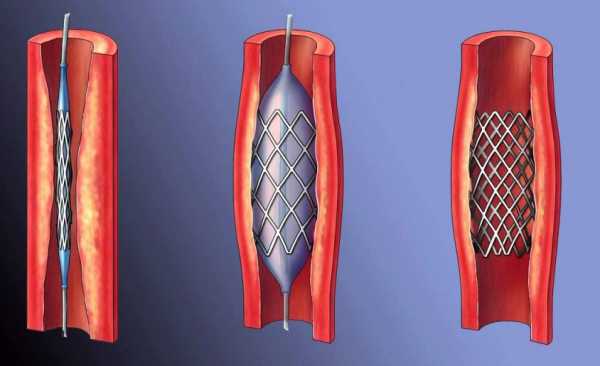 Стент в артерии
Стент в артерии
Предоперационная подготовка
Хоть коронарное стентирование и не требует проведения сложной подготовки, но всё же некоторые процедуры придётся сделать. В этом случае предоперационная подготовка сводится в следующему:
- общий анализ крови и коагулограмма, которая определяет способность крови сворачиваться;
- биохимический анализ крови;
- ЭКГ;
- рентген лёгких.
Если ситуация не критическая, а операция плановая, то человек проходит комплексное обследование. Оперативное вмешательство часто проводится при экстренных случаях, когда дорога каждая минута. Например, в случае с инфарктом, после начала которого прошло более 5 часов, операцию начинают без результатов анализов. Бригада врачей постоянно следит за тем, как себя ведёт больной, и вносит изменения по ходу проведения стентирования сосудов сердца.
Процедура операции
Операция стентирования сосудов сердца выполняется в операционных, в условиях абсолютной стерильности. Также в распоряжении хирургов должно быть точное современное оборудование, которое обеспечит постоянный контроль состояния больного и позволит мониторить ход операции. Операция выполняется по следующему плану, который может меняться в зависимости от конкретной ситуации:
- Обезболивание местного типа за счёт введения, например, «Новокаина». Обезболивание проводится на пахово-бедренной области одной из ноги.
- В бедренную артерию вводится катетер-манипулятор через предварительно сделанную пункцию-прокол.
- По мере передвижения катетера по сосуду производится введение йодосодержащего препарата. Он хорошо виден на рентгене. В итоге сосуды хорошо просматриваются, и хирург может контролировать процесс передвижения катетера.
- Когда катетер приблизится к месту повреждения артерии, ставят стент. Для этого баллон, который располагается на конце катетера, раздувается путём введения воздуха. От этого расширяются и стент, и артерия до необходимого размера.
Возможные осложнения
Вероятность развития ранних осложнений после операции, а также во время её проведения составляет не более 5%. К таким ситуациям относятся следующие состояния:
- гематома в области бедра;
- повреждение коронарных артерий;
- нарушения в кровообращении мозга и почек;
- образование тромбов на стенте;
- кровоизлияния.
Жизнь после стентирования сосудов сердца
После стентирования сосудов сердца обязателен реабилитационный период. Важно придерживаться всех правил. В этом случае можно снизить вероятность развития осложнений, которые могут возникать после стентирования сосудов сердца. Первые сутки после операции соблюдается постельный режим. При хорошем состоянии больного и отсутствии осложнений на 3 день уже может быть оформлена выписка домой.
Сколько живут после операции стентирования, сказать сложно. Очень многое зависит от соблюдения человеком принципов реабилитации. Захочет ли он менять свою жизнь, беречь сердце и сосуды, правильно питаться, не нервничать и нормировать нагрузки. Именно об этом мы и будем сейчас говорить.
Строгая диета
Каждый человек обязательно должен придерживаться особого питания после стентирования сосудов сердца. Таким образом можно снизить вероятность образования тромбов и прочих осложнений. Суть диеты заключается в следующем:
- исключение из рациона питания жирных продуктов животного происхождения;
- отказ от легкоусвояемых углеводов и продуктов, которые являются источником холестерина;
- сокращение ежедневной нормы соли;
- включение в рацион овощей, круп, диетического мяса и рыбы.

Щадящий режим нагрузок
Физические нагрузки после стентирования сосудов сердца противопоказаны на протяжении первой недели после операции. Допустима только ходьба по ровной местности. Дальше физические нагрузки добавляются постепенно. Необходимо выработать такой график добавления нагрузки, чтобы максимум через 6 недель вернуться к привычному образу жизни.
Желательно заниматься лечебной физкультурой и выполнять комплекс специальных упражнений. Каждый человек должен не только знать, как вести себя после стентирования сосудов сердца, но и чётко придерживаться этих правил. При этом ночная работа и тяжёлый труд, а также сильные нервные потрясения противопоказаны на всё время жизни.
Обязательный приём медикаментов и обследования
Некоторое время после операции за состоянием организма нужно наблюдать. Для этого назначаются определённые методы диагностики.
- ЭКГ, в том числе диагностика с нагрузочными пробами не ранее, чем через 2 недели после операции;
- анализ на свёртываемость крови и её липидный спектр;
- плановая коронарография проводится через год спустя проведения операции.
Если врач назначил все эти исследования или одно из них, необходимо без промедления проходить диагностику. Это позволит выявить развитие осложнений ещё на этапе их зарождения и оперативно устранить.
Также в период после стентирования требуется приём лекарств, которые будут выписаны специалистом. Нужно помнить, что хоть работа артерии и была восстановлена, но причина, которая привела к таким последствиям, осталась. В некоторых случаях приём медикаментов может продолжаться на протяжении года, хотя никто не исключает пожизненного лечения. Обычно назначаются следующие препараты:
Стентирование сосудов сердца — необходимая операция, которая позволяет вернуть сосудам их работоспособность и восстановить кровоток. В некоторых случаях проведение такого оперативного вмешательства является единственным вариантом сохранить человеку жизнь. Но дальнейшее самочувствие и состояние здоровья зависит исключительно от самого человека. Можно вернуться к нормальному образу жизни, а можно свести на нет все усилия врачей.
Коронарное кровообращение — Википедия
Материал из Википедии — свободной энциклопедии
| Коронарное кровообращение | |
|---|---|
| Сердце, вид спереди: визуализируется правая коронарная артерия и передняя нисходящая ветвь левой коронарной артерии. | |
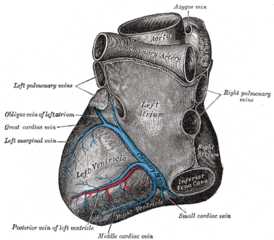 Диафрагмальная поверхность сердца. | |
| Медиафайлы на Викискладе |
Коронарное кровообращение — циркуляция крови по кровеносным сосудам миокарда. Сосуды, которые доставляют к миокарду насыщенную кислородом (артериальную) кровь, называются коронарными артериями. Сосуды, по которым от сердечной мышцы оттекает деоксигенированная (венозная) кровь, называются коронарными венами.
Коронарные артерии, располагающиеся на поверхности сердца, называются эпикардиальными. Эти артерии в норме способны к саморегуляции, обеспечивающей поддержание коронарного кровотока на уровне, соответствующем потребностям миокарда. Эти сравнительно узкие артерии обычно поражаются атеросклерозом и подвержены стенозу с развитием коронарной недостаточности. Коронарные артерии, располагающиеся глубоко в миокарде, называются субэндокардиальными.
Коронарные артерии относятся к «конечному кровотоку», являясь единственным источником кровоснабжения миокарда: избыточный кровоток крайне незначителен, в связи с чем стеноз этих сосудов может быть столь критичным.
Анатомия кровоснабжения миокарда индивидуальна для каждого человека. Полная оценка анатомии коронарных артерий возможна лишь посредством коронарографии или коронарной КТ-ангиографии.
Различают два основных ствола коронарного кровоснабжения — правую (англ. RCA) и левую (англ. LCA) коронарные артерии. Обе этих артерии отходят от начального отдела (корня) аорты, непосредственно над аортальным клапаном. Левая коронарная артерия исходит из левого аортального синуса, правая — из правого.
Правая коронарная артерия является источником кровоснабжения большей части правого желудочка сердца, части сердечной перегородки и задней стенки левого желудочка сердца. Остальные отделы сердца снабжаются левой коронарной артерией.[1]
Левая коронарная артерия разделяется на две или три, реже четыре артерии, из которых наиболее клинически значимыми являются передняя нисходящая и огибающая ветви. Передняя нисходящая ветвь является непосредственным продолжением левой коронарной артерии и спускается к верхушке сердца. Огибающая ветвь отходит от левой коронарной артерии в её начале приблизительно под прямым углом, огибает сердце спереди назад, иногда достигая по задней стенке межжелудочковой борозды.
Варианты[править | править код]
В 4 % случаев имеется третья, задняя коронарная артерия. В редких случаях наблюдается единственная коронарная артерия, огибающая корень аорты.
Иногда отмечается удвоение коронарных артерий (коронарная артерия замещается двумя артериями, располагающимися параллельно друг другу).
Доминантность[править | править код]
Артерия, отдающая заднюю нисходящую артерию (англ. PDA, задняя межжелудочковая артерия)[2], определяет доминантность кровоснабжения миокарда.[3]
- Если задняя нисходящая артерия отходит от правой коронарной артерии, говорится о правом типе доминантности кровоснабжения миокарда.
- Если задняя нисходящая артерия отходит от огибающей артерии (англ. LCX, ветви левой коронарной артерии), говорится о левом типе доминантности кровоснабжения миокарда.
- Ситуация кровоснабжения задней нисходящей артерии и правой, и огибающей коронарными артериями называется содоминантным кровоснабжением миокарда.
Приблизительно в 70 % случаев наблюдается правый тип доминантности, 20 % — содоминантность, 10 % — левый тип доминантности[3].
Доминантность отражает источник кровоснабжения артерии, питающей предсердно-желудочковый узел.
Сердечный кровоток в состоянии покоя составляет 0,8 — 0,9 мл/г в мин (4 % общего сердечного выброса). При максимальной нагрузке коронарный кровоток может возрастать в 4 — 5 раз. Скорость коронарного кровотока определяется давлением в аорте, частотой сердечных сокращений, вегетативной иннервацией и, в наибольшей степени, метаболическими факторами.
От миокарда кровь оттекает преимущественно (2/3 коронарной крови) в три вены сердца: большую, среднюю и малую. Сливаясь, они образуют венечный синус, открывающийся в правое предсердие. Остальная кровь оттекает по передним сердечным венам и тебезиевым венам.[1]
Сердце человека — Википедия
Сердце человека — это конусообразный полый мышечный орган, в который поступает кровь из впадающих в него венозных стволов и перекачивающий её в артерии, которые примыкают к сердцу. Полость сердца разделена на два предсердия и два желудочка. Левое предсердие и левый желудочек в совокупности образуют «артериальное сердце», названное так по типу проходящей через него крови, правый желудочек и правое предсердие объединяются в «венозное сердце», названное по тому же принципу. Сокращение сердца называется систола, а расслабление — диастола[B: 1].
Форма сердца не одинакова у разных людей. Она определяется возрастом, полом, телосложением, здоровьем и другими факторами. В упрощенных моделях описывается сферой, эллипсоидами, фигурами пересечения эллиптического параболоида и трёхосного эллипсоида. Мера вытянутости (фактор) формы есть отношение наибольших продольного и поперечного линейных размеров сердца. При гиперстеническом типе телосложения отношение близко к единице и астеническом — порядка 1,5. Длина сердца взрослого человека колеблется от 10 до 15 см (чаще 12—13 см), ширина в основании 8—11 см (чаще 9—10 см) и переднезадний размер 5—8,5 см (чаще 6,5—7 см). Масса сердца в среднем составляет у мужчин 332 г (от 274 до 385 г), у женщин — 253 г (от 203 до 302 г)[B: 2]
Сердце находится в центре грудной клетки и смещено нижним левым краем в левую сторону, в так называемой околосердечной сумке — перикарде, который отделяет сердце от других органов.
По отношению к средней линии тела сердце располагается несимметрично — около 2/3 слева от неё и около 1/3 — справа. В зависимости от направления проекции продольной оси (от середины его основания до верхушки) на переднюю грудную стенку различают поперечное, косое и вертикальное положение сердца. Вертикальное положение чаще встречается у людей с узкой и длинной грудной клеткой, поперечное — у лиц с широкой и короткой грудной клеткой.
Сердце состоит из четырёх отдельных полостей, называемых камерами: левое предсердие, правое предсердие, левый желудочек, правый желудочек. Они разделены перегородками. В правое предсердие входят полые, в левое предсердие — лёгочные вены. Из правого желудочка и левого желудочка выходят, соответственно, лёгочная артерия (лёгочный ствол) и восходящая аорта. Правый желудочек и левое предсердие замыкают малый круг кровообращения, левый желудочек и правое предсердие — большой круг. Сердце расположено в нижней части переднего средостения, большая часть его передней поверхности прикрыта лёгкими с впадающими участками полых и лёгочных вен, а также выходящими аортой и лёгочным стволом. В полости перикарда содержится небольшое количество серозной жидкости.[B: 2]
Стенка левого желудочка приблизительно в три раза толще, чем стенка правого желудочка, так как левый должен быть достаточно сильным, чтобы вытолкнуть кровь в большой круг кровообращения для всего организма (сопротивление потоку крови в большом круге кровообращения в несколько раз больше, а давление крови в несколько раз выше, чем в малом круге кровообращения).
Существует необходимость поддержания тока крови в одном направлении, в противном случае сердце могло бы наполниться той самой кровью, которая перед этим была отправлена в артерии. Ответственными за ток крови в одном направлении являются клапаны, которые в соответствующий момент открываются и закрываются, пропуская кровь или ставя ей заслон. Клапан между левым предсердием и левым желудочком называется митральный клапан или двухстворчатый клапан, так как состоит из двух лепестков. Клапан между правым предсердием и правым желудочком носит название трёхстворчатый клапан — он состоит из трёх лепестков. В сердце находятся ещё аортальный и лёгочный клапаны. Они контролируют вытекание крови из обоих желудочков.
Кровоснабжение[править | править код]
Каждая клетка сердечной ткани должна иметь постоянное поступление кислорода и питательных веществ. Этот процесс обеспечивается собственным кровообращением сердца по системе его коронарных сосудов; его принято обозначать как «коронарное кровообращение». Название происходит от 2 артерий, которые, как венец, оплетают сердце. Коронарные артерии непосредственно отходят от аорты. Через коронарную систему проходит до 20 % вытолкнутой сердцем крови. Только такая мощная порция обогащенной кислородом крови обеспечивает непрерывную работу животворного насоса человеческого организма.
Иннервация[править | править код]
Сердце получает чувствительную, симпатическую и парасимпатическую иннервацию. Симпатические волокна от правого и левого симпатических стволов, проходя в составе сердечных нервов, передают импульсы, которые ускоряют ритм сердца, расширяют просвет венечных артерий, а парасимпатические волокна проводят импульсы, которые замедляют сердечный ритм и сужают просвет венечных артерий. Чувствительные волокна от рецепторов стенок сердца и его сосудов идут в составе нервов к соответствующим центрам спинного и головного мозга.
Стенка сердца состоит из трёх слоёв — эпикарда, миокарда и эндокарда. Эпикард состоит из тонкой (не более 0,3—0,7 мм) пластинки соединительной ткани, эндокард состоит из эпителиальной ткани, а миокард состоит из сердечной поперечно-полосатой мышечной ткани. Клетки миокарда принято называть кардиомиоцитами.
Миокард густо пронизан кровеносными сосудами и нервными волокнами, образующими несколько нервных сплетений. На каждый капилляр миокарда приходится примерно четыре нервных волокна.[B: 3]
Биофизический взгляд на строение сердца[править | править код]
Схема пространственно-временной организации нормальной работы сердца человека. Зеленые надписи и стрелки указывают время прихода волны возбуждения в данную область сердца. Голубые врезки показывают форму профиля бегущей волны (т. н. «потенциала действия») в разных областях сердца, обусловленную различием свойств элементов возбудимой среды, которую формируют ткани сердца. Бежевая врезка — нормальное распространение бегущей волны возбуждения из пейсмейкерной зоны в центре (синусового узла) в сторону краев (по рабочему миокарду) в простейшей имитационной математической модели.С точки зрения кардиофизики, сердце представляет собой многокомпонентную полимерную неоднородную активную среду естественного происхождения. Тонкая организация структуры этой среды и обеспечивает её основные биологические функции.
Неоднородная структура сердца, лежащая в основе его тонкой организации, была многократно подтверждена сначала при помощи методов электрофизиологии, а затем и методами вычислительной биологии (см. рисунок).
Автоволновые свойства сердечной ткани уже более чем полстолетия активно исследуются и российской, и мировой наукой.
Новый научный взгляд на этот биологический объект позволяет по-новому подойти к решению проблемы создания искусственного сердца: задача сводится к налаживанию базирующегося на современных нанотехнологиях производства искусственной полимерной активной среды с аналогичной автоволновой функцией[B: 4][B: 5].
Сердечная деятельность[править | править код]
Исторически принято[B: 1] выделять следующие физиологические свойства сердечной ткани:
Автоматия сердца — это способность сердца ритмически сокращаться под влиянием импульсов, зарождающихся в нём самом.
Возбудимость сердца — это способность сердечной мышцы возбуждаться от различных раздражителей физической или химической природы, сопровождающееся изменениями физико-химических свойств ткани.
Проводимость сердца — осуществляется в сердце электрическим путём вследствие образования потенциала действия в клетках пейс-мейкерах. Местом перехода возбуждения с одной клетки на другую, служат нексусы.
Сократимость сердца — сила сокращения сердечной мышцы прямо пропорциональна начальной длине мышечных волокон.
Рефрактерность миокарда — такое временное состояние невозбудимости тканей.
Явления автоматии, возбудимости и проводимости могут объединяться понятием «автоволновая функция сердца»[B: 4][B: 5].
Считается, что сердечная деятельность нацелена на обеспечение насосной функции сердца, то есть «основной физиологической функцией сердца является ритмическое нагнетание крови в сосудистую систему»[B: 6].
Кровообращение[править | править код]
Выполняя в системе кровообращения насосную функцию, сердце постоянно нагнетает кровь в артерии. Сердце человека — это своеобразный насос, который обеспечивает постоянное и непрерывное движение крови по сосудам в нужном направлении.
Двухстворчатый и трёхстворчатый клапаны обеспечивают ток крови в одном направлении — из предсердий в желудочки.
Цикл работы сердца[править | править код]
Здоровое сердце ритмично и без перерывов сжимается и разжимается. В одном цикле работы сердца различают три фазы:
- Наполненные кровью предсердия сокращаются. При этом кровь через открытые клапаны нагнетается в желудочки сердца (они в это время остаются в состоянии расслабления). Сокращение предсердий начинается с места впадения в него вен, поэтому устья их сжаты и попасть назад в вены кровь не может.
- Происходит сокращение желудочков с одновременным расслаблением предсердий. Трёхстворчатые и двустворчатые клапаны, отделяющие предсердия от желудочков, поднимаются, захлопываются и препятствуют возврату крови в предсердия, а аортальный и лёгочный клапаны открываются. Сокращение желудочков нагнетает кровь в аорту и лёгочную артерию.
- Пауза (диастола) короткий период отдыха этого органа. Во время паузы из вен кровь попадает в предсердия и частично стекает в желудочки. Когда начнётся новый цикл, оставшаяся в предсердиях кровь будет вытолкнута в желудочки — цикл повторится.
Один цикл работы сердца длится около 0,85 сек., из которых на время сокращения предсердий приходится только 0,11 сек., на время сокращения желудочков 0,32 сек., и самый длинный — период отдыха, продолжающийся 0,4 сек. Сердце взрослого человека, находящегося в покое, работает в системе около 70 циклов в минуту.
Автоматизм сердца[править | править код]
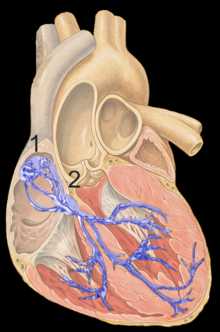 Схематическое изображение проводящей системы сердца (выделено синим цветом): (1) синусо-предсердный узел, (2) предсердно-желудочковый узел
Схематическое изображение проводящей системы сердца (выделено синим цветом): (1) синусо-предсердный узел, (2) предсердно-желудочковый узел Определённая часть сердечной мышцы специализируется на выдаче остальному сердцу управляющих сигналов в форме соответствующих импульсов автоволновой природы; эта специализированная часть сердца получила название Проводящая система сердца (ПСС). Именно она обеспечивает автоматизм сердца.
| Автоматизм — способность сердца возбуждаться под влиянием импульсов, возникающих в кардиомиоцитах без внешних раздражителей. В физиологических условиях наивысшим автоматизмом в сердце обладает САУ, поэтому его называют автоматическим центром первого порядка.А.В. Ардашев и др., 2009 [B: 7] |
Синусно-предсердный узел, называемый водителем ритма 1-го порядка и расположенный на своде правого предсердия, является важной частью ПСС.[2] Путём отправки регулярных автоволновых импульсов он управляет частотой сердечного цикла. Эти импульсы через пути проведения предсердий поступают в предсердно-желудочковый узел и дальше — в отдельные клетки рабочего миокарда, вызывая их сокращение.
Таким образом, ПСС при помощи координации сокращений предсердий и желудочков обеспечивает ритмичную работу сердца, то есть нормальную сердечную деятельность.
Регуляция работы сердца[править | править код]
Работа сердца регулируется при помощи миогенных, нервных и гуморальных механизмов.
Миогенный, или гемодинамический, механизм регуляции разделяют на: гетерометрический и гомеометрический[B: 8].
Нервная система регулирует частоту и силу сердечных сокращений: (симпатическая нервная система обуславливает усиление сокращений, парасимпатическая — ослабляет).
Воздействие эндокринной системы на сердце происходит при посредстве гормонов, которые могут усиливать или ослаблять силу сердечных сокращений, изменять их частоту. Основной эндокринной железой, регулирующей работу сердца, можно считать надпочечники: они выделяют гормоны адреналин и норадреналин, помимо них также ускоряют сердечные сокращения: серотонин, тироксин, Ca2+ действие которых на сердце соответствуют функциям симпатической нервной системы. Эффект на работу сердца оказывают также ионы кальция и калия, а также эндорфины и множество иных биологически активных веществ. Однако существуют вещества способствующие замедлению работы сердца: ацетилхолин, брадикинин, K+.
Инструментальные методы диагностики работы сердца[править | править код]
Ультразвуковое исследование сердца[править | править код]
Достаточно информативным методом визуализации структуры, физиологических процессов, патологий, и гемодинамики (допплерография). В отличие от методов, основанных на рентген технологии, не имеет лучевой нагрузки. К достоинствам метода можно также отнести быстроту исследования, безопасность, доступность.
Электрические явления[править | править код]
Работа сердца (как и любой мышцы) сопровождается электрическими явлениями, которые вызывают появление электромагнитного поля вокруг работающего органа. Электрическую активность сердца можно зарегистрировать при помощи различных методов электрокардиографии, дающей картину изменений во времени разности потенциалов на поверхности тела человека, либо электрофизиологического исследования миокарда, позволяющее проследить пути распространения волн возбуждения непосредственно на эндокарде. Эти методы играют важную роль в диагностике инфаркта и других заболеваний сердечно-сосудистой системы.
Акустические явления[править | править код]
Акустические явления, называемые тонами сердца, можно услышать, прикладывая к грудной клетке ухо или стетоскоп. Каждый сердечный цикл в норме разделяют на 4 тона. Ухом при каждом сокращении слышны первые 2. Более долгий и низкий связан с закрытием дву- и трёхстворчатого клапанов, более короткий и высокий — это закрываются клапаны аорты и лёгочной артерии. Между одним и вторым тоном идёт фаза сокращения желудочков.
Механическая активность[править | править код]
Сердечные сокращения сопровождаются рядом механических проявлений, регистрируя которые, также можно получить представление о динамике сокращения сердца. Например, в пятом межреберье слева, на 1 см внутри от среднеключичной линии, в момент сокращения сердца ощущается верхушечный толчок. В период диастолы сердце напоминает эллипсоид, ось которого направлена сверху вниз и справа налево. При сокращении желудочков форма сердца приближается к шару, при этом продольный диаметр сердца уменьшается, а поперечный возрастает. Уплотненный миокард левого желудочка касается внутренней поверхности грудной стенки. Одновременно опущенная к диафрагме при диастоле верхушка сердца в момент систолы приподнимается и ударяется о переднюю стенку грудной клетки. Все это и вызывает появление верхушечного толчка.[B: 6]
Для анализа механической активности сердца используют ряд специальных методов.
Кинетокардиография[прим. 1] — метод регистрации низкочастотных вибраций грудной клетки, обусловленных механической деятельностью сердца; позволяет изучить фазовую структуру цикла левого и правого желудочков сердца одновременно.
Электрокимография — метод электрической регистрации движения контура сердечной тени на экране рентгеновского аппарата[3]. К экрану у краев контура сердца прикладывают фотоэлемент, соединенный с осциллографом. При движениях сердца изменяется освещенность фотоэлемента, что регистрируется осциллографом в виде кривой. Получаются кривые сокращения и расслабления сердца.
Баллистокардиография — метод, основанный на том, что изгнание крови из желудочков и её движение в крупных сосудах вызывают колебания всего тела, зависящие от явлений реактивной отдачи, подобных тем, которые наблюдаются при выстреле из пушки (название методики «баллистокардиография» происходит от слова «баллиста» — метательный снаряд). Кривые смещений тела, записываемые баллистокардиографом и зависящие от работы сердца, имеют в норме характерный вид. Для их регистрации существует несколько различных способов и приборов.
Динамокардиография — метод, основан на том, что движения сердца в грудной клетке и перемещение крови из сердца в сосуды сопровождаются смещением центра тяжести грудной клетки по отношению к той поверхности, на которой лежит человек.[4] Обследуемый лежит на специальном столе, на котором смонтировано особое устройство с датчиками — преобразователями механических величин в электрические колебания. Устройство находится под грудной клеткой исследуемого. Смещения центра тяжести регистрируются осциллографом в виде кривых. На динамокардиограмме отмечаются все фазы сердечного цикла: систола предсердий, периоды напряжения желудочков и изгнания из них крови, протодиастолический период, периоды расслабления и наполнения желудочков кровью.
Фонокардиография — метод регистрации тонов сердца на фонокардиограмме. Если в левой половине грудной клетки на уровне IV—V ребра обследуемого приложить чувствительный микрофон, соединенный с усилителем и осциллографом, то возможно зарегистрировать на фотобумаге тоны сердца в виде кривых. Этот метод используется для диагностики поражений клапанов сердца.[4]
- ↑ 1 2 Foundational Model of Anatomy
- ↑ Бабский Е. Б. Физиология человека. — 2-е изд. — М: Медицина, 1972. — С. 69.
- ↑ Косицкий Г. И. Физиология человека. — 3-е изд. — М: Медицина, 1985. — С. 255.
- ↑ 1 2 Косицкий Г. И. Физиология человека. — 3-е изд. — М: Медицина, 1985. — С. 256.
- ↑ 1 2 Дудель Й., Рюэгг Й., Шмидт Р. и др. Физиология человека: в 3-х томах. Пер. с англ = Human Physiology / под ред. Р. Шмидта и Г. Тевса. — 3. — М.: Мир, 2010. — Т. 1. — 323 с илл. с. — 1000 экз. — ISBN 978-5-03-003834-6.
- ↑ 1 2 Привес М. Г., Лысенков Н. К., Бушкович В. И. Анатомия человека. — 11-е переработанное и дополненное. — М.: Медицина, 1985.
- ↑ Гистология. — М.
- ↑ 1 2 Елькин Ю. Е., Москаленко А. В. Базовые механизмы аритмий сердца // Клиническая аритмология / Под ред. проф. А. В. Ардашева. — М.: МЕДПРАКТИКА-М, 2009. — С. 45—74. — 1220 с. — ISBN 978-5-98803-198-7.
- ↑ 1 2 Tachycardia as “Shadow Play” // Tachycardia / Takumi Yamada, editor. — Croatia: InTech, 2012. — P. 97—122. — 202 p. — ISBN 978-953-51-0413-1.
- ↑ 1 2 Физиология человека / под ред. В. М. Покровского и Г. Ф. Коротько. — 3. — М.: Медицина, 2007. — 656 с. — (Учебная литература для студентов медицинских вузов). — 10 000 экз. — ISBN 5-225-04729-7.
- ↑ Анатомия и физиология проводящей системы сердца // Клиническая аритмология / Под ред. проф. А. В. Ардашева. — М.: МЕДПРАКТИКА-М, 2009. — С. 35—41. — 1220 с. — ISBN 978-5-98803-198-7.
- ↑ Судаков К. В. Нормальная физиология. — М.: Медицинское информационное агентство, 2006. — С. 329. — 920 с. — ISBN 5-89481-294-1.
Искусственное сердце — Википедия
Артериальный насос «CardioWest»Искусственное сердце — представляет собой технологическое устройство, предназначенное для поддержания достаточных для жизнедеятельности параметров гемодинамики.
В настоящее время под искусственным сердцем понимается две группы технических устройств.
- К первой относятся гемооксигенаторы (аппараты искусственного кровообращения). Они состоят из артериального насоса, перекачивающего кровь, и блока оксигенатора, который насыщает кровь кислородом. Данное оборудование активно используется в кардиохирургии, при проведении операций на сердце.
- Ко второй относятся кардиопротезы, то есть технические устройства, имплантируемые в организм человека, призванные заменить сердечную мышцу и повысить качество жизни больного. Следует отметить, что в настоящее время данные устройства являются лишь экспериментальными и проходят клинические испытания.
Пионером в разработке искусственного сердца являлся советский учёный В. П. Демихов, который ещё в 1937 году показал принципиальную возможность поддержания кровообращения в организме собаки с помощью пластикового насоса, приводимого в движение электродвигателем. Два с половиной часа, которые прожила собака с этим механическим устройством, имплантированным на место удаленного собственного сердца, стали отсчётом новой эры в медицине.
Эстафету подхватили американские ученые, но лишь два десятилетия спустя В. Кольф и Т. Акутсу разработали искусственное сердце из полихлорвинила, состоящее из двух мешочков, включённых в единый корпус. Оно имело 4 трёхстворчатых клапана из того же материала и работало от пневмопривода, расположенного снаружи. Эти исследования положили начало целой серии конструктивных решений искусственного сердца с внешним приводом.[1]
Идея имплантации искусственного сердца для поддержания жизни реципиента на период поиска подходящего донора была реализована в 1969 году, когда американский хирург Д. Кули произвёл имплантацию искусственного сердца больному, которого после резекции обширной аневризмы левого желудочка не удавалось отключить от аппарата искусственного кровообращения. Через 64 часа работы искусственное сердце было заменено на аллотрансплантат, однако еще через 36 часов больной погиб от пневмонии. Это был первый случай двухэтапной операции трансплантации сердца, которая сегодня широко распространена.[1]
В СССР в конце 1960-х годов в ОКБ Сухого была создана группа по созданию пневмогидравлического насоса, способного временно заместить естественное сердце человека и поддержать его жизнедеятельность до того момента, когда появится возможность установить донорское сердце взамен искусственного. В 1974 году в период пребывания президента США Р. Никсона в Москве было заключено соглашение между СССР и США «О совместных исследованиях и разработке искусственного сердца». Приказом Минавиапрома ОКБ Сухого было определено головным исполнителем по разработке искусственного сердца с пневмоприводом. Совместные работы по проблеме искусственного сердца с медиками США велись в течение 20 лет.
Экспериментальное искусственное сердце «Герц-02» производства СКБ МТРуководителем программы искусственного сердца в СССР стал возглавивший в 1975 году Институт трансплантации и искусственных органов Минздрава РСФСР (НИИТиИО) профессор В. И. Шумаков.
В 1976 году на основании постановления Совета Министров СССР в СКБ МТ КЧХЗ, входившего в Минсредмаш и являвшегося единственным в стране производителем искусственных клапанов сердца, была организована Лаборатория искусственного сердца. Итогом её работы стало создание опытного образца искусственного сердца «Герц-02» в ранцевом исполнении, и в 1985 году в НИИТиИО были проведены его успешные испытания на животных — впервые в стране животное (телёнок) жило с искусственным сердцем более двух недель. Однако в дальнейшем эти исследования по финансовым причинам были прекращены.[2]
В НИИТиИО длительность работы модели искусственного сердца с внешним приводом «Поиск-10М» была доведена к 1985 году до 100 суток, что позволило начать его клинические испытания. Показаниями к применению искусственного сердца были определены резкое ухудшение состояния пациентов, включенных в лист ожидания на пересадку сердца; критические ситуации у больных, которые после окончания операции не могут быть отключены от аппарата искусственного кровообращения; резко прогрессирующие явления отторжения трансплантата. С декабря 1986 года специалистами НИИТиИО было выполнено 17 трансплантаций искусственного сердца «Поиск-10М», из них 4 в Польше, куда бригада выезжала по экстренному вызову. К сожалению, несмотря на усилия врачей, максимальная продолжительность работы искусственного сердца не превысила 15 суток.[1]
По состоянию на 2010 год не было создано эффективного имплантируемого человеку протеза всего сердца. В кардиохирургических клиниках проводят успешные частичные замены органических компонентов на искусственные. Например, производится замена клапанов, крупных сосудов, предсердий, желудочков. Кроме того, успешно производится пересадка донорского сердца.
Разработаны несколько прототипов эффективных имплантируемых человеку протезов всего сердца. В НЦССХ им. А. Н. Бакулева 26 марта 2010 года была произведена операция по полной замене сердца человека на искусственный аналог кардиохирургом Лео Бокерия, совместно с его американским коллегой. Данный аппарат обеспечивает адекватное кровоснабжение органов и тканей пациента, главным его недостатком является наличие аккумулятора массой 10 кг, нуждающегося в перезарядке каждые 12 часов. В настоящее время такие протезы рассматриваются как временная мера, позволяющая пациенту с тяжелой сердечной патологией дожить до момента пересадки сердца.[3]
В 2016 году новосибирские ученые из НИИ патологии кровообращения представили свою разработку - искусственное сердце, которое снижает риск образования тромбов благодаря дисковому насосу для поверхностного натяжения. Медики уверены, что это более эффективно работающий механизм, чем его модели-предшественники, и цена его в несколько раз ниже импортных аналогов[4].
Помимо кардиохирургического, существует и медико-психологический аспект проблемы искусственного сердца.[5] Так, у четверти пациентов после операции протезирования клапанного аппарата сердца в послеоперационный период формируется специфический психопатологический симптомокомплекс, получивший наименование «кардиопротезный психопатологический синдром»[6], описанный в 1978 году.
Не исключено, что с подобной проблемой придётся столкнуться при проведении более масштабных операций по имплантации искусственного сердца.[6]
Проводящая система сердца — Википедия
| Проводящая система сердца | |
|---|---|
| лат. Systema conducens cordis | |
| Элементы проводящей системы сердца | |
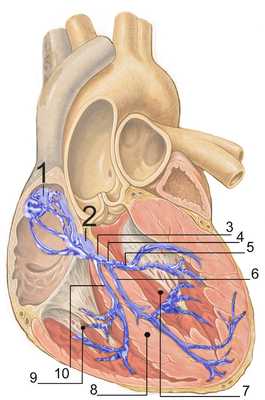 | |
| Медиафайлы на Викискладе |
Проводящая система сердца (ПСС) — комплекс анатомических образований сердца (узлов, пучков и волокон), состоящих из атипичных мышечных волокон (сердечные проводящие мышечные волокна) и обеспечивающих координированную работу разных отделов сердца (предсердий и желудочков), направленную на обеспечение нормальной сердечной деятельности.
ПСС состоит из двух взаимосвязанных частей: синоатриальной (синусно-предсердной) и атриовентрикулярной (предсердно-желудочковой).
К синоатриальной относят синоатриальный узел (узел Кис-Флака), три пучка межузлового быстрого проведения, связывающие синоатриальный узел с атриовентрикулярным и межпредсердный пучок быстрого проведения, связывающий синоатриальный узел с левым предсердием.
Атриовентрикулярная часть состоит из атриовентрикулярного узла (узел Ашоффа–Тавара), пучка Гиса (включает в себя общий ствол и три ветви: левая передняя, левая задняя и правая) и проводящих волокон Пуркинье.[B: 1]
Кровоснабжение[править | править код]
Иннервация[править | править код]
ПСС морфологически отличается как от мышечной, так и от нервной ткани, но находится в тесной связи и с миокардом, и с внутрисердечной нервной системой.[B: 2]
Атипичные мышечные волокна сердца — это специализированные проводящие кардиомиоциты, богато иннервированные, с небольшим количеством миофибрилл и обилием саркоплазмы.[B: 1]
Синусовый узел[править | править код]
Синусовый узел или синоатриальный узел (САУ) (лат. nódus sinuatriális), открытый в 1907 году Артуром Кейтом[en] и Мартином Флаком[en][2], расположен субэндокардиально в стенке правого предсердия латеральнее устья верхней полой вены, между отверстием верхней полой вены и правым ушком предсердия; отдаёт ветви к миокарду предсердий.[B: 1][B: 2]
Микрофотография синусового узла. Мышечные волокна в узле напоминают миоциты сердца, однако они тоньше, имеют волнистую форму и менее интенсивно окрашиваются гематоксилин-эозином. На фотографии к узлу прилегает нервное волокно: синусовый узел взаимодействует с ответвлениями блуждающего нерва.Длина САУ ≈ 15 мм, ширина его ≈ 5 мм и толщина ≈ 2 мм. У 65% людей артерия узла берёт своё начало из правой венечной артерии, у остальных — из огибающей ветви левой венечной артерии. САУ богато иннервирован симпатическими и правым парасимпатическим нервами сердца, которые вызывают, соответственно, положительный и отрицательный хронотропные эффекты.[B: 2].
Клетки, составляющие синусовый узел, гистологически отличаются от клеток рабочего миокарда. Хорошим ориентиром служит выраженная a.nodalis (узловая артерия). Клетки синусового узла по размерам меньше клеток рабочего миокарда предсердия. Они группируются в виде пучков, при этом вся сеть клеток погружена в развитый матрикс. На границе синусового узла, обращенной к миокарду устья верхней полой вены, определяется переходная зона, которая может расцениваться как присутствие клеток рабочего миокарда предсердий в пределах синусового узла. Такие участки вклинения клеток предсердия в ткань узла чаще всего встречаются на границе узла и пограничного гребня (выступа стенки правого предсердия сердца, которым заканчиваются вверху гребенчатые мышцы).[B: 3]
Гистологически синусовый узел состоит из т.н. типичных клеток узла. Они располагаются беспорядочно, имеют веретенообразную форму, а иногда разветвления. Для этих клеток характерно слабое развитие сократительного аппарата, случайное распределение митохондрий. Саркоплазматический ретикулум развит хуже, чем в миокарде предсердий, а система T-трубочек отсутствует. Это отсутствие, правда, не является критерием, по которому выделяются "специализированные клетки": часто система T-трубочек отсутствует и в рабочих кардиомиоцитах предсердия.
По краям синусового узла наблюдаются переходные клетки, отличающиеся от типичных лучшей ориентацией миофибрилл наряду с более высоким процентом межклеточных соединений - нексусов. Находимые ранее "вставочные светлые клетки", по последним данным, являются не более чем артефактом.
Согласно концепции, предложенной T.James и соавт. (1963-1985), связь синусового узла с АВ-узлом обеспечивается за счет наличия 3-х трактов: 1) короткий передний (пучок Бахмана), 2) средний (пучок Венкебаха) и 3) задний (пучок Тореля), более длинный. Обычно импульсы попадают в АВУ по короткому переднему и среднему трактам, на что расходуется 35-45 мсек. Скорость распространения возбуждения по предсердиям составляет 0,8—1,0 м/с. Описаны и другие проводящие тракты предсердий; к примеру, по данным B.Scherlag (1972), по нижнему межпредсердному тракту возбуждение проводится из передней части правого предсердия в нижнезаднюю часть левого предсердия. Считается, что в физиологических условиях эти пучки, а также пучок Тореля находятся в латентном состоянии.[B: 2]
Тем не менее, многими исследователями оспаривается существование каких-либо специализированных пучков между САУ и АВУ. Так, к примеру, в хорошо известной коллективной монографии[B: 3] сообщается следующее:
Полемика по вопросу об анатомическом субстрате для проведения импульсов между синусовым и атриовентрикулярным узлами ведётся уже сто лет, сколько насчитывает и сама история изучения проводящей системы. (...) По мнению Aschoff, Monckeberg и Koch, ткань между узлами является рабочим миокардом предсердий и не содержит гистологически различимых трактов. (...) На наш взгляд, в качестве трёх указанных выше специализированных путей James дал описание практически всего миокарда предсердной перегородки и пограничного гребня. (...) Насколько нам известно, никто до сих пор на основе морфологических наблюдений не доказал, что в межсердечной перегородке и пограничном гребне проходят узкие тракты, каким-либо образом сравнимые с атриовентрикулярным трактом и его ответвлениями.
Область атриовентрикулярного соединения[править | править код]
Предсердно-желудочковый узел (лат. nódus atrioventriculáris) лежит в толще передне-нижнего отдела основания правого предсердия и в межпредсердной перегородке. Длина его составляет 5-6 мм, ширина 2-3 мм. Кровоснабжается он одноименной артерией, которая в 80-90% случаев является ветвью правой коронарной артерии, а в остальных — ветвью левой огибающей артерии.[B: 2]
АВУ представляет собой ось проводящей ткани. Располагается на гребне входного и верхушечного трабекулярного компонентов мышечной части межжелудочковой перегородки. Архитектонику АВ-соединения удобнее рассматривать по восходящей - от желудочка к миокарду предсердий. Ветвящийся сегмент АВ-пучка расположен на гребне апикального трабекулярного компонента мышечной части межжелудочковой перегородки. Предсердный отрезок АВ-оси может быть разделен на компактную зону АВ-узла и переходную клеточную зону. Компактный участок узла по всей своей длине сохраняет тесную связь с фиброзным телом, которое образует его ложе. Он имеет два удлинения, проходящие вдоль фиброзного основания направо к трёхстворчатому клапану и налево — к митральному.
Переходная клеточная зона — это область, диффузно расположенная между сократительным миокардом и специализированными клетками компактной зоны АВ-узла. В большинстве случаев переходная зона более выражена сзади, между двумя удлинениями АВ-узла, но она также образует полуовальное покрытие тела узла.
С точки зрения гистологии, клетки предсердного компонента АВ-соединения мельче, чем клетки рабочего миокарда предсердий. Клетки переходной зоны имеют вытянутую форму и иногда разделены тяжами фиброзной ткани. В компактной зоне АВ-узла клетки расположены более тесно и часто организованы во взаимосвязанные пучки и завитки. Во многих случаях выявляется разделение компактной зоны на глубокий и поверхностный слои. Дополнительным покрытием служит слой переходных клеток, придающий узлу трехслойность. По мере перехода узла в проникающую часть пучка наблюдается увеличение размеров клеток, но в основном клеточная архитектоника сравнима с таковой в компактной зоне узла. Границу между АВ-узлом и проникающей частью одноименного пучка трудно определить под микроскопом, поэтому предпочтительней чисто анатомическое разделение в районе точки входа оси в фиброзное тело. Клетки, составляющие ветвящуюся часть пучка, по своим размерам напоминают клетки миокарда желудочков.
Коллагеновые волокна делят АВУ на кабельные структуры. Эти структуры создают анатомическую основу для продольной диссоциации проведения. Проведение возбуждения по АВУ возможно как в антероградном, так и в ретроградном направлениях. АВУ, как правило, оказывается функционально разделённым продольно на два проводящих канала (медленный α и быстрый β) — это создаёт условия для возникновения пароксизмальной узловой реципроктной тахикардии.
Продолжением АВУ является общий ствол пучка Гиса.
Пучок Гиса[править | править код]
Предсердно-желудочковый пучок (лат. fascículus atrioventriculális), или пучок Гиса, связывает миокард предсердий с миокардом желудочков. В мышечной части межжелудочковой перегородки этот пучок делится на правую и левую ножки (лат. crus déxtrum et crus sinístrum). Концевые разветвления волокон (волокна Пуркинье), на которые распадаются эти ножки, заканчиваются в миокарде желудочков.[B: 1]. Описан немецким кардиологом Вильгельмом Гисом[3].
Длина общего ствола пучка Гиса 8-18 мм в зависимости от размеров перепончатой части межжелудочковой перегородки, ширина около 2 мм. Ствол пучка Гиса состоит из двух сегментов — прободающего и ветвящегося. Прободающий сегмент проходит через фиброзный треугольник и доходит до мембранной части межжелудочковой перегородки. Ветвящийся сегмент начинается на уровне нижнего края фиброзной перегородки и делится на две ножки: правая направляется к правому желудочку, а левая — к левому, где распределяется на переднюю и заднюю ветви. Передняя ветвь левой ножки пучка Гиса разветвляется в передних отделах межжелудочковой перегородки, в передне-боковой стенке левого желудочка и в передней сосочковой мышце. Задняя ветвь обеспечивает проведение импульса по средним отделам межжелудочковой перегородки, по задне-верхушечным и нижним частям левого желудочка, а также по задней сосочковой мышце. Между ветвями левой ножки пучка Гиса существует сеть анастомозов, по которым импульс при блокаде одной из них попадает в блокированный области за 10-20 мсек. Скорость распространения возбуждения в общем стволе пучка Гиса составляет около 1,5 м/с, в разветвлениях ножек пучка Гиса и проксимальных отделах системы Пуркинье она достигает 3-4 м/с, а в терминальных отделах волокон Пуркинье снижается и в рабочем миокарде желудочков равняется примерно 1 м/с. [B: 2]
Прободающая часть ствола Гиса кровоснабжается из артерии АВУ; правая ножка и передняя ветвь левой ножки — от передней межжелудочковой венечной артерии; задняя ветвь левой ножки — от задней межжелудочковой венечной артерии.[B: 2]
Волокна Пуркинье[править | править код]
Бледные или набухшие клетки (так называемые клетки Пуркинье) редко встречаются в специализированной области атриовентрикулярного соединения у младенцев и детей младшего возраста.
Координируя сокращения предсердий и желудочков, ПСС обеспечивает ритмичную работу сердца, т.е нормальную сердечную деятельность. В частности, именно ПСС обеспечивает автоматизм сердца.
Функционально синусовый узел является водителем ритма первого порядка. В состоянии покоя в норме он генерирует 60-90 импульсов в минуту.[B: 2]
В АВ-соединении, главным образом в пограничных участках между АВУ и пучком Гиса, происходит значительная задержка волны возбуждения. Скорость проведения сердечного возбуждения замедляется до 0,02-0,05 м/с. Такая задержка возбуждения в АВУ обеспечивает возбуждение желудочков только после окончания полноценного сокращения предсердий. Таким образом, основными функциями АВУ являются: 1) антероградная задержка и фильтрация волн возбуждения от предсердий к желудочкам, обеспечивающие скоординированное сокращение предсердий и желудочков и 2) физиологическая защита желудочков от возбуждения в уязвимой фазе потенциала действия (с целью профилактики рециркуляторных желудочковых тахикардий). Клетки АВУ также способны брать на себя функции центра автоматизма второго порядка при угнетении функции САУ. Они обычно вырабатывают 40-60 импульсов в минуту. [B: 2] Патологии:
- Синдром слабости синусового узла.
- Патологические добавочные проводящие пути между предсердиями и желудочками.
- Блокада проведения.
Добавочные пучки между предсердиями и желудочками являются анатомическим субстратом для классического варианта предвозбуждения желудочков (синдром Вольфа-Паркинсона-Уайта)[B: 3].
- ↑ 1 2 3 4 Борзяк Э. И., Бочаров В. Я., Сапин М. Р. и др. Анатомия человека. В 2 томах / Под ред. акад. РАНМ, проф. М. Р. Сапина. — М.: Медицина, 1993. — Т. 2. — 560 с. — 40 000 экз. — ISBN 5-225-00879-8.
- ↑ 1 2 3 4 5 6 7 8 9 Анатомия и физиология проводящей системы сердца // Клиническая аритмология / Под ред. проф. А. В. Ардашева. — М.: МЕДПРАКТИКА-М, 2009. — С. 35—41. — 1220 с. — ISBN 978-5-98803-198-7.
- ↑ 1 2 3 Аритмии сердца. Механизмы. Диагностика. Лечение. В 3 томах / Пер. с англ./Под ред. В. Дж. Мандела. — М.: Медицина, 1996. — Т. 1. — 10 000 экз. — ISBN 0-397-50561-2.
- ↑ 1 2 Foundational Model of Anatomy
- ↑ Глязер Г. Исследователи человеческого тела. От Гиппократа до Павлова = Die Entdecker des Menschen. Von Hippokrates bis Pawlow / Пер. с нем. Ю. А. Федосюка. Под ред. Б. Д. Петрова. — М.: Государственное издательство медицинской литературы, 1956. — С. 200. — 7000 экз.
- ↑ Гаврилов Л. Ф. Гис Вильгельм (младший) // Большая Медицинская Энциклопедия / Главный редактор Б. В. Петровский. — М.
Овальное окно (сердце) — Википедия
Материал из Википедии — свободной энциклопедии
Овальное окно (лат. Foramen ovale) — отверстие в межпредсердной перегородке, работающее по типу дверки, с помощью которого в фетальном периоде происходит сброс крови справа (малый круг кровообращения) налево (большой круг кровообращения). Лёгкие еще не активны и не расправлены, их кровообращение минимально. Поэтому кровь в основном течет через овальное окно в левое предсердие и через артериальный проток (иначе называемый Боталловым протоком) из лёгочного ствола в аорту.
Овальное окно обычно физиологически закрывается в первые дни-недели после рождения. Впоследствии на месте овального окна определяется небольшое углубление, называемое «овальным углублением» (лат. Fossa ovalis). Если закрытия овального окна не происходит, говорят о персистирующем, или просто открытом, овальном окне. Открытое овальное окно наблюдается у приблизительно 25 % взрослого населения. С помощью ультразвукового исследования определяется небольшой поток крови через это отверстие. В зависимости от размера окна и его гемодинамической значимости говорят о дефекте предсердной перегородки, имеющем значение в этиологии церебральных эмболий (как правило, во взрослом возрасте).[1]
Диагностика открытого овального окна[править | править код]
Как правило обычное УЗИ сердца не даёт четкого подтверждения о наличии открытого овального окна (ООО). Для визуализации сброса крови слева направо или наоборот, необходимо провести УЗИ сердца с пузырьковым контрастированием (англ. bubble test).
Для проведения теста не требуется особой подготовки пациента. В качестве расходного материала требуется комплект из периферического катетера диаметром 18G, трёхходового краника стоп-кок (англ. stop-cock) и двух перфузорных шприцев.
В локтевую вену пациента вводится катетер, к которому присоединяют трёхходовой краник. В один шприц набирают физраствор. Затем оба шприца присоединяют к кранику.
Пациент находится лежа на левом боку, эхокардиографист устанавливает ультразвуковой датчик трансторакальной эхокардиографии в области позиции верхушки сердца для лучшего выведения эхокартины в четырёхкамерной проекции.
Тест проводится в два этапа: «чистый» тест и тест во время пробы Вальсальвы.
«Чистый» тест[править | править код]
- Установка периферического катетера d=18G в локтевую вену.
- Переходник стоп-кок соединяется к катетеру.
- Соединение 2 перфузорных шприцев к стоп-коку, один из которых наполнен физраствором.
- Набрать 2 мл крови через шприц с физраствором.
- С помощью двух шприцев добиваются образования пузырьков.
- По команде доктора образованную пузырьковую эмульсию с силой вводят в вену.
- При положительном тесте ООО на картинке будет наблюдаться сброс пузырьков из одного предсердия в другое.
Тест во время пробы Вальсальвы[править | править код]
- Все этапы теста проводятся аналогично как при «чистом» тесте.
- Перед вводом раствора в вену пациент делает глубокий вдох с кратковременным натуживанием и последующим выдохом.
сердце лежачее - это... Что такое сердце лежачее?
- сердце легочное хроническое
- сердце микседематозное
Смотреть что такое "сердце лежачее" в других словарях:
сердце гиперстеника — (син. сердце лежачее) конституциональный вариант формы сердца, характеризующийся приближающимся к горизонтальному положением анатомической оси и относительно большими линейными размерами рентгеновской тени; наблюдается у лиц гиперстенического… … Большой медицинский словарь
Сердце — мускулистое, ритмически сокращающееся расширение сосудистой системы. Такие расширения могут быть как в лимфатической, так и в кровеносной системах. В первом случае они называются лимфатическими С. (см. Лимфатическая система), во втором просто С.… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Сердце* — мускулистое, ритмически сокращающееся расширение сосудистой системы. Такие расширения могут быть как в лимфатической, так и в кровеносной системах. В первом случае они называются лимфатическими С. (см. Лимфатическая система), во втором просто С.… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Се́рдце гиперсте́ника — (син. сердце лежачее) конституциональный вариант формы сердца, характеризующийся приближающимся к горизонтальному положением анатомической оси и относительно большими линейными размерами рентгеновской тени; наблюдается у лиц гиперстенического… … Медицинская энциклопедия
ЭЛЕКТРОКАРДИОГРАФИЯ — ЭЛЕКТРОКАРДИОГРАФИЯ, регистрация электрических явлений, появляющихся в сердце при его возбуждении, имеющая большое значение в оценке состояния сердца. Если история электрофизиологии начинается с знаменитого опыта Гальвани (Garvani), доказавшего в … Большая медицинская энциклопедия
ПЛЕВРИТ — ПЛЕВРИТ. Содержание: Этиология..................... 357 Патогенез и пат. физиология ..."....... ЗБЭ Пат. анатомия ................... 361 Сухой П........... . ............ 362 Эксудативный П................... 365 Гнойный П … Большая медицинская энциклопедия
ПОРОКИ СЕРДЦА — ПОРОКИ СЕРДЦА. Содержание: I. Статистика ...................430 II. Отдельные формы П. с. Недостаточность двустворчатого клапана . . . 431 Сужение левого атглю вентрикулярного отверстия ......"................436 Сужение устья аорты … Большая медицинская энциклопедия
АНЕМИЯ — АНЕМИЯ. Содержание: I. Местное малокровие............. 702 II. Общее малокровие: Острая анемия............... 704 Хроническая анемия........... 705 III. Анемия злокачественная.......... 708 ІV. Хлороз.................... 715 V. Анемия в детском… … Большая медицинская энциклопедия
Стенокардия — I Стенокардия (stenokardia; греч. stenos узкий, тесный + kardia сердце: синоним: болезнь Гебердена, грудная жаба, angina pectoris) симптом острой ишемии миокарда, выражающийся приступом загрудинной боли, нередко в сочетании с чувством страха и… … Медицинская энциклопедия
СКОЛИОЗ — (от греч. skolios кривой, термин введен Галеном во 2 в.), боковое, resp. фронтальное, искривление позвоночника. Весьма распространенная деформация, особенно в прежнее время, до популяризации методов физ. воспитания подрастающего поколения. Так, у … Большая медицинская энциклопедия

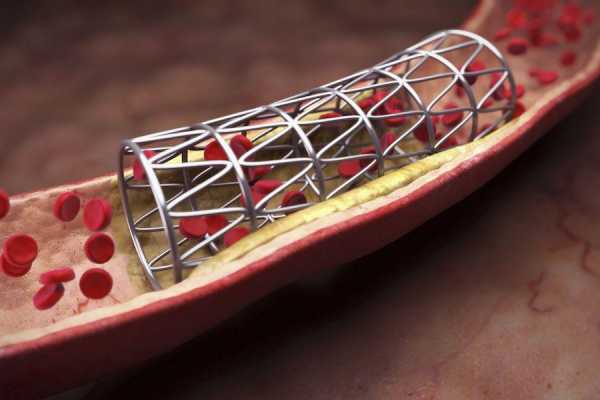
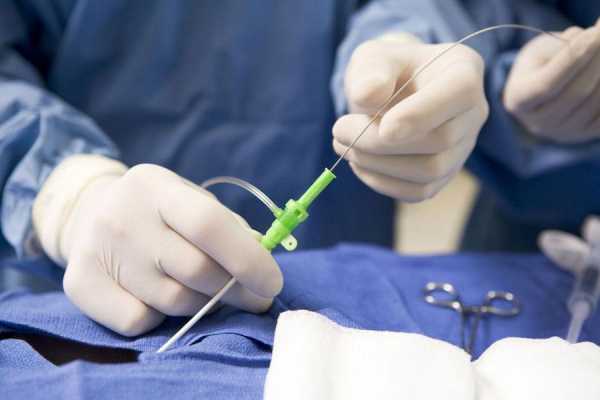
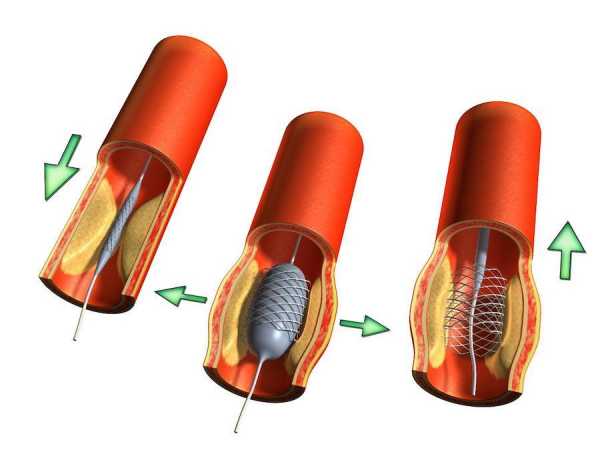

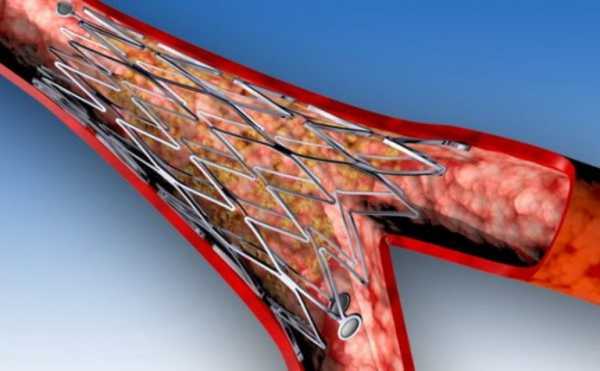

 При отсутствии осложнений и противопоказаний, врач разрешит постепенно увеличить нагрузку. В зависимости от индивидуальных особенностей организма, 100% восстановление занимает до 6 недель. Спешить не стоит. Пациенты должны знать, что на протяжении оставшейся жизни категорически запрещено подвергать себя сильным эмоциональным и психологическим нагрузкам. Под запретом оказывается работа в ночную смену.
При отсутствии осложнений и противопоказаний, врач разрешит постепенно увеличить нагрузку. В зависимости от индивидуальных особенностей организма, 100% восстановление занимает до 6 недель. Спешить не стоит. Пациенты должны знать, что на протяжении оставшейся жизни категорически запрещено подвергать себя сильным эмоциональным и психологическим нагрузкам. Под запретом оказывается работа в ночную смену. Под запретом оказываются силовые нагрузки и слишком частый секс.
Под запретом оказываются силовые нагрузки и слишком частый секс.